Острые кишечные инфекции (ОКИ) занимают второе место в структуре инфекционной заболеваемости у детей. В 2015 г. показатель заболеваемости ОКИ в Российской Федерации составил 545,89 на 100 тыс. населения, что практически не отличается от показателя 2014 г. При этом на долю ОКИ неустановленной этиологии приходится 63,44% случаев.
Сохраняются выраженные различия в эффективности диагностики ОКИ на различных территориях Российской Федерации, наряду со снижением заболеваемости по отдельным нозологиям, отмечался рост заболеваемости кампилобактериозом - на 30,3%, ротавирусной - на 14%> и норовирусной - на 26,47о инфекциями.
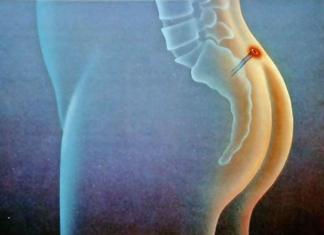
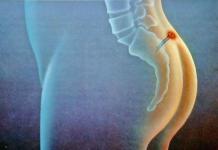
При инфекционной диарее тяжесть состояния больного определяется наличием и выраженностью ряда патологических симптомов. Речь, в частности, идет об общеинфекционном синдроме (лихорадке, интоксикации, вялости), синдроме дегидратации (токсикозе с эксикозом), синдроме метаболического ацидоза, синдроме местных изменений (диарее, рвоте, метеоризме, парезе кишечника). Скорость и тяжесть развития последствий обезвоживания зависит от вида обезвоживания, его выраженности и своевременности лечебных мероприятий, направленных на его устранение.
Причиной частого возникновения дегидратации (эксикоза) у детей принято считать анатомо-физиологические особенности, обусловливающие быстрый срыв адаптационных механизмов и развитие декомпенсации функций органов и систем в условиях инфекционной патологии, сопровождаемых потерей воды и электролитов. Синдром дегидратации у детей со среднетяжелыми и тяжелыми формами острых вирусных гастроэнтеритов обусловлен значительными потерями жидкости со рвотой и патологическим стулом.
Как следствие - ухудшение центральной и периферической гемодинамики, развитие патологических изменений всех видов обмена веществ, накопление в клетках и межклеточном пространстве токсических метаболитов и их вторичное воздействие на органы и ткани больных. Доказано, что основной причиной развития синдрома дегидратации является ротавирусный гастроэнтерит.
Алгоритм терапии ОКИ у детей предполагает целенаправленное воздействие, прежде всего на макроорганизм, обуславливающее коррекцию водно-электролитных расстройств и элиминацию возбудителя. Основополагающей считается патогенетическая терапия: регидратация, диетотерапия, энтеросорбция и использование пробиотиков. При водянистой диарее эксперты Всемирной организации здравоохранения (ВОЗ) признают абсолютно доказанной эффективность только двух терапевтических мероприятий - регидратации и адекватного питания (2006).
Как показал наш опыт (преподавательский и экспертный), к сожалению, именно при проведении регидратационной терапии допускают самое большое количество ошибок. Даже при парентеральном введении жидкости для купирования дегидратации в большинстве историй болезни расчет необходимой жидкости либо отсутствует, либо выполнен некорректно. При проведении оральной регидратации расчет не проводится совсем.
Однако больше всего впечатляет тот факт, что даже при наличии солидного стажа практической работы врачи различных специальностей не понимают, зачем регидратирующую соль растворять в строго определенном объеме жидкости, почему нельзя смешивать глюкозо-солевые и бессолевые растворы. Не секрет, что нередки случаи проведения необоснованной инфузионной терапии, поскольку законные представители ребенка или медицинский персонал не хотят затруднять себя проведением оральной регидратации или не имеют для этого эффективных средств.
Прежде чем приступить к коррекции дефицита жидкости при ОКИ необходимо определить степень дефицита жидкости и объем патологических потерь. Мы попытались осветить различные подходы к оценке степени синдрома дегидратации: традиционный подход российских педиатров-инфекционистов и анестезиологов-реаниматологов и широко вошедшие в повседневную практику критерии ВОЗ и ESPGHAN/ESPID (European Society for Paediatric Gastroenterology, Hepatology, and Nutrition - Европейская ассоциация детских гастроэнтерологов, гепатологов и диетологов/European Society for Paediatric Infectious Diseases - Европейская ассоциация детских инфекционистов) (2008, 2014). Тяжесть синдрома дегидратации оценивается в первую очередь по проценту потери массы тела.
Тяжесть дегидратации в процентах от массы тела ребенка до заболевания
Используя критерии ВОЗ , оценивая степень дегидратации, можно сразу определить дефицит жидкости.
- Нет признаков обезвоживания – < 5 % массы тела, < 50 мл/кг
- Некоторая степень обезвоживания – 5-10 % массы тела, 50-100 мл/кг
- Обезвоживание в тяжелой форме – более 10 % массы тела, более 100 мл/кг
Универсальных лабораторных тестов, способных оценить тяжесть дегидратации, не существует. Целью определения тяжести дегидратации является объем дефицита (в мл) для последующего восполнения. Оценка тяжести дегидратации по клиническим данным, естественно, субъективна. Для этих целей ESPGHAN рекомендует использовать клиническую шкалу дегидратации CDS (Clinical Dehydration Scale): 0 баллов - дегидратация отсутствует, от 1 до 4 баллов - легкая дегидратация, 5-8 баллов соответствуют дегидратации средней и тяжелой степени.
Шкала дегидратации Clinical Dehydration Scale (CDS)
- Нормальный
- Жажда, беспокойство, раздражительность
- Вялость, сонливость
Глазные яблоки
- Тургор нормальный
- Слегка запавшие
- Запавшие
Слизистые оболочки
- Влажные
- Липкие, суховатые
- Сухие
- Слезоотделение в норме
- Слезоотделение снижено
- Слезы отсутствуют
Перед началом лечения ребенка с инфекционной диареей необходимо тщательно собрать и проанализировать анамнез заболевания, оценить тяжесть состояния. Особое внимание обращают на частоту, консистенцию, ориентировочный объем фекалий, наличие и кратность рвоты, возможность приема жидкости (объем и состав), частоту и темп диуреза, наличие или отсутствие лихорадки. Обязательно определяют массу тела до начала лечения, далее взвешивают пациента ежедневно. В ходе терапии ведут строгий учет полученной и выделенной жидкости (взвешивание подгузников и памперсов, измерение объема рвотных масс, установка урологического катетера и т. д.).
Комплексный подход к диагностике синдрома дегидратации представлен нашими белорусскими коллегами В.В. Курек и А.Е. Кулагиным (2012), данный подход не сложен в использовании в практическом здравоохранении.
Клиническая оценка дегидратации
Дефицит объема
- Анамнез заболевания, объективный осмотр ребенка
Нарушение осмолярности
- Концентрация натрия в плазме, осмолярность плазмы
Нарушение кислотно-основного состояния
- рН, рСО2, НСО3 капиллярной крови
Уровень калия
- Калий плазмы
Функция почек
- Мочевина и креатинин плазмы, удельный вес мочи (или осмолярность мочи), рН мочи, микроскопия осадка мочи
Синдром дегидратации возникает при потере воды и электролитов, причем их количественная потеря может быть разной. В зависимости от этого различают три вида дегидратации: гипертоническую, гипотоническую и изотоническую. Повышение уровней белка крови, гемоглобина, гематокрита и эритроцитов характерно для всех видов, но при изотонической дегидратации эти показатели иногда могут быть в норме.
Гипертоническая (вододефицитная, внутриклеточная) возникает на фоне потери преимущественно воды, которая вследствие повышения концентрации натрия в плазме перемещается в кровеносное русло. Потери происходят в основном с диареей. В результате возникает внутриклеточное обезвоживание, которое клинически проявляется неутолимой жаждой, афонией, «плачем без слез». Кожа сухая, теплая, большой родничок не западает вследствие увеличения объема ликвора. Лабораторные данные: высокий уровень натрия плазмы > 150 ммоль/л, уменьшенный объем эритроцита и высокое содержание гемоглобина в нем. Осмолярность плазмы и мочи повышены. Потери натрия - 3-7 ммоль/кг.
Гипотоническая (соледефицитная, внеклеточная) возникает в случае преимущественной потери электролитов (натрия, калия), встречается при преобладании рвоты над диареей. Потеря солей приводит к снижению осмолярности плазмы и перемещению жидкости из сосудистого русла в клетки (внутриклеточный отек). При этом виде дегидратации жажда умеренная. Внешние признаки дегидратации выражены слабо: кожа холодная, бледная, влажная, слизистые не столь сухие, большой родничок западает. Характерно снижение уровня натрия плазмы менее 135 ммоль/л, увеличение объема эритроцита и уменьшение концентрации гемоглобина в нем. Осмолярность плазмы и мочи понижены. Потери натрия - 8-10 ммоль/кг.
Изотоническая (нормотоническая) дегидратация считается наиболее распространенной и сопровождается одновременной потерей жидкости и солей. Как правило, содержание натрия плазмы нормальное, хотя уровень его потерь колеблется от 11 до 13 ммоль/кг. Средний объем эритроцита и концентрация гемоглобина, осмолярность плазмы и мочи - в пределах нормы.
Обычно при ОКИ не бывает изолированной вне- или внутриклеточной дегидратации. Наблюдается тотальное обезвоживание, но в большей степени из внеклеточного сектора. Симптомы гипонатриемии заключаются в развитии неврологической симптоматики: от тошноты, головной боли, потери сознания до комы, судорожного статуса и летального исхода. Тяжесть симптомов зависит как от степени гипонатриемии, так и от темпов ее нарастания. Быстрое снижение содержания внутриклеточного натрия осложняется перемещением воды внутрь клетки, что может привести к отеку головного мозга.
Как показывает клинический опыт, в большинстве случаев синдрома эксикоза имеют место пропорциональные потери воды и электролитов. В результате в 80% случаев развивается изотоническая дегидратация, в 15% - гиперосмолярная, в 5%> - гипоосмолярная.
Основной принцип оральной регидратации - дробное и постепенное введение жидкости. На наш взгляд, наиболее удобен расчет возмещаемой жидкости при оральной регидратации, принятый российским медицинским сообществом. Оральная регидратация проводится в два этапа:
- этап I - в первые шесть часов после поступления больного ликвидируют водно-солевой дефицит, возникший до начала лечения. При синдроме дегидратации первой степени количество жидкости для первичной регидратации на этом этапе составляет 40-50 мл/кг массы тела за первые шесть часов, при синдроме дегидратации второй степени - 80-90 мл/кг массы тела за первые шесть часов;
- этап II - весь последующий период проводят поддерживающую терапию с учетом суточной потребности ребенка в жидкости и солях, а также их потерь. Поддерживающую терапию проводят в зависимости от продолжающихся потерь жидкости и солей с рвотой и испражнениями. За каждый последующий шестичасовой отрезок времени ребенок должен выпить столько раствора, сколько он потерял жидкости с испражнениями и рвотными массами за предыдущие шесть часов. Этот этап регидратации продолжают до прекращения диареи. Ориентировочный объем раствора для поддерживающей регидратации - от 80 до 100 мл/кг массы тела в сутки (при массе не более 25 кг).
Необходимое количество жидкости для пероральной регидратации при синдроме дегидратации у детей, мл
| Эксикоз 1 степени | Эксикоз 2 степени | |||
| Масса тела | За 1 час | За 6 часов | За 1 час | За 6 часов |
| 5 | 42 | 250 | 66 | 400 |
| 10 | 83 | 500 | 133 | 800 |
| 15 | 125 | 750 | 200 | 1200 |
| 20 | 167 | 1000 | 266 | 1600 |
| 25 | 208 | 1250 | 333 | 2000 |
Можно воспользоваться расчетом возмещения жидкости, рекомендуемым ВОЗ для стран с развивающейся экономикой. В отсутствие значимой дегидратации реализуется план А: дети младше 24 месяцев - 50-100 мл после каждого эпизода диареи, дети старше 24 месяцев - 100-200 мл после каждого эпизода диареи. При умеренной дегидратации реализуется план В, при тяжелой - план С. Последний в странах с хорошей доступностью медицинской помощи не применяется, поскольку при серьезной дегидратации (второй-третьей степени) должна проводиться инфузионная терапия.
Оральная регидратация - план В
Оральная регидратация - план С
При проведении оральной регидратации используются не только глюкозо-солевые растворы, которые чередуют с приемом бессолевых растворов: рисового отвара, кипяченой воды, чая с небольшим количеством сахара, неконцентрированного изюмного отвара. Самым главным принципом оральной регидратации является дробность введения жидкости, для этого медицинский персонал или родители должны поить ребенка малыми порциями через 8-12 минут.
Эффективность оральной регидратации оценивается по уменьшению объема потерь жидкости, исчезновению клинических признаков обезвоживания, нормализации диуреза, улучшению общего состояния ребенка.
Противопоказаниями для проведения оральной регидратации является инфекционно-токсический шок (септический), гиповолемический шок, дегидратация 2-3-й степени, протекающая с нестабильной гемодинамикой, неукротимая рвота, потеря жидкости с рвотой и диарей, превышающей 1,5 л/ч (у взрослых), олигоанурия как проявление острой почечной недостаточности, сахарный диабет, нарушения всасывания глюкозы.
ВОЗ рекомендует проводить оральную регидратацию с использованием глюкозо-солевых растворов при ОКИ, сопровождающихся водянистой диареей (холера, энтеротоксигенные эшерихиозы), а также при диареях другой этиологии, характеризующихся развитием энтерита, гастроэнтерита и гастроэнтероколита. При использовании глюкозо-солевых растворов происходит замещение утрачиваемых солей. Глюкоза не только позволяет восполнить энергетические потери макроорганизма, но и обеспечивает транспорт натрия и калия через мембрану клеток слизистой оболочки тонкой кишки, что приводит к более быстрому восстановлению водно-солевого гомеостаза.
Регидратационная терапия, история становления которой началась в 1950-х гг., широко внедрена в повседневную практику. До начала 1990-х гг. использовались растворы с нормальной осмолярностью (290-315 мОсм/л), с начала 2000-х гг. стали применять растворы со сниженной осмолярностью (220-260 мОсм/л).
Согласно результатам многочисленных исследований, осмолярность улучшенных регидратационных растворов не должна превышать 245 мОсм/л (рекомендовано ВОЗ в 2004 г.). К растворам предъявляются следующие требования: соотношение «натрий/глюкоза» - 60/90 ммоль/л, осмолярность - 200-240 мОсм/л, энергетическая ценность - до 100 ккал. Только при использовании растворов с пониженной осмолярностью улучшается всасывание в кишечнике воды и электролитов, сокращаются объем и длительность диареи, реже возникает потребность в проведении инфузионной терапии. Причем эти наблюдения относятся даже к холере.
В нашей стране уже более десяти лет используются растворы со сниженной осмолярностью (ОРС 200, Хумана электролит). В работах Л.Н. Мазанковой показано, что на фоне применения раствора со сниженной осмолярностью сокращаются длительность и выраженность диареи, рвоты и лихорадки.
На отечественном фармацевтическом рынке представлен регидратирующий раствор, в состав которого, кроме солей, входят мальтодекстрин, диоксид кремния и Lactobacillus rhamnosus GG - 1 x 109 КОЕ. Диоксид кремния оказывает сорбирующее, регенерирующее действие в просвете кишечника, то есть обеспечивает дополнительный детоксицирующий эффект. Мальтодекстрин обеспечивает более низкую осмолярность раствора и обладает бифидогенным действием.
Добавление в регидратирующий раствор Lactobacillus rhamnosus GG гарантирует получение высокоэффективного и безопасного пробиотического штамма, рекомендованного (с высоким уровнем доказательности) ESPGHAN для лечения инфекционных диарей у детей. Как известно, Lactobacillus rhamnosus GG обладает устойчивостью к действию кислой среды желудка, высокой адгезивной способностью к эпителиальным клетка, выраженной антагонистической активностью в отношении патогенных и условно патогенных микроорганизмов, влияет на продукцию противовоспалительных цитокинов и характеризуется высоким профилем безопасности.
Результаты исследований, проведенных В.Ф. Учайкиным, подтвердили высокую эффективность регидратирующего раствора при инфекционных диареях, как водянистых, так и осмотических. Его использование приводит к более быстрому купированию симптомов дегидратации, интоксикации, абдоминальных болей, явлений метеоризма и нормализации характера стула. Кроме того, Lactobacillus rhamnosus GG способствует нормализации количества в кишечнике лактобактерий и энтерококков, но не влияет на уровень анаэробов и кишечной палочки.
Наш опыт использования регидратирующего раствора у 40 детей с вирусными гастроэнтеритом показал более быстрое купирование диареи, а самое главное - высокую приверженность терапии. 90% пациентов, получавших данный препарат, использовали весь назначенный на сутки раствор. Среди пациентов (30 человек), получавших раствор с нормальной осмолярностью, только 40% могли выпить весь рассчитанный объем глюкозо-солевого раствора. К преимуществам данного раствора относятся хорошие органолептические свойства.
Таким образом, оральная регидратация является основным методом лечения инфекционных диарей у детей. Важно правильно оценивать степень дегидратации и использовать регидратирующие растворы со сниженной осмолярностью. При лечении гастроэнтеритов у детей энтеральная регидратация эффективна в большинстве случаев. Эффективность такой терапии по некоторым показателям превосходит парентеральную регидратационную терапию.
М.К. Бехтерева, И.В. Раздьяконова, С.Г. Семенова, В.В. Иванова
АННОТАЦИЯ
В исследовании был проведен ретроспективный анализ случаев диарейных заболеваний у детей до 5 лет с дегидратацией. Все случаи были оценены по трем принятым шкалам оценки тяжести дегидратации (Шкала ВОЗ, Шкала CDC, Клиническая шкала дегидратации), вычислены эпидемиологические показатели (чувствительность, специфичность) каждого фактора, участвующего в развитии дегидратации при диарейных заболеваниях у детей: возраст, наличие дистрофии и степень ее выраженности, наличие пареза кишечника, уровень калия, натрия, мочевины в сыворотке крови, уровень натрия в моче, паттерны электрокардиограммы, сопровождающие дисэлектролитемию. Анализ анамнестических и клинических показателей выявили умеренные чувствительность и специфичность данных факторов: возраст до 6 месяцев (чувствительность – 62 %, специфичность – 53 %), возраст 6–12 месяцев (чувствительность – 59 %, специфичность – 44 %), дистрофия 2 степени (чувствительность – 55 %, специфичность – 33 %), дистрофия 3 степени (чувствительность – 74 %, специфичность – 69 %), гипокалиемия с парезом кишечника (чувствительность – 68 %, специфичность – 57 %), гипонатриемия с концентрацией натрия в сыворотке крови более 140 ммоль/л гипонатриемия в моче менее 10 ммоль/л (чувствительность – 60 %, специфичность – 51 %), скорость нарастания гипонатриемии менее чем 12 часов (чувствительность – 84 %, специфичность – 64 %), содержание мочевины в сыворотке крови более 9 ммоль/л (чувствительность – 52 %, специфичность – 40 %), гиперкалиемия 6,0-6,5 ммоль/л (чувствительность - 54 %, специфичность – 42 %) , высокий зубец Т (чувствительность – 55 %, специфичность – 44 %), широкий QRS комплекс (чувствительность – 77 %, специфичность – 63 %), наслоение сегмента S-T на зубец Т (чувствительность – 59 %, специфичность – 43 %).
Оценка прогностической ценности шкал по данным верифицированных ретроспективных данных показала, что они не являются достаточно точным диагностическим инструментом прогнозирования исхода диарейных заболеваний у детей. Работа демонстрирует, что проблема требует дальнейших исследований по разработке точного диагностического инструмента.
ABSTRACT
In research a retrospective analysis of cases of diarrhoeal diseases in children under 5 years with dehydration is carried out. All cases are evaluated according to three accepted scales of the severity assess of dehydration (ECOG Scale, CDC Scale, Clinical scale of dehydration), epidemiological parameters (sensitivity, specificity) of each factor involved in the development of dehydration during diarrheal diseases in children are calculated: age, the presence of degeneration and the degree of its severity, presence of intestinal paresis, level of potassium, sodium, urea in blood serum, level of sodium in the urine, electrocardiogram patterns accompanying dyselectrolytemia.
The analysis of anamnestic and clinical parameters shows moderate sensitivity and specificity of these factors: the age of 6 months (sensitivity - 62%, specificity - 53%), age 6-12 months (sensitivity - 59%, specificity - 44%), 2-degree degeneration (sensitivity - 55%, specificity - 33%), 3-degree degeneration (sensitivity - 74%, specificity - 69%), hypokalemia with intestinal distention (sensitivity - 68%, specificity - 57%), hyponatremia with sodium concentration in the blood serum of 140 mmol / l in urine hyponatremia less than 10 mmol / l (sensitivity - 60%, specificity - 51%), hyponatremia slew rate of less than 12 hours (sensitivity - 84%, specificity - 64%), serum urea content of more than 9 mmol / l (sensitivity - 52%, specificity - 40%), 6.0-6.5 mmol/l of hyperkalemia / l (sensitivity - 54%, specificity - 42%), tall T wave (sensitivity - 55%, specificity - 44%), a wide QRS complex (sensitivity - 77%, specificity - 63%), the layering of the S-T segment on the T wave (sensitivity - 59%, specificity - 43%).
Evaluation of prognostic value scales according to the verified historical data has shown that they are not sufficiently accurate diagnostic tool for predicting the outcome of diarrheal diseases in children. The work demonstrates that the issue requires further research on the development of an accurate diagnostic tool.
Актуальность
Диарея является второй по значимости причиной смерти детей в возрасте до пяти лет: ежегодно в мире от нее умирает 760 тысяч детей. Причиной смерти является гиповолемия, обусловленная тяжелой дегидратацией. Наибольшему риску заболевания диареей с угрозой для жизни подвергаются дети, страдающие от недостаточности питания или имеющие ослабленный иммунитет .
Каждый год во всем мире регистрируется 1,7 млрд диарейных эпизодов у детей, что приводит к 124 млн амбулаторных посещений и 9 млн госпитализаций .
В 2010 году в мире было зарегистрировано 1,731 млрд эпизодов диареи у детей, из которых в 36 млн случаях наблюдалось прогрессирование симптомов диареи вплоть до тяжелого течения. В свою очередь, исследования, проведенные в 2011 году, выявили 700 000 смертельных случаев, вызванных диареей.
Поскольку тяжесть диареи у детей колеблется в широких пределах, точная оценка состояния обезвоживания имеет решающее значение для предотвращения смертности и заболеваемости. Дети с тяжелой дегидратацией требуют немедленных внутривенных вливаний, чтобы предотвратить гемодинамические нарушения, ишемию органов и смерть .
Точная оценка состояния дегидратации может также повысить экономическую эффективность лечения диареи.
Большой мета-анализ показал, что ни один клинический признак, симптом или лабораторный тест не продемонстрировал адекватную чувствительность, специфичность и надежность для обнаружения обезвоживания у детей .
Всемирная организация здравоохранения (ВОЗ) в руководящих принципах Интегрированного ведения болезней детского возраста (ИВБДВ) рекомендует использовать сочетание клинических признаков для распознавания и классификации детей с дегидратацией .
Однако алгоритм, разработанный ВОЗ, в основном, базируется на мнении экспертов, а недавние исследования не нашли его достаточным, чтобы считать точным для прогнозирования течения дегидратации у детей .
В целом только 2 % случаев диареи у детей будет прогрессировать до тяжелой степени .
Развитие неблагоприятного течения и исхода при диарейных заболеваниях, вероятно, зависит от этиологического фактора, отличающегося патогенностью. Однако, вероятно, существуют эндогенные факторы, обусловленные особенностями фоновых состояний. Выявление дополнительных факторов и использование их в качестве диагностических критериев может улучшить качество прогнозирования и снизить вероятность развития тяжелой дегидратации, поможет в выборе мероприятий неотложной медицинской помощи.
Цель: определить диагностическую ценность факторов, участвующих в развитии дегидратации, на течение и его исход при диарейных заболеваний у детей.
Пациенты и методы
Для того чтобы преодолеть ограниченную точность отдельных клинических признаков, Всемирная организация здравоохранения (ВОЗ) рекомендует для выявления тяжелого обезвоживания у детей с диареей использовать комбинацию из четырех различных клинических признаков, которая считается стандартом лечения во многих странах .
В то же время Центр США по контролю и профилактике заболеваний (CDC) рекомендует использовать более сложную шкалу из 12 признаков и симптомов для оценки состояния обезвоживания у детей с диареей .
Также в Канаде разработана клиническая шкала дегидратации (Clinical Dehydration Scale) .
Несколько исследований, проведенных в городских больницах в странах с высоким и средним уровнем дохода, обнаружили, что клинические шкалы, состоящие из различных комбинаций признаков и симптомов, могут достаточно точно прогнозировать тяжесть обезвоживания у детей с диареей .
Однако точность этих клинических шкал не была подтверждена в странах с ограниченными ресурсами, где фиксируется высокая заболеваемость и смертность от диарейных заболеваний, и поэтому точность клинических шкал, полученных в более богатых странах, ставится под сомнение .
Нами было проведено исследование случай-контроль на ретроспективном материале, состоящим из 98 историй болезней детей, умерших при лечении диарейного заболевания, и 102 историй болезней с благоприятным исходом.
Исследуемые документы выбирались в трех городских детских инфекционных больницах города Ташкента за 2011–2015 гг. в отделениях кишечных инфекций и интенсивной терапии. В историях болезнях были выставлены клинические и заключительные диагнозы вирусных (норовирусы – 22 %, ротовирусы – 18 %, кишечные штаммы аденовируса 7 %, другие – 5 %), бактериальных (преимущественно токсигенные штаммы кишечной палочки – 18 %, шигелы – 12 %, сальмонеллы – 7 %, иерсинии – 4 %, другие 3 %), протозойных (лямблии – 2 %, амебы – 2 %) инфекций. Все имели описание дегидратации разной степени тяжести (1 степени – 14 %, 2 степени – 18 %), 68 % имели описание гиповолемического шока, из них 48 % – с критериями тяжелой дистрофии. Неблагоприятным исходом закончилось 0,5 % детей с дегидратацией 1 степени, 2 % с дегидратацией 2 степени, с гиповолемическим шоком – 82 % (из них 65 % – с тяжелой дистрофией).
Критериями включения были наличие признаков диарейного заболевания, дегидратации, выполнение рекомендаций ВОЗ (планы А, Б, В, противошоковые мероприятия при шоке с наличием и без тяжелой дистрофии, отраженные в медицинских стандартах и приказах Министерства здравоохранения Республики Узбекистан).
Критериями исключения были заболевания с высокой долей смертности, хирургические и эндокринологические случаи.
Все случаи были оценены по трем шкалам оценки тяжести дегидратации (таблица 1):
Таблица 1.
Шкалы оценки дегидратации у детей
Шкала ВОЗ (WHO Severe Scale) |
|||
Характеристика | 0 балл | 1 балл |
|
Уровень сознания | В сознании или беспокойный | Сонливый или без сознания |
|
Запавшие |
|||
Пьет нормально или с жадностью | Не может пить или пьет плохо |
||
Кожная складка | Кожная складка расправляется быстро или медленно | Кожная складка расправляется очень медленно |
|
Общий балл |
|||
Шкала CDC |
|||
0 балл | 1 балл | 2 балл |
|
Уровень сознания | В сознании | Беспокойный или возбужденный | Сонливый или без сознания |
Пьет нормально | Жажда или хочет пить | Не может пить |
|
Увеличено | Тахикардия |
||
Качество пульса | Слабый или не ощущается |
||
Ускорено | Глубокое |
||
Слегка запавшие | Выраженно запавшие |
||
Слезы есть | Уменьшено выделение слез | ||
Рот и язык | Увлажненный | Очень сухой |
|
Кожная складка | Расправляется быстро | Расправляется < 2 секунды | Расправляется > 2 секунды |
Капиллярный тест | Удлиненный | Минимальный |
|
Конечности | Холодные | Холодная, мраморная или синюшная |
|
Мочеотделение | Минимальное |
||
Общий балл |
|||
Клиническая шкала дегидратации (Clinical Dehydration Scale) |
|||
0 балл | 1 балл | 2 балл |
|
Общий вид | Жажда. Беспокойный и раздражительный | Сонливый или без сознания |
|
Слегка запавшие | Очень запавшие |
||
Слизистые оболочки | Увлажненные | Очень сухие |
|
Слезы есть | Уменьшено слезотечение | ||
Было анализированы все анамнестические и клинические показатели в обеих группах, приведенные в историях болезней. Были выбраны данные, доступные для их анализа: возраст, степень дистрофии, выявленная по дефициту веса и толщины кожно-жировой складки на животе (менее 1 см для умеренной дистрофии и менее 7 мм для тяжелой дистрофии), признаки пареза кишечника (рвота, отсутствие дефекации более суток, вздутый живот, ослабленные перильстальтические шумы или их отсутствие), уровень калия, натрия в сыворотке крови, скорость их нарастания, паттерны электрокардиограммы, отражающие дисэлектролитемию (ширина QRS комплекс, указывающая на низкий уровень магния или калия, высота зубца Т по отношению к зубцу R и его форма, наслоение сегмента S-T на зубец Т, связанная с содержанием в сыворотке калия).
Были вычислены чувствительность, специфичность, отношение шансов каждого фактора.
Результаты исследования
Были выявлены факторы с доверительным интервалом 95 %, достаточной репрезентативностью группы (20 и более случаев) и отношением шансов более единицы (повышенный риск) для следующих факторов:
- возраст до 6 месяцев (чувствительность – 62 %, специфичность – 53 %),
- возраст 6–12 месяцев (чувствительность – 59 %, специфичность – 44 %),
- дистрофия 2 степени (чувствительность – 55 %, специфичность – 33 %),
- дистрофия 3 степени (чувствительность – 74 %, специфичность – 69 %),
- гипокалиемия с парезом кишечника (чувствительность – 68 %, специфичность – 57 %) гипонатриемия с концентрацией натрия в сыворотке крови более 140 ммоль/л гипонатриемия в моче менее 10 ммоль/л (чувствительность – 60 %, специфичность – 51 %),
- скорость нарастания гипонатриемии менее чем 12 часов (чувствительность – 84 %, специфичность – 64 %),
- содержание мочевины в сыворотке крови более 9 ммоль/л (чувствительность – 52 %, специфичность – 40 %),
- гиперкалиемия 6,0-6,5 ммоль/л (чувствительность – 54 %, специфичность – 42 %),
- высокий зубец Т (чувствительность – 55 %, специфичность – 44 %),
- широкий QRS комплекс (чувствительность – 77 %, специфичность – 63 %),
- наслоение сегмента S-T на зубец Т (чувствительность – 59 %, специфичность – 43 %)
Оценка прогностической ценности шкал по данным верифицированных ретроспективных данных показала, что они мало различаются с данными, полученными Adam C. et al. , и не являются достаточно точным диагностическим инструментом (Таблица 2).
Таблица 2.
Доля позитивных случаев, вошедших в 95% доверительный интервал
Выводы
Выявленные факторы достоверно прогнозируют неблагоприятный исход течения диарейного заболевания у детей раннего возраста, но подтверждают вывод Steiner M et al, что ни один клинический признак, симптом или лабораторный тест не демонстрирует адекватную чувствительность, специфичность и надежность для обнаружения дегидратации и прогнозирования его тяжелого течения у детей .
Вероятно, это связано с существованием различных причин и механизмов формирования тяжелой дегидратации.
Это требует дальнейших исследований по разработке точного диагностического инструмента для решения этой проблемы.
Список литературы:
1. Диарея. Информационный бюллетень ВОЗ № N°330 Апрель 2013 г. / [Электронный ресурс]. – Режим досту-па: http://www.who.int/mediacentre/factsheets/fs330/ru/ (дата обращения: 27.07.2016).
3. Farthing M, Salam MA, Lindberg G, Dite P, Khalif I, Salazar-Lindo E, et al. WGO . Acute diarrhea in adults and children: a global perspective. J Clin Gastroenterol. 2013;47(1): 12–20. . 10.1097/MCG.0b013e31826df662
4. Fischer Walker CL, Perin J, Aryee MJ, Boschi-Pinto C, Black RE.. Diarrhea incidence in low- and middle-income countries in 1990 and 2010: a systematic review. BMC Public Health. 2012;12(1): 220. . 10.1186/1471-2458-12-220
6. Jauregui J, Nelson D, Choo E, Stearns B, Levine AC, Liebmann O, et al. External validation and comparison of three pediatric clinical dehydration scales. PLoS One. 2014;9(5): e95739. . 10.1371/journal.pone.0095739).
8. Levine AC, Munyaneza RM, Glavis-Bloom J, Redditt V, Cockrell HC, Kalimba B, et al. Prediction of severe dis-ease in children with diarrhea in a resource-limited setting. PLoS One. 2013;8(12): e82386. 10.1371/journal.pone.0082386
11. Parashar UD, Hummelman EG, Bresee JS, Miller MA, Glass RI.. Global illness and deaths caused by rotavirus dis-ease in children. Emerg Infect Dis. 2003;9(5): 565–572. 10.3201/eid0905.020562}