Залевский Тимур Романович, 2 года 6 месяцев (30.08.2014 г.рожд.) Принимаемые АЭП: не получает. Видео-ЭЭГ-мониторинг проводился в течение 4 часов в состоянии активного и пассивного бодрствования, во время дневного сна и после пробуждения, с проведением функциональных проб. Параметры записи: Исследование проводилось с использованием международной схемы наложения электродов «10-20». Дополнительные электроды: ЭКГ. Система видео-ЭЭГ-мониторирования – Nihon Kohden, Japan. ЭЭГ в состоянии бодрствования. Запись бодрствования проводилась преимущественно при открытых глазах, ребенок двигательно активен, отмечается большое количество двигательных и миографических артефактов. Основная активность оценивалась при пристальном взгляде на предмет и в момент закрывания глаз – в затылочных отделах полушарий фрагментарно регистрируется ритмичная активность частотой 6-7 Гц, амплитудой до 70 мкВ – эквивалент альфа ритма. В состоянии активного бодрствования в лобно-центральных отделах регистрируется аркообразный сенсомоторный ритм, частотой 8 Гц, амплитудой до 50 мкВ. Бета активность представлена максимально в лобно-височных отделах полушарий, с переменной латерализацией, частотой 14-24 Гц, амплитудой до 20 мкВ, нередко трудно дифференцируема на фоне миографических артефактов. Биокципито-темпорально, периодически с переменной латерализацией, регистрируются нерегулярные полифазные потенциалы тета-дельта диапазона – окципитальные дельта волны детей. Медленные формы активности представлены широко, диффузно в виде низкоамплитудных волн, преимущественно тета-, реже дельта- диапазона, незначительно В бодрствовании крайне низким индексом регистрируется региональная эпилептиформная активность в левой и правой затылочных областях независимо в виде единичных пиков и острых волн, амплитудой до 80 мкВ. Функциональные пробы. Проба с открыванием и закрыванием глаз не проводилась. Проба с ритмической фотостимуляцией проводилась частотами 3, 6, 9, 12, 15, 18, 21, 24, 27, 30, 33 Гц фотопароксизмальные формы активности не зарегистрированы. Четкая реакция усвоения ритма не выявлялась. Проба с гипервентиляцией не проводилась. Запись во время сна. По мере засыпания отмечалось снижение индекса основной активности, вплоть до редукции и нарастание диффузной медленноволновой активности тета-диапазона. На этом фоне регистрируются билатерально-синхронные вспышки медленных волн дельта-диапазона, амплитудой до 220 мкВ, с амплитудным преобладанием бифронтально, периодически со смещением в центральные области – явление гипнагогической гиперсинхронизации (физиологический феномен стадии дремы). В первую и вторую стадии сна регистрируется появление вертексных потенциалов в центральных отделах полушарий, амплитудой до 170 мкВ. Также зарегистрированы заостренные потенциалы, схожие с комплексами острая-медленная волна в лобно-центральных отделах с амплитудным преобладанием по вертексным отведениям. С учетом морфологических и локализационных особенностей, данные паттерны можно рассматривать в рамках атипичных физиологических транзитов сна – вертексных потенциалов. Непосредственно 2-я стадия представлена «сонными веретенами» - быстрыми ритмичными формами активности в лобно-центральных отделах полушарий, частотой 12-14 Гц, амплитудой до 80 мкВ и К-комплексами в виде диффузных медленных волн или полифазных потенциалов, максимальной амплитудой в центральных отделах полушарий, до 260 мкВ. В ходе записи сна периодически регистрируются волны аркообразной заостренной формы частотой 6-7 Гц, 14 Гц в височных отделах полушарий, нередко с тенденцией к диффузному распространению - физиологические неэпилептические транзиты сна «6-14 Гц». Дельта сон сопровождался на части эпох записи нарастанием представленности диффузной высокоамплитудной медленноволновой активности сначала до 50%, а затем до 80% записи с одновременной постепенной редукцией физиологических паттернов сна. По ходу сна выявляется периодическое региональное тета-дельта замедление в правой височной области, а также левой затылочно-височной области независимо. На этом фоне в структуре регионального замедления невысоким индексом регистрируется региональная эпилептиформная активность в левой и правой затылочных областях независимо, реже – в правой задневисочной области (Т6) с распространением на височные отделы ипсилатерального полушария, а также биокципитально в виде одиночных и сгруппированных пиков и острых волн, комплексов пик-медленная волна, острая-медленная волна, амплитудой до 160 мкВ. Клинические события в ходе исследования не зарегистрированы. Заключение: Основной ритм соответствует возрасту. Сон модулирован на стадии. Физиологические паттерны сна визуализируются. По ходу сна выявлено периодическое региональное тета-дельта замедление в правой височной области, а также левой затылочно-височной области независимо. В бодрствовании крайне низким индексом зарегистрирована региональная эпилептиформная активность в левой и правой затылочных областях независимо в виде единичных пиков и острых волн. Во сне в структуре регионального замедления невысоким индексом зарегистрирована региональная эпилептиформная активность в левой и правой затылочных областях независимо, реже – в правой задневисочной области (Т6) с распространением на височные отделы ипсилатерального полушария, а также биокципитально в виде одиночных и сгруппированных пиков и острых волн, комплексов пик-медленная волна, острая-медленная волна. Эпилептических приступов не зарегистрировано. Беспокоит задержка развития речи (отдельные слова по картинкам, в быту не использует, речь тихая, в нос), обращённую речь понимает, выполняет простые инструкции, по мнению дефектолога есть элементы аутизации. Слух, зрение - норма. Беременность и раннее развитие по возрасту. Живем в Ярославской области, подскажите есть ли необходимость, по заключению ЭЭГ очной консультации.
В статье представлена группа пациентов с фокальной эпилепсией, ассоциированной с ДЭПД, у детей с перинатальным органическим поражением головного мозга, которая по своим клинико-электро-нейровизуализационным характеристикам занимает особое «промежуточное» положение между идиопатической и симптоматической эпилепсией. Под нашим наблюдением находилось 35 пациентов в возрасте от 2 до 20 лет. На основании полученных результатов предложены диагностические критерии синдрома. Для заболевания характерно: преобладание пациентов мужского пола; дебют эпилептических приступов в возрасте до 11 лет с максимумом в первые 6 лет (82,9%) с двумя пиками: в первые 2 года жизни и в возрасте от 4 до 6 лет; нередко дебют с инфантильных спазмов; преобладание фокальных гемиклонических приступов, фокальных затылочных приступов и ВГСП. Возможно сочетание фокальных и псевдогенерализованных приступов (эпилептические спазмы, негативный миоклонус, атипичные абсансы). Характерна относительно невысокая частота фокальных и вторично-генерализованных приступов, приуроченных ко сну (возникновение при пробуждении и засыпании). Неврологический дефицит выявляется у большинства пациентов, включая двигательные и когнитивные нарушения; часто встречается ДЦП. Характерно выявление на ЭЭГ паттерна ДЭПД. Во всех случаях констатируются признаки перинатального поражения головного мозга, преимущественно, гипоксически-ишемического генеза. Ремиссия приступов достигается во всех случаях; позже блокируется эпилептиформная активность на ЭЭГ. Неврологические (двигательные и когнитивные) нарушения, как правило, остаются неизменными.
Согласно современным представлениям, фокальные эпилептические приступы возникают вследствие локальных разрядов в нейрональных сетях, ограниченных одной гемисферой, с большим или меньшим распространением (Engel J.Jr., 2001, 2006). Фокальные (локализационно-обусловленные) эпилепсии традиционно подразделяются на симптоматические, криптогенные (синоним — вероятно симптоматические) и идиопатические формы . Под симптоматическими подразумеваются формы эпилепсии с известным этиологическим фактором и верифицированными структурными изменениями в мозге, являющимися причиной эпилепсии. Как видно из названия, симптоматическая эпилепсия представляет собой проявление другого заболевания нервной системы: опухоли, дисгенезии мозга, метаболические энцефалопатии, последствие гипоксически-ишемического, геморрагического поражения головного мозга и др. . Для этих форм эпилепсии характерны неврологические нарушения, снижение интеллекта, резистентность к антиэпилептической терапии (АЭП). Вероятно симптоматическими (синоним криптогенные, от греческого criptos — скрытый) формами эпилепсии называют синдромы с неуточненной, неясной этиологией. Подразумевается, что криптогенные формы являются симптоматическими, однако на современном этапе при применении методов нейровизуализации не удается выявить структурные нарушения в головном мозге [26]. При идиопатических фокальных формах отсутствуют заболевания, которые могут быть причиной эпилепсии. В основе идиопатических эпилепсий лежит наследственная предрасположенность к нарушениям созревания мозга или генетически детерминированные мембрано- и каналопатии . При идиопатических фокальных формах эпилепсии (ИФЭ) у пациентов неврологический дефицит и нарушение интеллекта не выявляются, а при проведении нейровизуализации отсутствуют признаки структурного поражения головного мозга. Пожалуй, важнейшая черта ИФЭ — абсолютно благоприятный прогноз заболевания со спонтанным прекращением приступов при достижении пациентами пубертатного периода . Идиопатические фокальные эпилепсии относятся к «доброкачественным эпилепсиям». Многие авторы не приемлют термин «доброкачественный» для характеристики такого заболевания как эпилепсия. Однако общепринято, что к доброкачественным эпилепсиям относятся формы, удовлетворяющие двум основным критериям: обязательное купирование приступов (медикаментозное или спонтанное) и отсутствие у пациентов интеллектуально-мнестических нарушений, даже при длительном течении заболевания .
Для идиопатических фокальных форм эпилепсии характерной особенностью является появление на ЭЭГ «доброкачественных эпилептиформных паттернов детства » — ДЭПД, специфических графоэлементов, состоящих из пятиточечного электрического диполя .
Характерными особенностями ДЭПД на ЭЭГ являются (Мухин К.Ю., 2007):
- Наличие пятиточечного электрического диполя, состоящего из острой и медленной волны.
- Максимум «позитивности» диполя в лобных отведениях, а «негативности» в центрально-височных отведениях, что наиболее характерно для роландической эпилепсии.
- Морфология комплексов напоминает зубцы QRS на ЭКГ.
- Региональный, мультирегиональный, латерализованный или диффузный характер активности.
- Нестойкость эпилептиформной активности с возможным перемещением (шифт) при последующих записях ЭЭГ.
- Активация в период I — II стадий фазы медленного сна.
- Отсутствие четкой корреляции с наличием эпилепсии и с клиникой эпилепсии.
ДЭПД легко узнаваемы на ЭЭГ благодаря своей уникальной морфологической характеристике: высокоамплитудный пятиточечный электрический диполь. При этом мы подчеркиваем важность именно морфологических характеристик данного ЭЭГ-паттерна, а не локализации . Ранее нами была представлена классификация «ДЭПД— ассоциированных состояний» . Показано, что ДЭПД — неспецифические эпилептиформные нарушения, возникающие в детском возрасте, которые могут наблюдаться при эпилепсии, заболеваниях, не связанных с эпилепсией, и у неврологически здоровых детей .
За последние годы в клинической практике мы наблюдали особую группу пациентов детского возраста с фокальной эпилепсией, которая по своим клинико-электро- нейровизуализационным характеристикам занимает особое «промежуточное» положение между идиопатической и симптоматической. Речь идет о фокальной эпилепсии, ассоциированной с ДЭПД, у детей с перинатальным органическим поражением головного мозга. Эта группа пациентов имеет четко очерченные клинические, электроэнцефалографические и нейровизуализационные критерии, ответ на терапию АЭП и прогноз.
Цель настоящего исследования: изучение клинических, электроэнцефалографических, нейровизуализационных характеристик, особенностей течения и прогноза фокальной эпилепсии, ассоциированной с ДЭПД у детей с перинатальным поражением головного мозга; установление диагностических критериев заболевания и определение оптимальных методов терапевтической коррекции.
ПАЦИЕНТЫ И МЕТОДЫ
Под нашим наблюдением находилось 35 пациентов, из них 23 мужского и 12 женского пола. Возраст пациентов на момент публикации варьировал от 2 до 20 лет (в среднем, 10,7 лет). Подавляющее большинство пациентов (94,3% случаев) было детского возраста: от 2 до 18 лет. Период наблюдения составил от 1 года 8 мес. до 14 лет 3 мес. (в среднем, 7 лет 1 мес.).
Критерии включения в группу:
— наличие у пациентов фокальной эпилепсии;
— анамнестические, клинические и нейровизуализационные признаки поражения головного мозга перинатального генеза;
— регистрация региональной/мультирегиональной эпилептиформной активности, по морфологии соответствующей «доброкачественным эпилептиформным паттернам детства» на ЭЭГ.
Критерии исключения из группы:
— прогрессирование неврологической симптоматики;
— верифицированные наследственные заболевания;
— структурные нарушенияпри нейровизуализации, приобретенные в постнатальном периоде (последствие перенесенных черепно-мозговых травм, нейроинфекций и пр.).
Все пациенты были обследованы клинически неврологом, нейропсихологом; проведено рутинное ЭЭГ исследование, а также продолженный видео-ЭЭГ мониторинг с включением сна (аппарат электроэнцефалограф-анализатор ЭЭГА-21/26 «ЭНЦЕФАЛАН-131-03», модификация 11, Медиком МТД; видео-ЭЭГ мониторинг «Нейроскоп 6.1.508», Биола). Всем больным было проведено МРТ исследование (магнитно-резонансная система Sigma Infinity GE с напряжением магнитного поля 1,5 Тесла). Для контроля антиэпилептической терапии в динамике исследовалось содержание АЭП в крови методом газо-жидкостной хроматографии; выполнялись общий и биохимический анализы крови (лаборатория Invitro).
РЕЗУЛЬТАТЫ
Среди обследованных нами больных отмечалось значительное преобладание в группе пациентов мужского пола (65,7 % случаев); соотношение мужчин и женщин составило 1,92:1.
Дебют приступов . Дебют приступов в нашей группе отмечался в широком возрастном диапазоне. Самое раннее возникновение приступов наблюдалось у пациента на 3 сутки жизни, наиболее поздний возраст начала эпилепсии — 11 лет. После 11 лет приступы не дебютировали.
Наиболее часто эпилептические приступы возникали у пациентов на первом году жизни — в 28,6% случаев. В более старшем возрасте дебют эпилептических приступов отмечался: на 2-ом и 4-ом годах жизни — по 11,4% случаев, на 1-ом и 5-ом годах — по 8,6% случаев, в возрасте 6, 7, 8 и 9 лет соответственно вероятность возникновения приступов составила по 5,7%. Реже всего дебют приступов отмечался в возрасте 3, 10 и 11 лет — по 2,9% соответственно (по 1 пациенту) (Рис. 1).
Анализируя возрастные интервалы дебюта в нашей группе пациентов, можно отметить значительное преобладание частоты возникновения приступов в период первых 6 лет жизни — 82,9% случаев с двумя пиками. Чаще всего приступы дебютировали в течение первых двух лет жизни. В этом интервале дебют отмечался в 37,1% случаев. Второй пик наблюдается в интервале от 4 до 6 лет — в 20%.
По мере взросления пациентов отмечается постепенное уменьшение вероятности возникновения первого приступа от 48,6% в первые 3 года жизни до 11,4% в возрастном интервале от 9 до 11 лет.
Приступы в дебюте эпилепсии . В дебюте эпилепсии в нашей группе пациентов преобладали фокальные приступы — 71,4%. Фокальные моторные приступы отмечены в 51,4% случаев, вторично-генерализованные судорожные — 14,3%. Другие типы фокальных приступов отмечались значительно реже: фокальные гипомоторные в 1 случае и негативный миоклонус — также в 1 случае.
Эпилептические спазмы в дебюте эпилепсии наблюдались у 17,1% больных; преобладали серийные тонические асимметричные приступы, нередко в сочетании с короткими фокальными версивными приступами. В 1 случае были выявлены миоклонические спазмы. Во всех случаях дебют эпилептических спазмов отмечался у детей в первый год жизни.
В 14,3% случаев эпилепсия дебютировала с появления фебрильных приступов: в 3 случаях — типичных, и в 2 — атипичных. Генерализованные судорожные приступы наблюдались лишь у 8,6% пациентов в дебюте заболевания; миоклонические — в 1случае.
Эпилептические приступы в развернутой стадии заболевания . Проводя анализ встречаемости эпилептических приступов в нашей группе, можно отметить значительное преобладание в клинической картине фокальных и вторично-генерализованных судорожных приступов. Среди фокальных приступов наиболее часто регистрировались фокальные клонические приступы, характерные по кинематике для роландической эпилепсии: гемифациальные, фацио-брахиальные, гемиклонические — 34,3% случаев. В 28,6% случаев были выявлены фокальные приступы, которые по клиническим особенностям и электроэнцефалографическим характеристикам можно отнести к фокальным затылочным. В этой группе преобладали приступы простых зрительных галлюцинаций, с вегетативными феноменами (головная боль, тошнота, рвота), версивные и пароксизмы обмяканий, часто с последующим переходом во вторично-генерализованный судорожный приступ. Фокальные версивные тонические приступы отмечены у 11,4% пациентов. Вторично-генерализованные судорожные приступы возникали в 40% случаев, в том числе, в большинстве случаев с фокальным началом. Псевдогенерализованные приступы наблюдались у 31,4% больных, из них чаще других — эпилептические спазмы — 20,0%; в единичных случаях встречались атипичные абсансы и атонические приступы. Фокальные аутомоторные приступы выявлены лишь в 2 случаях.
В 45,7% случаев у пациентов выявлялся только один тип приступов и также у 45,7% — сочетание двух типов. У пациентов, у которых наблюдался 1 тип приступов за весь период заболевания, преобладали фокальные моторные (в 17,1% случаев), вторично-генерализованные судорожные приступы (14,3% случаев) и фокальные пароксизмы, исходящие из моторной коры (8,6%). В группе пациентов с двумя типами приступов обращала на себя внимание частая ассоциация фокальных моторных (25,7% случаев), вторично-генерализованных (20% пациентов) и фокальных приступов, исходящих из затылочных отделов (17,1% пациентов) с другими типами приступов. Сочетание 3 и 4 типов приступов наблюдалось в единичных случаях (в 1 и 2 случаях соответственно). Наиболее часто выявлялось сочетание фокальных моторных приступов и эпилептических спазмов — в 11,4% случаях, фокальных моторных и вторично-генерализованных приступов — 8,6%, вторично-генерализованных и фокальных, исходящих из затылочной коры — в 8,6%.
По частоте возникновения мы разделили эпилептические приступы на единичные (1—3 за весь период заболевания), редкие (1—3 раза в год), частые (несколько приступов в неделю) и ежедневные. В 57,6% случаев приступы были редкими (27,3%) или единичными (30,3%). Приступы, возникавшие с частотой несколько раз в месяц, отмечены у 15,2% пациентов. Ежедневные приступы выявлены у 27,3% пациентов, и были представлены преимущественно псевдогенерализованными пароксизмами: эпилептическими спазмами, атипичными абсансами, негативным миоклонусом.
Продолжительность эпилептических приступов у пациентов была различной. В 56,6% случаев приступы самостоятельно оканчивались в течение 1—3 мин, при этом короткие приступы (до 1 мин) наблюдались в 33,3% случаев (преимущественно псевдогенерализованные). Обращает на себя внимание высокий процент длительных приступов. Так приступы, длящиеся 5—9 мин , отмечены у 13,3% больных. В 36,7% случаев продолжительность приступов превышала 10 мин, и у части пациентов пароксизмы носили характер эпилептического статуса.
Исследование показало высокую хронологическую зависимость эпилептических приступов от ритма «сон—бодрствование», которая наблюдалась у 88,6% пациентов нашей группы. Наиболее часто приступы отмечались в период при пробуждении или при засыпании — в 42,9%. Во сне приступы возникали в 25,7% случаев; в бодрствовании и во сне — 17,1%. Лишь у 11,4% пациентов эпилептические приступы не имели четкой связи со сном.
Неврологический статус. В 100% случаев выявлялась очаговая неврологическая симптоматика. Пирамидные нарушения отмечались в 82,9% случаев, из них у 40% пациентов выявлены парезы или параличи. Из других неврологических симптомов наиболее часто встречалась атаксия — в 20% случаев, мышечные дистонии — 11,4%, тремор в конечностях — 8,6%. Снижение интеллекта различной степени выраженности выявлено в 57,1% случаев. Синдром детского церебрального паралича констатировался у 40% пациентов. Из них: гемипаретическая форма наблюдалась в 57,2% случаев всех форм ДЦП, спастическая диплегия — в 21,4% случаев, двойная гемиплегия — в 21,4% случаев.
Результаты ЭЭГ исследования . Основная активность была близка или соответствовала возрастной норме в 57,2% случаев. Однако в большинстве случаев даже на фоне сохранного альфа-ритма определялось диффузное или биокципитальное тета-замедление фоновой ритмики. Дельта-замедление с акцентом в задних отделах выявлялось в 14,3% случаев, преимущественно, у детей с эпилептическими спазмами и дебютом приступов на первом году жизни. При этом дельта-волны сочетались с мультирегиональной эпилептиформной активность в затылочных отделах. Более чем в 50% случаев на ЭЭГ в состоянии бодрствования и во сне отмечался повышенный индекс экзальтированной бета-активности (exsessive fast). В целом, для пациентов нашей группы характерной картиной ЭЭГ в состоянии бодрствования являлось тета-замедление основной активности в сочетании с убыстрением корковой ритмики.
Обязательным критерием включения в группу было выявление на ЭЭГ доброкачественных эпилептиформных паттернов детства (ДЭПД). ДЭПД были представлены в виде региональной/мультирегиональной эпилептиформной активности в 100% случаев, а также в виде латерализованных, значительно реже — билатеральных и диффузных разрядов.
В 75% случаев региональная эпилептиформная активность отмечалась в центрально-темпоро-фронтальных отделах (рис. 2), в 30% ДЭПД регистрировались в затылочных отведениях (рис. 3). Следует отметить, что в нашей группе нередко выявлялся фокус и в вертексных отделах. В 57,1% случаев региональная/мультирегиональная эпилептиформная активность была ограничена одним полушарием, в 42,9% отмечались независимые фокусы эпилептиформной активности в двух полушариях (рис. 4). У 57,1% пациентов отмечалось билатеральное распределение эпилептиформной активности, которое в себя включало: случаи продолженных разрядов в симметричных областях в двух полушариях с формированием картины билатерально-асинхронных комплексов (рис. 3), билатеральное распространение разрядов из одного фокуса на гомологичные отделы контралатерального полушария, билатеральных комплексов острая-медленная волна, диффузных разрядов комплексов острая-медленная волна.
Исследование показало, высокую хронологическую приуроченность ДЭПД ко сну. В 100% случаев ДЭПД зарегистрированы во сне, в 77,1% — эпилептиформная активность выявлена и во сне и в бодрствовании. Важно отметить, что ни в одном случае не отмечено появление эпилептиформной активности ДЭПД изолированно в состоянии бодрствования.
Анализ результатов видео-ЭЭГ мониторинга позволил выделить характерные особенности эпилептиформной активности в обследованной группе. Для доброкачественных эпилептиформных паттернов детства была характерна тенденция к формированию групп в виде дуплетов, триплетов и более длительных групп (псевдо-ритмичные разряды). Индекс ДЭПД нарастал в состоянии пассивного бодрствования и был максимален при переходе в состояние дремоты и во сне. В состоянии активного бодрствования индекс ДЭПД значительно блокировался. Во сне представленность ДЭПД максимальна в стадиях медленного сна, во время REM-сна отмечалась значительная редукция данного паттерна ЭЭГ. Именно во сне у наших пациентов регистрировались продолженная пик-волновая эпилептиформная активность в медленном сне (ПЭМС) и электрический эпилептический статус медленного сна — ПЭМС с индексом более 85% записи сна.
Исследование показало отсутствие достоверной связи между индексом ДЭПД и частотой фокальных моторных приступов. ДЭПД не являлись ЭЭГ-паттерном фокальных приступов. Однако в случае латерализованных или диффузных разрядов была высока вероятность возникновения эпилептического негативного миоклонуса или атипичных абсансов.
Представляет интерес динамика эпилептиформной активности у пациентов в процессе лечения. Появившись на ЭЭГ сна однократно, ДЭПД продолжали регистрироваться постоянно во всех последующих записях ЭЭГ многие месяцы или годы. Во всех случаях вначале отмечалось купирование эпилептических приступов и лишь затем — исчезновение ДЭПД. На фоне терапии АЭП со временем постепенно наблюдалось снижение индекса и амплитуды эпилептиформных комплексов. В случаях ПЭМС эпилептиформная активность и особенно электрический статус постепенно «затухали» и «освобождали» все большие и большие эпохи записи ЭЭГ для нормального ритма. ПЭМС становилась менее регулярной и ритмичной, появлялись все большие промежутки, свободные от эпилептиформной активности. Вместе с тем, региональные паттерны несколько усиливались, как во сне, так и в бодрствовании, замещая диффузную активность. Сначала эпилептиформная активность полностью исчезала при записи в бодрствовании, а затем — и в период сна. К наступлению пубертатного периода эпилептиформная активность не регистрировалась ни в одном из случаев.
Данные нейровизуализации .При проведении нейровизуализации в 100% случаев констатировались различные структурные нарушения в головном мозге. Наиболее часто выявлялись признаки гипоксически-ишемической перинатальной энцефалопатии (62,8% случаев): диффузные атрофические/субатрофические изменения различной степени выраженности — 31,4%, перивентрикулярная лейкомаляция — 31,4% (рис. 5). Арахноидальные кисты (рис. 6) выявлялись у 13 (37,1%) пациентов, из них в 7 случаях обнаружены кисты височной доли (53,9% среди пациентов с кистами), у 4 пациентов — теменной доли (30,8%), у 2 пациентов — лобной (15,4%), у 2 — затылочной области (15,4%). Изменения в мозжечке (гипоплазия червя мозжечка, атрофия мозжечка) выявлялись в 11,4% случаев. Кортикальные туберсы наблюдались у 1 пациента; в 2 случаях определялись признаки полимикрогирии.
Клинико-электро-нейровизуализационные корреляции . Отдельно мы проанализировали корреляции клинических, электроэнцефалографических и нейровизуализационных данных у обследованных больных. Степень корреляции проводилась на основании сравнения данных обследования, указывающих на общий очаг. Оценивалась взаимосвязь 4 основных параметров: неврологический статус (сторонность поражения), семиология приступов (локализация очага), данные ЭЭГ и результаты нейровизуализации:
- 1-ая степень корреляции: совпадение всех клинических, электроэнцефалографических и нейровизуализационных параметров (4 указанных выше параметра).
- 2-ая степень корреляции: совпадение трех из четырех параметров.
- 3-ая степень корреляции: совпадение 2-х из 4-х параметров.
- Отсутствие четкой корреляции.
Отдельно оценивалась частота встречаемости диффузной симптоматики в структуре указанных выше параметров. К ней мы относили: двустороннюю неврологическую симптоматику, псевдогенерализованный характер приступов, диффузные разряды на ЭЭГ и диффузные изменения в головном мозге при МРТ исследовании.
Четкая корреляция (совпадение всех 4 параметров) отмечена лишь у 14,3% пациентов; 2-я степень корреляции — 25,7% случаев; 3-я степень — 22,9%. Достоверное отсутствие корреляции было выявлено у 37,1% больных. Различные диффузные симптомы отмечались в 94,3% случаев. Однако не было ни одного пациента, у которого встречались бы исключительно диффузные симптомы.
Терапия и прогноз .Исследование показало хороший прогноз в отношении контроля эпилептических приступов и высокую эффективность антиэпилептической терапии. В ходе лечения купирования приступов удалось добиться у всех, за исключением одного, пациентов — 97,1%! В 28,6% достигнута полная электро-клиническая ремиссия, что составляет 32,3% от всех пациентов с клинической ремиссией более года. В 1 случае у пациента с гемиклоническими и вторично-генерализованными приступами и признаками гипоксически-ишемической перинатальной энцефалопатии на МРТ была достигнута ремиссия приступов, продолжавшаяся в течение 3 лет. Далее был отмечен рецидив приступов. В настоящее время после коррекции АЭП приступы купированы, но на момент публикации длительность ремиссии составила 1 месяц. Ремиссия более 1 года отмечена у 31 пациента, что составило в 88,6% случаев. Следует отметить, что, не смотря на столь высокий процент ремиссий, в большинстве случаев на начальных этапах терапии заболевание отличалось резистентностью в отношении приступов и эпилептиформной активности на ЭЭГ. Только в 8 случаях (22,9%) приступы купировались при монотерапии. В остальных случаях ремиссия достигнута при дуо- и политерапии, включая применение кортикостероидов. Наиболее эффективными препаратами в лечении пациентов обследованной группы были: вальпроаты (конвулекс) и топирамат (топамакс), как в монотерапии, так и в комбинации. При применении карбамазепина в монотерапии в ряде случаев отмечена высокая эффективность, но нередко отмечались и явления аггравации в виде учащения фокальных приступов и появления псевдогенерализованных пароксизмов, а также в виде нарастания индекса диффузной эпилептиформной активности на ЭЭГ. При резистентности фокальных приступов хороший ответ был получен при назначении комбинаций: конвулекс + топамакс, конвулекс + тегретол или трилептал. Высокой эффективностью обладали сукцинимиды (суксилеп, петнидан, зарантин), которые применялись только в комбинации, главным образом, с вальпроатами. Сукцинимиды были эффективны, как в отношении псевдогенерализованных приступов, так и эпилептиформной активности на ЭЭГ. Также с успехом применялся сультиам (осполот) в комбинации с вальпроатами. В резистентных случаях, преимущественно у пациентов с инфантильными спазмами, а также при наличии «электрического эпилептического статуса медленного сна» на ЭЭГ, нами назначались кортикостероидные гормоны (синактен-депо, гидрокортизон, дексаметазон) с высочайшим эффектом: купирование приступов, блокирование или значительное снижение индекса эпилептиформной активности во всех случаях. Ограничивала применение гормонов высокая частота побочных эффектов терапии.
Анализ результатов показал, что на начальных этапах лечения в большинстве случаев не удается блокировать или даже снизить индекс ДЭПД на ЭЭГ. Особенной резистентностью отличались случаи диффузного распространения ДЭПД с формированием картины продолженной эпилептиформной активности в фазу медленного сна. В этих случаях наибольшую эффективность показало добавление к базовым АЭП сукцинимидов или осполота. Назначение этих препаратов оказывало значительное блокирование региональной и диффузной эпилептиформной активности на ЭЭГ. Также высокую эффективность в отношении ДЭПД показало применение кортикостероидов.
Следует отметить положительное действие АЭП, наблюдаемое у обследованных пациентов, в отношении когнитивных функций и двигательного развития. Этот эффект, в первую очередь, можно связать с «освобождением» мозга от приступов и эпилептиформной активности, а также с проведением более интенсивной реабилитационной помощи, которая стала возможна после установления контроля над приступами. Однако полного или значительного восстановления моторных и когнитивных функций не было отмечено ни в одном случае, даже после полного купирования приступов и блокирования эпилептиформной активности.
ОБСУЖДЕНИЕ
Изучение описанной группы пациентов проводились в Центре детской неврологии и эпилепсии (К.Ю. Мухин, М.Б. Миронов, К.С. Боровиков), совместно с немецкими коллегами (H. Holthausen и соавт.) в период с 2002 по 2009 годы. В настоящее время под нашим наблюдением находится более 130 пациентов, отвечающим критериям, описанным в статье. По нашему мнению, эта группа представляет совершенно особый эпилептический синдром с благоприятным течением эпилепсии, но с тяжелыми неврологическими нарушениями. Мы назвали его «фокальная эпилепсия детского возраста со структурными изменениями в мозге и доброкачественными эпилептиформными паттернами на ЭЭГ », сокращенно — ФЭДСИМ-ДЭПД . Не совсем удачный синоним, применяемый ранее, — «двойная патология», так под этим термином разные авторы подразумевают различные патологические состояния, в частности, сочетание мезиального височного склероза с диспластическими изменениями гиппокампа .
Хотелось бы обратить внимание, что в доступной нам отечественной и зарубежной литературе мы не нашли подобных исследований. В отдельных публикациях описаны лишь единичные наблюдения пациентов с фокальными моторными приступами, напоминающими таковые при ИФЭ, благоприятным прогнозом по течению эпилепсии и с наличием структурных изменений в мозге . Авторы называют данные случаи «идиопатической копией симптоматических фокальных эпилепсий» . Фактически, эти единичные случаи идентичны описанной нами группе пациентов с ФЭДСИМ-ДЭПД. Однако принципиально различие в названии, что коренным образом меняет представление о данном синдроме.
ФЭДСИМ-ДЭПД не является в строгом смысле симптоматической эпилепсией. Во-первых, во многих случаях иктогенная зона не совпадает с локализацией структурных изменений в мозге, причем не только в пределах доли мозга, но даже и гемисферы. У 28,6% обследованных нами пациентов констатируется диффузная кортикальная атрофия, а локальные структурные изменения в мозге отсутствуют. Во-вторых, эпилептиформная активность у пациентов данной группы представлена, главным образом, мультирегиональными и диффузными ДЭПД, а не четко региональными ЭЭГ-паттернами, как при симптоматических фокальных эпилепсиях. При этом если возникает феномен вторичной билатеральной синхронизации, то зона генерации разряда далеко не всегда совпадает с зоной патологического субстрата. В-третьих (это — главное!), в подавляющем большинстве случаев эпилептические приступы исчезают в пубертатном периоде, несмотря на персистирование морфологического субстрата в мозге.
Отсутствие четкой корреляции иктогенной зоны и локализации эпилептиформной активности с локализацией структурных изменений в мозге, исчезновение, в конечном итоге, эпилептических приступов практически у всех пациентов, ставит под сомнение симптоматический характер эпилепсии, то есть ее развитие непосредственно в результате воздействия морфологического субстрата. С другой стороны, высокая частота случаев эпилепсии в семьях пробандов; дебют эпилепсии исключительно в детском возрасте; приступы, идентичные по характеру ИФЭ с их приуроченностью ко времени пробуждения и засыпания; наличие на ЭЭГ ДЭПД; купирование приступов в пубертате (под действием терапии или самопроизвольно) — четко указывают на идиопатический характер эпилепсии. Однако при идиопатической фокальной эпилепсии нет структурных изменений в мозге, нет очаговых неврологических симптомов и интеллектуального дефицита, нет замедления основной активности фоновой записи на ЭЭГ и продолженного регионального замедления. Также для ИФЭ не характерны продолжительные приступы нередко со статусным течением и с формированием тоддовского паралича. По нашему мнению, указанные симптомы не вызваны эпилепсией, а являются результатом перинатальной патологии. Таким образом, речь идет об уникальном синдроме, при котором эпилепсия по своей сути является идиопатической, а сопутствующие симптомы (неврологический и интеллектуальный дефицит) обусловлены структурным поражением мозга. Из этого следует, что ФЭДСИМ-ДЭПД — не «идиопатическая копия симптоматической эпилепсии», а, вероятнее всего, идиопатическая фокальная эпилепсия, развивающаяся у больных с морфологическими изменениями в мозге перинатального генеза. Эта форма является идиопатической, но отнюдь не доброкачественной. Понятие «доброкачественная эпилепсия» включает в себя не только возможность купирования (или самокупирования) приступов, но и отсутствие неврологических и когнитивных нарушений у пациентов , чего не бывает при ФЭДСИМ-ДЭПД, по определению. ФЭДСИМ-ДЭПД представляет собой идиопатическую (по характеру приступов и особенностям течения) эпилепсию у детей с локальными или диффузными изменениями в мозге перинатального генеза. Эта группа пациентов с учетом клинико-электро-нейровизуализационных особенностей, по нашему мнению, является отдельным четко очерченным эпилептическим синдромом у детей, который занимает особое промежуточное место в ряду фокальных форм эпилепсии различной этиологии.
Патогенез развития столь уникального эпилептического синдрома, вероятно, будет предметом последующего изучения. Нам хотелось бы обсудить некоторые возможные механизмы возникновения ФЭДСИМ-ДЭПД. С нашей точки зрения, в основе развития ФЭДСИМ-ДЭПД лежат два механизма: врожденное нарушение созревания мозга и патология перинатального периода, главным образом, гипоксически-ишемическое поражение ЦНС. Термин “hereditary impairment of brain maturation ” — врожденное нарушение созревания головного мозга — был впервые применен знаменитым немецким детским неврологом и эпилептологом Германом Доозе . Гипотеза Doose, которую мы всецело поддерживаем, заключается в существовании у ряда пациентов генетически детерминированного нарушения созревания мозга во внутриутробном периоде. По нашему мнению, можно выделить 3 основных диагностических критерия состояния, обозначенного как «врожденное нарушение созревания мозга».
1. Наличие у больных «патологии нервно-психического развития»: глобальное нарушение когнитивных функций, задержка психического развития, дисфазия, дислексия, дискалькулия, синдром гиперактивности с дефицитом внимания, аутистикоподобное поведение и пр.
2. Сочетание данных нарушений с интериктальной эпилептиформной активностью, соответствующей по морфологии доброкачественным эпилептиформным паттернам детства.
3. Улучшение течения заболевания и полное исчезновение эпилептиформной активности при достижении пациентами пубертатного периода.
Самые различные эндогенные и экзогенные факторы, действующие во внутриутробном периоде, способны вызвать врожденное нарушение процессов созревания головного мозга . При этом возможно, «генетическая предрасположенность» играет ведущую роль. H. Doose (1989), H. Doose и соавт. (2000) показали, что доброкачественные эпилептиформные паттерны детства на ЭЭГ (изолированно, в сочетании с эпилепсией или иной «патологией развития») генетически детерминированы, наследуясь по аутосомно-доминантному типу с низкой пенетрантностью и вариабельной экспрессивностью . Каждый локус гена или аллельные гены влияют на синтез определенного полипептида или энзима. В основе патологии развития лежит нарушение пренатальной дифференцировки нейронов, формирования дендритного древа и реорганизации синаптических контактов, благодаря чему нейроны должны связываться в «клеточные ансамбли» или нейрональные сети . Под влиянием различных повреждающих факторов могут возникать ошибочные нейрональные связи — аберрантная синаптическая реорганизация . По мнению некоторых исследователей, нарушенная пластичность (аберрантный спруттинг) наиболее характерна для детского возраста и может быть одной из причин эпилепсии, а также развития когнитивных расстройств . Нарушенная нейрональная пластичность в период развития мозга, приводит к формированию «сломанных», «извращенных» клеточных ансамблей кортикальных нейронов, что клинически выражается стойкими врожденными нарушениями когнитивных функций . Филогенетически наиболее молодые отделы мозга — лобные доли — являются особенно ранимыми к нарушениям нейрональной организации .
Врожденное нарушение созревания мозга, проявляется различной «патологией развития» (табл. 1). Данные патологические состояния возникают, главным образом, с рождения. Однако появление эпилептиформной активности, а в ряде случаев и приступов, происходит, как правило, в определенный «критический» период развития ребенка — чаще в возрасте от 3 до 6 лет . При этом важно отметить, что по мере роста ребенка и созревания мозга, наблюдается постепенное улучшение психического развития, купирование приступов и полное блокирование ДЭПД с наступлением пубертатного периода. Важнейшую роль в развитии мозга играют половые гормоны . А.С. Петрухин (2000) считает, что нарушения при воздействии гормонов во внутриутробном периоде могут индуцировать механизмы, ведущие к извращенной дифференциации мозга. С другой стороны, начало функционирования половых гормонов в пубертатном периоде приводит к «сглаживанию» симптоматики когнитивной эпилептиформной дезинтеграции и, во многих случаях, к полной нормализации электроэнцефалограммы . Мы считаем, что механизм врожденного нарушения процессов созревания мозга, является основным в развитии симптомокомплекса «идиопатической фокальной эпилепсии». При этом доброкачественные эпилептиформные паттерны детства правильнее считать не маркерами эпилепсии, а признаком незрелости мозга .
Второй механизм развития ФЭДСИМ-ДЭПД наличие морфологических изменений в мозге, обусловленных патологией пренатального периода. Х. Хольтхаузен (Holthausen, 2004, личное сообщение) для обозначения подобных случаев предложил термин «двойная патология ». Речь идет о пациентах с двумя патологическими состояниями: морфологическими изменениями в мозге и наличием ДЭПД на ЭЭГ и/или эпилептических приступов. Структурные изменения, по данным МРТ, имеют всегда врожденный характер, обусловленный патологией пренатального периода. С другой стороны, эпилептические приступы у пациентов с «двойной патологией» и эпилептиформная активность типа ДЭПД не имеет четкой локализационной взаимосвязи с морфологическими субстратами в мозге. Среди обследованных нами пациентов, корреляция 1 степени (совпадение локализации очага по данным неврологического осмотра, характера приступов, результатов ЭЭГ и МРТ) отмечалась лишь в 14,3% случаев. А полное отсутствие корреляции было выявлено у 34,3% больных, то есть, более чем у 1/3 пациентов!
Эпилепсия, возникающая у данных больных, носит все черты идиопатической фокальной (чаще — роландической, реже — затылочной), а ДЭПД-активность обычно наблюдается мультирегионально. Наиболее типично появление фаринго-оральных, гемифациальных, фацио-брахиальных, версивных и вторично-генерализованных приступов. Приступы возникают почти исключительно при пробуждении и засыпании, частота их невысокая, и они обязательно (!) исчезают к пубертатному периоду — в результате терапии или спонтанно. В процессе лечения наших пациентов купирования приступов удалось добиться у всех, за исключением одного больного — 97,1%!
Таким образом, несмотря на наличие морфологических изменений в мозге, как локальных, так и диффузных, клиническая картина (характер приступов, данные ЭЭГ) и течение эпилепсии идентичны таковым при идиопатической фокальной эпилепсии. Однако проблема заключается в том, что, несмотря на абсолютно благоприятное течение эпилепсии (имеется ввиду облигатное купирование приступов), прогноз в отношении двигательных и когнитивных функций у данной категории больных может быть очень тяжелым. В связи с этим, ФЭДСИМ-ДЭПД никак нельзя называть «доброкачественной» формой эпилепсии. При сохранении первого критерия доброкачественной эпилепсии (облигатное купирование приступов), второй критерий (нормальное двигательное и психическое развитие детей) — обычно отсутствует. В этом кардинальное отличие ФЭДСИМ-ДЭПД от ИФЭ.
Наиболее частыми врожденными морфологическими субстратами у больных ФЭДСИМ-ДЭПД служат: арахноидальные кисты, перивентрикулярная лейкомаляция, диффузная кортикальная атрофия гипоксически-ишемического генеза, полимикрогирия, врожденная окклюзионная шунтированная гидроцефалия. При визуализации на МРТ перивентрикулярной лейкомаляции (недоношенные дети с гипоксически-ишемической перинатальной энцефалопатией) и шунтированной окклюзионной гидроцефалии типично развитие детского церебрального паралича (атонически-астатическая форма или двойная диплегия) с эпилепсией и/или мультирегиональными ДЭПД на ЭЭГ. При наличии полимикрогирии формируется клиника гемипаретической формы детского церебрального паралича с эпилепсией и/или ДЭПД . У больных с арахноидальными и порэнцефалическими кистами возможно выявление врожденного гемипареза, речевых, поведенческих (в том числе, аутизма) и интеллектуально-мнестических нарушений в сочетании с ДЭПД на ЭЭГ. Еще раз следует обратить внимание, что течение эпилепсии у пациентов данной группы всегда благоприятное. Вместе с тем, двигательные нарушения и интеллектуально-мнестические расстройства могут быть очень серьезными, приводящими к тяжелой инвалидизации.
В некоторых публикациях указывается на роль раннего органического поражения таламуса в результате гипоксически-ишемических нарушений в перинатальном периоде . Структурные нарушения в таламусе могут приводить к гиперсинхронизации нейронов, их «воспламенению» (“firing”), способствуя поддержанию «повышенной судорожной готовности» вплоть до наступления пубертатного периода. Guzzetta и соавт. (2005) представили описание 32 пациентов с поражением таламуса в перинатальном периоде; при этом у 29 из них были выявлены электро-клинические признаки эпилепсии с электрическим эпилептическим статусом в фазу медленного сна. Было высказано предположение, что вентролатеральные и ретикулярные ядра таламуса, а также дисбаланс ГАМК-медиаторных систем ответственны за развитие постоянной продолженной эпилептиформной активности (по морфологии — ДЭПД) в фазу медленного сна. По мнению Х. Хольтхаузен (Holthausen, 2004, личное сообщение), ДЭПД являются электроэнцефалографическим отражением перинатальной лейкопатии. Именно поражение белого вещества (проводящих путей) головного мозга приводит к развитию «идиопатической по течению» фокальной эпилепсии, сочетающейся с ДЭПД. Поэтому, ФЭДСИМ-ДЭПД нередко возникает у недоношенных детей с детским церебральным параличом и перивентрикулярной лейкомаляцией на МРТ. Однако это не объясняет появления ДЭПД у неврологически здоровых детей и при ИФЭ, в случаях, когда двигательные нарушения отсутствуют, то есть отсутствует поражение белого вещества.
Когнитивные нарушения при ФЭДСИМ-ДЭПД обусловлены тремя основными причинами. Во-первых, морфологическими изменениями в головном мозге, возникающими во внутриутробном периоде. Данные изменения необратимы, мы не может на них воздействовать медикаментозно, однако, они не прогрессируют. Во-вторых, частые эпилептические приступы и, особенно, постоянная продолженная эпилептиформная активность могут приводить к выраженным нарушениям праксиса, гнозиса, речи, поведения. Формируясь в развивающемся мозге ребенка, эпилептиформная активность приводит к постоянной электрической «бомбардировке» корковых центров праксиса, гнозиса, речи и движений; приводит к их «перевозбуждению», а затем функциональному «блокированию» данных центров . Происходит функциональный разрыв нейрональных связей за счет длительно существующей эпилептиформной активности. При этом для нас важен индекс эпилептиформной активности, ее распространенность (наиболее неблагоприятен диффузный характер и бифронтальное распространение), а также возраст, в котором данная активность проявляется.
Существует и третий механизм формирования когнитивных нарушений у больных ФЭДСИМ-ДЭПД. С нашей точки зрения, важным фактором в развитии когнитивного дефицита у данной категории больных служит «врожденное нарушение процессов созревания мозга ». Этиология данного процесса неизвестна. По-видимому, он определяется совокупностью двух причин: генетической предрасположенностью и наличием различных стресс-факторов, воздействующих на внутриутробное развитие ребенка. Специфический маркер незрелости мозга — появление на ЭЭГ «доброкачественных эпилептиформных паттернов детства» — ДЭПД . В связи с этим, применение именно стероидных гормонов, способствующих «созреванию мозга», а не АЭП, оказывает наиболее эффективное воздействие в отношении улучшения когнитивных функций у больных ФЭДСИМ-ДЭПД. Doose H., Baier W.K. (1989) предположили, что ЭЭГ паттерн ДЭПД контролируется аутосомно-доминантным геном с возраст-зависимой пенетрантностью и вариабельной экспрессивностью . К сожалению, антиэпилептическая терапия, воздействуя на эпилептиформную активность, далеко не всегда оказывает отчетливое положительное воздействие по уменьшению нейропсихологических расстройств. По мере роста и созревания (прежде всего, — полового созревания) наблюдается постепенное улучшение когнитивных функций, способности к обучению и социализация пациентов. Однако нарушение когнитивных функций, различной степени выраженности, может персистировать в течение всей жизни, не смотря на купирование приступов и блокирование эпилептиформной активности.
На основании полученных результатов и данных литературы, мы разработали диагностические критерии синдрома ФЭДСИМ-ДЭПД.
1. Преобладание по полу пациентов мужского пола.
2. Дебют эпилептических приступов в возрасте до 11 лет с максимумом в первые 6 лет (82,9%) с двумя пиками: в первые 2 года жизни и в возрасте от 4 до 6 лет. Нередко дебют с инфантильных спазмов.
3. Преобладание фокальных моторных приступов (гемифациальные, брахиофациальные, гемиклонические), фокальных приступов, исходящих из затылочной коры (зрительные галлюцинации, версивные приступы, приступы обмякания) и вторично-генерализованных судорожных приступов.
4. Возможно сочетание фокальных и псевдогенерализованных приступов (эпилептические спазмы, негативный миоклонус, атипичные абсансы).
5. Относительно невысокая частота фокальных и вторично-генерализованных приступов.
6. Хронологическая приуроченность фокальных приступов ко сну (возникновение при пробуждении и засыпании).
7. Неврологический дефицит у большинства пациентов, включающий двигательные и когнитивные нарушения; нередко наличие детского церебрального паралича.
8. Фоновая активность ЭЭГ: характерно тета-замедление основной активности на фоне повышенного индекса диффузной бета-активности.
9. Наличие на ЭЭГ, преимущественно, в центрально-темпоральных и/или в затылочных отведениях специфического ЭЭГ-паттерна — доброкачественных эпилептиформных паттернов детства, которые чаще возникают мультирегионально и диффузно с нарастанием в фазу медленного сна.
10. При нейровизуализации во всех случаях констатируются признаки перинатального поражения головного мозга, преимущественно, гипоксически-ишемического генеза. Данные морфологические изменения могут быть, как локальными, так и диффузными, с преимущественным поражением белого вещества (лейкопатия).
11. Ремиссия эпилептических приступов достигается во всех случаях; позже блокируется эпилептиформная активность на ЭЭГ. Неврологические (двигательные и когнитивные) нарушения, как правило, остаются неизменными.
Таким образом, 5 основных критериев остаются во всех случаях синдрома ФЭДСИМ-ДЭПД: дебют эпилептических приступов в детском возрасте; наличие фокальных приступов (варианты гемиклонических или фокальных, исходящие из затылочной коры) и/или вторично-генерализованных судорожных приступов, приуроченных ко сну; наличие доброкачественных эпилептиформных паттернов детства (ДЭПД) на ЭЭГ; наличие структурных изменений в головном мозге перинатального генеза при нейровизуализации; полное купирование эпилептических приступов до достижения больными взрослого возраста.
Рис. 1. Частота дебюта приступов в каждом годовом интервале (%).Рис. 2. Пациент З.Р.
Видео-ЭЭГ мониторинг: Во сне регистрируется мультирегиональная эпилептиформная активность: в правой центрально-височной области с распространением на правую теменно-затылочную область, в лобно-центрально-теменных вертексных отделах, в левой лобной области в виде единичных низкоамплитудных спайков. Эпилептиформные изменения имеют морфологию доброкачественных эпилептиформных паттернов детства (ДЭПД).

Рис. 3. Пациент М.А. , 8 лет. Диагноз: ФЭДСИМ-ДЭПД. Задержка психоречевого развития.
Видео-ЭЭГ мониторинг: Регистрируется эпилептиформная активность, представленная в виде билатеральных разрядов ДЭПД амплитудой до 200—300 мкВ различной степени синхронизации в затылочно-задневисочных отделах с выраженным распространением на вертексные отделы с альтернативным началом как в правых задних отделах (чаще) так и в левых отделах.

Рис.4. Пациент А.Н., 10 лет. Диагноз: ФЭДСИМ-ДЭПД. Правосторонние гемиконвульсивные приступы.
Видео-ЭЭГ мониторинг: Регистрируется региональная эпилептиформная активность (ДЭПД), представленная независимо в левой височно-центрально-лобной области с периодическим распространением на левые задние отделы и в правой центрально-лобной области с тенденцией к распространению на все электроды правого полушария.

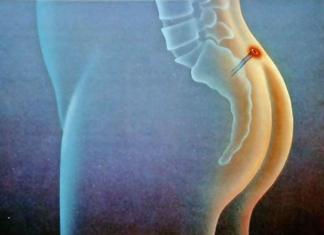
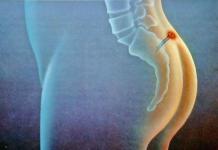
Рис. 5. Пациент З.Р. , 2 года. Диагноз: ФЭДСИМ-ДЭПД. Левосторонние гемиклонические приступы с тоддовским параличом.
МРТ головного мозга: Явления остаточной постгипоксической лейкопатии перивентрикулярного белого вещества обеих теменных долей: четко ограниченные зоны повышения Т2-сигнала, гиперинтенсивные во FLAIR, локализованные в белом веществе лобно-теменных и теменно-затылочных долей. Вторичная вентрикуломегалия боковых желудочков.
5. Зенков Л.Р. Непароксизмальные эпилептические расстройства. — М.: МЕДпресс-информ., 2007. — 278 с.
6. Карлов В.А. Эпилепсия. — М., 1990. — 336 с.
7. Карлов В.А. Эпилептическая энцефалопатия // Журн неврол и психиат. — 2006. — Т. 106(2). — С. 4—12.
8. Крыжановский Г.Н. Пластичность в патологии нервной системы // Журн неврол и психиат. — 2001. — Т. 101(2). — С. 4—7.
9. Мухин К.Ю. Доброкачественные эпилептиформные нарушения детского возраста и их специфичность // К.Ю. Мухин, А.С. Петрухин, Л.Ю. Глухова / Эпилепсия: атлас электро-клинической диагностики. — 2004, М.:Альварес Паблишинг. — С. 277—288.
10. Мухин К.Ю. Идиопатическая фокальная эпилепсия с псевдогенерализованными приступами — особая форма эпилепсии в детском возрасте // Рус. жур. дет. невр. — 2009. — Т. 4(2). — С. 3—19.
11. Мухин К.Ю. Понятие об идиопатической эпилепсии: диагностические критерии, патофизиологические аспекты // В книге: К.Ю. Мухин, А.С. Петрухин / Идиопатические формы эпилепсии: систематика, диагностика, терапия. — М.: Арт-Бизнес-Центр., 2000. — С. 16—26.
12. Мухин К.Ю., Петрухин А.С., Миронов М.Б. Эпилептические синдромы. Диагностика и терапия. Справочное руководство для врачей. Системные решения. — М., 2008. — 224 с.
13. Мухин К.Ю., Петрухин А.С., Миронов М.Б., Холин А.А., Глухова Л.Ю., Пилия С.В., Волкова Э.Ю., Головтеев А.Л., Пылаева О.А. Эпилепсия с электрическим эпилептическим статусом медленного сна: диагностические критерии, дифференциальный диагноз и подходы к терапии. — М., 2005. — 32 с.
14. Мухин К.Ю., Петрухин А.С. Идиопатические формы эпилепсии: систематика, диагностика, терапия. — М: Арт-Бизнес-Центр, 2000. — С. 176—192.
15. Ноговицын В.Ю., Нестеровский Ю.Е., Осипова Г.Н., Сандуковская С.И., Калинина Л.В., Мухин К.Ю. Полиморфизм электроэнцефалографического паттерна доброкачественных эпилептиформных нарушений в детстве // Журн неврол психиат. — 2004. — Т. 104(10). — С. 48—56.
16. Петрухин А.С., Мухин К.Ю., Благосклонова Н.К., Алиханов А.А. Эпилептология детского возраста. — М.: Медицина, 2000. — 623 с.
17. Ambrosetto G. Unilateral opercular macrogyria and benign childhood epilepsy with centrotemporal (rolandic) spikes: report of a case // Epilepsia. — 1992. — V. 33(3). — P. 499—503.
18. Beaumanoir A., Bureau M., Deonna T., Mira L., Tassinari C.A. Continuous spikes and waves during slow sleep. Electrical status epilepticus during slow sleep. Acquired epileptic aphasia and related conditions. — London: John Libbey, 1995. — 261 p.
19. Ben-Zeev B., Kivity S., Pshitizki Y., Watemberg N., Brand N., Kramer U. Congenital hydrocephalus and continuous spike wave in slow sleep — a common association? // J. Child Neurol. — 2004. — V. 19 (2). — P. 129—134.
20. Caraballo R.H., Cersosimo R., Fejerman N. Symptomatic focal epilepsies imitating atipical evolutions of idiopathic focal epilepsies in childhood // In: Eds. N. Fejerman, R.H. Caraballo / Benign focal epilepsies in infancy, childhood and adolescence. — J.L., UK., 2007. — P. 221—242.
21. De Negri M. Hyperkinetic behaviour, attention deficit disorder, conduct disorder and instabilite psychomotrice: identity, analogies, and misunderstandings // Brain Dev. — 1995. — V. 17(2). — P. 146—7; discussion 148.
22. Doose H. EEG in childhood epilepsy. — Hamburg, John Libbey, 2003. — P. 191—243.
23. Doose H. Symptomatology in children with focal sharp waves of genetic origin // Eur. J. Pediatr. — 1989. — V. 149. — P. 210—215.
26. Dreifuss F. Classification and recognition of seizures // Clin. Ther. — 1985. — V. 7. — N. 2. — P. 240—245.
27. Engel J. Jr. A proposed diagnostic scheme for people with epileptic seizures and with epilepsy: Report of the ILAE Task Force on Classification and Terminology // Epilepsia. — 2001. — V. 42(6). — P. 796—803.
28. Engel J. Jr. Report of the ILAE Classification Core Group // Epilepsia. —2006. — V. 47(9). — P. 1558—1568.
29. Fejerman N., Caraballo R.H. Definition of syndromes, seizure types and nosologic spectrum // In: Eds. N. Fejerman, R.H. Caraballo / Benign focal epilepsies in infancy, childhood and adolescence. — J.L., UK., 2007. — P. 3—13.
30. Guerrini R., Genton P., Bureau M. et al. Multilobar polymicrogiria, intractable drop attack seizures, and sleep-related electrical status epilepticus // Neurology. — 1998. — V. 51. — P. 504—512.
31. Guzzetta F., Battaglia D., Veredice Ch., Donvito V., Pane M., Lettori D., Chiricozzi F., Chieffo D., Tartaglione T., Dravet Ch. Early thalamic injury associated with epilepsy and continuous spike-wave during slow sleep // Epilepsia. — 2005. — V. 46/6. — P. 889—900.
32. Holthausen H., Teixeira V.A., Tuxhorn I. et al. Epilepsy surgery in children and adolescents with focal cortical dysplasia // In: I. Tuxhorn, H. Holthausen, H-E Boenigk / Pediatric epilepsy syndromes and their surgical treatment. — London, JL., 1997. — P. 199—215.
33. Kim H.L., Donnelly J.H., Tournay A.E. et al. Absence of seizures despite high prevalence of epileptiform EEG abnormalities in children with autism monitored in a tertiary care center // Epilepsia. — 2006. — V. 47(2). — P. 394—398.
34. Luders H.-O., Noachtar S. Epileptic seizures. Pathophysiology and clinical semiology. — Churchill Livingstone, N.Y., 2000. — 796 p.
35. Sutula T.P. Mechanisms of epilepsy progression: current theories and perspectives from neuroplasticity in adulthood and development // Epilepsy Res. — 2004. — V. 60(2—3). — P. 161—171.

ЭЭГ паттерны в клинической эпилептологии
Наиболее изученные паттерны:
- фокальные доброкачественные острые волны (ФОВ);
- фотопароксизмальная реакция (ФПР);
- генерализованные спайк-волны (во время гипервентиляции и в покое).
ФОВ чаще регистрируется в детском возрасте, в периоде между 4 и 10 годами, а ФПР у детей до 15-16 лет.
При ФОВ наблюдаются следующие негативные отклонения:
- отставание в умственном развитии;
- фебрильные судороги;
- развитие роландической эпилепсии;
- расстройства психики;
- различные функциональные расстройства.
Развивается примерно у 9%.
При наличии ФПР выявляются:
- фотогенная эпилепсия;
- симптоматическая парциальная эпилепсия;
- идиопатическая парциальная эпилепсия;
- фебрильные судороги.
При отсутствии приступов, даже на фоне патологических волн на ЭЭГ, лечение назначаться не должно, так как патологические изменения могут регистрироваться и без симптомов заболеваний нервной системы (наблюдается примерно у 1% здоровых людей).
При наличии синдрома Ландау-Клеффнера, ESES, различных бессудорожных эпилептических энцефалопатиях назначаются антиэпилептические препараты, так как эти заболевания вызывают нарушение памяти и речи, психические расстройства, у детей – задержку роста и трудности в обучении.
Под понятием «ритм» на ЭЭГ подразумевается определённый тип электрической активности, соответствующий некоторому определённому состоянию мозга и связанный с определёнными церебральными механизмами. При описании ритма указывается его частота, типичная для определённого состояния и области мозга, амплитуда и некоторые характерные черты его изменений во времени при изменениях функциональной активности мозга.
- Альфа(а)-ритм : частота 8-13 Гц, амплитуда до 100 мкВ. Регистрируется у 85-95% здоровых взрослых. Лучше всего выражен в затылочных отделах. Наибольшую амплитуду а-ритм имеет в состоянии спокойного расслабленного бодрствования при закрытых глазах. Помимо изменений, связанных с функциональным состоянием мозга, в большинстве случаев наблюдают спонтанные изменения амплитуды а-ритма, выражающиеся в чередующемся нарастании и снижении с образованием характерных «веретён», продолжительностью 2-8 с. При повышении уровня функциональной активности мозга (напряжённое внимание, страх) амплитуда а-ритма уменьшается. На ЭЭГ появляется высокочастотная низкоамплитудная нерегулярная активность, отражающая десинхронизацию активности нейронов. При кратковременном, внезапном внешнем раздражении (особенно вспышке света) эта десинхронизация возникает резко, и в случае если раздражение не носит эмоциогенного характера, достаточно быстро (через 0,5-2 с) восстанавливается а-ритм. Этот феномен называется «реакция активации», «ориентировочная реакция», «реакция угасания а-ритма», «реакция десинхронизации».
- Бета-ритм : частота 14-40 Гц, амплитуда до 25 мкВ. Лучше всего бета-ритм регистрируется в области центральных извилин, однако распространяется и на задние центральные и лобные извилины. В норме он выражен весьма слабо и в большинстве случаев имеет амплитуду 5-15 мкВ. Бета-ритм связан с соматическими сенсорными и двигательными корковыми механизмами и даёт реакцию угасания на двигательную активацию или тактильную стимуляцию. Активность с частотой 40-70 Гц и амплитудой 5-7 мкВ иногда называют у-ритмом, клинического значения он не имеет.
- Мю-ритм : частота 8-13 Гц, амплитуда до 50 мкВ. Параметры мю-ритма аналогичны таковым нормального а-ритма, но мю-ритм отличается от последнего физиологическими свойствами и топографией. Визуально мю-ритм наблюдают только у 5-15% испытуемых в роландической области. Амплитуда мю-ритма (в редких случаях) нарастает при двигательной активации или соматосенсорной стимуляции. При рутинном анализе мю-ритм клинического значения не имеет.
Виды активности, патологические для взрослого бодрствующего человека
- Тета-активность : частота 4-7 Гц, амплитуда патологической тета-активности>40 мкВ и чаще всего превышает амплитуду нормальных ритмов мозга, достигая при некоторых патологических состояниях 300 мкВ и более.
- Дельта-активность : частота 0,5-3 Гц, амплитуда такая же, как у тета-активности.
Тета- и дельта-колебания могут в небольшом количестве присутствовать на ЭЭГ взрослого бодрствующего человека и в норме, но их амплитуда при этом не превышает таковую а-ритма. Патологической считают ЭЭГ, содержащую тета- и дельта-колебания амплитудой >40 мкВ и занимающие более 15% общего времени регистрации.
Эпилептиформная активность - феномены, типично наблюдаемые на ЭЭГ больных эпилепсией. Они возникают в результате высокосинхронизованных пароксизмальных деполяризационных сдвигов в больших популяциях нейронов, сопровождающихся генерацией потенциалов действия. В результате этого возникают высокоамплитудные острой формы потенциалы, имеющие соответствующие названия.
- Спайк (англ. spike - остриё, пик) - негативный потенциал острой формы, длительностью менее 70 мс, амплитудой >50 мкВ (иногда до сотен или даже тысяч мкВ).
- Острая волна отличается от спайка растянутостью во времени: её длительность 70-200 мс.
- Острые волны и спайки могут комбинироваться с медленными волнами, образуя стереотипные комплексы. Спайк-медленная волна - комплекс из спайка и медленной волны. Частота комплексов спайк-медленная волна составляет 2,5-6 Гц, а период, соответственно, - 160-250 мс. Острая-медленная волна - комплекс из острой волны и следующей за ней медленной волны, период комплекса 500-1300 мс.
Важная характеристика спайков и острых волн - их внезапное появление и исчезновение и чёткое отличие от фоновой активности, которую они превышают по амплитуде. Острые феномены с соответствующими параметрами, нечётко отличающиеся от фоновой активности, не обозначаются как острые волны или спайки.
Комбинации описанных феноменов обозначаются некоторыми дополнительными терминами.
- Вспышка - термин, обозначающий группу волн с внезапным возникновением и исчезновением, чётко отличающихся от фоновой активности частотой, формой и/или амплитудой.
- Разряд - вспышка эпилептиформной активности.
- Паттерн эпилептического припадка - разряд эпилептиформной активности, типично совпадающей с клиническим эпилептическим приступом. Обнаружение таких феноменов, даже если не удаётся чётко оценить клинически состояние сознания пациента, также характеризуется как «паттерн эпилептического припадка».
- Гипсаритмия (греч. «высокоамплитудный ритм») - непрерывная генерализованная высокоамплитудная (>150 мкВ) медленная гиперсинхронная активность с острыми волнами, спайками, комплексами спайк-медленная волна, полиспайк-медленная волна, синхронными и асинхронными. Важный диагностический признак синдромов Уэста и Леннокса-Гасто.
- Периодические комплексы - высокоамплитудные вспышки активности, характеризующиеся постоянством формы для данного пациента. Наиболее важные критерии их распознавания: близкий к постоянному интервал между комплексами; непрерывное присутствие в течение всей записи, при условии постоянства уровня функциональной активности мозга; интра-индивидуальная стабильность формы (стереотипность). Чаще всего они представлены группой высокоамплитудных медленных волн, острых волн, сочетающихся с высокоамплитудными, заострёнными дельта- или тета-колебаниями, иногда напоминают эпилептиформные комплексы острая-медленная волна. Интервалы между комплексами составляют от 0,5-2 до десятков секунд. Генерализованные билатерально-синхронные периодические комплексы всегда сочетаются с глубокими нарушениями сознания и указывают на тяжёлое поражение мозга. Если они не обусловлены фармакологическими или токсическими факторами (алкогольная абстиненция, передозировка или внезапная отмена психотропных и гипноседативных препаратов, гепатопатия, отравление оксидом углерода), то, как правило, являются следствием тяжёлой метаболической, гипоксической, прионовой или вирусной энцефалопатии. Если интоксикации или метаболические нарушения исключены, то периодические комплексы с высокой достоверностью указывают на диагноз панэнцефалита или прионового заболевания.
Варианты нормальной электроэнцефалограммы взрослого бодрствующего человека
ЭЭГ в существенной степени однородна для всего мозга и симметрична. Функциональная и морфологическая неоднородность коры определяет особенности электрической активности различных областей мозга. Пространственная смена типов ЭЭГ отдельных областей мозга происходит постепенно.
У большинства (85-90%) здоровых взрослых при закрытых глазах в покое на ЭЭГ регистрируется доминирующий а-ритм с максимальной амплитудой в затылочных отделах.
У 10-15% здоровых обследуемых амплитуда колебаний на ЭЭГ не превышает 25 мкВ, во всех отведениях регистрируется высокочастотная низкоамплитудная активность. Такие ЭЭГ называют низкоамплитудными. Низкоамплитудные ЭЭГ указывают на преобладание в мозге десинхронизирующих влияний и являются вариантом нормы.
У части здоровых обследуемых вместо а-ритма регистрируют активность 14-18 Гц амплитудой около 50 мкВ в затылочных отделах, причём, подобно нормальному альфа-ритму, амплитуда снижается по направлению кпереди. Такая активность называется «быстрый а-вариант».
Очень редко (0,2% случаев) на ЭЭГ при закрытых глазах в затылочных отделах регистрируются регулярные, близкие к синусоидальным, медленные волны частотой 2,5-6 Гц и амплитудой 50-80 мкВ. Этот ритм имеет все остальные топографические и физиологические характеристики альфа-ритма и называется «медленный альфа-вариант». Не будучи связан с какой-либо органической патологией, он рассматривается как пограничный между нормой и патологией и может указывать на дисфункцию диэнцефальных неспецифических систем мозга.
Изменения электроэнцефалограммы в цикле бодрствование-сон
- Активное бодрствование (при умственной нагрузке, визуальном слежении, обучении и других ситуациях, требующих повышенной психической активности) характеризуется десинхронизацией нейрональной активности, на ЭЭГ преобладает низкоамплитудная высокочастотная активность.
- Расслабленное бодрствование - состояние обследуемого, покоящегося в удобном кресле или на постели с расслабленной мускулатурой и закрытыми глазами, не занятого какой-либо специальной физической или психической активностью. У большинства здоровых взрослых в этом состоянии на ЭЭГ регистрируется регулярный альфа-ритм.
- Первая стадия сна эквивалентна дремоте. На ЭЭГ наблюдают исчезновение альфа-ритма и появление одиночных и групповых низкоамплитудных дельта- и тета-колебаний и низкоамплитудной высокочастотной активности. Внешние стимулы вызывают вспышки альфа-ритма. Продолжительность стадии 1-7 мин. К концу этой стадии появляются медленные колебания амплитудой
- Вторая стадия сна характеризуется появлением сонных веретён и К-комплексов. Сонные веретёна - вспышки активности частотой 11-15 Гц, преобладающие в центральных отведениях. Продолжительность веретён - 0,5-3 с, амплитуда приблизительно 50 мкВ. Они связаны с срединными подкорковыми механизмами. К-комплекс - вспышка активности, типично состоящей из двухфазной высокоамплитудной волны с начальной негативной фазой, сопровождаемой иногда веретеном. Амплитуда его максимальна в области макушки, продолжительность не менее 0,5 с. К-комплексы возникают спонтанно или в ответ на сенсорные стимулы. В этой стадии эпизодически наблюдаются также вспышки полифазных высокоамплитудных медленных волн. Медленные движения глаз отсутствуют.
- Третья стадия сна: веретёна постепенно исчезают и появляются дельта- и тета-волны амплитудой более 75 мкВ в количестве от 20 до 50% времени эпохи анализа. В этой стадии часто трудно дифференцировать К-комплексы от дельта-волн. Сонные веретёна могут полностью исчезнуть.
- Четвёртая стадия сна характеризуется волнами частотой
- Во время сна у человека эпизодически возникают периоды десинхронизации на ЭЭГ - так называемый сон с быстрыми движениями глаз. В течение этих периодов регистрируется полиморфная активность с преобладанием высоких частот. Этим периодам на ЭЭГ соответствует переживание сновидения, падение мышечного тонуса с появлением быстрых движений глазных яблок и иногда быстрых движений конечностей. Возникновение этой стадии сна связано с работой регуляторного механизма на уровне моста мозга, её нарушения свидетельствуют о дисфункции этих отделов мозга, что имеет важное диагностическое значение.
Возрастные изменения электроэнцефалограммы
ЭЭГ недоношенного ребёнка в возрасте до 24-27 нед гестации представлена вспышками медленной дельта- и тета-активности, эпизодически комбинирующимися с острыми волнами, продолжительностью 2-20 с, на фоне низкоамплитудной (до 20-25 мкВ) активности.
У детей 28-32 нед гестации дельта- и тета-активность амплитудой до 100-150 мкВ становится более регулярной, хотя также может включать вспышки более высокоамплитудной тета-активности, перемежающиеся периодами уплощения.
У детей старше 32 нед гестации на ЭЭГ начинаются прослеживаться функциональные состояния. В спокойном сне наблюдают интермиттирующую высокоамплитудную (до 200 мкВ и выше) дельта-активность, сочетающуюся с тета-колебаниями и острыми волнами и перемежающуюся периодами относительно низкоамплитудной активности.
У доношенного новорождённого на ЭЭГ чётко определяются различия между бодрствованием с открытыми глазами (нерегулярная активность частотой 4-5 Гц и амплитудой 50 мкВ), активным сном (постоянная низкоамплитудная активность 4-7 Гц с наложением более быстрых низкоамплитудных колебаний) и спокойным сном, характеризующимся вспышками высокоамплитудной дельта-активности в комбинации с веретёнами более быстрых высокоамплитудных волн, перемежающихся низкоамплитудными периодами.
У здоровых недоношенных детей и доношенных новорождённых в течение первого месяца жизни наблюдают альтернирующую активность во время спокойного сна. На ЭЭГ новорождённых присутствуют физиологические острые потенциалы, характеризующиеся мультифокальностью, спорадичностью появления, нерегулярностью следования. Амплитуда их обычно не превышает 100-110 мкВ, частота возникновения в среднем составляет 5 в час, основное их количество приурочено к спокойному сну. Нормальными также считают относительно регулярно возникающие острые потенциалы в лобных отведениях, не превышающие по амплитуде 150 мкВ. Нормальная ЭЭГ зрелого новорождённого характеризуется наличием ответа в виде уплощения ЭЭГ на внешние стимулы.
В течение первого месяца жизни зрелого ребёнка исчезает альтернирующая ЭЭГ спокойного сна, на втором месяце появляются веретёна сна, организованная доминирующая активность в затылочных отведениях, достигающая частоты 4-7 Гц в возрасте 3 мес.
В течение 4-6-го месяцев жизни количество тета-волн на ЭЭГ постепенно увеличивается, а дельта-волн - уменьшается, так что к концу 6-го месяца на ЭЭГ доминирует ритм частотой 5-7 Гц. С 7-го по 12-й месяц жизни формируется альфа-ритм с постепенным уменьшением количества тета- и дельта-волн. К 12 мес доминируют колебания, которые можно охарактеризовать как медленный альфа-ритм (7-8,5 Гц). С 1 года до 7-8 лет продолжается процесс постепенного вытеснения медленных ритмов более быстрыми колебаниями (альфа- и бета-диапазона). После 8 лет на ЭЭГ доминирует альфа-ритм. Окончательное формирование ЭЭГ происходит к 16-18 годам.
Граничные значения частоты доминирующего ритма у детей
На ЭЭГ здоровых детей могут присутствовать избыточные диффузные медленные волны, вспышки ритмичных медленных колебаний, разряды эпилептиформной активности, так что с точки зрения традиционной оценки возрастной нормы даже у заведомо здоровых лиц в возрасте до 21 года к «нормальным» могут быть отнесены только 70-80% ЭЭГ.
С 3-4 и до 12 лет нарастает (с 3 до 16%) доля ЭЭГ с избыточными медленными волнами, а затем этот показатель достаточно быстро снижается.
Реакция на гипервентиляцию в форме появления высокоамплитудных медленных волн в возрасте 9-11 лет более выражена, чем в младшей группе. Не исключено, однако, что это связано с менее чётким выполнением пробы детьми младшего возраста.
Представленность некоторых вариантов ЭЭГ в здоровой популяции в зависимости от возраста
Уже упомянутая относительная стабильность характеристик ЭЭГ взрослого человека сохраняется приблизительно до 50 лет. С этого периода наблюдается перестройка спектра ЭЭГ, выражающаяся в уменьшении амплитуды и относительного количества альфа-ритма и нарастании количества бета- и дельта-волн. Доминирующая частота после 60-70 лет имеет тенденцию к снижению. В этом возрасте у практически здоровых лиц также появляются видимые при визуальном анализе тета- и дельта-волны.
Н.А. Ермоленко 1 , А.Ю. Ермаков 2 , И.А. Бучнева 3
1 -Воронежская Государственная медицинская академия им. Н.Н. Бурденко;
2 -Московский НИИ педиатрии и детской хирургии Росмедтехнологий;
3 -Воронежская областная детская клиническая больница №1
Открытие новой категории эпилепсий, возникающих вследствие локальной дисфункции коры, с региональными эпилептиформными разрядами на ЭЭГ и доброкачественным прогнозом в отношении исчезновения приступов, считается наиболее интересным вкладом в эпилептологию за последние 50 лет (Fejerman N. et al., 2007). Электроэнцефалографическим коррелятом этих состояний служат возраст-зависимые паттерны, по морфологии представляющие собой трехфазный электрический диполь с периодом острой волны более 70 мс, с последующей медленной волной и постоянной активацией во сне (Panayiotopoulos C.P., 2005). ЭЭГ-паттерны, известные в литературе как «роландические спайки» (Lundberg S. et al., 2003) или «доброкачественные фокальные эпилептиформные разряды детства» (Panayiotopoulos C.P., 2005), имеют тенденцию группироваться в серии, а в некоторых случаях занимать значительную часть записи ЭЭГ, регистрируясь практически непрерывно. Несмотря на употребление слова «доброкачественный» в названии единичного комплекса, продолженная активность паттернов ДЭРД может быть причиной психических, коммуникативных, познавательных, поведенческих и социальных нарушений у детей. Длительно персистирующая фокальная или диффузная эпилептиформная активность в виде паттернов ДЭРД с высоким индексом представленности на ЭЭГ во сне вызывает функциональный разрыв нейрональных связей, оказывает неблагоприятное влияние на развитие мозга во время критического периода синаптогенеза и служит причиной нейропсихологических расстройств, даже при отсутствии эпилептических приступов (Зенков Л.Р., 2007; Aarts J., 1984; Gobbi G., 2002). Поэтому эти состояния поздно диагностируются и имеют плохой прогноз.
Целью настоящего исследования было определение клинико-нейрофизиологических особенностей эпилепсий у детей, ассоциированных с продолженной эпилептиформной активностью во сне, и подходов к рациональной терапии этих состояний.
Пациенты и методы
Проведено предварительное скрининговое обследование 1862 детей в возрасте от 2 до 18 лет, поступавших в специализированное психоневрологическое отделение ГУЗ «ВОДКБ №1» по поводу эпилептических приступов и заболеваний нервной системы, не сопровождающихся эпилептическими приступами, в период с 2004 по 2007 гг.
Пациенты были обследованы с применением клинического метода, включая исследование неврологического статуса, нейропсихологическое тестирование с помощью методик А.Р. Лурия, проб Тулуз-Пьерона и Векслера, а также видео-ЭЭГ-мониторинга (с целью продолжительной непрерывной регистрации ЭЭГ и поведения пациента). Видео-ЭЭГ-мониторинг проводился с использованием компьютерного комплекса электроэнцефалографа-анализатора «Энцефалан 9», Медиком МТД, г. Таганрог с применением 19 каналов по международной системе «10–20» и дополнительного полиграфического канала ЭКГ. Продолжительность непрерывной записи варьировала от 4 до 8 ч. При регистрации эпилептиформной активности во сне подсчитывался индекс спайк-волновой насыщенности (ИСВ/SWI) (Patry G. et al., 1971; Tassinari C.A. et al., 1982). Нейрорадиологическое исследование проводилось на магнитно-резонансном томографе Siemens (с напряжением магнитного поля 1,5 Тесла).
Результаты
В процессе обследования ДЭРД были обнаружены в фоновой записи ЭЭГ и во сне у 229 (12,3%) пациентов, в том числе у 190 (22,6%) пациентов с верифицированным диагнозом эпилепсия (n=840) и у 39 (3,8%) пациентов с неврологической патологией (n=1022), не сопровождавшейся эпилептическими приступами (табл. 1).
Таблица 1. Частота встречаемости изменений на ЭЭГ с паттерном ДЭРД у больных с различными нозологическими формами
У детей с детским церебральным параличом (ДЦП), эпилепсией и мальформациями головного мозга паттерны ДЭРД на ЭЭГ регистрировались в 10,3%, 22,6% и 52% случаев соответственно, что в 2–10 раз превышало общепопуляционные значения (Panayiotopoulos C.P., 2005; Covanis A., 2009).
У пациентов с ДЦП в 46% случаев встречалась гемипаретическая форма, что значительно превышает общепопуляционную частоту встречаемости данной формы ДЦП - до 13% в популяции больных ДЦП (Ермоленко Н.А., 2006).
У 122 пациентов (53%) отмечалось сочетание эпилептических приступов и/или когнитивных расстройств с продолженной (диффузной или региональной) эпилептиформной активностью в виде паттернов ДЭРД во время медленного сна (ПЭМС), занимающей от 30% до 100% эпохи записи.
На основании данных нейрорадиологического обследования все дети с ПЭМС (n=122), были распределены в 2 группы: первую группу (группа I; n=62) составили пациенты, у которых не было выявлено структурных изменений в головном мозге и очаговой неврологической симптоматики - идиопатический вариант (соотношение девочек и мальчиков - 1,1:1); во вторую группу (группа II; n=60) вошли пациенты с очаговыми структурными изменениями в головном мозге и/или с очаговой неврологической симптоматикой - симптоматический вариант (соотношение девочек и мальчиков - 1:1,2).
У пациентов группы II в 22% случаев были верифицированы различные мальформации головного мозга; у 19% пациентов обнаружены арахноидальные кисты в области латеральных щелей, которые трудно дифференцируются от полимикрогирии по данным МРТ (Алиханов А.А., 2000), в 53,7% случаев выявлены изменения атрофического характера вследствие инсультов, перивентрикулярной лейкомаляции, внутриутробных инфекций; у 5,6% пациентов изменения на МРТ не были верифицированы, однако выявлялся выраженный неврологический дефицит в сочетании с нарушением формирования когнитивных функций. Комиссия ILAE по классификации и терминологии (2001) рекомендует трактовать эти случаи как вероятно симптоматические (Engel J., 2001). Преимущественной локализации очаговых изменений по отделам головного мозга выявлено не было, однако достоверно чаще (p<0,05) они обнаруживались в левой гемисфере по сравнению с правой (в 35,3% (n=18) и в 25,5% (n=13) случаев соответственно).
На основании данных анамнеза, клинического течения и результатов видео-ЭЭГ-мониторинга у пациентов с продолженной эпилептиформной активностью во сне (n=122), были верифицированы следующие нозологические формы: доброкачественная фокальная эпилепсия детского возраста с центрально-темпоральными спайками (18,9% (n=23) случаев); доброкачественная затылочная эпилепсия детского возраста с ранним дебютом (4,8% (n=6) пациентов); симптоматические фокальные эпилепсии (14,6% (n=18) пациентов); эпилепсия с электрическим эпилептическим статусом медленного сна (42,2% (n=52) больных), в том числе, с идиопатическим (35% (n=18) и симптоматическим (65% (n=34)) вариантами; эпилептиформная когнитивная дезинтеграция (17,1% (n=21) больных); синдром Ландау-Клеффнера (1,6% (n=2) пациентов).
Нормальная фоновая биоэлектрическая активность достоверно чаще отмечалась у пациентов группы I по сравнению с группой II (47% (n=29) и 20% (n=12), p<0,05 соответственно). В бодрствовании у пациентов в двух группах достоверно чаще регистрировалась региональная продолженная эпилептиформная активность с индексом от 15 до 85% (46% случаев) по сравнению с диффузной (24% больных), мультифокальной (20% пациентов) и унилатеральной (10% детей) активностью. У всех обследованных пациентов отмечалось усиление эпилептиформной активности во сне с появлением диффузной продолженной активности в 40% случаев и достоверным увеличением индекса эпилептиформной активности более 85% - у 41% пациентов, индексом 30–80% - у 59% больных.
Лобно-центрально-височная региональная акцентуация ПЭМС (77% (n=43) больных) регистрировалась достоверно чаще (p<0,05), чем теменно-затылочная и затылочная (14% (n=8) пациентов), лобная (9% (n=5 случаев) и центрально-височная (5% (n=3) детей). В 5% (n=6) случаев было зарегистрировано перемещение (шифт) эпилептиформной активности из одной гемисферы в другую при последующих записях ЭЭГ, без достоверной разницы между группами I и II. Смещение региона в пределах одной гемисферы отмечалось в 6% (n=7) случаев. У 11,6% пациентов зарегистрировано несовпадение региональной продолженной эпилептиформной активности на ЭЭГ со стороной локализации очаговых структурных изменений в головном мозге, выявленных при нейровизуализации.
У 89% пациентов, вошедших в исследование, были верифицированы когнитивные расстройства различной степени тяжести. У 11% детей наблюдалось аутистическое расстройство поведения без достоверной разницы между группами I и II (13% и 8% соответственно). У пациентов группы II достоверно чаще, по сравнению с пациентами группы I, верифицировались более тяжелые когнитивные расстройства с тотальным нарушением развития всех высших психических функций (60% и 24% соответственно, p<0,05), а также «преморбидная» задержка их формирования с раннего возраста (у 50%), с резким нарастанием когнитивного дефицита после появления эпилептических приступов и/или продолженной эпилептиформной активности на ЭЭГ.
Эпилептические приступы отсутствовали на протяжении всего периода наблюдения у 24,6% (n=30) больных. У пациентов группы I выявлено преобладание фокальных моторных приступов (100% в сравнении с 61%, p<0,05), связанных со сном (78% против 41%, p<0,05). Однако гемиклонические (22% в сравнении с 11%, p<0,05) и вторично-генерализованные судорожные приступы (30% в сравнении с 9%, p<0,05) чаще отмечались у пациентов группы II (рис. 1) и достоверно чаще возникали в бодрствовании, по сравнению с больными группы I (35% в сравнении с 17%, p<0,05). Ингибиторные моторные эпизоды отмечались у 23% (n=21) детей, достоверно чаще у больных в группе I, чем в группе II (76% (n=16) и 24% (n=5) соответственно, p
Установлено, что отдаленный прогноз заболевания (через 3 года после начала лечения) определяют следующие факторы: продолжительность эпилептиформной активности, возраст дебюта заболевания, степень выраженности когнитивных нарушений до начала лечения и эффективность антиэпилептической терапии в течение первого года. Дебют заболевания до 3 лет, продолженная эпилептиформная активность во сне, персистирующая более 1 года, преморбидная задержка формирования когнитивных функций, а также отсутствие клинико-электроэнцефалографической ремиссии в течение первого года терапии достоверно утяжеляют прогноз заболевания. Для таких параметров, как частота и характер эпилептических приступов, характер и стойкость ингибиторных симптомов, индекс эпилептиформной активности на ЭЭГ во сне и изменения на МРТ, статистически значимой связи с отдаленным прогнозом заболевания выявлено не было.
Анализ эффективности антиэпилептической терапии на первом году лечения выявил более высокую эффективность дуотерапии по сравнению с монотерапией, в связи с достоверно более высокой частотой достижения клинико-электроэнцефалографической ремиссии (23% в сравнении с 12%, p<0,05). Наиболее эффективными оказались комбинации вальпроатов с этосуксимидом и леветирацетамом, при этом, клинико-электроэнцефалографическая ремиссия была достигнута в 30–75% случаев (табл. 2). В лечении эпилепсии с эпилептическим электрическим статусом медленного сна был наиболее эффективен леветирацетам: на фоне приема леветирацетама в монотерапии у всех детей (n=3) зарегистрирована клинико-электроэнцефалографическая ремиссия. Однако сопоставление данных по эффективности для сравнения с вальпроатами не представляется возможным из-за малого числа наблюдений.
У пациентов, получавших карбамазепин (n=25) в стартовой монотерапии (n=16) и дуотерапии (n=9), было отмечено ухудшение состояния в виде аггравации и атипичной эволюции с последующим формированием резистентности к АЭП в 64% (n=16) случаев.
Полный фармакоиндуцированный регресс продолженной эпилептиформной активности паттернов ДЭРД отмечался в 29% (n=35) случаев, в 2 раза чаще у пациентов группы I - 37% (n=23) по сравнению с пациентами группы II - 20% (n=12). Средний возраст исчезновения продолженной эпилептиформной активности паттернов ДЭРД на фоне лечения составил 8,4?1,2 лет без достоверной разницы между группами I и II (8,3?1,6 и 8,7?1,7 лет соответственно).
Таблица 2. Дуотерапия у пациентов (n=52) с продолженной эпилептиформной активностью в виде паттернов ДЭРД на ЭЭГ во сне
| АЭП | Число детей | Клиническая ремиссия | Клинико-электроэнцефалографическая ремиссия | Отсутствие динамики | Ухудшение |
| Вальпроаты + этосуксимид | 31 (57%) | 13 (42%) | 9 (29%) | 8 (26%) | 1 (3%) |
| Вальпроаты + леветирацетам | 4 (7%) | 1 (25%) | 3 (75%) | - | - |
| Леветирацетам+ топирамат | 1 (2%) | 1(100%) | - | - | - |
| Вальпроаты + топирамат | 6 (11%) | 1 (17%) | - | 5 (83%) | - |
| Карбамазепин + бензодиазепины | 1 (2%) | 1 (100%) | - | - | - |
| Вальпроаты + бензодиазепины | 1 (2%) | 1 (100%) | - | - | - |
| Вальпроаты + Карбамазепин | 8 (15%) | - | - | 1 (12,5%) | 7 (87,5%) |
| Всего | 52 (100%) | 18 (35%) | 12 (23%) | 14 (27%) | 8 (15%) |
Обсуждение
Электроэнцефалографический паттерн ДЭРД, обнаруженный впервые у больных с роландической эпилепсией (Loiseau P. et al., 1961, 1967), выявлен также у пациентов с разнообразной неврологической патологией; в том числе, у пациентов с симптоматическим фокальными эпилепсиями, у которых структурные изменения в головном мозге в 41% случаев локализовались в эпилептогенных зонах, и, таким образом, могли быть самостоятельным источником эпилептогенеза с паттерном ДЭРД. Риск возникновения эпилепсий, ассоциированных с ПЭМС, у детей с ДЦП, особенно с гемипаретическими формами, и мальформациями головного мозга превышает общепопуляционные значения в 2–10 раз. Вместе с тем, у пациентов со структурным дефектом головного мозга не исключена «двойная патология» (Мухин К.Ю., 2005), в основе который лежит универсальный механизм фокальной корковой дисфункции (Doose H. et al., 1989). Доказано более доброкачественное течение идиопатических форм эпилепсии с паттерном ДЭРД по сравнению с симптоматическими.
Пятилетний катамнез пациентов с продолженной эпилептиформной активностью паттернов ДЭРД с индексом не менее 30% во сне показал эволюцию в эпилептическую энцефалопатию в 66% случаев: в 49% случаев - в эпилепсию с эпилептическим электрическим статусом во сне и в 17% - в когнитивную эпилептиформную дезинтеграцию. Таким образом, спайк-волновый индекс более 30% на ЭЭГ сна у детей, даже без клинических проявлений эпилептических приступов, служит показанием к назначению антиэпилептических препаратов.
Доказано, что стартовая терапия и время ее назначения имеют решающее значение для отдаленного прогноза в отношении сохранности или восстановления когнитивных функций у детей и подростков. Наиболее эффективными являются комбинации вальпроатов с этосуксимидом или леветирацетамом в дуотерапии.
Литература :
- Алиханов А.А. Методы нейровизуализации в диагностике эпилепсии у детей // Эпилептология детского возраста: руководство для врачей / под ред. А.С. Петрухина. - М.: Медицина, 2000. - С. 407–501.
- Дюк В . Обработка данных на ПК в примерах - СПб: Питер, 1997. - 240 с.
- Ермоленко Н.А . Варианты психоневрологического развития в норме и патологии у детей первых пяти лет жизни: автореф. дис. … д-ра мед. наук. - Воронеж, 2006. - 47 с.
- Мухин К.Ю., Петрухин А.С., Миронов М.Б., Холин А.А., Глухова Л.Ю., Пилия С.В., Волкова Э.Ю., Головтеев А.Л., Пылаева О.А. Эпилепсия с электрическим эпилептическим статусом медленного сна: диагностические критерии, дифференциальный диагноз и подходы к терапии. - М., 2005. - 32 с.
- Covanis A . Panayiotopoulos syndrome // Epilepsy in modern medicine: proceedings of the conference. - M., 2009. - P. 250–258.
- Doose H., Baier W.K . Benign partial epilepsy and related conditions: Multifactorial pathogenesis with hereditary impairment of brain maturation // Eur. J. Pediat. - 1989. - V. 149. - P. 152–158.
- Engel J.Jr . A proposed diagnostic scheme for people with epileptic seizures and with epilepsy: Report of the ILAE Task Force on Classification and Terminology // Epilepsia. - 2001. - V. 42. - P. 796–803.
- Fejerman N., Caraballo R., Definition of syndromes, seizure types and nosologic spectrum. / In: Fejerman N., Caraballo R. (Eds). Benign focal epilepsies in infancy, childhood and adolescence. - France: John Libbey, 2007. - 266–15.
- Lundberg S., Eeg-Olofsson O . Rolandic epilepsy: a challenge in terminology and classification // Eur J Paediatr Neurol. - 2003. - V. 7. - P. 239–241.
- Panayiotopoulos C.P. Benign childhood focal seizures and related epileptic syndromes / In: C.P. Panayiotopoulos The Epilepsies: Seizures, Syndromes and Management. - 2005. - P. 223–269.
- Patry G., Lyagoubi S., Tassinari C.A. Subclinical electrical status epilepticus induced by sleep in children // Neurol. - 1971. - V. 24. - P. 242–252.
- Tassinari C.A., Bureau M., Dravet C., Roger J., Daniele-Natale O . Electrical status epilepticus during sleep in children (ESES) / In: Sterman M.B., Shouse M.M., Passouant P. (eds). Sleep and epilepsy. - San Diego: Academic Press, 1982. - P. 465–479.