В данной статье можно ознакомиться с инструкцией по применению лекарственного препарата Превенар 13 . Представлены отзывы посетителей сайта - потребителей данного лекарства, а также мнения врачей специалистов по использованию Превенара в своей практике. Большая просьба активнее добавлять свои отзывы о препарате: помогло или не помогло лекарство избавиться от заболевания, какие наблюдались осложнения и побочные эффекты, возможно не заявленные производителем в аннотации. Аналоги Превенара 13 при наличии имеющихся структурных аналогов. Использование для профилактики пневмококковой инфекции и вакцинации у взрослых, детей (в том числе грудничков и новорожденных), а также при беременности и кормлении грудью. Состав препарата.
Превенар 13 - вакцина для профилактики пневмококковых инфекций.
Иммунологические свойства
Введение вакцины Превенар 13 вызывает выработку антител к капсулярным полисахаридам Streptococcus pneumoniae (стрептококк), обеспечивая тем самым специфическую защиту от инфекций, вызываемых включенными в вакцину 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F серотипами пневмококка.
Согласно рекомендациям ВОЗ для новых конъюгированных пневмококковых вакцин определена эквивалентность иммунного ответа Превенар 13 по трем критериям: процент пациентов, достигших концентрации специфических антител IgG более 0.35 мкг/мл; средние геометрические концентрации (СГК) иммуноглобулинов и опсонофагоцитарная активность (ОФА) бактерицидных антител (ОФА титр более 1:8 и средние геометрические титры (СГТ)). Для взрослых лиц не определен защитный уровень противопневмококковых антител и используется серотип-специфическая ОФА (СГТ).
Вакцина Превенар 13 включает до 90% серотипов, являющихся причиной инвазивных пневмококковых инфекций (ИПИ), в том числе устойчивых к лечению антибиотиками.
Иммунный ответ при использовании трех или двух доз в серии первичной вакцинации
После введения трех доз Превенар 13 при первичной вакцинации детей в возрасте до 6 месяцев отмечен значительный подъем уровня антител ко всем серотипам вакцины.
После введения двух доз при первичной вакцинации Превенар 13 в рамках массовой иммунизации детей той же возрастной группы также отмечается значительный подъем титров антител ко всем компонентам вакцины, для серотипов 6В и 23F уровень IgG более 0.35 мкг/мл определялся у меньшего процента детей. Вместе с тем, отмечен выраженный бустерный ответ на ревакцинацию (повторную вакцинацию) для всех серотипов. Формирование иммунной памяти показано для обеих указанных выше схем вакцинации. Вторичный иммунный ответ на ревакцинирующую дозу у детей второго года жизни при использовании трех или двух доз в серии первичной вакцинации сравним для всех 13 серотипов.
При вакцинации недоношенных детей (родившихся при сроке гестации менее 37 недель), включая глубоко-недоношенных детей (родившихся при сроке гестации менее 28 недель), начиная с возраста двух месяцев, отмечено, что уровень защитных специфических противопневмококковых антител и их ОФА после законченного курса вакцинации достигали значений выше защитных у 87-100% привитых ко всем тринадцати включенным в вакцину серотипам.
Иммуногенность у детей и подростков в возрасте от 5 до 17 лет
Дети в возрасте от 5 до 10 лет, которые до этого получили как минимум одну дозу пневмококковой 7-валентной конъюгированной вакцины, а также ранее не вакцинированные дети и подростки в возрасте от 10 до 17 лет, получив по одной дозе вакцины Превенар 13, продемонстрировали иммунный ответ на все 13 серотипов, эквивалентный таковому у детей 12-15 месяцев, вакцинированных четырьмя дозами препарата Превенар 13.
Однократное введение Превенар 13 детям в возрасте 5-17 лет способно обеспечить необходимый иммунный ответ на все серотипы возбудителя, входящие в состав вакцины.
Эффективность Превенар 13
Инвазивная пневмококковая инфекция (ИПИ)
После внедрения Превенар в схеме 2+1 (две дозы на первом году жизни и ревакцинация однократно на втором году жизни) через четыре года при 94% охвате вакцинацией отмечено 98% (95% ДИ: 95; 99) снижение частоты ИПИ, вызванных вакцин-специфичными серотипами. После перехода на Превенар 13 отмечено дальнейшее снижение частоты ИПИ, вызванных вакцин-специфичными дополнительными серотипами, от 76% у детей в возрасте младше 2 лет до 91% у детей в возрасте 5-14 лет.
Серотип-специфическая эффективность в отношении ИПИ по дополнительным серотипам Превенар 13 у детей в возрасте до 5 лет, колебалась от 68% до 100% (серотип 3 и 6А, соответственно) и составила 91% для серотипов 1, 7F и 19А), при этом не наблюдалось случаев ИПИ, вызванных серотипом 5. После включения Превенар 13 в национальные программы иммунизации частота регистрации ИПИ, вызванных серотипом 3, снизилась на 68% (95% ДИ 6-89%) у детей до 5 лет. В исследовании случай-контроль, выполненном в данной возрастной группе, показано снижение заболеваемости ИПИ, вызванных серотипом 3, на 79.5% (95% ДИ 30.3-94.8).
Средний отит (СО)
После внедрения вакцинации Превенар с последующим переходом на Превенар 13 по схеме 2+1 выявлено снижение на 95% частоты возникновения СО, вызванных серотипами 4, 6В, 9V, 14, 18С, 19F, 23F и серотипа 6А, а также на 89% снижение частоты СО, вызванных серотипами 1, 3, 5, 7F и 19A.
Пневмония
При переходе с Превенар на Превенар 13 отмечено 16% снижение частоты всех случаев внебольничной пневмонии (ВБП) у детей в возрасте от 1 месяца до 15 лет. Случаи ВБП с плевральным выпотом уменьшились на 53% (р менее 0.001), пневмококковые ВБП снизились на 63% (р менее 0.001). Во второй год после внедрения Превенар 13 отмечено 74% снижение частоты ВБП, вызванных 6 дополнительными серотипами Превенар 13. У детей в возрасте младше 5 лет после внедрения вакцинации Превенар 13 по схеме 2+1 отмечено 68% (95% ДИ: 73; 61) снижение числа амбулаторных визитов и 32% (95% ДИ: 39; 22) уменьшение числа госпитализаций по поводу альвеолярной ВБП любой этиологии.
Носительство и популяционный эффект
Продемонстрирована эффективность Превенар 13 в отношении снижения носительства в носоглотке вакцин-специфичных серотипов, как общих с вакциной Превенар (4, 6В, 9V, 14, 18С, 19F, 23F), так и 6 дополнительных (1, 3, 5, 6А, 7А, 19А) и родственного серотипа 6С.
Популяционный эффект (серотип-специфическое снижение заболеваемости невакцинированных лиц) отмечен в странах, где Превенар 13 используется в рамках массовой иммунизации в течение более 3 лет с высоким охватом вакцинацией и соблюдением схемы иммунизации. У невакцинированных Превенар 13 лиц 65 лет и старше продемонстрировано уменьшение ИПИ на 25%, при этом ИПИ, вызванные серотипами 4, 6В, 9V, 14, 18С, 19F, 23F, снизились на 89% и на 64% уменьшились ИПИ, обусловленные 6 дополнительными серотипами (1, 3, 5, 6А, 7А, 19А). Частота инфекций, вызванных серотипом 3, снизилась на 44%, серотипом 6А - на 95%, серотипом 19А - на 65%.
Иммуногенность вакцины Превенар 13 у взрослых
Клинические исследования Превенар 13 предоставляют данные по иммуногенности у взрослых в возрасте 18 лет и старше, включая лиц в возрасте от 65 лет и тех, кто ранее получил вакцинацию одной или более дозами полисахаридной пневмококковой 23-валентной вакциной (ППВ23) за 5 лет до включения в исследование. В каждом исследовании были здоровые взрослые и иммунокомпетентные пациенты с хроническими заболеваниями в стадии компенсации, включая сопутствующую патологию, формирующую повышенную восприимчивость к пневмококковой инфекции (хронические сердечно-сосудистые заболевания, хронические заболевания легких, включая астму; заболевания почек и сахарный диабет, хронические заболевания печени, включая алкогольные поражения), и взрослых с социальными факторами риска - курением и злоупотреблением алкоголем. Иммуногенность и безопасность Превенар 13 продемонстрирована для взрослых в возрасте 18 лет и старше, включая пациентов, ранее вакцинированных ППВ23. Иммунологическая эквивалентность установлена для 12 общих с ППВ23 серотипов. Кроме того, для 8 общих с ППВ23 серотипов и по серотипу 6A, уникального для вакцины Превенар 13, продемонстрирован статистически значимо более высокий иммунный ответ на Превенар 13. У взрослых в возрасте 18-59 лет СГТ опсонофагоцитарной активности (ОФА СГТ) ко всем 13 серотипам Превенар 13 были не ниже таковых у взрослых в возрасте 60-64 лет. Более того, лица в возрасте 50-59 лет дали статистически более высокий иммунный ответ на 9 из 13 серотипов по сравнению с людьми в возрасте 60-64 лет.
Продемонстрирована клиническая эффективность Превенар 13 в рандомизированном двойном слепом плацебо-контролируемом исследовании CAPITA (более 84 000 пациентов) в отношении внебольничной пневмококковой пневмонии (ВПП) у взрослых в возрасте 65 лет и старше: 45% в отношении первого эпизода ВПП, вызванной серотипами, перекрываемыми Превенар 13 (инвазивной и неинвазивной); 75% в отношении инвазивных инфекций, вызванных серотипами, перекрываемыми Превенар 13.
Иммунный ответ у взрослых, ранее вакцинированных ППВ23
У взрослых в возрасте 70 лет и старше, однократно вакцинированных ППВ23 более 5 лет назад, введение Превенар 13 продемонстрировало иммунологическую эквивалентность для 12 общих серотипов по сравнению с ответом на ППВ23, при этом на 10 общих серотипов и серотип 6А иммунный ответ на Превенар 13 был статистически значимо выше по сравнению с ответом на ППВ23. Превенар 13 дает более выраженный иммунный ответ по сравнению с ревакцинацией ППВ23.
Иммунный ответ в особых группах пациентов
Пациенты с описанными ниже заболеваниями подвержены повышенному риску пневмококковой инфекции.
Серповидноклеточная анемия
В открытом несравнительном исследовании с участием 158 детей и подростков в возрасте более 6 и менее 18 лет с серповидноклеточной анемией, ранее вакцинированных одной или более дозами ППВ23 как минимум за 6 месяцев до включения в исследование показало, что введение первой дозы Превенар 13 при двукратной иммунизации с интервалом 6 месяцев приводило к статистически значимо высокому иммунному ответу (СГКIgG к каждому серотипу, определяемые методом иммуноферментного анализа (ИФА), и ОФА СГТ к каждому серотипу). После ведения второй дозы иммунный ответ был сопоставим с таковыми после первой дозы препарата.
ВИЧ-инфекция
ВИЧ-инфицированные дети и взрослые с количеством CD4 более 200 клеток/мкл (в среднем 717.0 клеток/мкл), вирусной нагрузкой менее 50 000 копий/мл (в среднем 2090.0 копий/мл), с отсутствием активных СПИД-ассоциированных заболеваний и ранее не получавшие вакцинации пневмококковой вакциной, получали 3 дозы Превенар 13. Показатели IgG СГК и ОФА были достоверно выше после первой вакцинации Превенар 13 по сравнению с довакцинальным уровнем. На вторую и третью дозы (через 6 и 12 месяцев) развивался более высокий иммунный ответ, чем после однократной вакцинации Превенар 13.
Трансплантация гемопоэтических стволовых клеток
Дети и взрослые, которым была выполнена аллогенная трансплантация гемопоэтических стволовых клеток (ТГСК), в возрасте более 2 лет с полной гематологической ремиссией основного заболевания или с удовлетворительной частичной ремиссией в случае лимфомы и миеломы, получали три дозы Превенар 13 с интервалом не менее 1 месяца между дозами. Первую дозу препарата вводили через 3-6 месяцев после ТГСК. Четвертую (бустерную) дозу Превенар 13 вводили через 6 месяцев после третьей дозы. В соответствии с общими рекомендациями, разовую дозу ППВ23 вводили через 1 месяц после четвертой дозы Превенар 13. Титры функционально активных антител (ОФАСГТ) в этом исследовании не определялись. Введение Превенар 13 вызывало повышение СГК серотип-специфических антител после каждой дозы. Иммунный ответ на бустерную дозу Превенар 13 был значимо выше для всех серотипов по сравнению с ответом на первичную серию иммунизации.
Состав
Пневмококковые конъюгаты (полисахарид + CRM197) серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F, 23F + вспомогательные вещества.
Показания
Профилактика пневмококковых инфекций, включая инвазивные (в т.ч. менингит, бактериемию, сепсис, тяжелые пневмонии) и неинвазивные (внебольничные пневмонии и средние отиты) формы заболеваний, вызываемые Streptococcus pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F с 2-х месяцев жизни и далее без ограничения по возрасту:
- в рамках национального календаря профилактических прививок;
- у лиц групп повышенного риска развития пневмококковой инфекции.
Вакцинация проводится в рамках национального календаря профилактических прививок согласно утвержденным срокам, а также лицам групп риска по развитию пневмококковой инфекции: с иммунодефицитными состояниями, в т.ч. ВИЧ-инфекцией, онкологическими заболеваниями, получающим иммуносупрессивную терапию; с анатомической/функциональной аспленией; с установленным кохлеарным имплантом или планирующиеся на эту операцию; пациентам с подтеканием спинномозговой жидкости; с хроническими заболеваниями легких, сердечно-сосудистой системы, печени, почек и сахарным диабетом; больным бронхиальной астмой; недоношенным детям; лицам, находящимся в организованных коллективах (детские дома, интернаты, армейские коллективы); реконвалесцентам острого среднего отита, менингита, пневмонии; длительно и часто болеющим детям; пациентам, инфицированным микобактерией туберкулеза; всем лицам старше 50 лет; табакокурильщикам.
Формы выпуска
Суспензия для внутримышечного введения (уколы в ампулах или шприцах для инъекций) (иногда ошибочно называют раствор).
Инструкция по применению и схема вакцинации
Способ введения
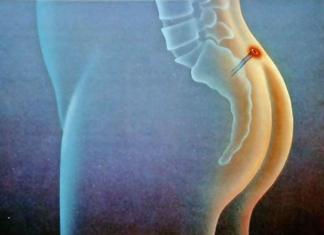
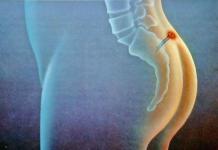
Вакцину вводят в разовой дозе 0.5 мл внутримышечно. Детям первых лет жизни прививки проводят в верхненаружную поверхность средней трети бедра, лицам старше 2-х лет - в дельтовидную мышцу плеча.
Перед применением шприц с вакциной Превенар 13 необходимо хорошо встряхнуть до получения гомогенной суспензии. Не использовать, если при осмотре содержимого шприца выявляются инородные частицы.
Не вводить Превенар 13 внутрисосудисто и внутримышечно в ягодичную область!
Схема вакцинации
Дети 2-6 месяцев:
Индивидуальная иммунизация: 3 дозы с интервалом не менее 4 недель между введениями. Первую дозу можно вводить с 2-х месяцев. Ревакцинация однократно в 11-15 месяцев.
Массовая иммунизация детей: 2 дозы с интервалом не менее 8 недель между введениями. Ревакцинация однократно в 11-15 месяцев.
Дети 7-11 месяцев:
2 дозы с интервалом не менее 4 недель между введениями. Ревакцинация однократно на втором году жизни.
Дети 12-23 месяцев:
2 дозы с интервалом не менее 8 недель между введениями.
Дети 2 года и старше:
Однократно.
Дети, ранее вакцинированные Превенар
Вакцинация против пневмококковой инфекции, начатая 7-валентной вакциной Превенар, может быть продолжена Превенар 13 на любом этапе схемы иммунизации.
Лица в возрасте 18 лет и старше
Превенар 13 вводится однократно. Необходимость ревакцинации Превенар 13 не установлена. Решение об интервале между введением вакцин Превенар 13 и ППВ23 следует принимать в соответствии с официальными методическими рекомендациями.
Особые группы пациентов
У пациентов после трансплантации гемопоэтических стволовых клеток рекомендуется серия иммунизации, состоящая из 4 доз препарата Превенар 13 по 0,5 мл. Первая серия иммунизации состоит из введения трех доз препарата: первая доза вводится с третьего по шестой месяц после трансплантации. Интервал между введениями должен составлять 1 месяц. Ревакцинирующую дозу рекомендуется вводить через 6 месяцев после введения третьей дозы.
Недоношенным детям рекомендуется четырехкратная вакцинация. Первая серия иммунизации состоит из 3-х доз. Первую дозу следует вводить в возрасте 2 месяцев независимо от массы тела ребенка с интервалом 1 месяц между дозами. Введение четвертой (бустерной) дозы рекомендуется в возрасте 12-15 месяцев.
Пожилые пациенты
Иммуногенность и безопасность вакцины Превенар 13 были подтверждены для пожилых пациентов.
Побочное действие
Безопасность вакцины Превенар 13 изучена у здоровых детей (4429 детей/14267 доз вакцины) в возрасте от 6 недель до 11-16 месяцев и 100 детях, родившихся недоношенными (в сроке менее 37 недель гестации). Во всех исследованиях Превенар 13 применялся одновременно с другими вакцинами (в том числе АДС, АКДС), рекомендованными для данного возраста.
Кроме того, безопасность вакцины Превенар 13 оценена у 354 детей в возрасте 7 месяцев - 5 лет, ранее не вакцинированных ни одной из пневмококковых конъюгированных вакцин. Наиболее частыми нежелательными реакциями были реакции в месте инъекции, повышение температуры, раздражительность, снижение аппетита и нарушение режима сна. У детей старшего возраста при первичной вакцинации Превенар 13 наблюдалась более высокая частота местных реакций, чем у детей первого года жизни.
При вакцинации Превенар 13 недоношенных детей (родившихся в сроке гестации менее 37 недель), включая глубоко недоношенных детей, родившихся при сроке беременности менее 28 недель и детей с экстремально низкой массой тела (менее 500 г) характер, частота и выраженность поствакцинных реакций (после прививки Превенар 13) не отличались от таковых у доношенных детей.
У лиц в возрасте 18 лет и старше отмечалось меньшее количество побочных эффектов вне зависимости от предшествующих вакцинаций. Однако частота развития реакций была такая же, как и у привитых более молодого возраста.
В целом частота побочных эффектов была одинакова у пациентов возрастных групп 18 - 49 лет и у пациентов старше 50 лет, за исключением рвоты. Данный побочный эффект у пациентов в возрасте 18 - 49 лет встречался чаще, чем у пациентов в возрасте старше 50 лет.
У взрослых пациентов с ВИЧ-инфекцией отмечалась такая же частота побочных реакций, как и у пациентов в возрасте 50 лет и старше, за исключением лихорадки и рвоты, которые наблюдались очень часто и тошноты, которая наблюдалась часто.
У пациентов после трансплантации гемопоэтических стволовых клеток частота развития побочных реакций была такая же, как и у здоровых взрослых пациентов, за исключением лихорадки и рвоты, которые у пациентов после трансплантации встречались очень часто. У детей и подростков с серповидноклеточной анемией, ВИЧ-инфекцией или после трансплантации гемопоэтических стволовых клеток отмечалась такая же частота побочных реакций, как и у здоровых пациентов в возрасте 2-17 лет, за исключением головной боли, рвоты, диареи, лихорадки, утомляемости, артралгии и миалгии, которые у таких пациентов встречались как очень частые.
Нежелательные реакции, выявленные в клинических исследованиях Превенар 13
- гипертермия;
- раздражительность;
- покраснение кожи, болезненные ощущения, уплотнение или отек размером 2.5-7.0 см в месте инъекции (после ревакцинации и/или у детей в возрасте 2-5 лет);
- тошнота, рвота (у пациентов возрасте 18 - 49 лет);
- диарея;
- сыпь;
- сонливость;
- ухудшение сна;
- ухудшение аппетита;
- головная боль;
- генерализованные новые или обострение имеющихся болей в суставах и мышечных болей;
- озноб;
- утомляемость;
- плаксивость;
- судороги (включая фебрильные судороги);
- реакции гиперчувствительности в месте инъекции (крапивница, дерматит, зуд);
- случаи гипотонического коллапса;
- приливы крови к лицу;
- одышка;
- бронхоспазм;
- отек Квинке разной локализации, включая отек лица;
- анафилактическая/анафилактоидная реакция;
- лимфаденопатия в области места инъекции.
Нежелательные явления, наблюдавшиеся в других возрастных группах, также могут проявляться у детей и подростков в возрасте 5-17 лет. Однако в клинических исследованиях их не отмечали из-за небольшого количества участников.
Значимых различий в частоте развития побочных эффектов у взрослых, ранее вакцинированных и невакцинированных ППВ23, не отмечено.
Противопоказания
- повышенная чувствительность на предшествующее введение Превенар 13 или Превенар (в т.ч. анафилактический шок, тяжелые генерализованные аллергические реакции);
- повышенная чувствительность к дифтерийному анатоксину и/или вспомогательным веществам;
- острые инфекционные или неинфекционные заболевания, обострения хронических заболеваний. Вакцинацию проводят после выздоровления или в период ремиссии.
Применение при беременности и кормлении грудью
Безопасность применения вакцины во время беременности и грудного вскармливания не установлена. Данные о применении Превенар 13 во время беременности отсутствуют. Отсутствуют данные о выделении антигенов вакцины или поствакцинальных антител с грудным молоком при лактации.
Применение у детей
Возможно использование вакцины у детей, в том числе грудничков согласно возрастным дозировкам и схемам прививки, указанным выше.
Особые указания
С учетом редких случаев анафилактических реакций, имеющихся при применении любых вакцин, вакцинированный пациент должен находиться под медицинским наблюдением в течение как минимум 30 минут после иммунизации. Места проведения иммунизации должны быть обеспечены средствами противошоковой терапии.
Вакцинацию недоношенных (как и доношенных) детей следует начинать со второго месяца жизни (паспортный возраст). При принятии решения о вакцинации недоношенного ребенка (родившегося в сроке до 37 недель беременности), особенно имеющего в анамнезе незрелость дыхательной системы, необходимо учесть, что польза иммунизации против пневмококковой инфекции у данной группы пациентов особенно высока и не следует ни отказываться от вакцинации, ни переносить ее сроки. В связи с потенциальным риском апноэ, имеющимся при применении любых вакцин, первая вакцинация Превенар 13 недоношенного ребенка возможна под врачебным наблюдением (не менее 48 ч) в стационаре на втором этапе выхаживания.
Как и другие внутримышечные инъекции, пациентам с тромбоцитопенией и/или другими нарушениями свертывающей системы крови и/или в случае лечения антикоагулянтами, вакцинация Превенар 13 должна проводиться с осторожностью, при условии стабилизации состояния пациента и достижения контроля гемостаза. Возможно подкожное введение вакцины Превенар 13 данной группе пациентов.
Превенар 13 не может обеспечить профилактику заболеваний, вызванных пневмококками других серотипов, антигены которых не входят в состав данной вакцины.
Детям из групп высокого риска в возрасте младше 2 лет следует проводить первичную вакцинацию Превенар 13 в соответствии с возрастом. У пациентов с нарушением иммунореактивности вакцинация может сопровождаться пониженным уровнем антителообразования.
Применение Превенар 13 и ППВ23
Для формирования иммунной памяти иммунизацию против пневмококковой инфекции предпочтительно начинать с вакцины Превенар 13. Необходимость ревакцинации не определена. Лицам из групп высокого риска для расширения охвата серотипов в последующем может быть рекомендовано введение ППВ23. Имеются данные клинических исследований вакцинации ППВ23 через 1 год, а также через 3,5-4 года после вакцины Превенар 13. При интервале между вакцинациями 3.5-4 года иммунный ответ на ППВ23 был выше без изменений реактогенности.
Детям, привитым вакциной Превенар 13 и входящим в группу высокого риска (например, с серповидно-клеточной анемией, аспленией, ВИЧ-инфекцией, хроническим заболеванием или иммунной дисфункцией), ППВ23 вводится с интервалом не менее 8 недель. В свою очередь пациенты, входящие в группу высокого риска пневмококковой инфекции (пациенты с серповидно-клеточной анемией или ВИЧ-инфекцией), включая пациентов, ранее вакцинированных одной или несколькими дозами ППВ23, могут получить как минимум одну дозу вакцины Превенар 13.
Решение об интервале между введениями ППВ23 и вакцины Превенар 13 должно приниматься в соответствии с официальными рекомендациями. В ряде стран (США) рекомендуемый интервал составляет не менее 8 недель (до 12 месяцев). Если пациент ранее был привит ППВ23, Превенар 13 следует вводить не ранее чем через 1 год. В РФ вакцинация ПКВ13 рекомендована всем взрослым лицам, достигшим возраста 50 лет, и пациентам групп риска, причем вакцина ПКВ13 вводится первой с возможной последующей ревакцинацией ППВ23 с интервалом не менее 8 недель.
Превенар 13 содержит менее 1 ммоль натрия (23 мг) на дозу, т. е. практически не содержит натрия.
В пределах указанного срока годности препарат Превенар 13 сохраняет стабильность в течение 4 дней при температуре до 25°C. По окончании этого периода препарат следует либо немедленно использовать, либо вернуть в холодильник. Эти данные не являются указаниями по условиям хранения и транспортирования, но могут являться основанием для решения по использованию вакцины в случае временных колебаний температуры при хранении и транспортировании.
Влияние на способность управлять транспортным средством или потенциально опасными механизмами
Превенар 13 не оказывает или оказывает незначительное влияние на способность управлять автомобилем и пользоваться техникой. Однако, некоторые побочные реакции могут временно влиять на способность управлять транспортным средством и потенциально опасными механизмами.
Лекарственное взаимодействие
Данные о взаимозаменяемости Превенар 13 на другие пневмококковые конъюгированные вакцины отсутствуют. При одновременной иммунизации Превенар 13 и другими вакцинами инъекции делаются в разные участки тела.
Дети в возрасте 2 месяцев - 5 лет
Превенар 13 сочетается с любыми другими вакцинами, входящими в календарь иммунизации детей первых лет жизни, за исключением БЦЖ. Одновременное введение вакцины Превенар 13 с любыми следующими антигенами, входящими в состав как моновалентных, так и комбинированных вакцин: дифтерийным, столбнячным, бесклеточным или цельноклеточным коклюшным, Haemophilus influenzae тип b, полиомиелитным, гепатита А, гепатита B, коревым, эпидемического паротита, краснухи, ветряной оспы и ротавирусной инфекции - не влияет на иммуногенность данных вакцин. В связи с более высоким риском развития фебрильных реакций детям с судорожными расстройствами, в т.ч. с фебрильными судорогами в анамнезе, а также получающим Превенар 13 одновременно с цельноклеточными коклюшными вакцинами, рекомендуется симптоматическое назначение жаропонижающих средств. При совместном применении Превенар 13 и Инфанрикс Гекса частота фебрильных реакций совпала с таковой для совместного применения Превенар (ПКВ7) и Инфанрикс Гекса. Повышение частоты репортирования судорог (с и без повышения температуры тела) и гипотонически-гипореспонсивных эпизодов (ГГЭ) наблюдалось при совместном использовании Превенар 13 и Инфанрикс Гекса. Применение жаропонижающих препаратов следует начинать в соответствии с местными рекомендациями по лечению детей с судорожными расстройствами или детей с наличием в анамнезе фебрильных судорог, и у всех детей, которым вводили Превенар 13 одновременно с вакцинами, содержащими цельноклеточный коклюшный компонент.
Согласно данным постмаркетингового исследования профилактического применения жаропонижающих средств на иммунный ответ на введение вакцины Превенар 13, предполагается, что профилактическое назначение ацетаминофена (парацетамола) может снижать иммунный ответ на серию первичной вакцинации Превенар 13. Иммунный ответ на ревакцинацию Превенар 13 в 12 месяцев при профилактическом применении парацетамола не меняется. Клиническое значение этих данных неизвестно.
Дети и подростки в возрасте 6 - 17 лет
Данные о применении препарата Превенар 13 одновременно с вакциной против папилломавирусной инфекции человека, конъюгированной менингококковой вакциной, вакциной против столбняка, дифтерии и коклюша, клещевого энцефалита отсутствуют.
Лица в возрасте 18-49 лет
Данные по одновременному применению препарата Превенар 13 с другими вакцинами отсутствуют.
Лица в возрасте 50 лет и старше
Вакцина Превенар 13 может использоваться совместно с тривалентной инактивированной вакциной против сезонного гриппа (ТГВ). При комбинированном использовании вакцин Превенар 13 и ТГВ, иммунные ответы на вакцину ТГВ совпадали с ответами, полученными при применении одной вакцины ТГВ, иммунные ответы на вакцину Превенар 13 были ниже, чем при использовании только Превенар 13. Клиническая значимость данного факта неизвестна. Частота развития местных реакций не увеличивалась при одновременном введении Превенар 13 с инактивированной гриппозной вакциной, тогда как частота общих реакций (головная боль, озноб, сыпь, снижение аппетита, боли в суставах и мышцах) при одновременной иммунизации повышалась. Одновременное применение с другими вакцинами не исследовалось.
Аналоги лекарственного препарата Превенар 13
Структурные аналоги по действующему веществу:
- Пневмо 23;
- Превенар (вакцина пневмококковая полисахаридная конъюгированная адсорбированная);
- Синфлорикс (Вакцина 10-валентная пневмококковая полисахаридная, конъюгированная с D-протеином нетипируемой Haemophilus influenzaе, столбнячным и дифтерийным анатоксинами, адсорбированная);
- Пневмовакс 23 (Вакцина пневмококковая, поливалентная).
При отсутствии аналогов лекарства по действующему веществу, можно перейти по ссылкам ниже на заболевания, от которых помогает соответствующий препарат, и посмотреть имеющиеся аналоги по лечебному воздействию.
Производитель: «НПО Петровакс Фарм» Россия
Код АТС: J07AL02
Фарм группа:
Форма выпуска: Жидкие лекарственные формы. Суспензия для инъекций.

Общие характеристики. Состав:
Состав на одну дозу (0,5 мл):
Активные вещества:
Пневмококковые конъюгаты (полисахарид - CRM197):
- Полисахарид серотипа 1 2,2 мкг
- Полисахарид серотипа 3 2,2 мкг
- Полисахарид серотипа 4 2,2 мкг
- Полисахарид серотипа 5 2,2 мкг
- Полисахарид серотипа 6A 2,2 мкг
- Полисахарид серотипа 6B 4,4 мкг
- Полисахарид серотипа 7F 2,2 мкг
- Полисахарид серотипа 9V 2,2 мкг
- Полисахарид серотипа 14 2,2 мкг
- Олигосахарид серотипа 18C 2,2 мкг
- Полисахарид серотипа 19A 2,2 мкг
- Полисахарид серотипа 19F 2,2 мкг
- Полисахарид серотипа 23F 2,2 мкг
- Белок-носитель CRM197 ~32 мкг
Вспомогательные вещества:
алюминия фосфат - 0,5 мг (в пересчете на алюминий 0,125 мг), натрия хлорид - 4,25 мг, янтарная кислота - 0,295 мг, Полисорбат 80 - 0,1 мг, вода для инъекций - до 0,5 мл.
ПРЕВЕНАР® 13 производится в соответствии с рекомендациями ВОЗ по производству и контролю качества пневмококковых конъюгированных вакцин.
Фармакологические свойства:
Введение вакцины Превенар® 13 вызывает выработку антител к капсулярным полисахаридам Streptococcus pneumoniae, обеспечивая тем самым специфическую защиту от инфекций, вызываемых включенными в вакцину 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F серотипами пневмококка.
Согласно рекомендациям ВОЗ для новых конъюгированных противопневмококковых вакцин, проведена оценка эквивалентности иммунного ответа при использовании вакцин Превенар® 13 и Превенар® по совокупности трёх независимых критериев: процент пациентов, достигших концентрации специфических антител IgG0,35 мкг/мл; средние геометрические концентрации иммуноглобулинов (IgG GMC) и опсонофагоцитарная активность бактерицидных антител (ОФА титр 1:8). Введение Превенар® 13 вызывает выработку иммунного ответа на все 13 вакцинальных серотипов, эквивалентного по вышеуказанным критериям вакцине Превенар®. Для взрослых лиц не определен защитный уровень противопневмококковых антител и используется серотип-специфическая ОФА.
Вакцина Превенар® 13 включает до 90% всех серотипов, являющихся причиной инвазивных пневмококковых инфекций (ИПИ), в том числе устойчивых к лечению антибиотиками. Наблюдения, проведенные в США с момента внедрения 7-валентной конъюгированной вакцины Превенар®, позволяют предположить, что наиболее тяжелые случаи инвазивной связаны с действием серотипов, включенных в Превенар® 13 (1, 3, 7F и 19А), в частности, серотип 3 непосредственно связан с заболеванием некротизирующей пневмонией.
Иммунный ответ при использовании трех или двух доз в серии первичной вакцинации
После введения трех доз Превенар® 13 при первичной вакцинации детей в возрасте до 6 мес отмечен значительный подъем уровня антител ко всем серотипам вакцины.
После введения двух доз при первичной вакцинации Превенар® 13 в рамках массовой иммунизации детей той же возрастной группы также отмечается значительный подъем титров антител ко всем компонентам вакцины, но уровень IgG0,35 мкг/мл для серотипов 6В и 23F определялся у меньшего процента детей. Вместе с тем, концентрация антител после введения ревакцинирующей дозы Превенар® 13 по сравнению с концентрацией антител перед введением ревакцинирующей дозы увеличивалась для всех 13-ти серотипов. Формирование иммунной памяти показано для обеих указанных выше схем вакцинации. Вторичный иммунный ответ на ревакцинирующую дозу у детей второго года жизни при использовании трех или двух доз в серии первичной вакцинации сравним для всех 13 серотипов. Превенар® 13 содержит общие с вакциной Превенар® семь серотипов и белок-носитель CRM197. Сравнительная идентичность обеих вакцин по иммуногенности и профилю безопасности позволяет перейти с Превенара® на Превенар® 13 на любом этапе вакцинации ребенка, а дополнительные 6 серотипов в Превенар® 13 обеспечивают более широкую защиту от ИПИ.
Показания к применению:
Профилактика заболеваний, вызываемых Streptococcus pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F (включая бактериемию, пневмонию и острый ) у детей в возрасте 2 мес - 5 лет.
профилактика пневмококковых заболеваний (в том числе пневмонии и инвазивных заболеваний), вызываемых Streptococcus pneumoniae серотипов 1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F и 23F, у взрослых в возрасте 50 лет и старше.
Важно! Ознакомься с лечением ,
Способ применения и дозы:
Вакцину вводят внутримышечно - в переднебоковую поверхность бедра (детям до 2-х лет) или в дельтовидную мышцу плеча (лицам старше 2-х лет), в разовой дозе 0,5 мл.
Перед применением шприц с вакциной Превенар® 13 необходимо хорошо встряхнуть до получения гомогенной суспензии. Не использовать, если при осмотре содержимого шприца выявляются инородные частицы, или содержимое выглядит иначе, чем в разделе «Описание» настоящей инструкции.
Не вводить Превенар® 13 внутривенно, внутрикожно и внутримышечно в ягодичную область!:
Схема вакцинации:
Возраст от 2 до 6 мес::
Серия трехкратной первичной вакцинации: вводят 3 дозы Превенар® 13 с интервалами между введениями не менее 1 мес. Первую дозу можно вводить детям с возраста 2 месяцев. Ревакцинацию проводят однократно в 11-15 мес. Схема используется при осуществлении индивидуальной иммунизации детей против пневмококковой инфекции.
Серия двукратной первичной вакцинации: вводят 2 дозы Превенар® 13 с интервалом между введениями не менее 2 мес. Первую дозу можно вводить детям с возраста 2 месяцев. Ревакцинацию проводят однократно в 11-15 мес. Схема используется при осуществлении массовой иммунизации детей против пневмококковой инфекции.
Для детей, которым вакцинация не была начата в первые 6 мес жизни, введение Превенар® 13 проводят по следующим схемам:
Возраст от 7 до 11 мес: две дозы с интервалом между введениями не менее 1 мес. Ревакцинацию проводят однократно на втором году жизни.
Возраст от 12 до 23 мес: две дозы с интервалом между введениями не менее 2 мес.
Возраст от 2 до 5 лет (включительно): однократно Если вакцинация начата Превенар® 13, рекомендуется завершить ее также вакциной Превенар® 13.
При вынужденном увеличении интервала между инъекциями любого из приведенных выше курсов вакцинации, введение дополнительных доз Превенар® 13 не требуется.
Дети, ранее вакцинированные Превенар®
Вакцинация против пневмококковой инфекции, начатая 7-валентной вакциной Превенар®, может быть продолжена Превенар® 13 на любом этапе схемы иммунизации.
Лица старше 50 лет
Взрослым, включая пациентов, ранее вакцинированных полисахаридной пневмококковой вакциной, Превенар® 13 вводят однократно.
Необходимость ревакцинации не установлена.
Особенности применения:
С учетом редких случаев анафилактических реакций вакцинированный пациент после вакцинации должен находиться под медицинским наблюдением в течение как минимум 30 мин. Места проведения иммунизации должны быть обеспечены средствами противошоковой терапии.
При принятии решения о вакцинации ребенка с тяжелой степенью недоношенности (беременность 28 недель), особенно имеющего в анамнезе незрелость дыхательной системы, необходимо учитывать, что польза иммунизации против пневмококковой инфекции у данной группы пациентов особенно высока и не следует ни отказываться от вакцинации, ни переносить ее сроки. Однако при этом, в связи с потенциальным риском апноэ, имеющимся при применении любых вакцин, проведение первой вакцинации Превенар® 13 рекомендуется в условиях стационара под врачебным наблюдением (не менее 48 ч).
Как и другие внутримышечные инъекции, пациентам с тромбоцитопенией и/или другими нарушениями свёртывающей системы крови и/или в случае лечения антикоагулянтами, вакцинация Превенар® 13 должна проводиться с осторожностью, при условии стабилизации состояния пациента и достижения контроля гемостаза. Возможно подкожное введение Превенара® 13 данной группе пациентов.
Превенар® 13 обеспечивает защиту только от тех серотипов Streptococcus pneumoniae, которые входят в его состав, и не защищает от других микроорганизмов, вызывающих инвазивные заболевания, пневмонию или средний отит. У пациентов с нарушением иммунореактивности вакцинация может сопровождаться пониженным уровнем антителообразования.
Имеются ограниченные сведения о том, что предшественник Превенар® 13, семивалентная вакцина Превенар®, вызывает адекватную иммунную реакцию у детей в возрасте до 6 мес с серповидно-клеточной анемией, причем профиль безопасности Превенар® у них аналогичен профилю безопасности у вакцинируемых, не относящихся к группам высокого риска.
В настоящее время отсутствуют данные о безопасности и иммуногенности вакцины у пациентов групп высокого риска по инвазивным пневмококковым инфекциям (например, у пациентов с врожденными или приобретенными дисфункциями селезенки, ВИЧ-инфекцией, злокачественными опухолями, после трансплантации штамма гемопоэтических стволовых клеток, нефротическим синдромом). Решение о проведении вакцинации пациентов из групп высокого риска следует принимать индивидуально.
Детям из групп высокого риска в возрасте младше 2 лет следует проводить первичную вакцинацию Превенар® 13 в соответствии с возрастом. В тех случаях, когда детям в возрасте 2 лет и старше, входящим в группу высокого риска (например, с серповидно-клеточной анемией, аспленией, ВИЧ-инфекцией, хроническим заболеванием или иммунологической дисфункцией) и ранее получившим курсы вакцинации Превенар® 13, назначена 23-валентная пневмококковая полисахаридная вакцина, интервал между введением вакцин должен быть не менее 8 недель.
Иммунизацию против пневмококковой инфекции взрослых желательно начинать с Превенара® 13.
В связи с тем, что причиной развития среднего отита могут быть самые различные возбудители (вирусы, бактерии, грибы, микст-инфекции), а не только пневмококки входящих в Превенар® 13 серотипов, предполагаемая профилактическая эффективность Превенар® 13 в отношении отита может быть менее выражена по сравнению с эффективностью для инвазивных заболеваний.
В связи с более высоким риском развития фебрильных реакций детям с судорожными расстройствами, в том числе с фебрильными судорогами в анамнезе, а также получающим Превенар® 13 одновременно с цельноклеточными коклюшными вакцинами, рекомендуется профилактическое назначение жаропонижающих средств.
Информация о влиянии препарата на способность управлять автомобилем и пользоваться техникой, отсутствует.
Побочные действия:
Безопасность вакцины Превенар® 13 изучена на здоровых детях (4429 детей/14267 доз вакцины) в возрасте от 6 недель до 11-16 мес. Во всех исследованиях Превенар® 13 применялся одновременно с другими вакцинами, рекомендованными для данного возраста.
Кроме того, безопасность вакцины Превенар® 13 оценена у 354 детей в возрасте от 7 мес. до 5 лет, ранее не вакцинированных ни одной из пневмококковых конъюгированных вакцин.
Наиболее частыми нежелательными реакциями были реакции в месте инъекции, повышение температуры, раздражительность, снижение аппетита и нарушение режима сна.
У детей старшего возраста при первичной вакцинации Превенар® 13 наблюдалась более высокая частота местных реакций, чем у детей первого года жизни.
У лиц в возрасте 65 лет и старше отмечалось меньшее количество побочных эффектов вне зависимости от предшествующих вакцинаций. Однако частота развития реакций была такая же, как и в более молодой популяции.
Нежелательные реакции, перечисленные ниже, классифицированы по органам и системам, а также в соответствии с частотой их проявления во всех возрастных группах.
Частота нежелательных реакций определялась следующим образом:
Очень частые (≥ 1/10), частые (≥ 1/100, но < 1/10), нечастые (≥ 1/1000, но < 1/100), редкие (≥ 1/10000, но < 1/1000) и очень редкие (≤ 1/10000).
Нежелательные реакции, выявленные в клинических исследованиях Превенар® 13 у детей
Общие и местные реакции:
| Очень частые: | гипертермия до 39° C; раздражительность; гиперемия кожи, болезненные ощущения, уплотнение или отек размером 2,5-7,0 см в месте инъекции; сонливость, ухудшение сна. |
| Частые: | гипертермия выше 39° C; болезненность в месте инъекции, приводящая к кратковременному ограничению объема движений конечности. |
| Нечастые: | гиперемия кожи, уплотнение или отек размерами более 7,0 см в месте инъекции; плаксивость. |
| Редкие: | случаи гипотонического , реакции гиперчувствительности в месте инъекции (крапивница, зуд)*; приливы крови к лицу*. |
Кровь и лимфатическая система:
Нервная система:
Желудочно-кишечный тракт:
* - отмечались при постмаркетинговых наблюдениях вакцины Превенар®; можно рассматривать как возможные и для Превенар® 13.
Нежелательные реакции, выявленные в клинических исследованиях Превенар® 13 у взрослых
Желудочно-кишечный тракт:
Иммунная система:
Кожа и подкожная клетчатка:
Общие и местные реакции:
В целом не было отмечено значительных различий в частоте развития побочных эффектов у взрослых, ранее вакцинированных 23-валентной пневмококковой полисахаридной вакциной и не вакцинированных этой вакциной.
Частота развития местных побочных реакций была одинакова для лиц в возрасте 50-59 лет и лиц старше 65 лет при вакцинации Превенар® 13, также число местных побочных реакций не увеличивалось при вакцинации одновременно с инактивированной гриппозной вакциной.
Частота обычных вакцинальных системных реакций была выше при одновременном введении Превенар® 13 и инактивированной гриппозной вакцины по сравнению с применением только инактивированной гриппозной вакцины (головная боль, сыпь, снижение аппетита, боли в суставах и мышцах) или только Превенар® 13 (головная боль, утомляемость, озноб, снижение аппетита и боль в суставах).
Взаимодействие с другими лекарственными средствами:
Данные о взаимозаменяемости Превенар® и Превенар® 13 на не-CRM197-основанные пневмококковые конъюгированные вакцины отсутствуют.
При одновременной вакцинации Превенар® 13 и другими вакцинами инъекции делаются в разные участки тела.
Дети в возрасте от 2 месяцев до 5 лет
Превенар® 13 сочетается с любыми другими вакцинами, входящими в календарь иммунизации детей первых лет жизни. Превенар® 13 можно вводить детям одновременно (в один день) с любыми следующими антигенами, входящими в состав как моновалентных, так и комбинированных вакцин: дифтерийным, столбнячным, бесклеточным или цельноклеточным коклюшным, Haemophilus influenzae тип b, инактивированным полиомиелитным, гепатита B, коревым, эпидемического паротита, краснухи и ветряной оспы - без изменения реактогенности и иммунологических показателей.
Лица в возрасте 50 лет и старше
Превенар® 13 можно вводить одновременно с тривалентной инактивированной гриппозной вакциной.
Одновременное применение с другими вакцинами не исследовалось.
Противопоказания:
Повышенная чувствительность на предшествующее введение Превенар® 13 или Превенар® (в том числе, тяжелые генерализованные аллергические реакции);
-повышенная чувствительность к дифтерийному анатоксину и/или вспомогательным веществам;
-острые инфекционные или неинфекционные заболевания, обострения хронических заболеваний. Вакцинацию проводят после выздоровления или в период ремиссии.
БЕРЕМЕННОСТЬ И ПЕРИОД КОРМЛЕНИЯ ГРУДЬЮ
Данные о применении Превенар® 13 во время беременности отсутствуют. Неизвестно, выделяется ли Превенар® 13 в грудное молоко.
Передозировка:
Передозировка Превенар® 13 маловероятна, так как вакцину выпускают в шприце, содержащем только одну дозу.
Условия хранения:
При температуре от 2 до 8 °C. Не замораживать.
Хранить в недоступном для детей месте.
Условия отпуска:
По рецепту
Упаковка:
Суспензия для внутримышечного введения 0,5 мл/доза. По 0,5 мл в шприц вместимостью 1 мл из прозрачного бесцветного стекла (тип I).
5 шприцев в пластиковую упаковку, запечатанную полиэтиленовой пленкой. 2 пластиковых упаковки и 10 стерильных игл вместе с инструкцией по применению в картонную пачку.
При упаковке ООО «НПО Петровакс Фарм», Российская Федерация:
1 шприц и 1 стерильная игла в пластиковую упаковку, запечатанную полиэтиленовой пленкой. 1 пластиковая упаковка вместе с инструкцией по применению в картонную пачку.
Инструкция по медицинскому применению
лекарственного средства
Пневмовакс 23
пневмококковая полисахаридная вакцина
Торговое название
Пневмовакс 23 пневмококковая полисахаридная вакцина
Международное непатентованное название
Лекарственная форма
Раствор для инъекций, 0,5 мл/ 1 доза
Состав
Один флакон (0,5 мл) вакцины содержит
активное вещество - пневмококковый полисахарид, состоящий из 23 датских серотипов пневмококков: 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20, 22F, 23F, 33F по 25 мкг каждого серотипа
вспомогательные вещества - натрия хлорид, фенол, вода для инъекций
Описание
Прозрачный бесцветный раствор
Фармакотерапевтическая группа
Противобактериальные вакцины. Противопневмококковые вакцины. Пневмококковый очищенный полисахаридный антиген
Код АТХ J07AL01
Фармакологические свойства
Фармакокинетика
Так как Пневмовакс 23 является вакциной, фармакокинетические исследования не проводились.
Фармакодинамика
Пневмовакс 23 - вакцина, применяемая для активной иммунизации против пневмококковых заболеваний, вызванных 23 серотипами Streptococcus pneumonia (1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20, 22F, 23F, 33F). Вакцина приготовлена из очищенных капсулярных полисахаридных антигенов пневмококков, полученных из 23 серотипов, которые вызывают приблизительно 90% инвазивных пневмококковых заболеваний.
Иммунобиологические свойства
Присутствие в сыворотке крови типоспецифических гуморальных антител обычно позволяет предполагать наличие эффективной защиты против инфекционных заболеваний, вызываемых Streptococcus pneumonia . Повышение уровня антител в ≥ 2 раза после вакцинации в клинических исследованиях ассоциировалось с эффективностью поливалентных пневмококковых полисахаридных вакцин. Однако концентрация антикапсулярных антител, необходимая для защиты от пневмококковой инфекции, вызванной любым специфическим капсулярным антигеном не установлена. Превалирующее число лиц в возрасте ≥ 2 лет (от 85 до 95%) реагируют на вакцинацию выработкой антител к большинству или ко всем 23 пневмококковым полисахаридам, содержащимся в вакцине. Бактериальные капсулярные полисахариды индуцируют образование антител, главным образом, по независимому от Т-клеток механизму и вызывают недостаточный или непостоянный антителогенез у детей в возрасте < 2 лет.
Антитела обнаруживаются на третьей неделе после вакцинации, но их уровни снижаются в течение от 3 до 5 лет после вакцинации, в некоторых группах может наблюдаться более быстрое снижение (например, у детей и у лиц пожилого возраста). Протективный уровень сывороточных антител вырабатываемых к капсулярным полисахаридным антигенам после введения вакцины варьируется от более 100 до 300 нг / мл в зависимости от серотипа.
В клинических исследованиях по изучению иммунного ответа на введение одной дозы вакцины Пневмовакс 23 у взрослых (50-64 лет и ≥ 65 лет), непривитых или получивших одну вакцинацию более 3-5 лет назад, установлены соотношения титра антител каждого серотипа до и после вакцинации (на 30 день после получения вакцины): 0.60 и 0.94 соответственно в группе старше 65 лет и 0.62 и 0.97 соответственно в группе 50-64 лет.
Клиническая значимость более низкой выработки антител, наблюдавшейся после ревакцинации по сравнению с вакцинацией, неизвестна.
Эффективность
Эффективность поливалентной пневмококковой полисахаридной вакцины при пневмококковой пневмонии и бактериемии установлена в рандомизированных контролируемых клинических исследованиях. Исследование проводилось среди мужчин в возрасте от 16 до 58 лет, которые находились в группе высокого риска по заболеваемости пневмококковой пневмонией и бактериемией. Критерием эффективности послужила частота возникновения пневмококковых заболеваний, вызванных специфичным серотипом. Защитная эффективность при пневмококковой пневмонии (первичная конечная точка в этих исследованиях) составила 76,1% при использовании 6-валентной (1,2,4,8,12F, и 25 серотипы Streptococcus pneumonia ) и 91,7% при применении 12-валентной вакцины (1,2,3,4,6A,8, 9N,12F,25, 7F, 18C, и 46 серотипы Streptococcus pneumonia). В исследованиях с участием людей, которым показано введение вакцины, например, лица с сахарным диабетом, хроническими заболеваниями сердца, легких или анатомической аспленией, сообщалось, что эффективность вакцинации составила от 50 до 70%.
В одном исследовании установлено, что вакцинация оказывает значительное защитное действие против инфекционных заболеваний, вызванных несколькими отдельными серотипами Streptococcus pneumonia (1, 3, 4, 8, 9V и 14). Для других серотипов количество случаев в этом исследовании было слишком малым, чтобы сделать выводы о специфической защите от этих серотипов.
В клиническом исследовании по иммунизации пациентов в возрасте от 2 до 25 лет с серповидно - клеточной анемией, врожденной аспленией (синдромом Ивемарка) и спленэктомией поливалентной пневмококковой полисахаридной вакциной, содержащей 8 капсулярных полисахаридных антигенов серотипов Streptococcus pneumonia (1,3,6,7,14,18,19 и 23), отмечена более низкая частота развития бактериальных пневмококковых заболеваний по сравнению с не вакцинированными.
Продолжительность иммунитета
Результаты одного эпидемиологического исследования указывают, что вакцинация может обеспечить защиту на протяжении как минимум 9 лет после получения начальной дозы вакцины. После вакцинации титр антител, вырабатываемых на каждый специфичный серотип, снижается в течение 5-10 лет. Титр антител снижается быстрее у детей и пожилых людей старше 60 лет. Может потребоваться ревакцинация у данных групп пациентов. При этом после ревакцинации титр антител может быть ниже, если интервал между вакцинациями превышает 10 лет, в частности, у лиц очень пожилого возраста (лица в возрасте ≥ 85 лет).
Показания к применению
Активная иммунизация против пневмококковой инфекции, вызванной серотипами Streptococcus pneumonia (1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20, 22F, 23F, 33F) взрослых и детей старше 2 лет
Контингент лиц с повышенным риском заболеваемости, подлежащих вакцинации
- плановая вакцинация лиц старше 50 лет
- взрослые и дети старше 2 лет с хроническими сердечно-сосудистыми заболеваниями (включая застойную сердечную недостаточность и кардиомиопатию), хроническими заболеваниями легких (включая хроническую обструктивную болезнь легких и эмфизему), сахарным диабетом, хроническими заболеваниями печени (включая цирроз) и алкоголизмом, функциональной или анатомической аспленией (включая серповидно-клеточную анемию и спленэктомию) и симптомами ликвореи*
- взрослые и дети старше 2 лет со сниженным иммунитетом (иммунодефицитные состояния при ВИЧ, лейкемии, лимфоме, болезни Ходжкина, множественной миеломе, злокачественных опухолях, хронической почечной недостаточности или нефротическом синдроме; вызванные иммуносупрессивной химиотерапией (включая кортикостероиды); после перенесенной трансплантации органов или трансплантации костного мозга)
Вакцинация не проводится в связи с неэффективностью:
- для профилактики острого среднего отита, синусита и других инфекций верхних респираторных путей
- *для профилактики пневмококковой пневмонии, у пациентов с ликвореей, вызванной врожденными повреждениями, переломами черепа, или нейрохирургическими процедурами.
Способ применения и дозы
Иммунизацию проводят в летне-осенний период.
Первичная вакцинация
Взрослые и дети в возрасте старше двух лет - одна разовая доза 0,5 мл вводится внутримышечно или подкожно в дельтовидную мышцу плеча или в среднюю треть передне-боковой части бедра.
Особенности применения при хронических заболеваниях, не ассоциированных с иммунодепрессией
Решение о необходимости вакцинации данной категории лиц необходимо принимать на основании оценки иммунного статуса и особенностей течения основного заболевания.
Особенности применения при заболеваниях, ассоциированных с иммунодепрессией
Рекомендуется, чтобы пневмококковая вакцина вводилась за две недели (предпочтительно) до плановой спленэктомии или начала химиотерапии или другой иммуносупрессивной терапии. Следует избегать вакцинации во время химиотерапии или лучевой терапии.
После завершения курса химиотерапии и/или лучевой терапии по причине неопластического заболевания, иммунный ответ на вакцинацию может оставаться сниженным. Вакцинацию не следует назначать раньше, чем через три месяца после завершения такой терапии. Более длительная отсрочка может быть целесообразной для пациентов, получавших интенсивную или пролонгированную терапию.
Лица с бессимптомной или симптоматической ВИЧ-инфекцией должны быть вакцинированы как можно скорее после подтверждения диагноза.
Ревакцинация
Одна разовая доза 0,5 мл вводится путем внутримышечной или подкожной инъекции в область дельтовидной мышцы плеча или в боковую часть середины бедра.
Схема и сроки вакцинации (ревакцинации) определяются в соответствии с местными официальными рекомендациями. У иммунокомпетентных пациентов не следует проводить плановую ревакцинацию. Вопрос о ревакцинации решается индивидуально в зависимости от уровня антител у пациентов.
Ревакцинация может быть рассмотрена для лиц с повышенным риском развития серьезной пневмококковой инфекции, которые получили пневмококковую вакцину не менее пяти лет назад, или для лиц с быстрым снижением уровней антипневмококковых антител. К лицам с повышенным риском относятся пациенты с функциональной или анатомической аспленией (например, со спленэктомией или серповидно-клеточной анемией), ВИЧ, лейкемией, лимфомой, болезнью Ходжкина, множественной миеломой, злокачественными опухолями, хронической почечной недостаточностью, нефротическим синдромом. Так же к данной группе относятся лица, получающие иммуносупрессивную химиотерапию или лица, перенесшие трансплантацию органов или костного мозга. Для пациентов с высоким риском развития фатальной пневмококковой инфекции, можно рассмотреть вопрос о проведении ревакцинации через три года.
Ревакцинация менее чем через три года не рекомендуется из-за повышенного риска развития побочных реакций. Установлено, что частота развития местных побочных реакций, а у лиц в возрасте ≥ 65 лет - некоторых системных побочных реакций, после ревакцинации выше, чем после первичной вакцинации при временном интервале между применением вакцины от трех до пяти лет.
Дети
Вопрос о ревакцинации детей в возрасте от 2 до 10 лет следует рассматривать только через 3 года после вакцинации, если существует повышенный риск развития пневмококковой инфекции (например, дети с нефротическим синдромом, удаленной селезенкой или серповидно-клеточной анемией).
Более подробные инструкции применения вакцины смотрите в рекомендациях Национального Календаря Республики Казахстан.
Техника введения вакцины
Вакцину следует использовать в том виде, в котором она поставляется, разведения или восстановления не требуется. Необходимо провести визуальный осмотр ампулы на целостность, изменение цвета, выпадение осадка. При наличии изменений такую вакцину вводить нельзя.
Вакцина вводится внутримышечно (в/м) или подкожно (п/к).
Не вводить внутривенно или внутрикожно .
Соблюдать меры предосторожности, чтобы убедиться, что игла не попала в кровеносный сосуд. Также вакцину не следует вводить внутрикожно, поскольку такой путь введения сопряжен с повышенным риском развития местных реакций.
Любой неиспользованный препарат или отходы следует уничтожить в соответствии с местными требованиями к утилизации биологических отходов.
Клинические исследования выявили, что наиболее частыми общими системными реакциями на введение вакцины были: слабость, усталость, миалгия и головная боль. Для устранения поствакцинальных реакций пациентам проводилось симптоматическое лечение.
Пожилые люди
В клинических исследованиях общее количество побочных реакций у пациентов в возрасте 50-64 года в месте введения вакцины при первичной вакцинации было 72.8%, при ревакцинации 79.6%. У пациентов ≥ 65 лет общее количество побочных реакций в месте введения вакцины при первичной вакцинации было 52.9% , при ревакцинации 79.3%.
Местные побочные реакции на введение вакцины проявлялись на третий день после вакцинации и полностью проходили на пятый день.
Общее количество системных побочных реакций при первичной вакцинации у пациентов в возрасте 50-64 года было 48.8%, при ревакцинации 47.4%. У пациентов ≥ 65 лет общее количество системных побочных реакций при первичной вакцинации составило 32.1%, при ревакцинации 39.1%.
Общее количество побочных реакций, связанных с вакцинацией, у пациентов в возрасте от 50 до 64 лет при первичной вакцинации было 35.5%, при ревакцинации 37.5%. У пациентов ≥ 65 лет общее количество побочных реакций, связанных с вакцинацией, при первичной вакцинации было 21.7%, при ревакцинации 33.1%
Дети
Клинические исследования по безопасности и эффективности применения Пневмовакс 23 у детей младше двух лет не проводились. Применение у данной возрастной категории не рекомендуется, т.к. уровень вырабатываемых антител может быть недостаточным.
Побочные эффекты распределены согласно частоте их возникновения в ходе клинических исследований и применения в постмаркетинговый период: очень часто (1/10); часто (от 1/100 до <1/10); нечасто (от1/1,000 до <1/100); редко (1/10,000 до <1/1,000); очень редко (<1/10,000), неизвестно - (частота не может быть определена из имеющихся данных).
Очень часто
Лихорадка (£ 38.8°C)
- эритема, отек, боль, болезненность, припухлость и местная гипертермия в месте инъекции
Редко
Воспаление подкожной жировой клетчатки, развившееся в месте введения вакцины в ближайшие сроки после вакцинации
Неизвестно
Астения, озноб, ограничение подвижности и периферический отек конечности, в которую произведена инъекция, недомогание
- гемолитическая анемия у пациентов с другими гематологическими нарушениями, лейкоцитоз, лимфаденит, лимфаденопатия, тромбоцитопения у пациентов с идиопатической тромбоцитопенической пурпурой со стабильным уровнем тромбоцитов
- анафилактоидные реакции, отек Квинке, сывороточная болезнь
Фебрильные судороги, синдром Гийена-Барре, головная боль, парестезия, радикулонейропатия
Тошнота, рвота
Сыпь, крапивница, мультиформная эритема
Артралгия, артрит, миалгия
Повышение уровня C-реактивного белка
Противопоказания
Повышенная чувствительность к любому компоненту вакцины
Анафилактическая реакция в анамнезе на предыдущее введение пневмококковых вакцин
Острое инфекционное заболевание или обострение хронического заболевания средней или тяжелой степени тяжести
Детский возраст до 2 лет
- беременность и период лактации
Лекарственные взаимодействия
Пневмококковую вакцину можно применять одновременно с вакциной против гриппа, используя индивидуальные иглы и разные конечности для инъекций.
Пневмовакс 23 и Зоставакс (противовирусная вакцина для профилактики опоясывающего лишая) не следует вводить одновременно, поскольку такое применение в клиническом исследовании приводило к снижению иммуногенности вакцины Зоставакс. Рекомендуется между введением этих двух вакцин соблюдать 4-недельный интервал.
Опыта одновременного применения с другими вакцинами нет.
Особые указания
Введение вакцины должно быть отстрочено в случае заболевания, сопровождающегося выраженной лихорадкой, другой активной инфекции, за исключением случаев, когда отсрочка может повлечь за собой еще больший риск заболеваемости пневмококковой инфекцией.
Как и при использовании любой другой вакцины, адекватное медикаментозное обеспечение, включая эпинефрин (адреналин), должно быть доступным для немедленного применения в случае развития острой анафилактической реакции.
Пациенты с иммунодефицитными состояниями
Как и при использовании любой другой вакцины, вакцинация препаратом Пневмовакс 23 может быть эффективной не у всех реципиентов. У пациентов с иммунодефицитом, обусловленном фоновыми состояниями или лечением (например, иммуносупрессивная терапия, химиотерапия или лучевая терапия при злокачественном новообразовании), ожидаемая выработка сывороточных антител может не наблюдаться после первой или второй дозы вакцины. Следовательно, у таких пациентов может не наблюдаться должного уровня защиты от заболеваний, вызванных пневмококковой инфекцией.
У лиц, получающих иммуносупрессивную терапию, промежуток времени для восстановления иммунного ответа варьирует в зависимости от болезни и лечения. Улучшение иммунного ответа наблюдалось в течение двух лет после завершения химиотерапии или другой иммуносупрессивной терапии (совместно или без применения лучевой терапии) и при увеличении интервала между окончанием лечения и введением пневмококковой вакцины.
После введения пневмококковой вакцины не следует прекращать соответствующую антибиотикотерапию для профилактики пневмококковой инфекции у пациентов с иммунодефицитными состояниями. Продолжительность антибиотикотерапии определяет лечащий врач в каждом клиническом случае.
Пациентам с повышенным риском развития серьезной пневмококковой инфекции (например, лица с удаленной селезенкой или получавшие иммуносупрессивную терапию по какой-либо причине) следует дать рекомендации о возможной необходимости в ранней антимикробной терапии в случае тяжелого, острого заболевания, сопровождающегося лихорадкой.
Пневмококковая вакцина может быть не эффективной в предотвращении инфекции, являющейся следствием перелома основания черепа, нейрохирургических процедур или контакта цереброспинальной жидкости с внешней средой.
Беременность и период лактации
Исследования на животных недостаточны для определения эффективности и безопасности вакцинации у беременных. Вакцина Пневмовакс 23 не оценивалась в исследованиях влияния на внутриутробное развитие и вынашиваемость плода. Поэтому Пневмовакс 23 не следует применять при беременности, за исключением случаев очевидной необходимости, когда потенциальная польза оправдывает потенциальный риск для плода. Вакцина Пневмовакс 23 не оценивалась в исследованиях по влиянию на репродуктивную функцию. Неизвестно, экскретируется ли эта вакцина в грудное молоко.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами
Нет данных, указывающих на то, что Пневмовакс 23 влияет на способность управлять автотранспортом или работать с механизмами.
Вакцинация занимает важное место в профилактике заболеваний, вызванных пневмококковой инфекцией. Ведь избежать контакта с этими бактериями не удаётся никому.
В этой статье мы обсудим вакцину для профилактики пневмококковой инфекции - «Пневмо 23», которая подходит и детям, и взрослым. Что это за вакцина, показания и противопоказания для её применения, действия после прививки, какая реакция организма на неё считается нормой и есть ли у этого препарата аналоги - давайте это выясним.
Чем опасна пневмококковая инфекция
Пневмококковая инфекция, которая объединяет группу заболеваний, вызванных особым подвидом стрептококка - пневмококком, считается чрезвычайно распространённой среди людей всех возрастов. Это связано с достаточно лёгкой передачей этого вида микробов (заражение происходит воздушно-капельным путём) и устойчивостью пневмококков ко многим антибиотикам.
Пневмококки являются наиболее частой причиной развития следующих болезней:

Опасность пневмококка связана также с частым развитием носительства, когда инфекция длительное время может находиться на слизистых оболочках человека-носителя, не вызывая у него тяжёлых форм болезни, но при разговоре или чихании бактерии выделяются в воздух и заражают окружающих. В семьях, где дети посещают дошкольные учреждения, случаи носительства пневмококковой инфекции регистрируются у 60% взрослых.
Не встретиться с пневмококком взрослому человеку, ведущему активный образ жизни, или ребёнку, посещающему любое образовательное заведение - практически невозможно. Для эффективного предупреждения заболевания или носительства пневмококковой инфекции используется вакцинация препаратом «Пневмо 23».
Что за вакцина «Пневмо 23»

Вакцина от пневмококковой инфекции «Пневмо 23» выпускается во Франции. Завод Санофи Пастер (это производитель «Пневмо 23») входит в структуру группы Санофи-Авентис, предприятия которой считаются одними из лидеров рынка иммунобиологических средств. Форма выпуска вакцины - одноразовый индивидуальный шприц, содержащий 1 дозу «Пневмо 23».
Состав вакцины позволяет обеспечить выработку активного иммунитета в отношении двадцати трёх серологических типов пневмококка (прививка содержит полисахариды 23 серотипов и фенольный буферный раствор).
В одном шприце прививки «Пневмо 23» согласно инструкции, содержится 0,5 мл препарата, что составляет одну прививочную дозу для всех возрастов.
Инструкция
Для того чтобы привиться от пневмококковой инфекции, следует посетить участкового врача поликлиники (или врача частного прививочного кабинета), который определит общее состояние здоровья и необходимость вакцинации. Также доктор произведёт осмотр, измерение температуры тела, оценку общих анализов крови и мочи, чтобы убедиться, что человек на момент вакцинации полностью здоров.
 Особой подготовки перед прививкой от самого пациента не требуется, но не желательно прививаться на голодный желудок и после изнуряющей физической активности, а также не рекомендуется в день прививки посещать бассейн или сауну и делать массаж или косметические процедуры той конечности, куда была введена вакцина «Пневмо 23». Место введения препарата выбирает медик - это либо плечо, либо бедро. Способ введения - внутримышечная или подкожная инъекция.
Особой подготовки перед прививкой от самого пациента не требуется, но не желательно прививаться на голодный желудок и после изнуряющей физической активности, а также не рекомендуется в день прививки посещать бассейн или сауну и делать массаж или косметические процедуры той конечности, куда была введена вакцина «Пневмо 23». Место введения препарата выбирает медик - это либо плечо, либо бедро. Способ введения - внутримышечная или подкожная инъекция.
Препарат разрешено вводить одномоментно с другими прививками (особенно часто делают вместе с АКДС у детей или с вакциной от гриппа у взрослых), кроме вакцины БЦЖ. Иммунитет после прививки выработается не ранее, чем через месяц, поэтому этот момент нужно учесть при выборе сроков вакцинации - для того, чтобы организм выработал иммунитет и мог полноценно противостоять пневмококкам в период повышенной заболеваемости респираторных инфекций, прививку нужно сделать за 4 недели до начала предполагаемой эпидемии.
Показания для вакцинации «Пневмо 23»
Многолетними научными исследованиями подтверждена высокая степень защиты организма человека, привитого этой вакциной, от большинства наиболее опасных пневмококков. Эффективность препарата «Пневмо 23» для взрослых и детей оценивали по снижению уровня заболеваемости: развитие бронхитов и пневмоний у вакцинированного контингента людей удаётся избежать почти в 90% случаев, а у тех привитых, которые всё-таки заболели респираторными инфекциями, отмечались только лёгкие формы болезни.
«Пневмо 23» не входит в обязательный календарь прививок, поэтому её делают по желанию или в зависимости от показаний лицам в возрасте от 2 лет и старше. Вакцинация от пневмококковой инфекции рекомендована всем тем, у кого есть высокие риски заболеть любым видом пневмококка и получить серьёзные осложнения, а это следующие категории пациентов.

Противопоказания для введения «Пневмо 23»
Существующие для вакцины «Пневмо 23» противопоказания можно разделить на абсолютные и относительные. Абсолютным противопоказанием, при котором вакцину нельзя вводить ни при каких условиях, является аллергия к какому-либо компоненту препарата. К относительным противопоказаниям для использования «Пневмо 23» можно отнести:

Во время беременности введение «Пневмо 23» разрешается только в третьем триместре беременности по решению врача, когда существует высокая опасность заболевания будущей мамы (например, в преддверии осенне-зимнего сезона вместе с вакциной от гриппа); у кормящей мамы нет противопоказаний для прививки, компоненты вакцины не проникают в молоко матери.
Бытует мнение, что противопоказанием для вакцинации от пневмококка является перенесённое ранее воспаление лёгких, ведь если человек переболел пневмонией и выработал иммунитет, то зачем в таком случае нужна прививка «Пневмо 23», и от чего она может защитить. Но это ошибочное утверждение, ведь после перенесённой пневмококковой инфекции будет иммунитет к 1–2 видам микробов, в то время как введение вакцины позволит выработать защиту против всех 23 наиболее опасных пневмококков.
Что делать после вакцинации «Пневмо 23»
После прививки нельзя покидать медучреждение как минимум в течение получаса. Это время нужно для того, чтобы в случае возникновения острой местной или общей реакции на прививку «Пневмо 23», была вовремя оказана необходимая медицинская помощь. Но в целом у 95% людей после вакцинации не возникает никаких неприятных ощущений или изменений в состоянии здоровья, поэтому тревоги тех, кто планирует привиться «Пневмо 23» о том, как переносится сама прививка, обычно необоснованны.
Ребёнок после вакцинации может гулять и посещать образовательные учреждения в прежнем режиме без ограничения.
Возможные реакции и осложнения после прививки
 В 5% случаев, возможно, появление местных реакций на введение вакцины (чувство жжения, покраснение, болезненные ощущение или уплотнение в месте инъекции). Такие неприятные симптомы обычно проходят в течение 24 часа после укола. В качестве общих реакций описывается повышение температуры после прививки «Пневмо 23», но поствакцинальная температура обычно быстро нормализуется самостоятельно или на фоне однократного приёма жаропонижающих средств.
В 5% случаев, возможно, появление местных реакций на введение вакцины (чувство жжения, покраснение, болезненные ощущение или уплотнение в месте инъекции). Такие неприятные симптомы обычно проходят в течение 24 часа после укола. В качестве общих реакций описывается повышение температуры после прививки «Пневмо 23», но поствакцинальная температура обычно быстро нормализуется самостоятельно или на фоне однократного приёма жаропонижающих средств.
Производители вакцины указывают на ничтожно малую вероятность возникновения таких осложнений после прививки «Пневмо 23», как увеличение лимфоузлов, болей в суставах, появление кожной сыпи, развитие аллергических реакций по анафилактическому типа на введение вакцины. Подобные осложнения бывают скорее исключениями, так как эта вакцина, в подавляющем большинстве случаев, хорошо переносится. Но пациент обязан знать обо всех возможных после введения Пневмо 23 последствиях, и быть готовым показаться врачам при возникновении любого изменения в состоянии здоровья после вакцинации, будь то местные изменения, или общее ухудшение самочувствия.
Ревакцинация «Пневмо 23»
При использовании для профилактики пневмококковой инфекции препарата «Пневмо 23», схема вакцинации заключается в однократном введении прививки (первичная иммунизация), что обеспечивает защиту на 5 лет. Повторную инъекцию препарата (ревакцинацию) назначают через 5 лет, а иногда через 3 года или даже раньше по решению врача в следующих случаях:
- пациентам с выраженным иммунодефицитом (отсутствие селезёнки, инфицирование ВИЧ);
- лицам, находящимся в группе риска по бронхолегочным, почечным и сердечным заболеваниям;
- людям старше 65 лет;
- курильщикам;
- детям старше 10 лет с установленным диагнозом серповидноклеточной анемии также рекомендуется более ранняя ревакцинация «Пневмо 23».
Аналоги «Пневмо 23»
 Кроме французской вакцины «Пневмо 23», существуют аналоги иммунобиологических препаратов от пневмококковой инфекции. Подобные вакцины выпускают:
Кроме французской вакцины «Пневмо 23», существуют аналоги иммунобиологических препаратов от пневмококковой инфекции. Подобные вакцины выпускают:
- США - «Превенар»;
- Бельгия - «Синфлорикс».
Препарат «Превенар» обеспечивает развитие иммунитета к 7 или 13 (в зависимости от вида вакцины) серотипам пневмококка, «Синфлорикс» - к 10, в то время как «Пневмо 23» - к 23 видам микроба (10 из них считаются «взрослыми» ведь чаще болеет взрослое население, 13 - детские). Ещё одним преимуществом «Пневмо 23» считается его цена - она значительно ниже, чем у «Синфлорикс» и тем более «Превенар».
Единственный минус «Пневмо 23» - то, с какого возраста можно эту вакцину применять. Если американская и бельгийская вакцины могут быть введены начиная с шести недель жизни ребёнка, то французская вакцина разрешена только для использования у детей старше двух лет - то есть для профилактики пневмококковых заболеваний у новорождённых «Пневмо 23» не подходит.
Доказанная безопасность и высокий клинический эффект вакцины «Пневмо 23» делает этот препарат незаменимым в качестве специфической профилактики пневмококковых заболеваний для широкого круга людей, поскольку выработанный после прививки иммунитет даёт возможность реже и легче болеть, меньше использовать для лечения антибиотики, и жить нормальной неизолированной жизнью в период подъёма респираторных инфекций.
Вакцина против пневмококковой инфекции
Пневмококковая инфекция включает группу таких тяжелых заболеваний, как менингит, бактериемия и пневмония, а также более легкие, но более распространенные заболевания, такие как синусит и средний отит. Вызывающий инфекцию возбудитель Streptococcus pneumoniaе часто присутствует в виде колоний в носоглотке человека, откуда распространяется, как правило, воздушно-капельным путем. Младенцы и дети раннего возраста, как полагают, являются основным резервуаром этого возбудителя с различной степенью пораженности носоглоточного носительства, колеблющегося от 27% в экономически развитых до 85% в развивающихся странах.
Имеется более 90 серотипов S.pneumoniaе. Распространение серотипов, вызывающих заболевание, варьирует в зависимости от возраста, клинических проявлений заболевания, тяжести течения, географического местоположения и времени. До внедрения пневмококковых конъюгированных вакцин 6-11 серотипов возбудителя ассоциировалось с 70% и более инвазивной пневмококковой инфекцией (ИПИ), встречающейся среди детей по всему миру. ИПИ обычно определяется, как заболевание, ассоциируемое с выделением пневмококка из обычно стерильной крови человека или, что следует за распространением возбудителя потоком крови из других частей тела, например, при менингите или септическом артрите; это не распространяется на такие места, как среднее ухо, куда инфекция распространяется непосредственно из носоглотки.
Большинство заболеваний спорадические. Вспышки пневмококковой инфекции необычны, но могут встречаться в замкнутых коллективах, например, в домах для престарелых лиц, детских дневных стационарах и других учреждениях такого рода.
Однако большие вспышки менингита, вызванные серотипом 1, были зарегистрированы в Африканском менингитном поясе. По оценкам, из 8,8 миллионов детей в возрасте до 5 лет, погибших в 2008 году, по оценке ВОЗ, 476 000 (333 000 – 529 000) случаев смерти было вызвано пневмококковой инфекцией. Уровни заболеваемости и смертности выше в развивающихся, нежели в экономически развитых странах; большинство случаев смерти наблюдается в Африке и Азии.
В Европе и США S.pneumoniaе вызывает, по оценкам, приблизительно 30-50% внебольничной пневмонии (САР), требующей госпитализации взрослых лиц.
Во многих странах плановое использование пневмококковых конъюгированных вакцин резко снизило заболеваемость ИПИ, а в некоторых территориях ИПИ, вызванное вакцинными серотипами бактерии, фактически исчезла, даже среди возрастных групп, которые не являлись целевыми для программы иммунизации (эффект коллективного иммунитета).
S.pneumoniaе представляет собой грамположительный инкапсулированный диплококк. Полисахаридная капсула бактерии является существенным фактором вирулентности у более чем 90 серотипов пневмококка, которые определяются на основе различий в композиции этой капсулы. В общем иммунитет, индуцируемый инфекцией, сероспецифичен, но может наблюдаться и перекрестная защита среди родственных серотипов. Вто время как большое разнообразие серотипов вызывает неинвазивные заболевания типа среднего отита и синуситов, серотипы 1, 5, 6А, 6В, 14, 19F и 23F обычно вызывают ИПИ среди детей в возрасте до 5 лет. Серотипы 1, 5 и 14 вместе по всем регионам ассоциируются с 28-43% ИПИ и с 30% ИПИ в 20 из наиболее бедных стран мира; серотипы 23F и 19F ответственныза 9-18% случаев ИПИ в мире. Серотип 18С широко распространен в регионах с большим числом стран с высокими доходами (т.е. в Европе, Северной Америке и Океании). Некоторые серотипы, такие как 6B, 9V, 14, 19A, 19F и 23F, вероятно более, чем другие, ассоциируются с резистентностью к медицинским препаратам.
Лабораторная диагностика S.pneumoniaе, базирующаяся на выделении вируса методом посева на питательную среду, может проводиться в большинстве клинических микробиологических лабораторий, хотя предварительное лечение антибиотиками, неправильное содержание и транспортировка проб или использование несоответствующей питательной среды могут привести к неудаче с изоляцией микроорганизма. Наблюдаемое некоторое географическое различие в распространенности серотипов может объясняться факторами, включающими различия в отборе пациентов, частоту использования и качество кровяной питательной среды, программы иммунизациипротив пневмококковой инфекции и политику в отношении применения антибиотиков.
Пневмококковая инфекция может поражать различные системы организма, что вызывает возникновение определенного числа синдромов заболевания. Хотя временная колонизация на слизистой носоглотки, что является первичным очагом инфекции, редко трансформируется в заболевание, определенные серотипы пневмококка иногда могут проникать в поток крови, вызывая бактериемию и, возможно, инфицирование вторичных органов, таких как мозг, с развитием менингита. В других случаях непосредственное распространение возбудителя из носоглотки может вызвать такие заболевания, как средний отит или синуситы. Пневмония часто возникает при вдыхании пневмококка из носоглотки. Когда возникновение пневмонии ассоциируется с бактериемией, заболевание классифицируется как ИПИ.
Благодаря высокой достоверности микробиологической диагностики,заболеваемость ИПИ часто используют в качестве оценки заболеваемости острой пневмококковой инфекцией в целом. Всреднем около 75% случаев ИПИ и 83% случаев пневмококкового менингита наблюдаются среди детей в возрасте младше 2-х лет, но эти показатели значительно варьируют, также как и распространение случаев в возрастной группе до 2-х лет. От 8,7% до 52% случаев пневмонии наблюдается среди младенцев в возрасте младше 6 месяцев.
Показатель летальности при ИПИ может быть высоким, колеблясь от 20% при септицемии до 50% при менингите в развивающихся странах. Показатели смертности наиболее высокие среди детей раннего возраста. Даже в промышленно развитых странах общий показатель летальности при пневмококковой бактериемии может достигать 15-20% среди взрослых и 30-40% среди лиц пожилого возраста, несмотря на соответствующую антибиотикотерапию и интенсивное лечение. Среди выздоровевших после менингита в 58% случаев наблюдаются долгосрочные неврологические последствия, такие как потеря слуха, психические нарушения и нарушения двигательной активности и судороги.
Факторами риска в отношении пневмонии, в том числе пневмококковой пневмонии младенцев и детей раннего возраста, являются недостаток грудного вскармливания, алиментарные нарушения, загрязнение воздуха внутри помещения. Помимо высокой заболеваемости среди детей в возрасте моложе 2-х лет, риск возникновения пневмококковой инфекции повышен среди лиц преклонного возраста (старше 65 лет) и среди злоупотребляющих алкоголем и табакокурением. Этот риск также повышен среди лиц, страдающих хроническими заболеваниями, такими как сердечно-сосудистые, легочные заболевания, диабет или аспления или другие состояния, при которых происходит подавление иммунной системы, как при прогрессирующей ВИЧ-инфекции.
Развитие резистентности к обычно применяемым антибиотикам, таким как пенициллин, макролиды, цефалоспориныи ко-тримоксазол, является серьезной проблемой в некоторых районах мира. Однако в результате широкомасштабного внедрения иммунизации против пневмококковой инфекции наблюдается снижение циркуляции штаммов, резистентных кмедицинским препаратам.
Четкий диагноз пневмококковой инфекции может быть поставлен путем изоляции микроорганизма из крови или других обычно стерильных компонентов организма, таких как цереброспинальнаяжидкость, но этиологическая диагностика проблематична в случаях пневмококковой пневмонии, не сопровождаемой бактериемией.
Вакцины для предотвращения пневмококковой инфекции используются более 30 лет. В настоящее время на рынке имеется два разных типа пневмококковых вакцин:
(1) 23-валентная пневмококковая полисахаридная вакцина (PPV23), которая доступна с 1980 года, и
(2) две пневмококковые конъюгированные вакцины, доступные на рынке с 2009 года,
Превенар (инструкция к вакцине)
В последнее время в среде мамочек пошла мода на вакцину Превенар . Родители уверены, что после этой вакцины их детям не страшны отиты, менингиты и тд. Обычно никто даже не пытается перед вакцинацией прочитать инструкцию. Для тех, кому небезразлично, что вкалывают их ребёнку в составе вакцины Превенар публикуем инструкцию. Обязательно дочитайте до побочного действия препарата.
Выбор должен быть информированным!
суспензия для внутримышечных инъекций 0.5мл/доза 1дз
Wyeth Pharmaceutical Division of Wyeth Holdings Corporation (USA)
Международное непатентованное наименование
Отпускается по рецепту
Введение вакцины вызывает выработку антител к капсулярным полисахаридам Streptococcus pneumoniae серотипов 4, 6В, 9V, 14, 18С, 19F, 23F, обеспечивая специфическую защиту организма от вызываемых ими инфекций. У детей первого года жизни, начиная с 2-х месячного возраста, при использовании различных схем вакцинации, продемонстрировано формирование защитного иммунного ответа после серии первичной вакцинации и вторичного иммунного ответа на последнюю дозу, т.е. при ревакцинации. После введения трех доз при первичной вакцинации и последующей ревакцинации отмечен значительный подъем уровня антител. У детей в возрасте от 2 до 5 лет выраженное образование антител ко всем серотипам вакцины наблюдается после однократного введения, при этом иммунный ответ практически совпадал с таковым у детей первых двух лет жизни после серии первичной иммунизации.
Повышенная чувствительность при предшествующем введении вакцины, повышенная чувствительность к вспомогательным веществам и/или дифтерийному анатоксину; острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний (в этих случаях вакцинацию проводят после выздоровления или в стадии ремиссии).
Общие и местные реакции: реакция в месте введения (покраснение, уплотнение/отек, боль/болезненность); гипертермия от 38°С и выше (измерение per rectum), раздражительность, сонливость, беспокойный сон, плаксивость, отек/уплотнение места инъекции и покраснение более 2,4см, болезненность в месте инъекции, приводящая к кратковременному орграничению объема движения конечности, гипертермия > 39°С (измерение per rectum), эпизоды гипотонии-гипореактивности, реакции гиперчувствительности в месте введения (дерматит, зуд, крапивница). Кроветворная и лимфатическая система: регионарная лимфоаденопатия. Иммунная система: реакции гиперчувствительности, включая анафилактический шок, ангионевротический отек, отек Квинке, бронхоспазм, диспноэ. Нервная система: судороги, в том числе фебрильные судороги. Желудочно-кишечный тракт: рвота, диарея, снижение аппетита. Кожа и подкожная клетчатка: крапивница, полиформная эритема.
Вакцину можно вводить детям одновременно (в один день) с другими вакцинами, включенными в Национальный календарь профилактических прививок (за исключением БЦЖ), а также с вакциной против Hemophilus influenzae тип b (Хиб) и гексавалентной вакциной Инфанрикс, согласно предписанной схеме иммунизации. Вводить вакцины необходимо всегда в разные участки тела. Превенар поставляется в уже готовом к использованию шприце, содержимое которого не следует переносить в другую емкость и смешивать с другими лекарственными средствами.
Симптомы: усиление побочных действий. Лечение: симптоматическое.
Способ применения и дозировка
Вакцину вводят только внутримышечно в переднебоковую поверхность бедра (детям до 2 лет) или в дельтовидную мышцу плеча (детям старше 2 лет). Не вводить Превенар внутривенно!
Необходимость в какой-либо дополнительной дозе после каждой из приведенных выше схем иммунизации не установлена.
Превенар не применяется у взрослых. Данные о безопасности применения вакцины Превенар при беременности и в период лактации отсутствуют. Введение вакцины следует отложить, если у пациента острое заболевание, сопровождающееся умеренной или выраженной гипертермией.
На случай развития возможных редких случаев анафилактических реакций в течение не менее 30 минут после введения вакцины пациент должен находиться под соответствующим медицинским наблюдением. В связи с потенциальным риском апноэ следует предусмотреть возможность наблюдения за состоянием пациента в течение 48-72 часов при первичной серии вакцинации у детей в возрасте до 28 недель, особенно в случаях незрелости органов дыхания в анамнезе.
Превенар не обеспечивает защиту от серотипов Streptococcus pneumoniae, не входящих в состав вакцины, а также от других микроорганизмов, вызывающих инвазивные заболевания или средний отит.
При ревакцинации описано незначительное уменьшение содержания антител к Хиб с сохранением защитного уровня. Описано непостоянное снижение ответа на коклюшные антигены, а также на инактивированную полиомиелитную вакцину (ИПВ). Имеются ограниченные данные о совместном применении Превенара с вакциной против кори, краснухи и паротита, а также вакциной против ветряной оспы.
Вакцину Превенар не следует назначать детям с тромбоцитопенией или другими нарушениями свертывающей системы крови, которым противопоказаны внутримышечные инъекции, за исключением случаев, когда потенциальная польза применения вакцины значительно превосходит риск, обусловленный введением вакцины. Применение вакцины Превенар не может заменить стандартную иммунизацию против дифтерии. Белок-носитель CRM197 является генно-модифицированной нетоксичной формой дифтерийного токсина.
ВИЧ-инфекции или других причин, может иметь место снижение образования антител в ответ на вакцинацию. Пока нет данных о безопасности и иммуногенности вакцины у детей из других групп высокого риска по инвазивным пневмококковым заболеваниям (например, дети с наследственной или приобретенной дисфункцией селезенки, ВИЧ-инфекцией, злокачественными новообразованиями, нефротическим синдромом). Решение о проведении вакцинации детей из групп высокого риска следует принимать индивидуально.
Профилактическое назначение жаропонижающих средств рекомендуется всем детям, получающим Превенар совместно с цельноклеточными коклюшными вакцинами ввиду более высокого риска развития фебрильных реакций; а также детям с судорожными расстройствами, в том числе «фебрильными» судорогами в анамнезе.
Хранить при температуре от 2 до 8 гр. С. Не замораживать.
Превенар (или Превнар) – одна из наиболее широко используемых в мире вакцин компании Уайэт, которая была недавно приобретена фармгигантом Pfizer.
Семивалентная конъюгатная вакцина Превнар (или Превенар) предназначена для защиты от семи штаммов пневмококков. Она разработана компанией Уайэт и лицензирована в Соединенных Штатах Америки и более чем в 70 других странах. Однако эта вакцина не включает два серотипа (типы 1 и 5), которые вызывают значительную долю пневмококковых инфекций в развивающихся странах.
Компания Уайэт также завершила испытания девятивалентной конъюгатной вакцины, включающей серотипы 1 и 5.
7-валентная вакцина Превенар (Превнар) используется и в России. По данным производителя, она защищает от 7штаммов пневмококка и предназначена для профилактики заболеваний, вызываемых Streptococcus pneumoniae, включая сепсис, менингит, пневмонию, бактериемию и острый средний отит у детей в возрасте от 2 месяцев до 5 лет.
Зато вакцина Превнар (Превенар) запрещена в Нидерландах
Власти Нидерландов временно запретили использование вакцины Превнар (Превенар) производства компании Уайэт/Wyeth (концерн Pfizer), предназначенной для профилактики пневмококковых инфекций, после того как трое детей умерли в течение 10 дней после вакцинации.
Представитель Института Здоровья Нидерландов RIVM сообщила, что в среднем фиксируется от 5 до 10 случаев смерти среди детей после вакцинации Превенаром. Точные причины смерти детей пока неизвестны. Проводится расследование.
Представитель компании Pfizer Гвен Фишер сообщает, что по предварительным результатам собственного расследования компании, связи между смертью детей и вакцинацией не обнаружено. Компания объявила временный «карантин» на применение этой партии вакцины (около 110 тысяч доз).
Прививка Превенар 13 — для чего ее делают, какая схема вакцинации детей предусмотрена инструкцией по применению?
На сегодняшний день вакцинация населения является одним самых мощных способов профилактики множества опасных заболеваний. Кроме обязательных (плановых прививок) иногда применяют дополнительные, как правило, в случае эпидемических показаний. До недавнего времени к ним относилась и вакцинация против пневмококковой инфекции. С 2015 года она внесена в национальный календарь прививок, однако ее применение носит рекомендательный характер. Сегодня наиболее популярна вакцина Превенар, которая считается максимально эффективной.
Вакцина Превенар 13 от пневмококковой инфекции
Состав и форма выпуска вакцины
В состав вакцины входит ряд пневмококковых конъюгатов, а точнее, 13. Так называются искусственные молекулы, объединяющие в себе две частицы с разными свойствами, то есть вакцина «не живая». В одной дозе препарата (0.5 мл) содержатся гибридные молекулы - полисахариды серотипов 1, 2, 3, 4, 5, 6, 7, 9, 14, 19, 23, олигосахарид серотипа 18 и белок-носитель.
Также в состав вакцины Превенар входят вспомогательные вещества:
От чего защищает Превенар?
Многие родители не видят смысла вакцинировать ребенка «против пневмонии». Однако это не единственное показание препарата. От чего еще защищает Превенар? Эта вакцина активизирует иммунитет против пневмококковой (Streptococcus pneumoniae) инфекции.
Пневмококки – бактерии рода стрептококков, которые вызывают массу опасных заболеваний. Среди них:
У детей пневмококковая инфекция обычно является осложнением какого-либо заболевания. Иногда пневмококковая пневмония диагностируется тогда, когда ребенок перенес ОРВИ или грипп. Эти бактерии часто являются причиной обострения хронического бронхита. Также отоларингологи отмечают возникновение отита среднего уха, вызванного Streptococcus pneumoniae на фоне ринита.
Кому показана вакцинация?
Вакцинация показана нескольким группам населения. Рассмотрим, в каких случаях назначают прививку Превенар малышам:
- всем детям в возрасте от 2 месяцев;
- недоношенным младенцам;
- часто болеющим детям;
- малышам с хроническими заболеваниями – сахарным диабетом, астмой, нарушениями работы сердечно-сосудистой системы, ВИЧ-инфицированным.
- Лица пожилого возраста. В развитых странах людям, достигших 65 лет, такую прививку ставят в обязательном порядке.
- Пациенты с обширным поражением печени (циррозом), эндокринными заболеваниями (сахарным диабетом), нарушениями работы почек, сердечно-сосудистыми отклонениями.
- Тем, кто имеет патологии крови (серповидную анемию).
- ВИЧ-инфицированные.
- Лица, вынужденные постоянно находиться в местах большого скопления людей.
- индивидуальную непереносимость одной из составляющих препарата;
- острую фазу ОРВИ, гриппа;
- детские инфекционные заболевания (ветрянка, корь и т.д.).
- Малышам в возрасте до 2 лет - в переднелатеральную поверхность бедра, так как именно в этом месте меньше нервных окончаний и жировой ткани, препятствующей активному всасыванию препарата.
- Не рекомендуется вводить средство грудничкам в ягодичную мышцу во избежание повреждения седалищного нерва.
- Малышам старше 2 лет инъекция делается в дельтовидную мышцу плеча.
- Производитель предостерегает – вакцину нельзя вводить внутривенно.
Взрослых людей обычно не вакцинируют. Связано это с тем, что у них есть иммунитет, который угнетает пневмококки, как только они попали в организм. Однако и среди взрослого населения выделяют несколько групп риска, которым показана вакцинация:
Противопоказаний у данной вакцины немного. К ним можно отнести:
Также не следует проводить вакцинацию Превенар, если ребенок чувствует недомогание, у него слегка повышена температура. Кроме того, не делают прививку в случае, если у малыша обострение хронической болезни.
Вакцинируют ребенка в поликлинике либо по желанию родителей в частном медкабинете. Вакцина продается в герметичной упаковке, поэтому ее можно купить в аптеке.
По инструкции перед введением суспензию следует взболтать, чтобы избавиться от возможного осадка. Не применяют вакцину в случае, если раствор мутный или имеет отличный от белого цвет. Рассмотрим схему введения препарата, а также дозировку в зависимости от возраста детей.
Превенар вводят внутримышечно. Рассмотрим, куда конкретно делают инъекцию:
Если Превенар вводится совместно с вакциной против коклюша, рекомендуется профилактическое применение жаропонижающих средств, поскольку существует вероятность возникновения фебрильных реакций.
Схема и сроки вакцинации ребенка
Схема и сроки вакцинации Превенар базируются на официальных рекомендациях. Если ребенку не более полугода – график подразумевает 3-кратное введение вакцины и последующую ревакцинацию. Малыши от шести месяцев до года подвергаются 2-кратной вакцинации. Дети старше 13 месяцев вакцинируются 1 или 2 раза по другой схеме. В таблице представлены все варианты введения вакцины.
Недоношенных детей, малышей до 28 недель, а также тех, у кого в анамнезе присутствует диагноз «недоразвитость органов дыхания», следует наблюдать после прививки не менее 2-3 суток. Это связано с риском возникновения апноэ.
Как подготовить малыша к прививке?
Подготовка к прививке не требуется. Обычно перед тем, как вводить вакцину, врач осматривает ребенка, измеряет температуру. Если никаких отклонений не обнаружено, малыша прививают.
Однако некоторые педиатры рекомендуют сдать анализ крови перед вакцинацией, чтобы убедиться в том, что в организме ребенка нет скрытых воспалительных процессов. Так как Превенар 13 может вызвать аллергию, детям-аллергикам рекомендуется подготовиться более основательно - начать прием антигистаминных препаратов за трое суток до процедуры и столько же времени продолжать их пить после нее.
Как переносится ребенком вакцинация?
Любая вакцинация может стать причиной неадекватной реакции со стороны организма. Прививка Превенар 13 не исключение. При этом педиатры отмечают, что в большинстве случаев вакцинация переносится хорошо. Однако стоит выяснить, каковы могут быть побочные эффекты от Превенар 13, а также возможные осложнения.
Рассмотрим нормальную реакцию организма, почему могут возникнуть осложнения, и как следует вести себя в случае появления нетипичных симптомов.
Нормальная реакция и побочные эффекты
Превенар - современная пневмококковая вакцина, обеспечивающая образование антител ко всем 13 серотипам. В этот период (около недели) возможно легкое недомогание и болезненность в месте инъекции. Подобные реакции организма считаются вполне нормальными и случаются нечасто. Повышение температуры отмечается у 1% вакцинированных, местная реакция – у 5%.
Стоит помнить и о других возможных побочных эффектах вакцины. Через сколько времени они могут проявиться? Как правило, если в течение трех суток после вакцинации проблем не возникло, можно вздохнуть спокойно.
Рассмотрим вероятные побочные эффекты, а также правильные действия родителей:
- Нарушение сна, раздражительность, потеря аппетита. Стоит переждать сложный период - аппетит и сон у ребенка наладятся.
- Повышение температуры до 39-40°С. В данном случае рекомендуется применение жаропонижающих средств - Парацетамола или Ибупрофена.
- Болезненность в месте инъекции, жалобы на ограничение в движении руки или ноги. Можно смазывать этот участок Траумелем, Гепарином, Троксевазином. К врачу придется обратиться, если проблема не исчезла на третьи сутки.
- Уплотнение в месте укола, отек тканей, превышающий в диаметре 7 см. Педиатры рекомендуют смазывать этот участок препаратами для рассасывания опухоли.
- Тошнота. Показаны абсорбирующие средства - Энтеросгель, Полисорб, Смекта.
- Аллергическая реакция в виде кожных проявлений – сыпь, зудящие розовые пятна по всему телу либо на некоторых участках. Подобные ситуации возникают при непереносимости какой-либо составляющей вакцины.
- Анафилактический шок, отек Квинке, удушье – это также аллергическая реакция, затрагивающая дыхательную систему.
- Воспаление тканей в месте инъекции – отек, уплотнение, гиперемия.
- Судороги.
- Лихорадка, ломота в суставах, головная боль, слабость. Все эти симптомы напоминают начало вирусного заболевания.
- В течение трех суток после процедуры лучше не водить ребенка в общественные места. Это необходимо для того, чтобы избежать заражения ОРВИ, которое может осложнить период адаптации и привести к непредсказуемым последствиям. При этом с малышом разрешается гулять на улице.
- Если грудничок получает прикорм, за неделю до и в течение 7 дней после прививки в его рацион не следует вводить новый продукт.
- При повышении температуры и местной реакции (покраснение, уплотнение тканей в месте инъекции) можно дать малышу жаропонижающее и антигистаминное средство.
- Форма выпуска: 1 шприц / 1 доза / 0,5 мл.
- Схема вакцинации: однократно детям с двух лет и взрослым.
- 7-11 мес : схема вакцинации включает 2 дозы по 0,5 мл с интервалом не менее 1 мес между дозами; 3-я доза рекомендуется на втором году жизни с интервалом не менее 2 мес;
- 12 мес-5 лет : схема вакцинации включает 2 дозы по 0,5 мл с интервалом не менее 2 мес между дозами.
- трехкратная первичная вакцинация с временным перерывом от 1 месяца;
- двукратная прививка от пневмонии с ограничением 2 месяца;
- первую порцию лекарства можно ввести до 2 месяцев жизни, а ревакцинацию лучше делать до года.
Возможные осложнения
Об осложнениях после прививки говорят, если для купирования симптомов приходится обращаться к медикам. Осложнения могут возникать по разным причинам – некачественная вакцина, нарушение правил введения препарата или индивидуальная реакция организма.
Рассмотрим возможные проблемы:
После вакцинации желательно в течение получаса не покидать стен клиники. Это необходимо сделать, если есть вероятность возникновения аллергической реакции. Далее важно наблюдать за состоянием ребенка дома и при необходимости вызывать врача.
При необходимости можно подобрать аналог вакцины с практически идентичным составом. Среди них выделяют такие:
vseprorebenka.ru
Вакцина пневмококковая «Пневмо 23»
«Санофи Пастер», Франция
Ревакцинация не ранее, чем через 3 года.
Инструкция по применению
Владелец регистрационного удостоверения:
SANOFI PASTEUR, S.A. (Франция)
Код ATX: J07AL01 (Pneumococcus, purified polysaccharides antigen)
Активное вещество: вакцина пневмококковая полисахаридная (pneumococcal polysaccharide vaccine)
Ph.Eur. Европейская Фармакопея
р-р д/в/м и п/к введения 0.5 мл/1 доза: шприцы 1 доза
рег. №: П N011092 от 02.07.10 — Бессрочно
Форма выпуска, состав и упаковка
полисахариды Streptococcus pneumoniae (23 серотипа; каждого серотипа по 25 мкг)
1 доза — шприцы (1) — упаковки контурные пластиковые (1) — пачки картонные.
Клинико-фармакологическая группа: Вакцина для профилактики заболеваний, вызванных Streptococcus pneumoniae
Фармако-терапевтическая группа: МИБП-вакцина
Приведенная научная информация является обобщающей и не может быть использована для принятия решения о возможности применения конкретного лекарственного препарата.
Фармакологическое действие
Высокоочищенная поливалентная вакцина. Представляет собой очищенный полисахарид Streptococcus pneumoniae 23 серотипов: 1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20, 22F, 23F, 33F. Вызывает формирование иммунитета к указанным серотипам Streptococcus pneumoniae. Иммунитет приобретается через 10-15 дней после однократной вакцинации и сохраняется в течение не менее 5 лет. После введения данной вакцины сероконверсия наблюдается, как минимум, у 90% вакцинированных лиц.
Профилактика инфекций пневмококковой этиологии, в особенности инфекций дыхательных путей, у лиц из групп риска, начиная с 2-летнего возраста.
Вакцину вводят п/к или в/м. Первичную вакцинацию проводят одной дозой данной вакцины однократно. Ревакцинации проводят каждые пять лет. Интервал между ревакцинациями может быть сокращен у лиц из групп повышенного риска или пациентов, которые получают иммунодепрессанты.
Возможны слабость, незначительное повышение температуры тела, озноб, головная боль (продолжительность — не более 24 ч); местные реакции — покраснение, легкая болезненность или уплотнение в месте инъекции.
Противопоказания к применению
Выраженная реакция на предыдущее введение вакцины; противопневмококковая вакцинация или перенесенная пневмококковая инфекция (вызванная одним из содержащихся в вакцине серотипов) в период времени до 5 лет перед планируемой вакцинацией данной вакциной.
Применение при беременности и кормлении грудью
Несмотря на то, что сведения о неблагоприятном воздействии на плод при использовании данной вакцины при беременности отсутствуют, вакцинацию беременных из групп риска проводить не рекомендуется.
Вакцинация особенно показана пациентам с серповидно-клеточной анемией, а также лицам с аспленией, перенесшим спленэктомию или перед спленэктомией.
При ревакцинации, проведенной ранее положенного срока, могут возникать тяжелые местные реакции.
В связи с возможностью развития серьезных побочных реакций (типа феномена Артюса) при проведении вакцинации следует строго соблюдать противопоказания, оценивать пользу вакцинации. При этом необходимо учитывать, что определение эффективности противопневмококковой вакцинации проводилось только у лиц из групп риска.
Иммунодепрессивная терапия может уменьшать или полностью подавлять иммунный ответ на введение данной вакцины.
В последние годы в мире складывается неоднозначное отношение к прививкам. Несмотря на то, что поголовная вакцинация против некоторых заболеваний привела к практически полному их исчезновению, ряды противников обязательных прививок растут. Этому способствует широкое распространение заблуждений, касающихся вакцинации.
Неизвестная инфекция - главная опасность
Кишечные инфекции, вал клещевых энцефалитов и южные инфекции, привезенные россиянами из отпусков,— таковы медицинские итоги лета.
Один из самых именитых инфекционистов России академик Виктор Малеев рассказал о наших самых маленьких, но от этого не менее опасных врагах.
Национальный календарь профилактических прививок включает в себя далеко не самый полный перечень вакцин, существующих в мире. При его составлении учитывается великое множество факторов, и далеко не последнюю роль.
Комплексный ответ простуде и гриппу
С наступлением холодного сезона ежегодно повышается заболеваемость острыми респираторными вирусными инфекциями (ОРВИ), гриппом и другими инфекциями дыхательных путей, на пике холодов приобретая масштабы эпидемии.
СИНФЛОРИКС™Вакцина для профилактики пневмококковой инфекции (полисахаридный антиген) и нетипированной гемофильной инфекции, конъюгированная, адсорбированная (SYNFLORIX™ pneumococcus purified polysaccharides antigen and Haemophilus influenzae, conjugated)
GlaxoSmithKline Biologicals s.a. J07A L52
сусп. д/ин. 1 доза фл. монодоз. 0,5 мл, № 1
сусп. д/ин. 1 доза шприц 0,5 мл, с 2-мя иглами, № 1
сусп. д/ин. 1 доза шприц 0,5 мл, с иглой, № 1
1 доза (0,5 мл) содержит: по 1 мкг пневмококкового полисахарида серотипов 1 1,2 , 5 1,2 , 6B 1,2 , 7F 1,2 , 9V 1,2 , 14 1,2 , 23F 1,2 и по 3 мкг пневмококкового полисахарида серотипов 4 1,2 , 18C 1,3 и 19F 1,4 .
1 адсорбированный на фосфате алюминия - 0,5 мг Al 3+ ;
3 конъюгированный с протеином столбнячного анатоксина ≈ 8 мкг;
№ UA/15363/01/01 от 15.08.2016 до 15.08.2021 По рецепту DC
Дата добавления: 17.01.2018 г.
В справочнике «Компендиум» 2016 года по данному препарату была представлена следующая информация
1 адсорбированный на фосфате алюминия — 0,5 мг Al 3+ ;
2 конъюгированный с протеином D (полученным из нетипованого штамма Haemophilus influenzae ) ≈ 13 мкг;
4 конъюгированный с протеином дифтерийного анатоксина ≈ 5 мкг.
эпидемиологические данные . 10 пневмококковых серотипов, включенных в эту вакцину, представляют собой основные болезнетворные серотипы в Европе, охватывающие примерно 56-90% инвазивных пневмококковых инфекций (ИПИ) у детей в возрасте <5 лет. В этой возрастной группе серотипы 1; 5 и 7F является причиной 3,3-24,1% ИПИ в зависимости от страны и исследуемого периода.
Пневмония различной этиологии является основной причиной детской заболеваемости и смертности во всем мире. В проспективных исследованиях установлено, что Streptococcus pneumoniae в 30-50% являлся вероятной причиной развития пневмонии.
Острый средний отит (ОСО) является частым детским заболеванием различной этиологии. Бактерии могут быть причиной 60-70% клинических эпизодов ОСО. Streptococcus pneumoniae и нетипируемый штамм Haemophilus influenzae являются наиболее частыми причинами возникновения бактериального ОСО во всем мире.
Эффективность при клинических исследованиях . Во время проведения многоцентрового двойного слепого кластерно-рандомизированного контролируемого клинического исследования фазы III/IV в Финляндии (FinIP) детей рандомизировали на 4 группы, в соответствии с двумя режимами вакцинации для младенцев: 2+1 (3-й и 5-й месяц с последующим введением бустерной дозы в 11-м месяце) или 3+1 (3-, 4- и 5-й месяц с последующим введением бустерной дозы в 11-м месяце) для получения или Синфлорикс™ (2/3 кластеров), или контрольных вакцин против гепатита (1/3 кластеров). В туровых когортах (довакцинация по возрасту) дети в возрасте 7-11 мес получали первую дозу вакцины Синфлорикс™ или контрольную вакцину против гепатита В, в соответствии с двухдозовым режимом, с последующим введением бустерной дозы, а дети в возрасте 12-18 мес при первой вакцинации получали две дозы вакцины Синфлорикс™ или контрольной вакцины против гепатита A. Средняя продолжительность периода последующего наблюдения, начиная от первой вакцинации, составляла 24-28 мес для инвазивного заболевания, диагностированной госпитальной пневмонии и амбулаторного лечения антимикробными препаратами. Во время кластерного исследования период последующего наблюдения младенцев составлял до 21 мес с целью оценки влияния на назофарингеальное носительство.
Во время многоцентрового рандомизированного двойного слепого клинического исследования III фазы (Клиническое исследование среднего отита и пневмонии — COMPAS), здоровые младенцы в возрасте 6-16 нед получали вакцину Синфлорикс™ или контрольную вакцину против гепатита B в 2; 4 и 6 мес с последующим применением вакцины Синфлорикс™ или контрольной вакцины против гепатита A в возрасте 15-18 мес.
ИПИ . Когорта младенцев в возрасте <7 мес на момент зачисления
Продемонстрирована эффективность вакцины (в исследовании FinIP) или эффективность вакцины (в исследовании COMPAS) в контексте предотвращения подтвержденных культуральным методом случаев ИПИ, в результате вакцинных пневмококковых серотипов (табл. 1).
Таблица 1. Предотвращение ИПИ у младенцев, получивших хотя бы 1 дозу вакцины Синфлорикс™ (общая когорта вакцинированных младенцев)
ЭВ — эффективность вакцины в клиническом исследовании вакцины (FinIP) или эффективность вакцины в клиническом исследовании (COMPAS); ДИ — доверительный интервал.
1 В ходе исследования FinIP другие серотипы, вызывающие ИПИ, включали 7F (1 случай в кластерах Синфлорикс™ 2+1), 18C, 19F и 23F (1 случай на каждый в контрольных кластерах). Во время исследования COMPAS серотипа 5 (2 случая), 18C (4 случая) и 23F (1 случай) также выявлены в контрольной группе дополнительно к серотипам 6B и 14. 2 Две группы контрольных кластеров младенцев были объединены. 3 p<0,0001. 4 p=0,0009.
5 93,0% (95% ДИ 74,9-98,9; 2 случая из 14) независимо от первичной схемы.
Пневмония . Эффективность вакцины Синфлорикс™ для профилактики внебольничной пневмонии (ВП) вероятно бактериальной этиологии продемонстрирована в когорте пациентов в соответствии с протоколом (иммунизированных менее тремя дозами первичной схемы) (р≤0,002), в качестве первичной цели исследования COMPAS в течение периода последующего наблюдения 38 нед с момента начала исследования: 22,0% (95% ДИ 7,7-34,2) 240 случаев/10 295 субъектов в группе Синфлорикс™ по сравнению с 304 случаями/10 201 субъекта в контрольной группе.
ВП вероятной бактериальной этиологии определялась как ренгенологично подтвержденые случаи ВП или альвеолярной консолидацией/плевральным выпотом на рентгенограмме органов грудной клетки или без альвеолярных инфильтратов, однако при уровне CРБ ≥40 мг/л.
Эффективность вакцины в профилактике ВП, вероятно, бактериальной этиологии с наличием альвеолярной консолидации или плеврального выпота составила 25,7% (95% ДИ 8,4-39,6) и в профилактике клинически подозреваемой ВП с направлением на рентгенографию грудной клетки составляла 6,7% (95% ДИ 0,7-12,3).
Во время исследования FinIP эффективность вакцины в уменьшении количества случаев госпитально диагностированной пневмонии составила 26,7% (95% ДИ 4,9-43,5) по схеме 3+1 для младенцев и 29,3% (95% ДИ 7,5-46,3) по схеме 2+1 для младенцев. Для туровой вакцинации эффективность вакцины составила 33,2% (95% ДИ 3,0-53,4) в когорте детей в возрасте 7-11 мес и 22,4% (95% ДИ от -8,7 до 44,8) в когорте детей в возрасте 12-18 мес.
ОСО . Эффективность вакцины в профилактике ОСО оценивали в ходе исследования COMPAS (табл. 2).
Таблица 2. Эффективность вакцины против ОСО 1 в ходе исследования COMPAS (в соответствии с протоколом 2: 5989 участников)
1 Первый эпизод; 2 период последующего наблюдения в течение максимум 40 мес, начиная со 2-й недели после 3-й дозы первичного курса вакцинации; 3 статистически незначимы по предварительно определенному критерию (односторонний р=0,032). Тем не менее, во всех вакцинированных когортах эффект вакцины в контексте клинических эпизодов ОСО составил 19% (95% ДИ 4,4-31,4).
Во время другого многоцентрового рандомизированного двойного слепого исследования (POET), которое проводили в Чешской Республике и Словакии, младенцы получали 11-валентную исследуемую вакцину (11Pn-PD), содержащую 10 серотипов Синфлорикс™ (вместе с серотипом 3, для которого продемонстрирована эффективность), или контрольную вакцину, согласно схеме вакцинации в 3-, 4-, 5- и 12-15-м месяце. Эффективность вакцины представлена в табл. 3.
Таблица 3. Эффективность вакцины против ОСО 1 в ходе исследования POET (в соответствии с протоколом 2: 4907 участников)
1 Все эпизоды; 2 период последующего наблюдения в течение максимум 24 мес, начиная со 2-й недели после 3-й дозы первичного курса вакцинации.
Во время исследования POET эффективность вакцины 11Pn-PD по профилактике первого эпизода ОСО, вызванного серотипами вакцин, составила 52,6% (95% ДИ 35,0-65,5). Продемонстрирована специфическая эффективность серотипов против первого эпизода ОСО, вызванного серотипами 6B, 14 19F и 23F.
Влияние на применение антимикробных препаратов
В общей когорте вакцинированных младенцев в исследовании FinIP вакцинация Синфлокс™ снизила уровень амбулаторного применения амоксициллина на 7,9% (95% ДИ 2,0-13,4) по схеме 3+1 для младенцев и 7,5% (95% ДИ 0,9-13,6) — по схеме 2+1 для младенцев.
Влияние на назофарингеальной носительство (НФН). Влияние вакцинации Синфлорикс™ на НФН изучали в исследованиях FinIP (5092 участника) и в исследовании COMPAS (1921 участник). Во время обоих исследований вакцина Синфлорикс™ значительно снижала носительство вакцинных серотипов (комбинированное и каждого по отдельности 6B, 19F и 23F) с тенденцией к повышению после повторной вакцинации в носительстве невакцинних серотипов или серотипов, которые не входят в состав вакцины против НФН, что привело к уменьшению общего пневмококкового носительства.
Пострегистрационный фармнадзор. В Бразилии вакцину Синфлорикс™ включили в Национальную программу иммунизации (НПИ) в марте 2010 г. для применения у новорожденных по схеме 3+1 с программой туровой иммунизации детей в возрасте до 2 лет. В исследования случай/контроль сообщалось о значительном снижении случаев ИПИ, подтвержденных бактериологическим методом или методом ПЦР, в результате любого вакцинного серотипа (83,8%; 95% ДИ 65,9-92,3) и ИПИ в результате серотипа 19A (82,2%; 95% ДИ 10,7-96,4).
В Финляндии вакцину Синфлорикс™ включили в НПИ в сентябре 2010 г. для применения у новорожденных по схеме 2+1 без программы туровой иммунизации. Оценивали относительное снижение частоты случаев ИПИ у детей в возрасте ≤5 лет в течение первых 3 лет после введения НПИ. До и после введения НПИ сравнения предусматривает значительное снижение частоты любого бактериологически подтвержденного ИПИ (80%; 95% ДИ 72-85), ИПИ любого вакцинного серотипа (92%; 95% ДИ 86-95) и ИПИ вследствие серотипа 19A (62%; 95% ДИ 20-85).
Данные по иммуногенности
Иммунологическая эффективность, не уступающая PCV7 . В прямом сравнительном исследовании с PCV7 продемонстрирована иммунологическая эффективность вакцины Синфлорикс™, не уступающая PCV7. установленная методом ELISA, для всех серотипов, кроме 6B и 23F. Для серотипов 6B и 23F соответственно 65,9 и 81,4% детей, вакцинированных в возрасте 2; 3 и 4 мес, достигли порога определения антител для ELISA через 1 мес после третьей дозы вакцины Синфлорикс™ по сравнению с 79,0 и 94,1% соответственно после трех доз PCV7.
Иммуногенность у младенцев в возрасте 6 нед-6 мес.
. Иммуногенность вакцины Синфлорикс™ оценивали при различных клинических исследований в странах Африки, Азии, Европы и Америки в соответствии с различными схемами (6-10-14 нед, 2-3-4, 3-4-5 или 2-4-6 мес). Во многих клинических исследованиях проводили ревакцинацию.
Первичная схема вакцинации, включающая 2 дозы . Во время клинического исследования оценивали иммуногенность вакцины Синфлорикс™ после 2- или 3-дозовой первичной схемы вакцинации. Несмотря на то что не отмечено значимой разницы между двумя группами относительно доли субъектов, достигших порога определения антител для ELISA, наблюдали меньшую долю субъектов, достигших порога определения OPA, для некоторых вакцинных серотипов, а также для перекрестно-реактивного серотипа 19A у субъектов, применявших 2-дозовую первичную схему. В обеих схемах наблюдали ответ на ревакцинацию, что указывало на иммунологическую подготовку, для каждого вакцинного серотипа и серотипа 19А.
Иммуногенность у невакцинированных младенцев и детей в возрасте ≥7 мес (туровая вакцинация) . Во время исследований у предварительно вакцинированных детей 7-11 мес (по схеме 2+1) и детей в возрасте от 12 мес до 5 лет (за 2-дозовой схемой), уровень антител GMC, определенных методом ELISA, и OPA GMT для всех вакцинных серотипов и перекрестно-реактивного серотипа 19A, был идентичным или выше уровня, индуцированного 3-дозовой первичной серией для младенцев.
Иммуногенность у недоношенных младенцев . Оценивали иммуногенность вакцины Синфлорикс™ у глубоко недоношенных и недоношенных младенцев (период гестации — 27-30 и 31-36 нед соответственно), а также у доношенных младенцев (3 первичные дозы в 2; 4; 6 мес с ревакцинацией в 15-18 мес).
После первичной вакцинации для каждого вакцинного серотипа доля лиц с концентрациями антител для ELISA ≥0,20 мкг/мл и титрами OPA ≥8 была идентичной, независимо от степени доношенности.
активная иммунизация детей грудного возраста и детей в возрасте от 6 нед до 5 лет для профилактики пневмококковой инфекции, вызванной серотипами Streptococcus pneumoniae 1, 4, 5, 6B, 7F, 9V, 14, 18C, 19F и 23F и перекрестно-реактивным серотипом 19A (включая сепсис, менингит, пневмонию, бактериемию и ОСО), а также инфекции, вызванной нетипированной Haemophilus influenzae .
вакцину вводят в/м.
Дети в возрасте от 6 нед до 6 мес
Первичная схема вакцинации, включающая 3 дозы . Рекомендуемая схема вакцинации, обеспечивающая оптимальную защиту, включает 4 дозы по 0,5 мл каждая. Первичная схема для детей грудного возраста включает 3 дозы, при этом первую дозу обычно вводят в возрасте 2 мес, с интервалом не меньше 1 мес между дозами. Первую дозу можно вводить уже в возрасте 6 нед; 4-я доза рекомендуется не ранее, чем через 6 мес после 3-й дозы, желательно в возрасте 12-15 мес.
Ранее не вакцинированные дети в возраста старше 6 мес и дети в возрасте :
Лицам, получившим первую дозу вакцины Синфлорикс™, рекомендуется завершить полный курс иммунизации вакциной Синфлорикс™.
повышенная чувствительность к действующему и вспомогательным веществам вакцины или любому белку-носителю.
Как и при применении других вакцин, назначение вакцины Синфлорикс™ должно быть отложено у лиц с острыми заболеваниями, сопровождающимися лихорадкой. Однако наличие легких незначительных проявлений инфекционных заболеваний, таких как простуда, не является основанием для отложения вакцинации.
в клинических исследованиях участвовали около 22 500 здоровых детей и 137 недоношенных младенцев, получивших примерно 64 тыс. доз вакцины Синфлорикс™ при первичной вакцинации. Около 19 500 здоровых детей и 116 недоношенных младенцев получили бустерную дозу вакцины Синфлорикс™ в течение 2-го года жизни. Безопасность также оценивали у 435 детей в возрасте 2-5 лет, из которых 285 человек получили 2 дозы Синфлорикс™. Во всех исследованиях вакцину применяли одновременно с другими вакцинами, рекомендованными для детей.
У новорожденных наиболее частыми побочными реакциями после первичной вакцинации были покраснение в месте введения и раздражительность (41 и 55%). После введения бустерной дозы наиболее частыми побочными реакциями были боль в месте инъекции и раздражительность (51 и 53% соответственно). Большинство из этих реакций были легкой и средней степени тяжести и продолжались недолго.
При введении последующих доз вакцины по схеме первичной вакцинации не отмечали повышения частоты или степени тяжести побочных реакций.
Реактогенность была более высокой у детей, одновременно привитых вакциной для профилактики коклюша с цельноклеточным компонентом.
Реактогенность была схожей как у у детей в возрасте до 12 мес, так и старше 12-месячного возраста, кроме боли в месте инъекции (39% — в возрасте до 12 мес и >58% детей старше 12 мес). После вакцинации бустерной дозой детей в возрасте старше 12-месячного возраста, более вероятными являются реакции в месте введения (сыпь и ненормальный плач) по сравнению с показателями у младенцев при первичной вакцинации.
Побочные реакции (для всех возрастных групп), о которых сообщалось, разделены на категории в зависимости от частоты возникновения: очень часто (≥1/10); часто (≥1/100, <1/10), нечасто (≥1/1000, <1/100), редко (≥1/10 000, <1/1000), очень редко (<10 000).
compendium.com.ua
Вакцинация против пневмококковой инфекции превенар
ВНИМАНИЕ! не вводить внутривенно
Инструкция по применению вакцины Превенар (краткая)
Вакцина пневмококковая полисахаридная конъюгированная адсорбированная включает семь активных веществ, представляющих собой пневмококковые полисахариды, полученные из грам-положительных бактерий Streptococcus pneumoniae серотипов 4, 6В, 9V, 14, 18С, 19F и 23F, индивидуально конъюгированные с дифтерийным белком-носителем CRM197, и адсорбированные на алюминия фосфате.
Вакцина для профилактики пневмококковых инфекций
Введение вакцины Превенар вызывает выработку антител к капсулярным полисахаридам Streptococcus pneumoniae серотипов 4, 6В, 9V, 14, 18С, 19F, 23F, обеспечивая специфическую защиту организма от вызываемых ими инфекций.
У детей первого года жизни, начиная с 2-х месячного возраста, при использовании различных схем вакцинации, продемонстрировано формирование защитного иммунного ответа после серии первичной вакцинации и вторичного иммунного ответа на последнюю дозу, т.е. при ревакцинации. Превенар индуцирует образование функциональных антител ко всем серотипам вакцины.
У детей в возрасте от 2 до 5 лет выраженное образование антител ко всем серотипам вакцины наблюдается после однократного введения Превенара, при этом иммунный ответ практически совпадал с таковым у детей первых двух лет жизни после серии первичной иммунизации.
Профилактика заболеваний, вызываемых Streptococcus pneumoniae серотипов 4, 6В, 9V, 14, 18С, 19F и 23F (включая сепсис, менингит, пневмонию, бактериемию и острый средний отит) у детей в возрасте от 2 месяцев до 5 лет.
Повышенная чувствительность при предшествующем введении Превенара, повышенная чувствительность к вспомогательным веществам и/или дифтерийному анатоксину; острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний (в этих случаях вакцинацию проводят после выздоровления или в стадии ремиссии).
Способ применения и дозы
Вакцину вводят только внутримышечно в переднебоковую поверхность бедра (детям до 2 лет) или в дельтовидную мышцу плеча (детям старше 2 лет).
1 доза однократно
Безопасность Превенара была изучена у здоровых детей в возрасте от 6 недель до 18 месяцев. Во всех случаях Превенар применялся одновременно с другими рекомендованными детскими вакцинами. Самыми частыми нежелательными реакциями были болезненность в месте инъекции и лихорадка (повышение температуры).
При ревакцинации наиболее часто наблюдались случаи быстро проходящей болезненности в месте инъекции (36,5%), а также случаи кратковременного ограничения объема движений конечности из-за болезненности в месте инъекции (18,5%).
У детей старшего возраста, получивших вакцину однократно, наблюдалась более высокая частота местных реакций, чем у детей до 1,5 лет, но эти реакции были непродолжительными.
Описано несколько случаев передозировки Превенара, а также введение последующей дозы раньше предписанных сроков. Наблюдаемые при передозировке нежелательные реакции соответствовали таковым при использовании рекомендуемых разовых доз Превенара.
Взаимодействие с другими лекарственными препаратами и прочие виды взаимодействий
Превенар можно вводить детям одновременно (в один день) с другими вакцинами, включенными в Национальный календарь профилактических прививок (за исключением БЦЖ), а также с вакциной против Hemophilus influenzae тип b (Хиб) и гексавалентной вакциной Инфанрикс, согласно предписанной схеме иммунизации. Вводить вакцины необходимо всегда в разные участки тела.
По 0,5 мл препарата в одноразовых шприцах из прозрачного бесцветного боросиликатного стекла.
Условия транспортирования и хранения
При температуре от 2 до 8 0C.
Срок годности: 3 года
Подробую информацию по применению препарата Превенар см. в полной инструкции по медицинскому применению.
От чего защищает прививка Превенар
Пневмококковая инфекция осложняет течение бронхита, менингита, отита, синусита и пневмонии. Требуется надежная профилактика во избежание серьезных последствий для здоровья. Современной педиатрии хорошо известна прививка Превенар: от чего спасает вакцинация, подробно изложено в инструкции. Врачи выполняют иммунизацию в условиях стационара, предварительно обследуя ребенка на предмет простудных заболеваний. Узнайте обо всех достоинствах и недостатках американского медикамента для профилактики пневмонии и французского аналога.
Инструкция к пневмококковой прививке Превенар
Об инновационном препарате Превенар наслышаны многие специалисты области педиатрии, некоторые настоятельно рекомендуют сделать выбор в пользу этой профилактической прививки. В описании к медицинскому препарату сказано, что активным компонентом являются пневмококковые полисахариды из грамположительных бактерий. Необходимо ввести дозу препарата – искусственная инфекция из него спровоцирует выработку антител. После такого взаимодействия организм взрослого человека и ребенка получает защиту против пневмококковой инфекции и ее последствий.
В медицинском календаре указано, когда требуется выполнять профилактическую вакцинацию. Действия врачей указаны в нормах ВОЗ – профилактическом календаре прививок. Чтобы обеспечить устойчивый иммунитет, вводить лекарство требуется несколько раз в разном возрасте. Прививку Превенар от чего назначают? Среди показаний следует выделить профилактику следующих диагнозов:
Прививка от пневмонии под названием Превенар вводится в детском возрасте. Разовая порция – 0,5 мл. Этой дозы хватает, чтобы не вызывать побочные эффекты, но обеспечить устойчивость антител. Если необходимо привить ребенка до 6 месяцев жизни, схема вакцинации Превенар предлагается на выбор:
Такая вакцина пневмококковая – это гарант здоровья, возможность избежать смертельных диагнозов и не подвергать риску жизнь маленького ребенка. Если грудным детям не выполнена Превенар или Пневмо 23, последовательность действий следующая:
- первичная вакцинация в период 7-11 месяцев с временным интервалом 1 месяц. Ревакцинация – в 2 года;
- в 1-2 года провести двукратную вакцинацию с временным промежутком 2 месяца;
- однократно ввести Превенар в возрасте 2-5 лет.
Кто производитель Превенар 13
Вакцина пневмококковая обладает высокой эффективностью, при этом не является разработкой отечественной фармакологии. Серийным выпуском препарата занимается американская фирма-производитель Пфайзер (США). Препарат дорогостоящий, доступен не всем семьям с маленькими детьми. Достойной альтернативой стала прививка Пневмо 23 – бюджетный вариант французского производства.