Всем мамам известно, что естественную защиту ребенка от болезней в первую очередь обеспечивает иммунитет. В организме каждого человека, даже младенца, присутствуют различные микроорганизмы, как оказывающие благотворное воздействие на состояние здоровья, так и отрицательное. Полезные бактерии в кишечнике малыша становятся непосредственными участниками процесса защитной реакции, оберегая кроху от атаки болезнетворных микроорганизмов. В желудочно-кишечном тракте находится большая часть иммунных клеток организма, основной функцией которых является предотвращение развития заболеваний.
Такой многоликий иммунитет
Существует 2 механизма формирования иммунитета - врожденный и приобретенный. Предназначение врожденного - защита организма от простейших вредоносных микроорганизмов в период, когда приобретенный иммунитет еще не сформирован. Приобретенный же иммунитет возникает непосредственно при контакте организма с новым видом бактерий при заболевании.
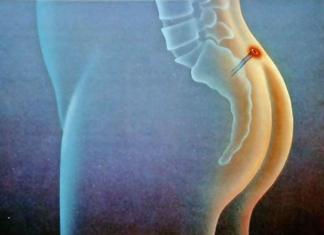
Примечательно, что самый быстрый и простой способ для болезнетворных бактерий попасть в кровь малыша - просочиться через стенки кишечника. Слизистая оболочка, выстилающая желудок крохи, обладает высокой всасываемостью, а незрелый иммунитет не сразу распознает потенциальную опасность и не успевает вовремя среагировать. В результате, слизистые оболочки ЖКТ могут заселить патогенные микроорганизмы. Это, в конечном итоге, приведет к возникновению дисбактериоза, диареи, нарушений стула и других расстройств желудка, связанных с нарушениями баланса микрофлоры кишечника.
Естественная защита иммунитета
Уже в процессе прохождения по родовым путям и после первого прикладывания к груди мамы, в организме малыша запускается естественный процесс формирования собственной микрофлоры кишечника. Если же ребенок появился на свет вследствие кесарева сечения и был лишен возможности получить первые бактерии естественным путем, то процесс заселения микрофлоры полезными бактериями нарушается.

К снижению защитных свойств организма также приводит лечение антибиотиками, искусственное вскармливание, неблагоприятные факторы окружающей среды, а также эмоциональные переживания. Разлука с мамой, введение первого прикорма, отлучение от груди или соски - все эти стрессовые моменты могут стать причиной снижения иммунных свойств и развития дисбактериоза. Для формирования здоровой микрофлоры кишечника малыша и поддержания иммунитета в любом возрасте целесообразно применение натурального и безопасного препарата Аципол, подходящего даже новорожденным малышам.
Аципол - натуральный синбиотик с активными, живыми лактобактериями. В составе препарата содержатся не только пробиотик - полезные бактерии, но и пребиотик -полисахарид кефирного грибка, который обеспечивает питательную среду для дальнейшего активного размножения полезных бактерий и способствует повышению иммунитета. Аципол не содержит лактозы, что особенно важно для младенцев, страдающих лактазной недостаточностью. Аципол быстро и бережно восстанавливает микрофлору кишечника, способствует устранению симптомов дисбактериоза - дискомфорта в животе, диареи, запора, вздутия и других, а также служит эффективным профилактическим средством для предотвращения проблем с кишечником.
Прием Аципола, прогулки на свежем воздухе, сеансы закаливания и другие полезные для естественного развития иммунитета процедуры позволят обеспечить малышу комфорт, хорошее самочувствие и полноценное развитие иммунитета
Иммунитет – способность организма распознать и обезвредить чужеродный объект. Задача иммунитета обеспечить постоянство организма на клеточном уровне и на общем. Осуществляется он с помощью иммунной системы.
Иммунная система состоит из:
- центральных органов;
- тимуса;
- красного костного мозга;
- периферических органов;
- лимфатических узлов;
- селезёнки;
- местноассоциированных бронхолегочных лимфоидных тканей;
- местноассоциированных кишечных лимфоидных тканей;
- местноассоциированных кожных лимфоидных тканей.
Функции иммунитета:
Алиментарный (через пищеварительную систему, болезнь «грязных рук») путь заражения – ведущий механизм попадания инфекции в организм. Помимо инфекции к нам в организм через желудочно-кишечный тракт могут попасть гельминты, простейшие, ядовитые вещества неживой природы. Со всеми этими угрозами нашему организму помогает справиться кишечник.
Кишечник – важнейший орган иммунной системы, ведь именно в нём содержится наибольшее количество иммунных клеток
Основные узлы в иммунной системе кишечника:
- пейеровы бляшки;
- аппендикс;
- лимфоузлы.
Механизм реализации иммунитета

Иммунитет кишечника осуществляется специальными клетками – лимфоцитами, которые вырабатывают специфические вещества – иммуноглобулины, которые в свою очередь и распознают инфекции, определяют степень угрозы, борются с ней. Иммуноглобулины бывают разных типов.
Секреторный иммуноглобулин А мешает чужим бактериям прикрепиться к стенкам кишечника – главный «санитар». Иммуноглобулин М – впервые поступает в наш организм ещё с грудным молоком матери, помогает распознать где опасность, а где вполне безобидная бактерия – это иммуноглобулин памяти. Удачное сотрудничество этих двух иммуноглобулинов и позволяет не только защититься от чужеродных патогенных бактерий, но и помочь полезным бактериям прикрепиться к стенке кишечника и встать на стражу нашего здоровья.
Не последнее место в иммунитете кишечника занимает биопленка, выстилая всю поверхность органа, она защищает наш организм не только от плохих бактерий, но и от химических и физических раздражителей.
Активность и состоятельность иммунного ответа на возбудителя инфекции зависит от ряда факторов:
- отсутствие или наличие повреждений биопленки органа;
- зрелости иммунной системы;
- острых и хронических инфекций кишечника;
- питания;
- общего потенциала иммунной системы человека.
Для того чтобы кишечник смог в полном объеме обеспечить защиту организма от чужеродного агрессора, существует ряд механизмов. На всем протяжении кишечник покрыт плотной пленкой гликокаликс, которая защищает его от механических повреждений. В слизистой оболочке есть лимфоциты, которые в случае необходимости не только будут бороться с врагом, но и «призовут» клетки из других иммунных органов, усилив кровоснабжение. Чередование отделов кишечника с кислой средой с отделами щелочной природы помогают не пропустить бактерии ни одного типа. И самое главное, вся поверхность слизистой оболочки густо заселена полезной микрофлорой, что просто не даёт заселиться патогенным бактериям.
Кишечная микрофлора и её роль в иммунитете

Вся поверхность кишечника заселена микроорганизмами, исключением является только начальный отдел тонкого кишечника по причине сильнокислой среды непригодной для жизни микрофлоры.
Основную долю микроорганизмов пищеварительной системы составляют лактобактерии и бифидобактерии. Эти кишечные бактерии – неотъемлемая часть биопленки. Нормофлора не только мешает чужеродным патогенным бактериям прикрепится к стенке органа, но и подавляет размножение уже прикрепившихся микроорганизмов, путём конкуренции за необходимые питательные средства.
Помимо этого, нормофлора кишечника помогает организму в переваривании пищи, они способны расщеплять растительные волокна. При снижении количества полезных бактерий повышается проницаемость слизистой к макромолекулам пищи. Также снижается способность кишечника вырабатывать иммуноглобулин А.
Подтверждением важности нормального баланса микрофлоры в кишечнике может служить то, что новорожденные адаптируются к самостоятельному перевариванию пищи в течении некоторого времени. Пока иммунитет ещё не созрел, необходимые иммуноглобулины, в частности А, новорожденный получает с молоком матери что помогает нормальной микрофлоре занять своё место в биопленке. Но в случае отсутствия грудного вскармливания этот процесс нарушается, как следствие, организм малыша заселяет условно патогенная микрофлора, то приводит к нарушениям иммунитета и частым возникновением аллергий.
Причины нарушения микрофлоры
Равновесие в системе микрофлоры кишечника очень просто нарушить, полезные бактерии из строя могут выбить различные факторы:
- Антибиотики. Часто пациентам для борьбы с инфекциями назначают антибиотики. Это очень эффективные лекарственные вещества, но их недостатком является слабая избирательность, проще говоря, им всё равно, кого убивать – злых микробов или полезную микрофлору.
- Лечение с применением химио либо лучевой терапии.
- Заболевания с нарушением ферментативного ряда.
- Системные заболевания – рак, СПИД.
- Водопроводная вода. Для обеззараживания и очистки питьевой воды в её состав вводятся химические вещества фтор, хлор. Эти вещества убивают микрофлору организма.
- Плохая экология.
- Нарушение питания и т.д.

Очень большое влияние на состав микрофлоры кишечника оказывает характер пищи, которую мы употребляем. Так, избыточное количество сахара в еде может привести к повышенному размножению грибов рода Кандида и, как следствие, к кандидозу. Сахар – любимое лакомство для кандид.
Также недопустимо переедание. Если пищеварительная система не успевает справиться со всем поступившим объёмом пищи, то в кишечнике начинаются процессы разложения и гниения, которые также приводят к гибели здоровой микрофлоры, а значит и к росту условно патогенной.
Наличие глистной инвазии оказывает очень неблагоприятное влияние на микрофлору и иммунитет всего организма. Наличие заболеваний, которые меняют среду кишечника (гепатит, гастрит, язвенная болезнь, холецистит) также не лучшим образом скажется на количестве полезных бактерий.
Низкое количество ферментов в результате нарушений функций поджелудочной железы, желудка, печени также нарушит состав микрофлоры.
Симптомы дисбактериоза
Диагноз дисбактериоз может поставить только ваш лечащий врач на основании результатов посева каловых масс на микрофлору. Но основными симптомами дисбактериоза можно считать:
- рвота;
- понос;
- тошнота;
- отрыжка;
- неприятный запах изо рта;
- вздутие живота;
- боли в животе и др.
Лечение при дисбактериозе

Обычно лечение дисбактериоза проводят в несколько этапов.
В первую очередь нужно нормализовать условия в кишечнике для нормальной микрофлоры. Потому следует избегать стрессов, чрезмерной физической нагрузки, следует соблюдать режим сна и бодрствования, а также наладить режим питания.
Не следует употреблять жирную, кислую, любую острую раздражающую пищу. Продукты питания должны быть богаты витаминами, с правильным балансом белков, жиров и углеводов. Не должно быть больших промежутков межу приёмами пищи. Последний приём пищи необходимо совершать не позднее, чем за 3 часа до сна. Важно также есть не спеша, тщательно пережёвывая пищу.
Вторым этапом должно стать снижение количества патогенных микробов. Это достигается путём применения лекарственных препаратов - нитроксолин, фуразолидон и подобных. Обычно антисептики назначают на 10-14 дней.
Далее необходимо заселить стенки кишечника полезной микрофлорой. Для этого необходимо комбинировать применение пробиотиков и пребиотиков. Пробиотики – препараты, состоящие из полезных кишечных бактерии. Наиболее правильные бактерии это бифидо и лактобактерии, а значит подойдут препараты энтерол, бифиформ, линекс, бифидумбактерин и другие. Пребиотики – препараты поддерживающие благоприятный микроклимат в кишечнике для нормальной микрофлоры. Из пребиотиков наибольшей популярностью пользуется хилак форте.
Также необходимо повышать общий иммунитет, пить витамины и сорбенты.
Народные методы укрепления кишечного иммунитета
Если вы не хотите применять лекарственные препараты, то в борьбе с дисбактериозом вам может помочь обычная сыворотка. Приготовить её не сложно, достаточно подогреть кефир, который свернётся и разделится на творог и сыворотку.
Также можно применить чесночную простоквашу. Для этого необходимо прокипятить молоко, дождаться полного остывания. Потом заквасить сухариками из черного хлеба в течении 24 часов. После этого добавить в неё ещё сухарики натертые чесноком. Можно хранить в холодильнике и есть по желанию.
Для повышения кишечного иммунитета также считается очень полезным есть натощак утром землянику, желательно по 1 стакану в течении 10 дней.
Заключение
Кишечный иммунитет важное звено всей иммунной системы организма, а значит нашей безопасности. Соблюдайте все принципы здорового образа жизни: полноценно питайтесь, качественно отдыхайте, избегайте стрессов, следите за общим состоянием организма! И тогда вашему кишечному иммунитету ничего не грозит! Будьте здоровы!
Многие общие закономерности иммунитета слизистых оболочек были выявлены и детально изучены на примере кишечного иммунитета. По массе иммунокомпетентных клеток кишечнику принадлежит ведущее место в иммунной системе слизистых покровов, и в этом отношении он значительно превосходит иммунную систему респираторного тракта.
Кишечник - важный иммунологический орган, в собственной пластике (lamina propria) которого содержится столько же лимфоидных клеток, сколько в селезенке. Среди этих клеток идентифицированы Т-, В-клетки, малые лимфоциты и плазматические клетки. Последние синтезируют иммуноглобулины преимущественно класса А и являются источником антител, секретируемых слизистой оболочкой кишечника. Многочисленные малые лимфоциты контролируют выработку антител и, кроме того, осуществляют реакции клеточного иммунитета. Иммунологическая функция кишечника опосредована действием, прежде всего, лимфоцитов, расположенных в пейеровых бляшках и в слизистой оболочке. Популяция лимфоцитов пейеровых бляшек состоит из предшественников В-(80%) и Т-(20%) клеток.
Лимфоциты эпителиального слоя кишечной стенки представлены исключительно Т-клетками, тогда как в подслизистом слое преобладают В-клетки, большинство из которых синтезируют IgA. Исключение составляют жвачные животные, у которых в подслизистом слое преобладают IgG, продуцирующие клетки.
Иммунитет против энтеропатогенных агентов в основном осуществляется посредством антител, секретируемых в просвет кишечника. Антитела, защищающие слизистую оболочку кишечника, могут поступать из двух источников: из сыворотки крови и плазматических клеток, расположенных в lamina propria. Сывороточные антитела, очевидно, менее эффективны, поскольку достаточное для местной защиты количество их накапливается в кишечнике только при наличии высоких уровней в сыворотке крови. Сывороточные антитела, участвующие в создании местного иммунитета, проникают в просвет кишечника в результате экссудации и относятся преимущественно к классу IgG.
Защитный эффект при гриппе обеспечивается главным образом продукцией циркулирующих антител и других факторов системного иммунитета, которые защищают от инфекции легкие, но слабо ограничивают размножение вируса в верхней части респираторного тракта. Подобным образом циркулирующие антитела (IgG) могут переноситься из крови в желудочно-кишечный тракт и защищать телят от ротавирусной инфекции.
Однако антитела , синтезируемые местно плазматическими клетками кишечника, обычно относятся к IgA и в силу устойчивости к протеолитическим ферментам в большей степени приспособлены к защите поверхности слизистой оболочки, чем IgG. Иммунная система кишечника во многом функционирует независимо от системных иммунных механизмов. Это прежде всего относится к иммунной системе кишечника свиней. Антигенная стимуляция В- и Т-клеток происходит в пейеровых бляшках, представленных отдельными скоплениями лимфоидных клеток, расположенных в подслизистом слое тонкого отдела кишечника.
Эпителий слизистой оболочки кишечника, покрывающий пейеровы бляшки, видоизменен: он образует лишь рудиментные ворсинки и обладает повышенной способностью к пиноцитозу Эти эпителиальные клетки обладают специализированной функцией «захвата» антигена из просвета кишечника и представляют его лимфоидным элементам бляшек. Они утратили характерную цилиндрическую форму, содержат много цитоплазматических вакуолей и называются мембранными или М-клетками, так как имеют микроскладки.
Эпителий кишечника способен распознавать микроорганизмы благодаря наличию трех типов клеток: дендритных клеток, М-клеток пейеровых бляшек и эпителиальных клеток кишечника. Взаимодействие с бактериями может обусловить возникновение иммунных Th1- и Th2-ответов, которые удерживаются в равновесии благодаря цитокинам и регуляторным Т-клеткам (Treg). Кроме того, воздействие бактерий может привести к продукции как хемокинов, так и цитопротективных факторов.IFN - интерферон;
IL - интерлейкин;
TCF - трансформирующий фактор роста;
Th - Т-хелперы;
TNF - фактор некроза опухоли;
ГКГС - главный комплекс гистосовместимости
Частота формирования ротавирусспецифичных Тц-лимфоцитов в пейеровых бляшках после перорального инфицирования в 25-30 раз превышала частоту образования соответствующих клеток после инокуляции вируса в лапу мышей. Эффективность энтеральной иммунизации ротавирусом связывают со способностью его проникать в ткань пейеровых бляшек. Полагают, что реовирусы преодолевают кишечный эпителий благодаря М-клеткам, играющим ведущую роль в доставке чужеродных антигенов и, в том числе, вирусов во внутреннюю среду организма и к его иммунной системе. Эпителиальные клетки, подобные М-клеткам кишечника, обнаружены и среди клеток BALT, их рассматривают как респираторные эквиваленты клеток GALT.
Первичное воздействие антигена вызывает пролиферацию В-клеток, часть которых превращается в иммунобласты и покидает бляшки. Большая часть клеток остается в бляшках в виде чувствительных к данному антигену В-клеток. При повторном контакте с тем же антигеном эти клетки превращаются в IgA-иммунобласты, которые пролифелируют и мигрируют сначала в брыжеечные лимфатические узлы, а затем через грудной лимфатический проток в кровеносное русло. Часть таких клеток может оседать в отдаленных IgA-секретирующих участках тела. Однако большинство клеток уже в качестве зрелых плазмоцитов осуществляет специфический homing в lamina propria, что обусловлено присутствием антигена и свидетельствует о его определяющей роли в данном процессе.
Вторичный иммунный ответ - сильный и быстрый. Он развивается в течение 48-60 ч, достигает максимума на 4-5-й день, а затем быстро снижается.
Мигрирующие Т-клетки также осуществляют homing в эпителиальном слое слизистой оболочки кишечника. Большинство из этих лимфоцитов обладают Т-хелперным фенотипом. Эти клетки, вероятно, могут вовлекаться в реакции клеточного иммунитета, иммунотолерантности, а также в регуляцию гуморального иммунитета.
Стимулированные местно или осевшие из кровяного русла lgA-продуцирующие клетки в собственной пластинке секретируют IgA в виде димера 9S, проникающего в эпителиальные М-клетки, соединяются с образующимся в них секреторным компонентом и выделяются на поверхность слизистой оболочки в виде иммуноглобулина. Одновременно на поверхность эпителиальных мембран выделяется секреторный компонент в виде свободных молекул. Слизь, обогащенная нековалентно связанными секреторными иммуноглобулинами, выстилает поверхность эпителиальных клеток наподобие ковра. Тем самым обеспечивается протективный эффект, предотвращающий адгезию и инвазию инфекционных агентов.
IgM также продуцируются местно и проявляют свойства, сходные со свойствами секреторного IgA. Показано, что пентамерные 19S молекулы IgM содержат секреторный компонент, хотя эта связь менее прочная.
Продолжительная защита слизистых оболочек местными антителами может быть обусловлена длительной, хотя и умеренной выработкой антител после окончания специфического антигенного воздействия или быстроактивизируемой иммунологической памятью. Обнаружение в системе слизистых оболочек первичного и вторичного иммунного ответа свидетельствует о наличии в ней местной иммунологической памяти, однако ее длительность и уровень вторичного ответа могут зависеть от многих факторов. Например, мыши, иммунизированные интраназально коронавирусом гепатита, имели более продолжительный иммунитет, чем привитые орально. На примере ротавирусной инфекции цыплят доказано, что IgA кишечника являются важным, но не единственным фактором защиты. IgA молозива не адсорбируются в кишечнике новорожденных и остаются там, проявляя местный защитный эффект, нейтрализуя вирус.