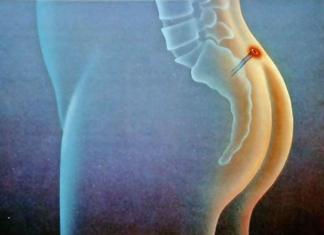
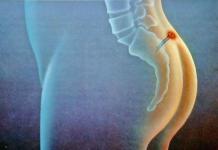
Anterior se credea că ALS afecta doar neuronii motori care controlează mușchii. Cu toate acestea, există acum o înțelegere a schimbărilor care apar în creier în timpul acestei boli, care afectează procesele de gândire, exprimarea emoțiilor și comportamentul pacienților. Acest articol vă va ajuta să înțelegeți natura schimbărilor în procesele funcțiilor mentale superioare în SLA.
Ce înseamnă „schimbarea funcțiilor mentale (cognitive) superioare”?
Funcții cognitive (lat. cognitio — cogniție) — acestea sunt funcții superioare ale creierului: memorie, atenție, coordonare psihomotorie, vorbire, numărare, gândire, orientare, planificare și control al activității mentale superioare. Acestea includ, de asemenea, comunicarea verbală, cum ar fi capacitatea de a pronunța cuvinte, de a răspunde și de a interacționa cu alte persoane.
În ceea ce privește afectarea funcțiilor mentale superioare, persoanele cu SLA pot fi împărțite în patru categorii în funcție de gradul de afectare:
- fără modificări cognitive;
- modificări subtile în comportament și cogniție;
- modificări pronunțate ale comportamentului și proceselor cognitive cu dezvoltarea demenței frontotemporale (FTD);
- persoanele cu DFT care dezvoltă tulburări de mișcare și care sunt diagnosticate cu SLA după demență.
Unii oameni experimentează schimbări ușoare, subtile, în timp ce alții experimentează schimbări mai vizibile.
FTD — Acesta este un tip de demență în care se dezvoltă modificări grave ale cogniției și comportamentului. Aproximativ 5% dintre persoanele cu SLA au, de asemenea, DFT. Acest tip este diferit de boala Alzheimer, care este cea mai comună formă de demență.
Cât de des se confruntă persoanele cu SLA schimbări în gândire și comportament?
Cercetări recente sugerează că până la 50% dintre pacienții cu SLA nu experimentează niciodată schimbări vizibile în gândire și comportament dincolo de reacțiile psihologice normale. În ceea ce privește a doua jumătate a pacienților, aproximativ 25% dintre aceștia pot prezenta demență frontotemporală.
Care sunt factorii de risc pentru dezvoltarea unor astfel de tulburări în SLA?
Vârsta înaintată, forma bulbară a bolii, alte antecedente familiale de demență și tulburările neurologice diagnosticate anterior sunt considerate factori care cresc probabilitatea de a dezvolta tulburări cognitive și comportamentale în SLA. Dar cazuri de dezvoltare a acestor simptome au fost identificate și la persoane care nu au întâlnit factorii de risc menționați. Până în prezent, singurul factor de risc confirmat pentru dezvoltarea tulburărilor cognitive și comportamentale este o defecțiune a genei C9ORF72.
Manifestări externe ale modificărilor în funcțiile mentale superioare
Schimbările în funcțiile mentale superioare se pot manifesta sub diferite forme. Unii oameni le este dificil:
- concentrați-vă, de exemplu, în timp ce citiți;
- a începe ceva nou sau a învăța să folosească echipamente noi;
- începe o conversație;
- menține o conversație dacă există o distragere a atenției;
- planificați orice succesiune de acțiuni;
- începe lucruri sau sarcini;
- duce lucrurile la capăt;
- a face mai mult de un lucru la un moment dat, cum ar fi să vorbești cu cineva în timp ce te uiți la televizor;
- amintiți-vă numele obiectelor pe care le cunoșteau anterior;
- înțelege propoziții complexe.
Ca urmare, se dezvoltă unele schimbări:
- comportament incomod, infantil sau pur și simplu necaracteristic pentru pacient;
- comentarii nepotrivite;
- consum mare de dulciuri sau un anumit tip de hrană sau mestecat prea mult timp;
- scăderea atenției la problemele de igienă, de exemplu, atunci când vizitați toaleta sau refuzul de a face baie regulată, de a vă tuns sau de a vă schimba hainele;
- pierderea judecății necesare pentru a lua decizii sau luarea unor decizii care sunt foarte diferite de ceea ce a spus pacientul anterior;
- lipsa de reacție sau indiferența față de stările emoționale ale celorlalți;
- fixare pe o anumită sarcină de rutină;
- agresivitate crescută;
- pacientul poate spune „da” în loc de „nu” sau invers, sau poate fi nesigur de răspunsul la întrebări simple;
- un sentiment de deconectare între gândul de a dori să miști o anumită parte a corpului și acțiunea în sine;
- construcția incorectă a frazelor;
- incapacitatea de a găsi cuvântul potrivit în timpul unei conversații;
- senzație de neliniște;
- întrebuinţare abuzivă a cuvintelor;
- folosirea de propoziții fără sens;
- incapacitatea de a urma instrucțiunile în timpul terapiei fizice sau a altor proceduri;
- uitarea a ceea ce pacientul a intenționat să facă;
- lipsa de motivație sau inițiativă;
- acțiuni impulsive fără a se gândi la consecințe.
Este posibil ca persoana bolnavă să nu fie conștientă de schimbările care au loc. Acest lucru este de obicei foarte supărător pentru alții și membrii familiei.
Schimbările de gândire și comportament în SLA pot fi asociate nu numai cu dezvoltarea bolii, ci și cu alți factori, de exemplu, procese respiratorii insuficiente (nivel scăzut de oxigen sau nivel ridicat de dioxid de carbon), efecte secundare medicamente, depresie sau anxietate, tulburări de somn sau o tulburare mentală sau neurologică preexistentă. Este important să raportați toate simptomele profesioniștilor din domeniul sănătății, astfel încât aceștia să poată determina cauza problemei, mai ales dacă aceasta poate fi corectată.
Ce se mai poate întâmpla dacă funcțiile mentale superioare sunt încălcate?
Dispozitie
Desigur, încercările de a vă adapta viața la SLA progresivă duc la schimbări ale dispoziției. Multe persoane cu această afecțiune se simt foarte goale.
Pentru unii, aceste sentimente sunt atât de puternice încât se dezvoltă depresia. Dacă o persoană are dificultăți în a finaliza o activitate sau are dificultăți de concentrare, aceasta se poate datora unei dispoziții scăzute, mai degrabă decât modificărilor de conștiență. Unii oameni iau medicamente, cum ar fi antidepresive, pentru aceste afecțiuni. Poate fi necesară consultarea de specialitate.
Labilitate emoțională
Unii oameni cu ALS devin instabili emoțional. Acest lucru duce la râs incontrolabil sau, dimpotrivă, la plâns ca răspuns la ceva care nu este suficient de amuzant sau trist pentru a da o reacție atât de puternică, de exemplu, un program de televiziune. Uneori pare foarte nepotrivit și îi încurcă pe alții. Pacienții cu SLA sunt susceptibili la labilitate emoțională fără prezența altor simptome cognitive, comportamentale sau psihologice.
Suflare
Dacă ALS afectează respirația, aceasta afectează calitatea somnului, ceea ce duce și la modificări ale concentrării și memoriei. Când un ventilator este utilizat pentru a ajuta respirația, merită să verificați setările acestuia pentru a vă asigura că funcționează corect.
Bunăstare
Uneori, gândirea confuză poate fi o consecință boli infecțioase tractului respirator sau sistemul genito-urinar. Prin urmare, merită să acordați atenție prezenței factorilor caracteristici infecției, cum ar fi febra și sănătatea precară.
Cum sunt diagnosticate tulburările cognitive și comportamentale în SLA?
Pentru a determina dacă simptomele se datorează ALS sau unui alt proces, trebuie efectuată o evaluare adecvată a stării pacientului. De obicei, acest lucru poate fi făcut de medicul dumneavoastră sau de neuropsiholog. Evaluarea se bazează pe diverse teste care reflectă modul în care o persoană procesează informațiile. De exemplu, medicul vă poate cere să numiți cât mai multe cuvinte care încep cu o anumită literă a alfabetului, sau să vă amintiți cât mai multe cuvinte și să le recitați sau să scrieți cuvinte. Rezultatele obținute sunt comparate cu indicatori standard pentru persoane de aceeași vârstă și cu același nivel de educație. Acest lucru face posibil să se determine dacă încălcările sunt efectiv prezente și, dacă da, de ce fel. Profesionist poate avea nevoie să discute situația nu numai cu pacientul, ci și cu persoanele care îl îngrijesc și/sau care îl cunosc bine.
Ce se întâmplă după ce diagnosticul este confirmat?
Unele familii și îngrijitori se simt ușurați după confirmarea deficienței, deoarece știu sigur că modificările cognitive și comportamentale la persoana cu SLA nu se datorează unor motive psihologice sau încercărilor de a rezista altor persoane. Dacă o persoană cu SLA este conștientă de acțiunile sale, își poate documenta dorințele cu privire la îngrijirea și terapia viitoare. Acest lucru este deosebit de important deoarece afectarea cognitivă și comportamentală, ca și alte simptome de SLA, se agravează pe măsură ce boala progresează.
Dacă pacientul este deja incapacitat, membrii familiei, îngrijitorii și profesioniștii medicali trebuie să își echilibreze așteptările față de pacient cu realitatea. În această situație, nu trebuie să vă așteptați ca persoana să-și schimbe comportamentul. Mediul trebuie să se schimbe. Așteptările pentru pacient trebuie să corespundă capacităților sale. Dacă pacientul devine distant sau anxios când i se cere să facă ceva, acesta poate fi un semn că așteptările îi depășesc capacitățile. Mai mult, dacă membrii familiei sau îngrijitorii încep să se simtă frustrați sau resentiți atunci când interacționează cu pacientul, așteptările situației trebuie simplificate. În cazul demenței, toți profesioniștii care lucrează cu pacientul trebuie să își concentreze eforturile pe educarea și implicarea îngrijitorilor și a membrilor familiei, deoarece pacientul nu se poate schimba din proprie voință.
Membrii familiei și îngrijitorii pot beneficia de asistența la consultații psihologice, grupuri suport psihologic, întâlniri spirituale, sau acordarea mai multă atenție la ei înșiși, ceea ce le va permite, de asemenea, să-și mărească resursele (fizice și emoționale) necesare pentru a avea grijă de cineva cu SLA.
Cum afectează prezența unor astfel de tulburări progresia SLA?
Există dovezi că persoanele cu deficiențe cognitive și comportamentale în SLA trăiesc o viață mai scurtă decât pacienții fără aceste simptome. Sunt efectuate multe studii pentru a determina dacă prezența sau absența acestor tulburări afectează eficacitatea medicamentelor, tratamentelor și altor tratamente pentru SLA. Acesta este un domeniu important al cercetării științifice.
Ce urmeaza?
Medicul dumneavoastră vă poate recomanda testarea. Acest lucru va ajuta la identificarea cauzei schimbării. Ei vă pot spune și despre opțiunile de depășire a unor dificultăți. Medicul poate da recomandări cu privire la modul de comunicare cu persoana, de exemplu, pune întrebări cu doar răspunsuri „da” sau „nu”, evita lung și propoziții complexe, necesitând clarificări.
Există multe modalități de a face comunicarea și sarcinile zilnice mai ușoare. Scopul final al acestor recomandări —
ajutați o persoană cu SLA să se controleze. De asemenea, va fi foarte benefic pentru îngrijitorii și membrii familiei.
Dacă înțelegem motivele schimbărilor în conștiința unei persoane, atunci îngrijitorii vor acționa cu mai multă încredere.
- Învață și îmbunătăți.
- Aveți grijă de dumneavoastră.
- Încercați să faceți comunicarea cu pacientul cât mai ușoară posibil. Folosiți fraze scurte. Puneți întrebări la care se poate răspunde cu „da” sau „nu”. Vorbește rar.
- Însoțiți pacientul în timpul oricăror întâlniri pentru a vă asigura că schimbul de informații între pacient și interlocutori are loc în mod corect.
- Aliniați-vă așteptările pentru pacientul cu SLA cu realitatea. Dacă cererea dumneavoastră provoacă iritare, resentimente sau respingere la pacient sau la dumneavoastră, așteptările trebuie modificate pentru a satisface nevoile și capacitățile persoanei aflate în îngrijirea dumneavoastră.
- Spuneți profesioniștilor implicați în tratamentul pacientului dumneavoastră și vă pasă de starea dumneavoastră.
- Continuați să urmăriți relații și activități care vă aduc bucurie și luați o pauză de la cele care vă provoacă stres.
Cine poate ajuta?
Scleroza laterală amiotrofică (SLA) este o boală neurodegenerativă însoțită de moartea neuronilor motori centrali și periferici și care se manifestă prin atrofie a mușchilor scheletici, fasciculații, spasticitate, hiperreflexie și semne piramidale patologice în absența tulburărilor oculomotorii și pelvine; caracterizat printr-un curs constant progresiv, care duce la moarte.
ICD-1O: G12.2. Boala neuronului motor: boala familială a neuronului motor, scleroza laterală amiotrofică; scleroza laterală primară; paralizie bulbară progresivă; atrofie musculară progresivă.
EPIDEMIOLOGIE
Incidența formei sporadice a sclerozei laterale amiotrofice în lume este în medie de 0,2-2,4 cazuri la 100.000 de locuitori pe an, prevalența fiind de 0,8-7,3 la 100.000 de locuitori. Raportul dintre bărbați și femei în rândul pacienților cu toate formele de SLA este de 1,5:1, după 65 de ani se uniformizează. Vârsta de debut a bolii este de 20-80 de ani (cel mai adesea - 50-65 de ani). În 90% din cazuri, SLA este sporadică; SLA cu debut bulbar este depistată la 10-28%, cu debut cervical - la 20-44%, cu debut toracic - la 2-3,5%, cu difuz - la 1-9% din cazuri. Atrofia musculară progresivă este depistată la 2,4-8%; scleroza laterală primară – în 2-3,7% din cazuri. În 10% din cazuri, SLA este familială (dacă există mai mult de un caz de SLA în cadrul aceleiași familii) sau ereditar (singurul caz stabilit în familie dacă pacientul are o mutație cauzală). Aproximativ 25% din cazurile familiale de SLA și 5-7% din cazurile sporadice de SLA sunt asociate cu mutații ale genei superoxid dismutază dependentă de cupru-zinc. În 75% din cazurile de SLA familială cauza genetica rămâne necunoscut. Date despre incidența și prevalența SLA în Federația Rusă lipsesc. În mai multe regiuni ale URSS în 1970, acestea se ridicau la 0,5-2,5 la 100.000 de locuitori.
CLASIFICARE
Nu există o clasificare unificată a SLA, deoarece nu există o înțelegere unificată a patogenezei SLA. Sunt utilizate trei clasificări: clasificarea nord-americană, britanică și națională O.A. Khondkariana (vezi Tabelul 34-1). Conform grupului de clasificare și studiu privind bolile neuromusculare al Federației Mondiale a Neurologilor, SLA este clasificată ca un grup de boli ale neuronilor motori cu cauze necunoscute.
Conform clasificării nord-americane, SLA se împarte în sporadice, familială (care include mai multe subtipuri în funcție de tipul de moștenire, inclusiv cele endemice) și alte două forme endemice sporadice care diferă clinic și patomorfologic. Forma sporadică de SLA include SLA clasică, însoțită de afectarea neuronilor motori centrali și periferici, care se caracterizează prin afectarea primară a unuia sau mai multor niveluri de inervație segmentară (vezi Tabelul 34-1), este progresivă în natură și se generalizează pe măsură ce progresează. .
Termenul „paralizie bulbară progresivă” din această clasificare se referă la o leziune progresivă rară, neînsoțită de generalizare, a neuronilor motori periferici care inervează mușchii bulbari.
Termenii „atrofie musculară progresivă” și „scleroză laterală primară” denotă un sindrom neereditar de afectare izolată lent progresivă a neuronului motor periferic sau central, cu debut la nivelul coloanei vertebrale. Această clasificare se bazează pe ideea unității patogenezei lezării neuronilor motori bulbari, spinali, centrali și periferici în SLA, care este considerată una dintre formele bolii motoneuronilor.
În clasificarea internă, precum și în cea nord-americană, ALS este considerată o formă nosologică unică cu debut (forme) bulbare și spinale, iar atrofia musculară progresivă și scleroza laterală primară sunt absente în ea, deoarece sunt considerate nosologice separate. forme (Tabelul 34-1) .
Tabelul 34-1. Clasificări ale ALS (boala neuronului motor)
Clasificarea ALS din America de Nord
Scleroza laterală amiotrofică sporadică
Scleroza laterală amiotrofică clasică
Debuturi:
- bulbare;
- cervical;
- cufăr *
;
- lombar;
- difuză *
;
- respiratorii *
;
Paralizie bulbară progresivă
Atrofie cervicală progresivă
Scleroza laterală primară
Scleroza laterală amiotrofică familială
Autozomal dominant:
- fără mutații superoxid dismutază - 1 (mutații ale altor gene, defect genetic necunoscut)
Autosomal recesiv:
- asociate cu mutații ale superoxid dismutazei - 1;
- alte forme (se cunosc un total de 10 loci de legătură)
Pacificul de Vest ALS-parkinsonism-complex demență
Clasificarea ALS O.A. Khondkariana (1978)
Forme de SLA:
- bulbare;
- cervicotoracic;
- lombo-sacral;
- primar generalizat
Înalt
Opțiuni:
- mixt (clasic) - afectare uniformă a neuronilor motori centrali și periferici;
- segmental-nuclear - afectarea predominantă a neuronului motor periferic;
- piramidal (forma inalta de SLA) - afectarea predominanta a neuronului motor central.
* d al naibii de SLA descrisă în alte surse.
Etiologie și patogeneză
Se crede că scleroza laterală amiotrofică este o boală neurodegenerativă care este „calea finală” a unei cascade de reacții patologice generale declanșate de diferiți factori declanșatori necunoscuți sau cunoscuți. În unele cazuri, ALS este asociată cu mutații ale genei superoxid dismutază-1 Se presupune că principalul factor patogenetic pentru mutațiile genei superoxid dismutază-1 este efectul citotoxic al enzimei defecte și nu o scădere a antioxidantului său. activitate. Superoxid dismutaza-1 mutant este capabil să se acumuleze între straturile membranei mitocondriale, perturbând transportul axonal și interacționând cu alte proteine, provocând agregarea acestora și perturbând degradarea. Cazurile sporadice ale bolii sunt probabil asociate cu expunerea la factori declanșatori necunoscuți, care (cum ar fi superoxid dismutaza-1 mutantă) își realizează efectele în condiții de încărcare funcțională crescută asupra neuronilor motori, ceea ce duce la vulnerabilitatea lor selectivă asociată cu costuri crescute de energie, cerere mare. pentru calciu intracelular, cu expresie scăzută a proteinelor care leagă calciul, receptori de glutamat de tip AMPA, unii antioxidanți și factori anti-apoptotici. Întărirea funcțiilor neuronilor motori determină eliberarea crescută de glutamat, excitotoxicitatea glutamatului, acumularea de calciu intracelular în exces, activarea enzimelor proteolitice intracelulare, eliberarea de radicali liberi în exces din mitocondrii, deteriorarea microgliei și astrogliei, precum și neuronii motori înșiși, cu degenerarea ulterioară.
Boala este moștenită de tip recesiv legat de X, doar bărbații se îmbolnăvesc.
Modificări morfologice în pacientii cu X-linked distonia-parkinsonismul include în principal moartea neuronală și glioza astrocitară mozaică în regiunea nucleului caudat și a putamenului; uneori procesul degenerativ este mai răspândit.
Boala debutează de obicei în decada 2-4 de viață. Pacienții dezvoltă hiperkinezie distonică focală a feței, mușchilor oromandibulari, gâtului, trunchiului și membrelor. Pe parcursul mai multor ani, apare o formă generalizată de distonie. Pe măsură ce boala progresează, sindromul parkinsonismului, care nu este sensibil la medicamentele levodopa, se dezvoltă treptat. Mai rar, parkinsonismul poate fi prima sau singura manifestare a bolii. Alte simptome neurologice nu sunt tipice.
Curentul este lent progresivă. Medicamentele anticolinergice, baclofenul și clonazepamul pot avea un efect pozitiv asupra severității distoniei și a parkinsonismului.
Complexul ALS-Parkinsonism-Demență.
Acest rar progresiv sindrom neurodegenerativ găsit aproape exclusiv în partea de vest a regiunii Pacificului (insula Guam, o serie de insule din Noua Guinee și Japonia). Majoritatea autorilor atribuie această boală unui tip particular de scleroză laterală amiotrofică (boala neuronului motor) și, prin urmare, în literatură termenii „ALS of Guam Island”, „varianta Pacificului de Vest a bolii neuronului motor”, etc. sunt adesea folosiți pentru a desemna aceasta.
Boala este sporadic. În etiologia acestui sindrom se asumă un anumit rol al intoxicației cronice cu aluminiu, asociat cu caracteristicile regionale ale solului și apei potabile, bogate în aluminiu și relativ sărace în săruri de calciu, ceea ce este tipic pentru teritoriile menționate mai sus. Se discută și efectele neurotoxice ale semințelor plantei de sago Cycas circinalis, folosite de nativi la fabricarea făinii. Unele descrieri ale acumulării familiale de cazuri de complex ALS-parkinsonism-demență se pot datora nu atât unor factori ereditari, cât și acelorași condiții de viață.
Cu toate acestea, există dovezi convingătoare în favoarea naturii toxice a acestei boli nu a fost încă obținut, iar mecanismele dezvoltării sale (inclusiv relația sa cu diverse forme de SLA, demență și parapareză spastică) necesită cercetări suplimentare.
În ultimii ani, a fost exprimată o ipoteză de origine prionică, sugerând că această boală poate fi o variantă clinică unică a encefalopatiilor spongiforme, în primul rând boala Creutzfeldt-Jakob.
Baza morfologică Sindromul ALS-parkinsonism-demență este o leziune multisistemică a sistemului nervos central, cu modificări degenerative care afectează în primul rând nucleii coarnelor anterioare ale măduvei spinării și nervii cranieni, substanța neagră, cortexul motor și tracturile piramidale. Prezența încurcăturilor neurofibrilare în neuronii degenerați este caracteristică.
Boala Cel mai adesea începe în copilărie și adolescență, dar au fost descrise și cazuri de manifestare ulterioară a simptomelor. Tabloul clinic este caracterizat de o combinație de sindrom de scleroză laterală amiotrofică (care este „nucleul” acestei boli și principala cauză de deces pentru pacienți) cu parkinsonism și demență progresivă de tip frontal. Unii pacienți pot prezenta tulburări cerebeloase (de exemplu, tremor de intenție), oftalmoplegie supranucleară. Uneori în tablou clinic domină parapareza spastică progresivă.
Clinica Parkinsonism se manifestă ca sindrom akinetic-rigid grade diferite expresivitate. Ca și în cazul altor boli neurodegenerative aparținând grupului „parkinsonism-plus”, acești pacienți prezintă rareori tremor de repaus, iar medicamentele cu levodopa sunt ineficiente sau au un efect moderat și de scurtă durată.
Se caracterizează schimbările mentale indiferența emoțională, încetineală, perseverențe, scăderea producției spontane de vorbire, afazie motorie. Cursul bolii este progresiv progresiv. Într-o etapă ulterioară, demența profundă se dezvoltă cu dezintegrarea personalității. Moartea apare din cauza tulburărilor respiratorii sau a complicațiilor infecțioase la câțiva ani de la apariția primelor simptome.
Sindromul Parkinsonism poate fi observată într-o serie de boli metabolice ereditare (în principal autosomal recesive), cum ar fi degenerescența hepatolenticulară, gangliozidozele GM1 și CM2, lipofuscinozele neuronale ceroid, hemocromatoza ereditară, boala Niemann-Pick, xantomatoza cerebrotendinală, neuroacantoyocitoza etc.
Diagnosticul acestor boli se bazează pe efectuarea unor teste biochimice adecvate (studiarea activității enzimelor lizozomale, a nivelului seric de cupru, ceruloplasmină, fier, identificarea acidozei lactice etc.), precum și pe depistarea unor modificări morfologice specifice (fenomenul de „ruptură”. fibre roșii” în encefalomiopatiile mitocondriale, incluziuni neuronale caracteristice în probele de biopsie ale pielii și mucoasei intestinului gros în lipofuscinoza ceroidă, eritrocite „în formă de stea” (acantocite) în neuroacantocitoză).
medicalplanet.su
Demența frontotemporală: simptome, tratament, prognostic
Se crede în mod obișnuit că demența este o boală exclusiv a persoanelor în vârstă, dar acest lucru nu este deloc adevărat. Demența frontotemporală, în care majoritatea modificări degenerative apare în lobii frontali ai creierului și în lobii temporali anteriori, afectând persoanele sub 65 de ani. Zonele creierului care sunt afectate la pacienții cu această formă de demență sunt cele responsabile de personalitate, comportament și vorbire. Această formă de demență a fost descrisă pentru prima dată de medicul ceh Arnold Pick în 1892, după care a fost numită după el. Acum boala Pick este considerată doar o formă de demență frontotemporală.
Medicii confundă adesea demența frontotemporală cu boala Alzheimer, dar una dintre ele trasaturi caracteristice este debutul bolii - simptomele apar de obicei la persoanele de 40-45 de ani.
Unul dintre cei mai tineri pacienți din lume care a murit din cauza acestei forme de demență a fost Gareth Wilmot, în vârstă de 40 de ani, un profesor din Marea Britanie. Primele semne ale bolii au apărut când avea 35 de ani, dar apoi a fost diagnosticat cu depresie. Medicamentele prescrise nu au ajutat, vorbirea și memoria au continuat să se deterioreze, Wilmot a fost supus unor examinări suplimentare, în timpul cărora a aflat diagnosticul teribil.
Nu există un răspuns clar la motivul pentru care apare demența frontotemporală. S-a demonstrat că factorul genetic joacă un rol important în dezvoltarea bolii – cercetătorii au reușit să descopere mai multe gene asociate cu demența frontotemporală. Unele dintre aceste gene sunt, de asemenea, asociate cu apariția sclerozei laterale amiotrofice.
Simptomele asemănătoare demenței pot apărea după leziuni cerebrale traumatice severe, dar cercetătorii nu au reușit să găsească o legătură între astfel de leziuni și apariția acestei forme de demență.
Simptome precoce
Semnele și simptomele bolii variază de la pacient la pacient și depind în mare măsură de zona creierului cea mai afectată. Oamenii au probleme cu memoria, mișcarea și acțiunile obișnuite. Ei încep să se plângă de pofta de mâncare scăzută și își pierd abilitățile de îngrijire de sine. Pacienții încep să vorbească mai rău: adesea nu găsesc cuvântul potrivit, nu pot formula o propoziție și uită sensul cuvintelor.
În unele cazuri, simptomele mai puțin frecvente includ dificultăți la înghițire și spasme musculare.
Diagnosticare
În stadiile incipiente, această formă de demență este greu de distins de alte boli însoțite de simptome similare. Pentru a confirma sau infirma diagnosticul, este necesar să se efectueze o serie întreagă de diverse teste și studii, inclusiv un test de sânge, examinare de către un neurolog și teste speciale, tomografie computerizată sau imagistică prin rezonanță magnetică. Folosind procedurile de scanare a creierului, un specialist poate observa „contracția” lobilor frontali și temporali, care este, de asemenea, unul dintre semnele bolii.
Tratament și prognostic
Speranța medie de viață după diagnostic este de 6 ani. Acest indicator, cu toate acestea, variază de la persoană la persoană – unii trăiesc cu demență frontotemporală mai mult de douăzeci de ani, în timp ce alții mor în decurs de un an și jumătate.
Nu există un remediu pentru demența frontotemporală, dar medicii pot prescrie medicamente și terapie pentru a ajuta la îmbunătățirea calității vieții pacienților.
Deteriorarea funcțiilor mentale și comportamentale superioare în SLA
Anterior se credea că ALS afecta doar neuronii motori care controlează mușchii. Cu toate acestea, există acum o înțelegere a schimbărilor care apar în creier în timpul acestei boli, care afectează procesele de gândire, exprimarea emoțiilor și comportamentul pacienților. Acest articol vă va ajuta să înțelegeți natura schimbărilor în procesele funcțiilor mentale superioare în SLA.
Atenţie! În ce cazuri ar trebui să consultați urgent un medic?
Ce înseamnă „schimbarea funcțiilor mentale (cognitive) superioare”?
Funcții cognitive (lat. cognitio - cogniție) - acestea sunt funcții superioare ale creierului: memorie, atenție, coordonare psihomotorie, vorbire, numărare, gândire, orientare, planificare și control al activității mentale superioare. Acestea includ, de asemenea, comunicarea verbală, cum ar fi capacitatea de a pronunța cuvinte, de a răspunde și de a interacționa cu alte persoane.
În ceea ce privește afectarea funcțiilor mentale superioare, persoanele cu SLA pot fi împărțite în patru categorii în funcție de gradul de afectare:
Unii oameni experimentează schimbări ușoare, subtile, în timp ce alții experimentează schimbări mai vizibile.
FTD - Acesta este un tip de demență în care se dezvoltă modificări grave ale cogniției și comportamentului. Aproximativ 5% dintre persoanele cu SLA au, de asemenea, DFT. Acest tip este diferit de boala Alzheimer, care este cea mai comună formă de demență.
Cât de des se confruntă persoanele cu SLA schimbări în gândire și comportament?
Cercetări recente sugerează că până la 50% dintre pacienții cu SLA nu experimentează niciodată schimbări vizibile în gândire și comportament dincolo de reacțiile psihologice normale. În ceea ce privește a doua jumătate a pacienților, aproximativ 25% dintre aceștia pot prezenta demență frontotemporală.
Care sunt factorii de risc pentru dezvoltarea unor astfel de tulburări în SLA?
Vârsta înaintată, forma bulbară a bolii, alte antecedente familiale de demență și tulburările neurologice diagnosticate anterior sunt considerate factori care cresc probabilitatea de a dezvolta tulburări cognitive și comportamentale în SLA. Dar cazuri de dezvoltare a acestor simptome au fost identificate și la persoane care nu au întâlnit factorii de risc menționați. Până în prezent, singurul factor de risc confirmat pentru dezvoltarea tulburărilor cognitive și comportamentale este o defecțiune a genei C9ORF72.
Manifestări externe ale modificărilor în funcțiile mentale superioare
Schimbările în funcțiile mentale superioare se pot manifesta sub diferite forme. Unii oameni le este dificil:
- concentrați-vă, de exemplu, în timp ce citiți;
- a începe ceva nou sau a învăța să folosească echipamente noi;
- începe o conversație;
- menține o conversație dacă există o distragere a atenției;
- planificați orice succesiune de acțiuni;
- începe lucruri sau sarcini;
- duce lucrurile la capăt;
- a face mai mult de un lucru la un moment dat, cum ar fi să vorbești cu cineva în timp ce te uiți la televizor;
- amintiți-vă numele obiectelor pe care le cunoșteau anterior;
- înțelege propoziții complexe.
- comportament incomod, infantil sau pur și simplu necaracteristic pentru pacient;
- comentarii nepotrivite;
- consum mare de dulciuri sau un anumit tip de hrană sau mestecat prea mult timp;
- scăderea atenției la problemele de igienă, de exemplu, atunci când vizitați toaleta sau refuzul de a face baie regulată, de a vă tuns sau de a vă schimba hainele;
- pierderea judecății necesare pentru a lua decizii sau luarea unor decizii care sunt foarte diferite de ceea ce a spus pacientul anterior;
- lipsa de reacție sau indiferența față de stările emoționale ale celorlalți;
- fixare pe o anumită sarcină de rutină;
- agresivitate crescută;
- pacientul poate spune „da” în loc de „nu” sau invers, sau poate fi nesigur de răspunsul la întrebări simple;
- un sentiment de deconectare între gândul de a dori să miști o anumită parte a corpului și acțiunea în sine;
- construcția incorectă a frazelor;
- incapacitatea de a găsi cuvântul potrivit în timpul unei conversații;
- senzație de neliniște;
- întrebuinţare abuzivă a cuvintelor;
- folosirea de propoziții fără sens;
- incapacitatea de a urma instrucțiunile în timpul terapiei fizice sau a altor proceduri;
- uitarea a ceea ce pacientul a intenționat să facă;
- lipsa de motivație sau inițiativă;
- acțiuni impulsive fără a se gândi la consecințe.
- Învață și îmbunătăți.
- Aveți grijă de dumneavoastră.
- Încercați să faceți comunicarea cu pacientul cât mai ușoară posibil. Folosiți fraze scurte. Puneți întrebări la care se poate răspunde cu „da” sau „nu”. Vorbește rar.
- Însoțiți pacientul în timpul oricăror întâlniri pentru a vă asigura că schimbul de informații între pacient și interlocutori are loc în mod corect.
- Aliniați-vă așteptările pentru pacientul cu SLA cu realitatea. Dacă cererea dumneavoastră provoacă iritare, resentimente sau respingere la pacient sau la dumneavoastră, așteptările trebuie modificate pentru a satisface nevoile și capacitățile persoanei aflate în îngrijirea dumneavoastră.
- Spuneți profesioniștilor implicați în tratamentul pacientului dumneavoastră și vă pasă de starea dumneavoastră.
- Continuați să urmăriți relații și activități care vă aduc bucurie și luați o pauză de la cele care vă provoacă stres.
Ca urmare, se dezvoltă unele schimbări:
Este posibil ca persoana bolnavă să nu fie conștientă de schimbările care au loc. Acest lucru este de obicei foarte supărător pentru alții și membrii familiei.
Schimbările de gândire și comportament în SLA pot fi asociate nu numai cu progresia bolii, ci și cu alți factori, de exemplu, procese respiratorii insuficiente (oxigen scăzut sau dioxid de carbon ridicat), efecte secundare ale terapiei medicamentoase, depresie sau anxietate, tulburări de somn sau tulburări mentale sau neurologice preexistente. Este important să raportați toate simptomele profesioniștilor din domeniul sănătății, astfel încât aceștia să poată determina cauza problemei, mai ales dacă aceasta poate fi corectată.
Ce se mai poate întâmpla dacă funcțiile mentale superioare sunt încălcate?
Dispozitie
Desigur, încercările de a vă adapta viața la SLA progresivă duc la schimbări ale dispoziției. Multe persoane cu această afecțiune se simt foarte goale.
Pentru unii, aceste sentimente sunt atât de puternice încât se dezvoltă depresia. Dacă o persoană are dificultăți în a finaliza o activitate sau are dificultăți de concentrare, aceasta se poate datora unei dispoziții scăzute, mai degrabă decât modificărilor de conștiență. Unii oameni iau medicamente, cum ar fi antidepresive, pentru aceste afecțiuni. Poate fi necesară consultarea de specialitate.
Labilitate emoțională
Unii oameni cu ALS devin instabili emoțional. Acest lucru duce la râs incontrolabil sau, dimpotrivă, la plâns ca răspuns la ceva care nu este suficient de amuzant sau trist pentru a da o reacție atât de puternică, de exemplu, un program de televiziune. Uneori pare foarte nepotrivit și îi încurcă pe alții. Pacienții cu SLA sunt susceptibili la labilitate emoțională fără prezența altor simptome cognitive, comportamentale sau psihologice.
Suflare
Dacă ALS afectează respirația, aceasta afectează calitatea somnului, ceea ce duce și la modificări ale concentrării și memoriei. Când un ventilator este utilizat pentru a ajuta respirația, merită să verificați setările acestuia pentru a vă asigura că funcționează corect.
Bunăstare
Uneori, gândirea confuză poate fi o consecință a bolilor infecțioase ale tractului respirator sau ale sistemului genito-urinar. Prin urmare, merită să acordați atenție prezenței factorilor caracteristici infecției, cum ar fi febra și sănătatea precară.
Cum sunt diagnosticate tulburările cognitive și comportamentale în SLA?
Pentru a determina dacă simptomele se datorează ALS sau unui alt proces, trebuie efectuată o evaluare adecvată a stării pacientului. De obicei, acest lucru poate fi făcut de medicul dumneavoastră sau de neuropsiholog. Evaluarea se bazează pe diverse teste care reflectă modul în care o persoană procesează informațiile. De exemplu, medicul vă poate cere să numiți cât mai multe cuvinte care încep cu o anumită literă a alfabetului, sau să vă amintiți cât mai multe cuvinte și să le recitați sau să scrieți cuvinte. Rezultatele obținute sunt comparate cu indicatori standard pentru persoane de aceeași vârstă și cu același nivel de educație. Acest lucru face posibil să se determine dacă încălcările sunt efectiv prezente și, dacă da, de ce fel. Profesionist poate avea nevoie să discute situația nu numai cu pacientul, ci și cu persoanele care îl îngrijesc și/sau care îl cunosc bine.
Ce se întâmplă după ce diagnosticul este confirmat?
Unele familii și îngrijitori se simt ușurați după confirmarea deficienței, deoarece știu sigur că modificările cognitive și comportamentale la persoana cu SLA nu se datorează unor motive psihologice sau încercărilor de a rezista altor persoane. Dacă o persoană cu SLA este conștientă de acțiunile sale, își poate documenta dorințele cu privire la îngrijirea și terapia viitoare. Acest lucru este deosebit de important deoarece afectarea cognitivă și comportamentală, ca și alte simptome de SLA, se agravează pe măsură ce boala progresează.
Dacă pacientul este deja incapacitat, membrii familiei, îngrijitorii și profesioniștii medicali trebuie să își echilibreze așteptările față de pacient cu realitatea. În această situație, nu trebuie să vă așteptați ca persoana să-și schimbe comportamentul. Mediul trebuie să se schimbe. Așteptările pentru pacient trebuie să corespundă capacităților sale. Dacă pacientul devine distant sau anxios când i se cere să facă ceva, acesta poate fi un semn că așteptările îi depășesc capacitățile. Mai mult, dacă membrii familiei sau îngrijitorii încep să se simtă frustrați sau resentiți atunci când interacționează cu pacientul, așteptările situației trebuie simplificate. În cazul demenței, toți profesioniștii care lucrează cu pacientul trebuie să își concentreze eforturile pe educarea și implicarea îngrijitorilor și a membrilor familiei, deoarece pacientul nu se poate schimba din proprie voință.
Membrii familiei și îngrijitorii pot beneficia de participarea la consiliere, grupuri de sprijin, întâlniri spirituale sau implicarea în mai multă îngrijire de sine, ceea ce va crește, de asemenea, resursele (fizice și emoționale) necesare pentru îngrijirea unei persoane cu SLA.
Cum afectează prezența unor astfel de tulburări progresia SLA?
Există dovezi că persoanele cu deficiențe cognitive și comportamentale în SLA trăiesc o viață mai scurtă decât pacienții fără aceste simptome. Sunt efectuate multe studii pentru a determina dacă prezența sau absența acestor tulburări afectează eficacitatea medicamentelor, tratamentelor și altor tratamente pentru SLA. Acesta este un domeniu important al cercetării științifice.
Ce urmeaza?
Medicul dumneavoastră vă poate recomanda testarea. Acest lucru va ajuta la identificarea cauzei schimbării. Ei vă pot spune și despre opțiunile de depășire a unor dificultăți. Medicul poate da recomandări despre cum să comunice cu o persoană, de exemplu, să pună întrebări cu doar răspunsuri „da” sau „nu” și să evite propozițiile lungi și complexe care necesită clarificări.
Există multe modalități de a face comunicarea și sarcinile zilnice mai ușoare. Scopul final al acestor recomandări -
ajutați o persoană cu SLA să se controleze. De asemenea, va fi foarte benefic pentru îngrijitorii și membrii familiei.
Dacă înțelegem motivele schimbărilor în conștiința unei persoane, atunci îngrijitorii vor acționa cu mai multă încredere.
Cine poate ajuta?
Dacă observați modificările descrise în acest articol sau dacă aveți întrebări, vă recomandăm insistent să vă adresați medicului dumneavoastră. Știind că schimbările de conștiință fac parte din SLA poate face uneori mai ușor pentru oameni să înțeleagă schimbările care apar după diagnostic. Toți membrii familiei aflați în această situație au nevoie de sprijin, sfaturi și îndrumări.
Pentru că ALS - Aceasta este o afecțiune rară și este posibil ca medicul dumneavoastră să nu constate că simptomele dumneavoastră sunt legate de aceasta.
Arată acest articol medicului tău, astfel încât acesta să poată vedea sursa informațiilor. În ciuda faptului că conștientizarea medicilor cu privire la legătura dintre afectarea conștiinței și ALS este în creștere, nu toată lumea are experiență în acordarea asistenței în această situație. Puteți contacta linia noastră de asistență ALS pentru a discuta preocupările dumneavoastră.
Neuroștiri
Intrări recente
Scleroza laterală amiotrofică: povestea unui expert
Se întâmplă că astăzi pe portalul Neuronovosti.Ru este ziua sclerozei laterale amiotrofice. Am scris deja despre primul neuroimplant „acasă”, care i-a oferit unui pacient cu SLA posibilitatea de a comunica și de a juca, ne-am amintit „10 fapte” despre această boală, iar seara îi dăm ocazia să-i spunem unui expert despre acest lucru. boala.
Se acordă cuvântul Marina Aleksandrovna Anikina, șef adjunct al Centrului pentru Boli Extrapiramidale al Agenției Federale Medicale și Biologice din Rusia. Ea va vorbi despre ceea ce se confruntă în fiecare zi la locul de muncă.
RMN-ul unui pacient cu SLA
Scleroza laterală amiotrofică (ALS) este o boală neurodegenerativă care afectează în primul rând neuronii motori superiori și inferiori. Afectarea neuronului motor inferior are ca rezultat atrofie musculară (pierderea funcției) și fasciculații (smucituri), în timp ce afectarea neuronului motor superior are ca rezultat spasticitate (rigiditate) și reflexe piramidale crescute (anormale). Combinația simultană de semne ale leziunilor neuronului motor superior și inferior rămâne piatra de temelie a procesului de diagnostic.
Deși „boala neuronului motor” și „ALS” sunt adesea folosite în mod interschimbabil, „boala neuronului motor” cuprinde o categorie largă de boli ale neuronului motor și include atrofia musculară progresivă, scleroza laterală primară și sindromul brațului cu batere (sindromul Vulpian-Bernardt). sindrom), sindromul piciorului batut (forma pseudopolineuritică), paralizie bulbară progresivă și ALS plus demență frontotemporală.
Câteva statistici
Scleroza laterală amiotrofică este cea mai frecventă boală din categoria bolilor neuronilor motori și reprezintă 60-85 la sută din toate cazurile.
Riscul pe parcursul vieții de a dezvolta SLA este de 1:350 pentru bărbați și 1:400 pentru femei și este mai mare pentru personalul militar. Boala se dezvoltă mai des la bărbați; Raportul dintre sexe este de 1,5:1. Incidența este de aproximativ 1,5-2,7/100.000 pe an. Prevalența 3-5/100.000. Incidența maximă a SLA apare între 55 și 65 de ani, dar există diferite variante de vârstă. Cazuri de simptome care apar tardiv adolescentşi până în deceniul al nouălea de viaţă.
Cei cu risc crescut de SLA includ veteranii, indiferent de rang sau vechime în serviciu, fumătorii de lungă durată și jucătorii de fotbal de elită și jucătorii de fotbal american. În același timp, stresul fizic și emoțional nu este un factor de risc pentru dezvoltarea SLA. De asemenea, diverse leziuni ale capului nu sunt direct asociate cu dezvoltarea SLA. Dar un indice de masă corporală scăzut, dimpotrivă, este direct legat de SLA.
Majoritatea cazurilor de SLA, până la 90 la sută, sunt sporadice. Motivele apariției sale, ca și pentru aproape toate neurodegenerările, rămân necunoscute. Există o ipoteză a originii prionice și a răspândirii SLA de la un simptom local la afectarea generalizată a neuronilor motori.
Care sunt motivele?
Cazurile familiale de SLA nu depășesc 10% și au semne predominante de moștenire. Majoritatea formelor familiale de SLA sunt asociate cu mutații la una sau mai multe gene responsabile de dezvoltarea bolii. În 40-50 la sută din cazuri, boala este asociată cu gena C9orf72. La purtătorii acestei gene, repetarea hexanucleotidică intrronică a primului intron se extinde, de obicei de până la sute sau mii de ori. Această expansiune a C9orf72 poate provoca dezvoltarea atât a SLA, cât și a demenței frontotemporale (FTD). Alte 20% din cazuri se datorează unei mutații a genei care codifică superoxid dismutaza citosolică (SOD1).
Diferite mutații sunt, de asemenea, asociate cu durate diferite ale bolii. Mutația A4V este cea mai frecventă în America de Nord și este responsabilă pentru un fenotip agresiv de neuron motor inferior. Rata medie de supraviețuire variază de la 1 la 1,5 ani. În schimb, varianta D90A, responsabilă pentru fenotipul neuronului motor superior, este relativ ușoară. ALS cu acest genotip se dezvoltă numai în cazul unei stări homozigote.
După C9orf72 și SOD1 sunt celelalte două motive comune Genele care codifică proteinele de legare a ARN-ului TDP43 și FUS devin ALS. Mutațiile din fiecare reprezintă 5% din cazurile familiale de SLA și sunt mai rare în fenotipul FTD.
În general, geneticienii au numărat deja mai mult de o duzină de mutații genetice și produsele lor care joacă un rol în dezvoltarea SLA.
Care este „fața” bolii?
Manifestările clinice ale SLA sunt slăbiciune musculară progresivă nedureroasă și atrofie, care duce la paralizia și moartea pacientului din cauza dezvoltării insuficienței respiratorii. Rata medie de supraviețuire este de la câteva luni la câțiva ani: pacienții trăiesc aproximativ 19 luni după diagnostic și 30 de luni după depistarea primelor simptome. Este important de remarcat faptul că există o variație semnificativă între pacienți și capacitatea de a prezice rata corectă a progresiei bolii în timp la diagnosticare este limitată.
Moartea neuronilor motori superiori duce la manifestările neurologice așteptate: spasticitate, hiperreflexie, semne Hoffman. Ocazional (mai puțin frecvent decât în cazul altor tipuri de leziuni ale neuronului motor superior), poate fi prezent semnul Babinski. Cauzele nu sunt încă clare, dar afectul pseudobulbar (labilitatea emoțională) este asociat cu degenerarea neuronului motor superior și apare adesea cu alte semne neurologice de afectare a neuronului motor superior.
Moartea neuronilor motori inferiori se manifesta prin fasciculatii, spasme musculare si atrofie musculara. Deoarece aceste semne sunt mai evidente, este mai probabil ca semnele neuronilor motori superiori să arate în direcția corectă de diagnostic. De exemplu, disfuncția neuronului motor inferior maschează adesea semnele de deteriorare a neuronului motor superior la examinare.
La aproximativ 2/3 dintre pacienți, primele simptome de SLA încep la extremități. Manifestarea tipică este simptomele localizate, cum ar fi „mâna stânjenită” sau „plesnirea piciorului”. Slăbiciunea axială duce la incapacitatea de a ține capul sus și la cifoză. Dacă ALS începe cu simptome bulbare, atunci pacientul se confruntă cu un prognostic mai rău, acest lucru se observă mai des la femeile în vârstă. Acești pacienți dezvoltă disartrie (disturbii de vorbire) urmate de disfagie (deteriorări de înghițire). În mod surprinzător, în SLA nu există tulburări ale mișcărilor extraoculare, ale funcției sfincterului sau ale tuturor modalităților senzoriale (organele de simț).
Cum se pune un diagnostic?
Diagnosticul clinic rămâne dificil și diagnosticul este de obicei întârziat. În medie, diagnosticul durează 11-12 luni. În același timp, 30-50 la sută dintre pacienți primesc inițial un diagnostic incorect și schimbă trei specialiști diferiți înainte de a stabili un diagnostic de SLA. Eforturile de reducere a timpului de diagnostic se bazează pe cea mai mare activitate a riluzolului (un medicament care interferează cu sinteza glutamatului) în stadiile incipiente ale bolii, când medicamentul poate oferi cel mai mare beneficiu. Utilizarea termenilor „oboseală excesivă”, „crampe musculare excesive”, „fasciculații progresive ale limbii” sau „slăbiciune progresivă” indică faptul că pacientul trebuie îndrumat către un specialist SLA.
Pe stadiu timpuriu ALS poate prezenta doar semne de disfuncție a neuronului motor superior sau inferior, iar simptomele sunt limitate la o regiune mică a corpului. Diagnostic diferentiatîn acest stadiu este pe termen lung și se bazează pe excluderea tuturor afecțiunilor asociate cu afectarea neuronului motor sau mimând lezarea generalizată a neuronului motor, inclusiv neuropatii motorii, miopatii acute, distrofii musculare, neuropatii paraneoplazice, deficit de vitamina B12, creier primar și măduva spinării. leziuni. Alte boli cu leziuni ale neuronilor motori pot imita SLA la debut. Atrofia spinomusculară a adulților, atrofia musculară spinobulbară (boala Kennedy), sindromul post-polio ar trebui să fie diferențiate de ALS. De exemplu, sindromul fasciculațiilor benigne provoacă fasciculații care nu duc la slăbiciune sau alte semne de denervare la electroneuromiografie (ENMG). Paraplegia spastică ereditară poate include semne de afectare a neuronului motor superior și membrele inferioare.
Singura metodă de diagnostic instrumentală de până acum rămâne ENMG, care poate distinge semnele de afectare difuză a neuronilor motori.
Pe baza distribuţiei predominante a simptomelor se disting formele anatomice de SLA: bulbară, cervicală, toracică, lombo-sacrală.
Combinația de date clinice și instrumentale determină severitatea diagnosticului de SLA: stabilit clinic, probabil sau numai posibil.
Există vreo modalitate de a vindeca?
În prezent tratament eficient ALS nu există. Riluzolul este singurul medicament care modifică boala aprobat de FDA din 1995, dar utilizarea acestuia crește doar speranța de viață cu 2-3 luni, dar nu schimbă cursul bolii de bază. simptome clinice boli. Dar chiar și acest lucru este uneori imposibil de utilizat din cauza greaței severe dezvoltate la pacienți.
Terapia simptomatică include utilizarea dextrometrefan-chinidinei pentru tulburările afective pseudobulbare, mexiletina pentru crampe dependente de SLA, anticolinergice pentru corectarea salivarii ca urmare a tulburărilor de deglutiție, antidepresive precum ISRS (inhibitorii selectivi ai recaptării serotoninei) pentru corectarea stării de spirit. tulburări, AINS pentru corectarea durerii asociate cu mobilitate redusă.
Necesitatea unei abordări multidisciplinare apare din numeroasele simptome severe ale stadiului avansat. Acestea includ pierderea semnificativă în greutate și deficiențe nutriționale, care indică un prognostic negativ.
1. Tulburarile de deglutitie se pot imbunatati cu logopedie activa, dar in unele cazuri cu disfagie severa necesita alimentatie printr-un tub de gastrostomie.
2. Disartria progresivă interferează cu comunicarea normală și necesită atât terapie logopedică, cât și ședințe neuropsihologice.
3. Riscul de cădere, care apare inevitabil odată cu slăbiciune musculară progresivă, este atenuat prin deplasarea într-un scaun cu rotile.
4. O sarcină importantă a terapiei simptomatice este menținerea unei respirații normale în timp util. Mai devreme sau mai târziu, un pacient cu SLA dezvoltă insuficiență respiratorie, ceea ce duce la moartea sa. Utilizarea ventilației neinvazive poate crește speranța de viață și calitatea vieții la pacienții cu SLA. Este deosebit de important să se efectueze ventilație neinvazivă noaptea, când insuficiența respiratorie este la apogeu. Dacă suportul respirator neinvaziv nu este posibil, pacienții sunt supuși unei traheostomii pentru a asigura ventilația mecanică.
Există o ușurare mecanică a tusei, care se efectuează cu echipamente speciale și previne sufocarea secrețiilor sau dezvoltarea pneumoniei.
În ultimii 20 de ani, ALS a fost una dintre cele mai interesante probleme pentru neurologi. Cercetările sunt în curs de desfășurare în întreaga lume, inclusiv testarea terapiilor cu celule stem, terapiilor genice și dezvoltarea unei varietăți de agenți cu molecule mici în diferite stadii de dezvoltare clinică și preclinică.
Ce îi așteaptă pe pacienți?
Rata de progresie a bolii variază foarte mult. În general, speranța medie de viață după diagnostic este de aproximativ 3 ani, unii pacienți decedând înainte de 1 an, iar alții trăind mai mult de 10 ani. Supraviețuirea este cea mai bună în rândul pacienților cu cea mai mare întârziere a diagnosticului din cauza ratelor lente de progresie, precum și la pacienții mai tineri cu implicarea primară a membrelor. De exemplu, patologii cum ar fi sindromul de batere a membrelor sau diplegia brahială amiotrofică progresează mai lent decât ALS. Împotriva, varsta in varsta, implicarea precoce a muşchilor respiratori, debutul bolii sub formă de simptome bulbare sugerează o progresie mai rapidă.
Text: Maria Anikina, Centrul pentru Boli Extrapiramidale, FMBA din Rusia
Revista Neurologică, 2002.-№4.-P.12-18.
N. N. Yakhno, M. S. Golovkova, I. S. Preobrazhenskaya, V. V. Zakharov
* Clinica de Boli Nervose numită după. A. Ya. Kozhevnikova Moscova academiei medicale lor. I. M. Sechenova
Sindromul de scleroză laterală amiotrofică (ALS)-demența aparține grupului de demențe frontotemporale (FTD). Potrivit unor studii recente, apariția lor în populație este destul de mare și se ridică la 12-20% din cazurile de demență degenerativă. FTD se manifestă prin tulburări cognitive și comportamentale progresive caracteristice leziunilor lobilor frontali și temporali ai creierului. Pe baza tabloului patomorfologic, FTD se împarte în 3 tipuri: 1) FTD cu modificări histologice nespecifice (vacuolizarea și moartea neuronilor, spongioza, glioza); 2) boala lui Pick; 3) combinarea FTD cu ALS - sindromul ALS-dementa.
Diferența fundamentală dintre sindromul ALS-demență și alte forme de FTD este prezența simptomelor ALS în tabloul clinic. Examen histologicîn sindromul ALS-demență, dezvăluie moartea neuronilor din coarnele anterioare și nucleii grupului caudal al nervilor cranieni. Spre deosebire de alte variante de FTD în sindromul ALS-demență, incluziunile intraneurale taunenegative pozitive pentru ubiquitină se găsesc și în stratul II al cortexului cerebral și al hipocampului. Alte modificări histologice, inclusiv vacuolizarea neuronilor în cortexul frontal și temporal, precum și atrofia și glioza în principal în regiunea ganglionilor bazali, nu sunt specifice și sunt observate în alte variante de FTD. Gradul de modificări în regiunile frontale și temporale în sindromul ALS-demență variază de la atrofie ușoară și formarea de microvacuole până la glioza transcorticală severă; în unele cazuri, pot fi observate modificări spongiforme. Nu există markeri histologici ai bolii Alzheimer, bolii Pick sau bolii difuze cu corp Lewy.
Prima descriere detaliată a unui caz de combinație de SLA și demență a fost făcută de A. Meyer în 1929, iar în 1932 A. von Braunmühl a remarcat asemănarea deficienței cognitive la un pacient cu SLA cu cei din boala Pick. Ulterior, cazuri de o combinație de SLA și demență au fost descrise în mod regulat și, conform lui J. Kew și N. Leigh, până în 1992 numărul lor era de aproximativ 200. Până în anii 90, aceste cazuri erau considerate ca o combinație de SLA și boala Pick. . De la începutul anilor 90, sindromul ALS-demență a fost identificat ca un subgrup separat în cadrul FTD.
Sindromul ALS-demență se dezvoltă de obicei în decada a șasea de viață. Bărbații suferă ceva mai des decât femeile. În cele mai multe cazuri, boala debutează cu disfuncție comportamentală și cognitivă, care indică leziuni ale părților frontale și (mai rar) temporale ale creierului. Din punct de vedere clinic, aceasta se manifestă prin inerție, instabilitate emoțională și adaptare socială afectată. Testarea neuropsihologică relevă tulburări de atenție, defecte de memorie modal-nespecifice, sărăcirea și scăderea fluenței vorbirii, tulburări de programare și control al activității voluntare. Simptomele bolii progresează treptat, pacientul devine inactiv, letargic și indiferent emoțional. Din cauza agravării tulburărilor comportamentale și cognitive se dezvoltă inadaptarea socială, adesea nerealizată de pacient. În acest stadiu al bolii, poate exista o revigorare a formelor primitive de activitate: bulimie până la consumul de obiecte necomestibile, comportament de reciclare, hipersexualitate. După 6-12 luni de la dezvoltarea deficienței cognitive, apar semne tipice de SLA. În același timp, pierderea musculară și slăbiciunea, de regulă, predomină în mușchii centurii scapulare și ai extremităților superioare, iar pacienții își păstrează capacitatea de a se mișca chiar și în etapele ulterioare ale bolii. Dezvoltarea simptomelor bulbare este tipică.
Metodele paraclinice relevă modificări tipice SLA și DFT. Astfel, neuroimagistica relevă grade variate de atrofie a lobilor frontali și temporali, adesea asimetrice. Regiunile occipitale și parietale rămân relativ intacte. EEG de obicei nu evidențiază modificări patologice, deși unii autori descriu o încetinire a activității de fond. Modelul EMG nu diferă de cel din SLA. Tomografia cu emisie pozitivă (PET) relevă o scădere a metabolismului în părțile anterioare ale creierului.
Deficiența cognitivă și simptomele SLA progresează rapid, iar decesul are loc în medie la 3 ani de la debutul bolii. Trebuie remarcat faptul că combinația dintre SLA și demență duce la o progresie mai rapidă atât a tulburărilor motorii, cât și cognitive în comparație cu variantele clinice „pure” ale ALS și FTD. Există descrieri de cazuri cu o perioadă lungă (până la 17 ani) de existență a demenței frontale înainte de apariția primelor simptome de SLA.
La un număr de pacienți cu DFT, examenul patologic evidențiază incluziuni intraneuronale pozitive pentru ubiquitină în al doilea strat al cortexului cerebral și al hipocampului, care sunt un marker histologic al sindromului de demență ALS. Cercetătorii subliniază absența altor semne histologice de afectare a neuronului motor (moartea neuronilor în coarnele anterioare ale măduvei spinării și nucleii nervilor cranieni), precum și manifestările clinice ale SLA. Aceste date au făcut posibilă identificarea unei forme suplimentare de FTD - „demență cu incluziuni ALS” (boala neuronului motor-demență cu includere).
Deși majoritatea cazurilor de sindrom ALS-demență sunt sporadice, există descrieri ale formelor familiale. Se sugerează o posibilă legătură între dezvoltarea acestei boli și o mutație a unei gene situate pe cromozomul 9q21-22. Manifestările fenotipice ale sindromului ALS-demență pot fi incomplete și diferă în diferite generații. Astfel, la una dintre familiile cu DFT, demența a fost observată în primele 3 generații în absența semnelor de SLA, în timp ce la a patra generație toți frații au dezvoltat sindromul ALS-demență. Aceste observații au permis autorilor să sugereze că FTD și ALS pot avea mecanisme patologice și genetice comune de dezvoltare. Această ipoteză este confirmată indirect de rezultatele testelor neuropsihologice ale pacienților cu SLA, conform cărora un număr de pacienți prezintă o deficiență cognitivă ușoară, tipică disfuncției. Lobii frontali. Aceste date sunt confirmate și de rezultatele PET. Pacienții cu SLA, comparativ cu grupul de control, pot prezenta o scădere a fluxului sanguin cerebral în lobii temporali frontal și anterior.
Prezentăm o descriere a observațiilor a 3 pacienți cu o combinație de SLA și demență de tip frontal.
Pacientul B., în vârstă de 50 de ani, a fost internat în clinică cu plângeri de slăbire la mâna stângă și antebraț, slăbiciune la mâna stângă, zvâcniri în mușchii brațelor și picioarelor, cu atât mai mult pe stânga. Din anamneză se știe că în urmă cu aproximativ 2 ani a devenit iritabilă, agresivă, inadecvată în comunicarea cu rudele și colegii de muncă, au apărut neglijență, distragere, sărăcire emoțională, iar gama ei de interese s-a restrâns. După 1 an, s-au instalat tulburările cognitive, ea a încetat gospodăria și a devenit apatică. Nu și-a putut face față meserii (fiind profesoară de matematică, nu a putut rezolva o problemă de matematică pentru fiica ei de 12 ani) și a fost concediată la inițiativa administrației. Ea însăși a crezut că se descurcă cu munca. La aproximativ șase luni de la debutul tulburărilor mintale, ea a observat zvâcniri musculare la brațul stâng, care 2 luni mai târziu au apărut și la brațul și picioarele drepte. Mai târziu, s-a dezvoltat slăbiciune și pierderea în greutate a mâinii stângi, care apoi s-a extins la antebraț.
Istoricul vieții fără nicio caracteristică. Istoricul ereditar al bolilor neurologice nu este împovărat. Sanatoasa din punct de vedere somatic. Stare neurologică: conștiință clară; se observă o ușoară hipomimie; Fasciculațiile sunt detectate în mușchii faciali din stânga, fibrilația și hipotrofia jumătății stângi a limbii. Reflexul mandibular este reînviat, sunt evocate reflexele automatismului oral (proboscis, Marinescu-Rodovici). Disartrie, disfonie. Fara disfagie. Există o scădere a forței la 3,5-4 puncte în degetele mâinii stângi și la 4-4,5 puncte în părțile proximale ale mâinii stângi; in alte grupe musculare forta este normala. Fenomenul de contra-ținere este dezvăluit de ambele părți. Reflexele tendinoase la brate sunt de vivacitate normala cu accent pe stanga in picioare sunt animate, fara asimetrie clara; Sunt evocate reflexe intermitente piramidale carpiene și picioare. Există fasciculații larg răspândite în mușchii brațelor, mai mult în stânga, și sporadice în mușchii picioarelor. Este stabilă la testul Romberg, se păstrează reflexele posturale, nu există tulburări de coordonare sau senzoriale. Mersul este lent, cu o bază largă. Urinarea este frecventă și există incontinență urinară, pe care pacientul o neagă.
Examen neuropsihologic: pacientul este clar conștient, comunicativ, corect orientat într-un loc, dar nu este exact la denumirea datei. Nu are nicio plângere cu privire la memorie sau la performanța mentală. Obiectiv, deficiențe pronunțate de memorie sunt relevate în toate modalitățile, în sarcini atât cu interferență, cât și fără interferență, la toate nivelurile de organizare semantică. În acest caz, reproducerea suferă într-o măsură mai mare decât memorarea: păstrarea urmei se manifestă prin reminiscențe spontane care nu sunt relevante pentru sarcină. În sfera motrică apar tulburări pronunţate în asimilarea şi reţinerea seriilor motrice, neremediate prin introducerea medierii vorbirii, imposibilitatea coordonării reciproce, perseverenţe pronunţate în testul grafic. Practica constructivă este încălcată într-o mică măsură în funcție de tipul de reglementare. În sfera gnozei - o ușoară lipsă de recunoaștere a obiectelor neterminate, încălcări pronunțate ale gnozei spațiale de natură reglementară. Gnoza subiectului este intactă. Vorbirea nu este afectată, cu excepția scăderii fluenței la testul „Asociere”. Operațiile formal-logice sunt încălcate grav: există o scădere a capacității de generalizare, de a analiza asemănările și diferențele și o încălcare a operațiunilor de numărare de tip reglementar. Concluzie: afectare cognitivă severă de tip frontal, ajungând la nivelul demenței.
generală şi teste biochimice sânge, analiză generală a urinei fără abateri de la normă; Reacția Wasserman, antigen australian negativ. ECG, fundus fără abateri semnificative de la normă. EEG în norma de vârstă.
EMG (realizat de E. A. Dubanova) arată natura neuronală a leziunii la nivelul segmentelor cervicale și lombare ale măduvei spinării.
RMN-ul creierului nu a evidențiat modificări focale atrofie pronunțată a regiunilor frontale și atrofie moderată a regiunilor temporale, mai mult pe stânga, și dilatarea moderată a ventriculilor laterali;
Pacientul N., 52 de ani, a fost internat în clinică cu plângeri de modificări ale vorbirii, sufocare la masă, slăbiciune a brațului și piciorului drept. Boala a început cu aproximativ 2 ani înainte de spitalizare, cu o schimbare treptată a vorbirii, la care după un timp i s-a alăturat slăbiciunea membrelor drepte și hipoxie. În ultimele luni înainte de spitalizare, a avut dificultăți în a face față îndatoririlor sale oficiale. O colecție mai detaliată de anamneză a fost dificilă din cauza afectarii memoriei pacientului și a altor funcții superioare ale creierului și absența rudelor. Istoricul vieții fără nicio caracteristică. Nu s-a putut clarifica istoricul ereditar, dar, conform pacientului, nu este împovărat.
Examinarea nu a evidențiat nicio modificare patologică în starea somatică. Statut neurologic: conștient, orientat în spațiu, timp, sine. Insuficiență ușoară de convergență. Se notează disartrie severă, disfonie, dispozodie și disfagie mai puțin severă. Reflexul faringian este viu, sunt evocate proboscisul, reflexele nazolabiale și palmo-mentale și apar episoade de râs violent. Limba și palatul moale pe linia mediană. Nu există atrofie a limbii, există fasciculații intermitente. Forța musculară la membrele drepte a fost redusă la 3 puncte, la stânga - la 4 puncte. Reflexele tendinoase sunt animate, puțin mai sus în dreapta.
Nu există reflexe patologice ale piciorului sau carpienului. Fasciculații larg răspândite în mușchii membrelor și ai trunchiului. La bratul drept si piciorul drept tonusul este crescut in functie de tipul piramidal, in stanga tonusul este normal, la muschii axiali se produce o oarecare modificare a tonusului in functie de tipul plastic. Fenomenul de rezistență musculară este clar exprimat. Mișcările sunt oarecum lente. Mersul este spastic-paretic, cu o bază largă la mers și se constată căderi; La efectuarea testelor de coordonare se exprimă fenomenul Stewart-Holmes. Se notează dismetria moderat exprimată, loviturile ratate și disdiadococineza. În ipostaza Romberg, el este instabil atât cu ochii deschiși, cât și cu ochii închiși. Nu există tulburări senzoriale. În ultimele 6 luni s-a observat enurezis nocturn.
Examen neuropsihologic (efectuat de Zh. M. Glozman): contactul cu pacientul este dificil din cauza negativității grosiere și inadecvării situației de examinare, pacientul are nevoie de stimulare constantă, este necritic, orientat, deși din cauza defectelor de concentrare poate face greșeli. în marcarea datelor. Memoria este grav afectată în toate modalitățile din cauza activității insuficiente, a forței și a selectivității memorării. În sfera motorie, pe fondul adinamiei motorii, sunt relevate epuizarea, dificultăți de control și activitate la îndeplinirea tuturor sarcinilor, încălcări grave ale coordonării reciproce, apraxie posturală, apraxie spațială, tulburări de tipar, apraxie orală cu păstrarea relativă a praxisului dinamic. Gnoză: simptome de agnozie acustică, încălcări ușoare, dar clare ale gnozei obiective, cum ar fi inactivitatea și fragmentarea percepției; gnoza spațială și tactilă nu este afectată. Vorbirea este grav perturbată în termeni prozodici, sfera percepției acustice este restrânsă. Nu există defecte afazice de vorbire. Inteligența este grav afectată atât din cauza perturbărilor generale în reglarea activității, cât și din cauza scăderii posibilității de generalizare și analiză logică. Concluzie: sindrom demență cu afectare severă a zonelor corticale și subcorticale cu accent pe structurile frontale.
Analize generale si biochimice de sange, analize generale de urina fara abateri de la norma; Reacția Wasserman în sânge și lichidul cefalorahidian este negativă. La examinarea lichidului cefalorahidian: transparență completă, proteină - 0,46 g/l, citoză - 1 celulă (limfocit).
EEG, cu excepția tendinței de a încetini ritmul a la 8,5 Hz, nu a evidențiat nicio modificare.
Datele EMG (realizate de E. A. Dubanova) confirmă natura neuronală a leziunii la nivelul segmentelor cervicale și lombare ale măduvei spinării.
RMN-ul creierului nu a evidențiat nicio modificare focală, semne distincte de atrofie cerebrală externă și internă.
Diagnostic: sindrom ALS-demență frontotemporală.
Pacientul K., în vârstă de 70 de ani, a fost internat în clinică cu plângeri de incertitudine, eșalonări la mers, căderi frecvente, în principal pe spate și lateral; spasme dureroase, spasme la nivelul mușchilor picioarelor și brațelor; sufocare cu alimente lichide, dificultate la înghițirea alimentelor solide. În urmă cu aproximativ 6 ani, a început să observe tulburări de mers: incertitudine, clătinare, încetineală, mers cu pași mici. Mai târziu, au apărut tulburările de vorbire - lentoare, sărăcire, precum și tulburări cognitive și comportamentale sub formă de scădere a inițiativei, letargie și impulsivitate. Cursul bolii este progresiv. În ultimele șase luni, au apărut un ton nazal al vocii, episoade de râs și plâns violent și de sufocare când mănâncă. Tulburările cognitive și comportamentale sub formă de inactivitate și scăderea criticii au crescut semnificativ.
Istoricul vieții fără nicio caracteristică. Istoricul ereditar, conform rudelor, nu este împovărat de boli neurologice. Boli concomitente: suferă de hipertensiune arterială timp îndelungat cu tensiunea arterială crescând la 200/110 mm Hg. Art., in timpul tratamentului cu Enap, tensiunea arteriala este de 140-150/80-90 mm Hg. Artă.; Hiperlipidemia de tip 4 a fost, de asemenea, diagnosticată.
Stare somatică: pacient cu nutriție ridicată, tensiune arterială 150/80 mm Hg. Art., angiopatie retiniană hipertensivă; boala ischemica inima, cardioscleroza aterosclerotică, ateroscleroza aortei, arterele coronare. Emfizem. Pneumoscleroza. Hiperlipidemie tip 4. Stare neurologică: conștiința este clară, reflexul mandibular animat, proboscisul, reflexele nazolabiale și reflexul instabil Marinescu-Rodovici sunt evocate de ambele părți. Reflexul faringian este animat. Mobilitate redusă a palatului moale. Disfagie, disfonie, disartrie și disfazie. Nu există pareze. Reflexele tendinoase sunt animate pe brate, cu atat mai mult pe stanga sunt animate si fara asimetrie clara. Reflexul Rossolimo pe ambele părți, alte reflexe piramidale patologice nu sunt evocate. Există un reflex de apucare în dreapta și contra-ținere pe ambele părți. Hipotropia tenarului și a primului spațiu interdigital al mâinii stângi. Fasciculațiile sunt observate în mușchii brațelor și picioarelor, mai mult pe stânga. Tonusul muscular nu este schimbat. Mișcările sunt lente. În poziția Romberg există o ușoară balansare, care se intensifică la închiderea ochilor. Reflexele posturale sunt sever afectate, se notează pro-, retro- și lateropulsii. Efectuați teste deget-nas și deget-ciocan cu lovituri ratate. Mersul este schimbat: se notează brusc lent, cu o bază largă, pași mici, eșalonări, pro și retropulsii. Sensibilitatea și funcțiile pelvine nu sunt afectate.
Examen neuropsihologic: pacienta este conștientă, comunicativă, neorientată complet în loc și timp (greșeli la denumirea datei), critica la adresa stării ei este redusă. Memorie: deficiențe modal-nespecifice moderat exprimate atunci când se lucrează cu material care nu este organizat în sens, deteriorări pronunțate în selectivitatea reproducerii, scăderea eficienței indicii în timpul reproducerii. Memorarea propozițiilor și memoria generală sunt intacte. Sfera motrică: reținere afectată a seriei motorii la testul „pumn-coasta-palmă”, perseverențe brute și impulsivitate la testul grafomotor, imposibilitatea coordonării reciproce. Încălcări grosolane ale praxisului constructiv, praxis posturală de tip reglator. Gnoza: fragmentarea pronunțată a percepției în toate testele iese în prim-plan. Testul de orientare a liniei nu poate fi finalizat deoarece nu înțelege sarcina. Nu există încălcări primare ale tipurilor obiective sau somatice de gnoză. Vorbirea independentă a pacientului este fără deficiențe vizibile și înțelegerea vorbirii este păstrată, cu excepția structurilor gramaticale complexe. În vorbirea repetată, sunt notate substituții de un singur sunet. Defecte grave în denumirea obiectelor, indiciile sonore fiind ineficiente. Operațiile formal-logice sunt grav încălcate din cauza unei încălcări a generalizării semantice și a impulsivității pronunțate în luarea deciziilor. Scorul nu este spart. Concluzie: afectare cognitivă severă de tip frontal, ajungând la nivelul demenței.
Analize generale și biochimice de sânge fără abateri de la normă. Spectru lipidic: hiperlipidemie tip 4. Analiza generala urina este normală; Reacția lui Wasserman este negativă. ECG: direcția orizontală a axei electrice a inimii, modificări moderate ale miocardului. EEG nu a arătat abateri semnificative de la normă.
Dopplerografia cu ultrasunete: modificări aterosclerotice în secțiunile extracraniene ale arterelor carotide și vertebrale fără semne de obstrucții semnificative hemodinamic ale fluxului sanguin. Ecografia aortei: modificări aterosclerotice, fără semne de stenoză. Cu EMG (efectuat de N.V. Vinogradova), datele obținute indică natura neuronală a leziunii. RMN-ul creierului nu a evidențiat nicio modificare focală în cortexul cerebral. Atrofie moderată în principal a regiunilor frontale și temporale, expansiune a ventriculilor laterali, mai mult pe stânga. Leucoaraioză moderat severă în zona coarnelor posterioare ale ventriculilor laterali.
Diagnostic: sindrom ALS-dementa frontotemporal; encefalopatie discirculatoare de gradul doi; hipertensiune arterială stadiul II, ateroscleroză sistemică cu afectare a aortei, vaselor coronare și cerebrale; hiperlipidemie tip 4.
Discuţie
Miezul tabloului clinic în cazurile descrise este o combinație de SLA și demență de tip frontal, ceea ce sugerează prezența sindromului ALS-demență.
La toți pacienții, boala a debutat cu simptome motorii și cognitive de afectare a regiunilor frontale, ceea ce este tipic pentru sindromul ALS-demență. Semnele de deteriorare a neuronului motor au apărut după dezvoltarea tulburărilor cognitive. Trebuie remarcat faptul că boala a durat mult timp înainte de apariția simptomelor ALS la al treilea pacient, ceea ce este o caracteristică a acestui caz clinic.
Toți pacienții au o leziune combinată a neuronului motor periferic și central, iar leziunea neuronului motor periferic este înregistrată clinic și electromiografic la două sau mai multe niveluri. O trăsătură caracteristică a cazurilor clinice descrise este predominanța slăbiciunii, amiotrofiei și fasciculațiilor la nivelul brațelor cu siguranță relativă a extremităților inferioare, ceea ce este în concordanță cu datele din literatură.
Toți pacienții au grade diferite de severitate a demenței frontale, manifestată printr-o combinație de tulburări comportamentale și cognitive. Ca parte a afectarii sferei emoțional-voliționale, se observă o scădere sau absență a motivației la acțiune, sărăcire emoțională, reacții emoționale inadecvate (negativism, agresivitate), distractibilitate crescută și scăderea criticii. Tulburările cognitive se manifestă prin tulburări de memorie, praxis și gnoză, care, spre deosebire de cele din demența de tip Alzheimer, sunt de natură reglatoare. În acest caz, mecanismul de reproducere a informației suferă în primul rând. Acest fenomen se manifestă mai ales clar atunci când se studiază caracteristicile tulburărilor de memorie. Astfel, demența de tip Alzheimer se caracterizează printr-o tulburare severă progresivă de memorie, iar cu demența frontală, chiar și în stadii destul de avansate, memoria pentru evenimentele vieții nu are de suferit, dar capacitatea de a învăța este afectată. Caracteristica este o încălcare a operațiunilor logice formale: previziune, planificare, abstractizare și generalizare.
Tulburările de vorbire, care se observă la toți pacienții descriși de noi, au o geneză complexă și sunt cauzate de o combinație de disartrie în cadrul tulburărilor bulbare și pseudobulbare și al disfaziei. În același timp, în ciuda diferitelor grade de severitate ale tulburărilor de vorbire, este de remarcat asemănarea lor semnificativă la toți pacienții: vorbirea este lentă, cu o nuanță nazală, sacadată, care amintește de „cantare”. Se notează semne de afazie dinamică: scurtarea frazelor și simplificarea structurilor gramaticale, scăderea producției spontane de vorbire, ecolalie și perseverență.
La toți pacienții, tabloul clinic al afectarii lobilor frontali nu se limitează la tulburările comportamentale și cognitive. Printre alte simptome caracteristice leziunilor părților anterioare ale creierului, se mai pot observa tulburări pelvine de origine centrală, reflexe de apucare, fenomenul de rezistență (gegenhalten) și tulburări de mers sub formă de lentoare, instabilitate, lărgire a bazei, scăderea lungimii pasului (apraxia mersului).
În ciuda tabloului clinic clar al sindromului ALS-demență, trebuie acordată atenție anumitor dificultăți care apar la diagnosticarea acestei boli. Acest lucru se datorează, în special, faptului că rezultatul degenerării cortexului frontal este o întrerupere a conexiunilor părților anterioare ale creierului cu alte structuri: ganglionii bazali, cerebel etc. Astfel, în clinica de Sindromul ALS-demență, simptome asemănătoare tulburărilor extrapiramidale și cerebeloase. Acest lucru este observat și la pacienții pe care i-am descris. Astfel, tulburările în timpul efectuării testelor de coordonare, observate în 2 cazuri, au fost considerate de noi ca un semn de deteriorare nu numai a structurilor cerebelului în sine, ci și a conexiunilor sale cu regiunile frontale. În plus, simptome precum incertitudinea și greșelile la efectuarea testelor de coordonare pot fi o manifestare a dispraxiei. Bradikinezia de severitate diferită observată în toate cazurile poate fi, de asemenea, rezultatul leziunilor părților frontale ale creierului și a conexiunilor acestora cu structurile subcorticale.
În cazul sindromului ALS-demență, ținând cont de prezența simptomelor piramidale, a tulburărilor cognitive, posturale și pelvine, precum și de posibila prezență a tulburărilor de coordonare și hipocinetice, se recomandă efectuarea unui diagnostic diferențial cu demența vasculară, paralizie supranucleară progresivă (PSP), atrofie a sistemelor multiple (MSA) și demență cu corpi Lewy (DLB).
Demența vasculară poate fi exclusă pe baza datelor neuroimagistice: un criteriu obligatoriu este o leziune multifocală pronunțată a cortexului și (sau) substanței albe a creierului. Putem vorbi despre prezența semnelor de encefalopatie discirculatoare la al treilea pacient, ținând cont de datele anamnezei (hipertensiune arterială, hiperlipidemie), caracteristici ale manifestărilor clinice, în special, severitatea și natura tulburărilor discoordonate, precum și detectarea. de leucoaraioza in periventricular prin RMN nici o regiune. Aparent, în acest caz, tulburările motorii sunt cauzate de o combinație de procese vasculare și degenerative care afectează axul fronto-cerebelos. Se poate presupune că tulburările motorii la debutul bolii sunt cauzate de leziuni vasculare cu adăugarea ulterioară a unui proces degenerativ.
În PSP, demența este predominant de natură subcorticală sunt obligatorii tulburările oculomotorii sub formă de pareză supranucleară a privirii și sindromul amiostatic. În DLB, demența este predominant cortical-subcorticală, deși în stadii avansate pot fi observate simptome de afectare a lobilor frontali. Pentru a pune un diagnostic de DLB, este necesară prezența fluctuațiilor deficiențelor cognitive și motorii, precum și a halucinațiilor vizuale. În plus, PSP și DLB se caracterizează prin prezența sindromului akinetic-rigid, în timp ce modificările de tonus observate la pacienții noștri reprezintă un fenomen de contracontinență, iar bradikinezia izolată nu ne permite să vorbim despre sindromul akinetic-rigid.
Prezența tulburărilor de coordonare, a simptomelor piramidale, a tulburărilor posturale, a tulburărilor pelvine, a modificărilor de tonus și a bradikineziei ne permite să considerăm MSA ca parte a diagnosticului diferențial. Potrivit majorității cercetătorilor, prezența tulburărilor cognitive în absența simptomelor de insuficiență autonomă periferică ne permite să excludem acest diagnostic.
Astfel, sindromul ALS-demență este o formă a bolii care are un tablou clinic foarte specific. În cele mai multe cazuri, boala debutează cu semne de afectare a regiunilor frontale și (mai rar) temporale, urmate de adăugarea simptomelor SLA. Prezența anumitor criterii morfologice care fac posibilă distingerea sindromului ALS-demență de alte variante de FTD confirmă independența sa nosologică. Principalele domenii care necesită studii suplimentare sunt clarificarea defectului genetic în această boală, compararea tulburărilor mintale în sindromul ALS-demență și alte forme de DFT, precum și studiul caracteristicilor clinice, patomorfologice și neurochimice ale afectarii centrale și periferice. neuroni motorii.
LITERATURĂ
1. Boli ale sistemului nervos: Un ghid pentru medici / Ed. N. N. Yakhno, D. P. Shtulman. - M.: Medicină, 2001. - T. 2.
2. Damulin I.V., Pavlova A.I Dementa de tip frontal // Nevpol. revistă - 1997. - Nr. 1. - P. 37-42.
3. Elkin M. N. Multiple system atrophy // Ibid. - Nr. 6. - P. 46-51.
4. Luria A. P. Funcțiile corticale umane superioare și tulburările lor în leziunile cerebrale locale. - M.: Proiect academic, 2000.
5. Stolyarov I. D., Golovkin V. I., Petrov A. M., Ilves A. G. Opinii moderne asupra patogenezei și abordărilor în tratamentul sclerozei laterale amiotrofice // Neurol. revistă - 1999. - Nr. 3. - P. 43-50.
6. Khatiashvili I.T., Yakhno N.N. Atrofia sistemului multiplu: caracteristici ale tulburărilor motorii și autonome // Ibid. - 2000. - Nr. 6. - P. 15-20.
7. Yakhno N.N., Shtulman D.R., Elkin M.N., Zakharov V.V. Sindromul de scleroză laterală amiotrofică - demență de tip frontal // Jurnal. neurol. si psihiatru. - 1995. - Nr. 1. - P. 20-23.
8. Bathgate B. şi colab. Comportament în demența frontotemporală, boala Alzheimer și demența vasculară // Acta Neurol. Scand. - 2001. - Vol. 103, N 6. - P. 367-378.
9. Bak T. H., Hodges J. R. Boala neuronului motor, demență și afazie: coincidență, concomitent sau continuu? // J. Neurol. - 2001. - Vol. 248. - P. 260-270.
10. Bergmann M. şi colab. Diferite variante ale demenței frontotemporale: un studiu neuropatologic și imunohistologic // Acta Neuropathol. - 1996. - Vol. 92. - P. 170-179.
11. Brion S. et al. Asociația Boala Picks și scleroza laterală amiotrofică // Encefală. - 1980. - Vol. 6, N 3. - P. 259-286.
12. Constantinidis J. Un sindrom familial: o combinație de boala Picks și scleroza laterală amiotrofică // Ibid. - 1987. - Vol. 13, N 5. - P. 285-293.
13. Gunnarson L.-G., Dahlbom K., Strandman E. Boala neuronului motor și demența raportate la 13 membri ai unei singure familii // Acta Neurol. Scand. - 1991. - Vol. 84. - P. 429-433.
14. Ikeda K. Unde ar trebui plasată demența fronto-temporală în istoria bolii Picks și a tulburărilor asociate // Seishin Shinkeigaku Zasshi. - 2000. - Vol. 102, N 6. - P. 529-542.
15. Jackson M., Lowe J. Noua neuropatologie a dementelor frontotemporale // Acta Neuropathol. - 1996. - Vol. 91. - P. 127-134.
16. Kawashima T. et al. Incluziuni asemănătoare scheiței în neostriat dintr-un caz de scleroză laterală amiotrofică cu demență // Ibid. - 1998. - Vol. 96. - P. 541-545.
17. Koller W. C. Handbook of Dementing Illnesses. - New York, 1994.
18. Mann D. M., South P. W., Snowden J. S., Neary D. Dementa of frontal lobe type: neuropathology and immunohistochemistry // J. Neurol. Neurochirurgie. Psihiatrie. - 1993. - Vol. 56, N 5. - P. 605-614.
19. Murakami N., Yoshida M. Reevaluarea sclerozei laterale amiotrofice cu demență // Rinsho Shinkeigaku. - 1995. - Vol. 35, N 12. - P. 1560-1562.
20. Nakano I. Dementa frontotemporal cu boala neuronului motor (scleroza laterala amiotrofica cu dementa) // Neuropatologie. - 2000. - Vol. 20, N 1. - P. 68-75.
21. Neary D. și colab. Demența lobului frontal și boala neuronului motor // J. Neurol. Sci. - 1990. - Vol. 53. - P. 23-32.
22. Neary D., Snowden J. S. Frontotemporal dementa: nosology, neuropsychology, and neuropathology // Brain Cogn. - 1996. - Vol. 31, N 2. - P. 176-187.
23. Neary D. și colab. Degenerescenta lobara frontotemporal. Un consens asupra criteriilor de diagnostic clinic // Neurologie. - 1998. - Vol. 51. - P. 1546-1554.
24. Neuropatologia demenței // Eds M. M. Esiri, J. H Morris. — 1997.
25. Niizato K. et al. Boala Picks cu scleroză laterală amiotrofică (ALS): raport a două cazuri de autopsie și revizuire a literaturii // J. Neurol. Sci. - 1997. - Vol. 1 (148), N 1. - P. 107-112.
26. Portet F., Cadilhac C., Touchon J., Camu W. Cognitive impairment in motor disease with bulbar debut // Amyotroph. Lateral. Scler. Neuronul motor. Discordie. - 2001. - Vol. 2, N 1. - P. 23-29.
27. Sam M., Gutmann L., Schochet S. S. Jr., Doshi H. Picks boala: un caz care seamănă clinic cu scleroza laterală amiotrofică // Neurologie. - 1991. - Vol. 41, N 11. - P. 1831-1833.
28. Talbot P. R. et al. Inter-relația dintre boala neuronului motor „clasic” și demența frontotemporală: studiu neuropsihologic și SPECT // J. Neurol. Neurochirurgie. Psihiatrie. - 1995. - Vol. 58, N 5. - P. 541-547.
29. Tolnay M., Probst A. Frontotemporal lobar degeneration. O actualizare asupra constatărilor clinice, patologice și genetice // Gerontologie. - 2001. - Vol. 47, N 1. - P. 1-8.
30. Tsuchiya K. și colab. Afazia rapid progresivă și boala neuronului motor: un studiu clinic, radiologic și patologic al unui caz de autopsie cu atrofie lobară circumscrisă // Acta Neuropathol. - 2000. - Vol. 99, N 1. - P. 81-87.
31. Tsuchiya K. și colab. Scleroza laterală amiotrofică atipică cu demență mimând boala Picks frontală: un raport al unui caz de autopsie cu un curs clinic de 15 ani // Ibid. - 2001. - Vol. 101. - P. 625-630.
32. Uchihara T. et al. Corpul buninei în demența lobului frontal fără manifestări clinice ale bolii neuronului motor // Ibid. - N 3. - P. 281-284.
33. Verma A., Bradley W. G. Atypical motor neuron disease and related motor syndromes // Semin. Neurol. - 2001. - Vol. 21, N 2. - P. 177-187.
34. Wakabayashi K. și colab. Incluziuni neuronale ubiquitinate în neostiatum la pacienții cu scleroză laterală amiotrofică cu sau fără demență — un studiu pe 60 de pacienți cu vârsta cuprinsă între 31 și 87 de ani // Clin. neuropathol. - 2001. - Vol. 20, N 2. - P. 47-52.
35. Wightman G. et al. Incluziuni ubiquitin-imuoreactive hipocampale și neocorticale în scleroza laterală amiotrofică cu demență // Neurosci. Lett. - 1992. - Vol. 139, N 2. - P. 269-274.
36. Woulfe J., Kertesz A., Munoz D. G. Frontotemporal dementa with ubiquitinated cytoplasmic and intranuclear inclusions // Acta Neuropathol. - 2001. - Vol. 102. - P. 94-102.
Boala este descrisă în 1961 și 1964 Adams, Van Bogart și Van der Eken, care au prezentat o descriere clinică și morfologică a 4 observații și au fundamentat independența nosologică a degenerescenței strio-nigrale. Diagnosticul diferențial, în opinia autorilor, este foarte dificil, deoarece tabloul clinic al degenerescării strionigrale reproduce cel mai adesea un tablou aproape complet al parkinsonismului, deosebindu-se de acesta din urmă doar prin caracteristicile substratului morfologic.
În ultimii ani, au existat indicii ale posibilității diagnosticului intravital al acestei suferințe.
Boala cel mai adesea începe cu apariția rigidității musculare la una sau ambele extremități inferioare, care se generalizează treptat odată cu adăugarea de tremor. Tremuratul este de obicei ușor și se retrage în fundal în tabloul clinic. În același timp, hipokinezia progresează cu hipomimie caracteristică, clipire rară, postură „flexorie”, modificări ale mersului și scrisului (micrografie).
Invaliditateîn această boală este de obicei asociată cu rigiditate pronunțată și akinezie. Tulburările de vorbire sunt caracteristice, care se observă la aproximativ 2/3 dintre pacienți și pot atinge gradul de disartrie severă. Uneori mestecatul și înghițitul încetinesc. Semnele piramidale sunt adesea detectate.
Mult mai putin caracteristică simptome cerebeloase ușor exprimate (în cele mai multe cazuri sunt absente cu totul) sub formă de tremor de intenție, ataxie cerebeloasă ușoară și nistagmus. Au fost descrise hipotensiune arterială ortostatică și sincopă. Demența moderată este posibilă. Apariția hiperkinezei este necaracteristică. Majoritatea cazurilor descrise sunt sporadice, deși există observații în care poate fi urmărit un mod de moștenire autosomal dominant.
Tabloul clinic această boală este adesea imposibil de distins de parkinsonism; judecând după modificările morfologice, degenerescenta strionigală ocupă o poziţie intermediară între parkinsonismul idiopatic, coreea Huntington şi degenerescenta olivo-ponto-cerebeloasă. Debutul bolii are loc în decada a 5-a-7 a vieții, iar cursul este lent progresiv. Moartea apare din cauza infecțiilor intercurente, de obicei la 3-7 ani de la debutul bolii.
Eficacitatea 1-dopa este controversat. Astfel, într-o serie de observații, 1-dopa nu a avut un efect terapeutic. Potrivit unor autori, lipsa efectului 1-dopa poate servi drept bază pentru suspectarea degenerescenței strio-nigrale. Aparent, eficacitatea 1-dopa nu poate servi ca un semn de diagnostic diferenţial de încredere. De asemenea, a fost descris efectul benefic al 1-dopa în această boală.
Parkinsonism - scleroza laterala amiotrofica(ALS) - demență și alte forme insuficient diferențiate de degenerescență sistemică. Combinațiile caracteristice ale sindroamelor „parkinsonism-demență”, „parkinsonism-ALS” și „parkinsonism-ALS-demență” au fost descrise pentru prima dată în studiul sclerozei laterale amiotrofice de pe insula Guam (Insulele Mariana).
In populatie trib Chamorro a dezvoltat sindromul parkinsonism-ALS-demență poate începe fie cu demența parkinsoniană, fie cu scleroza laterală amiotrofică, care reprezintă astfel doar una dintre etapele formării unui complex neurologic mai complex. Sindromul parkinsonismului în rândul pacienților din tribul Chamorro a fost caracterizat de o predominanță a akineziei asupra rigidității. La pacienții cu complexul parkinsonism-ALS-demență din regiunea Rostov, au fost detectate mai des forme tremuroase sau rigide de parkinsonism.