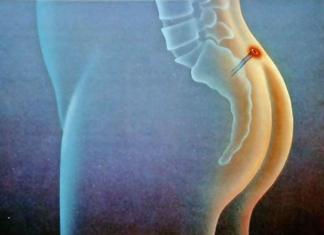
Heç bir yan təsiri yoxdur, buna görə də maraqlanmağa dəyər: ümumiyyətlə işləyirmi? Bu bəlkə də sərt sözlərlə mən narkotik təhlükəsizliyi monitorinqinin ən vacib elementlərindən birinin təhlilinə başlamaq istərdim.
Milli Əczaçılıq Nəzarəti Mərkəzinin baş direktoru LekOboz-a farmakonazarət sistemində düzgün fəaliyyət göstərməyi izah edib. Anatoli Krasheninnikov və müstəqil GCP və GLP auditoru Yevgeni Roqov.
Ümumdünya Səhiyyə Təşkilatının tövsiyələrinə görə, norma 100 min əhaliyə 60 mənfi reaksiya hesabatıdır. Rusiyada bu rəqəm 14 ilə 47 mesaj arasında dəyişir (regiondan asılı olaraq). Bunda həm xəstələrin, həm həkimlərin, həm də əczaçıların məlumatsızlığı mühüm rol oynayır.
Bu gün ölkəmizdə milli təhlükəsizlik məsələlərinə böyük diqqət yetirilir. Şübhəsiz ki, istənilən dövlətdə onun sisteminin bir hissəsi əhalinin sağlamlıq vəziyyətinin yaxşılaşdırılmasına, o cümlədən səhiyyə sisteminin inkişafına yönəlmiş tədbirləri əhatə etməlidir. Və bu, öz növbəsində, adekvat olmadan ağlasığmazdır dərman təminatı. Ona görə də dövlət nəzarət etməlidir.
Amma nə olmalıdır? dərmanların dövriyyəsinə nəzarət?
Dar spesifik mənada dövlət nəzarəti cəmiyyətdə dərman vasitəsinə inam yaradan tədbirlər kompleksidir:
- təhlükəsiz, effektiv (və onun təhlükəsizliyi və effektivliyi tibbi istifadə üçün təlimatlara uyğundur);
- bütün keyfiyyət standartlarına cavab verir.
Dövlət nəzarəti dərmanın "həyatının" bütün mərhələlərində həyata keçirilir:
- inkişaf mərhələsində, xüsusən də tədqiqat mərhələsində;
- dərman vasitəsinin dövlət qeydiyyatı mərhələsində;
- və mütləq olaraq dərman dövriyyəyə daxil olduqdan sonra (farmakoviqilans sistemi yaratmaqla).
Dərman dövlət qeydiyyatından keçməzdən və bazara çıxmazdan əvvəl onun haqqında hərtərəfli məlumat əldə etmək lazımdır səmərəlilik və təhlükəsizlik. İnkişaf mərhələsində 10.000 potensial perspektivli molekuldan yalnız 1 dərman bazara çıxır, və "narkotik namizədlərin" əksəriyyəti təhlükəsizlik məsələlərində dəqiq olaraq aradan qaldırılır.
Dərman təhlükəsizliyinin əsas fərziyyəsi əvvəlki prosesdə təsdiqlənir klinik sınaqlarən azı iki növ test sistemindən (laboratoriya heyvanları) istifadə etməklə. Təəssüf ki, elmin hazırkı inkişaf səviyyəsi insanın iştirakı ilə aparılan tədqiqatlardan yan keçərək yenilərinin yaradılmasına imkan vermir, çünki heç bir bioloji model dərmanın insan orqanizmində “davranışını” təkrar etməyə qadir deyil. Buna görə də, klinik sınaqlar mərhələsində dərmanın effektivliyi və təhlükəsizliyinin sübut edilməsi son dərəcə vacibdir - bu tədqiqatların əsasını təşkil edən məlumatlardır. tibbi istifadə üçün təlimat.
Başqa sözlə, dərman vasitəsinin dövlət qeydiyyatına alınması və bazara daxil olduğu andan etibarən bu inkişaf mərhələsindəki uğursuzluqlar hüquqi baxımdan qeyri-müəyyən sayda insanların həyat və sağlamlığı üçün təhlükə yaradır. Bu, həm təhlükəsizlik məlumatlarına, həm də effektivlik məlumatlarına tamamilə aiddir. Ərizə dərman məhsulu elan ediləndən (həm az, həm də çox) fərqlənən effektivliyi ilə, onu qəbul edən xəstələrin həyatı və sağlamlığı üçün təhlükə yaradır.
Dünyada Yan təsirləri olmayan dərmanlar yoxdur, və bu təsirlər tibbi istifadə üçün təlimatlarda mümkün qədər ətraflı təsvir edilməlidir. Hətta qədim dünyada şəfaçılar kimyəvi maddələrin insan orqanizminə zərərli təsiri barədə xəbərdarlıq edirdilər. Beləliklə, in Qədim Yunanıstan bir sözlə "farmakon" təkcə dərman deyil, həm də zəhər demək idi. O dövrlərdən bəri elm çox irəli getdi və bu gün dərmanların faydaları istifadə risklərini əhəmiyyətli dərəcədə üstələyir, lakin buna baxmayaraq, belə risklər qalmaqdadır.
Rusiya ilk on ölkə sırasındadır narkotik istehlakının ən yüksək həcmi ilə mütləq mənada (bu göstəricini sakinlərin sayı ilə müqayisə etsəniz, ev xəstələrinin davranışında çox şey aydın olacaq). Ölkəmizdə əczaçılıq bazarının payı ÜDM-in təxminən 1%-ni təşkil edir.
Əczaçılıq məhsullarının, xüsusən də qocalmış əhali tərəfindən istehlakın bu qədər yüksək səviyyədə olması ilə onların düzgün istifadəsinə və təhlükəsizliyinə nəzarət problemi ictimai səhiyyə sahəsində aktuallıqdan daha çox aktualdır. Mümkün olanları müəyyən etməyə, qiymətləndirməyə və dərk etməyə yönəlmiş fəaliyyətlər mənfi nəticələr narkotik vasitələrin istifadəsi, onların baş verməsinin qarşısının alınması və xəstələrin qorunması- Bu farmakovigilans sisteminin əsasını təşkil edir.
Həm xəstələr, həm də həkimlər arasında ümumi bir yanlış fikir var ki, praktikada istifadə üçün təsdiqlənmişlər və hamısı hərtərəfli öyrənilib. yan təsirlər tibbi istifadə üçün təlimatlarda əks olunur. Bu yalnız qismən doğrudur.
Əslində, qeydiyyat zamanı Yeni dərman məhdud sayda xəstə üzərində sınaqdan keçirilir və süni yaradılmış şəraitdə, fənlərin seçilməsi üçün müəyyən meyarlardan istifadə edildikdə. Buna görə də, bu mərhələdə nisbətən nadir yan təsirlər aşkar edilə bilməz.
Statistik qanunlar göstərir ki, 10.000-də 1 tezliyi ilə baş verən yan təsirlərin aşkar edilməsini təmin etmək üçün (və bu, nisbətən ümumi sayılır) 30.000 xəstə üzərində tədqiqat aparılmalıdır. Dərmanların qeydiyyatı çox vaxt daha az sayda xəstə üzərində klinik sınaqlardan sonra həyata keçirilir.
Üstəlik, dərmanın real praktikada istifadəsi ideal klinik sınaq şəraitindən fərqlənir: xəstələrdə müşayiət olunan xəstəliklər var, başqa dərmanlar qəbul edir və s. Bir çox amillər var (xəstələrin yaşı, dərmanların bir-biri ilə qarşılıqlı təsiri, kimi eləcə də qida ilə və s.) dərmanın təhlükəsizlik profilinə əhəmiyyətli dərəcədə təsir göstərə bilər.
Ancaq bu, hamısı deyil. Ənənəvi olaraq Rusiya bazarında generiklərin böyük bir payı var. Rusiyada, eləcə də bütün dünyada bir generik qeydiyyatdan keçmək üçün istehsalçı tənzimləyiciyə dərmanların insan orqanizmində eyni tərkibə və eyni farmakokinetik parametrlərə malik olduğunu sübut etməlidir. Bu parametrləri qiymətləndirmək üçün həyata keçirilir sağlam könüllülərdə bioekvivalentlik tədqiqatı, onların sayı dərmandan asılı olaraq dəyişir və 18 ilə bir neçə onlarla nəfər arasında dəyişir. Eyni tərkibə və bir-birinə bioekvivalentə malik olan dərmanların oxşar effektivlik və təhlükəsizlik profilinə malik olacağı gözlənilir.
Və ya başqa bir vəziyyət: bəzən yan təsirlər dərman qeydiyyata alındıqdan bir neçə il sonra görünə bilər. Məsələn, yalnız 35 illik istifadədən sonra amidopirin aqranulositoza səbəb ola biləcəyi aşkar edilmişdir.
Dərmanları qeydiyyata alındıqdan və aptek rəflərində göründükdən sonra öyrənməyə davam etmək çox vacibdir. Dərmana arzuolunmaz reaksiyanın nəticələrini minimuma endirmək üçün profilaktik tədbirlərin görülməsi əsasən həkim və əczaçının məsuliyyətindən asılıdır. Mənfi reaksiyaların vaxtında bildirilməsinin vacibliyini yalnız peşəkar anlayır.
Buna görə də, dərman müalicəsinin təhlükəsizliyini artırmaq - və qayğı keyfiyyətini artırmaq tibbi yardım Dərman vasitələrinin effektivliyinin və təhlükəsizliyinin monitorinqi proqramlarının bir hissəsi olaraq səhiyyə müəssisələri həkimlər arasında mənfi reaksiyalar barədə məlumat verilməsinin vacibliyi ilə bağlı maarifləndirmə işi aparmalıdırlar. Həm də: çətin hallarda xəstələrə məsləhət vermək, regional və federal farmakovigilans mərkəzlərini məlumatlandırmaq, tibb işçilərini yerli və beynəlxalq monitorinqin ən vacib nəticələri ilə tanış etmək mənfi reaksiyalar, Rusiyada və digər ölkələrdə dərman vasitələrinin bazardan geri çağırılması və ya istifadəsinə məhdudiyyətlərin qoyulması halları haqqında.
Roszdravnadzor-un 15 fevral 2017-ci il tarixli 1071 nömrəli “Farmakovigiraniyanın həyata keçirilməsi qaydasının təsdiq edilməsi haqqında” əmrinə əsasən, dərmanların istifadəsinin təhlükəsizliyi və effektivliyinə dair əlavə reaksiyaların və digər məlumatların müəyyən edilməsi üzrə tibb təşkilatlarının işi tənzimlənməlidir. təşkilatın daxili sənədləri ilə. Praktikada bu o deməkdir ki, hər bir səhiyyə müəssisəsində bu problemləri həll etmək üçün məsul şəxs (adətən klinik farmakoloq) təyin olunmalıdır. Farmakovigilans məsələləri ilə bağlı izahat işi Roszdravnadzor və onun ərazi orqanları tərəfindən həyata keçirilir.
Dərman təhlükəsizliyi monitorinqinin effektivliyi birbaşa əczaçılıq şirkətlərinin, tibb işçilərinin və xəstələrin fəaliyyətindən asılıdır. Yalnız birlikdə biz onu daha səmərəli və təhlükəsiz edə bilərik.
Tibb nə vaxtsa farmakovigilans olmadan edə biləcəkmi?
Bütün göstərişlər xəstəyə tam aydın olsa belə, cavab aydındır: Yox . Ancaq effektiv təhlükəsizlik monitorinqi dərmanlar bir şərtlə mümkündür: əgər xəstə, həkim və səhiyyə sistemi arasında qarşıdurma yox, qarşılıqlı əlaqə qurularsa...
Açar sözlər
EKSpress HESABAT/ MESAJ / XƏBƏRDARLIQ / MƏNS HADİSƏ / MƏNS REAKSİYA / DÖVRİ HESABAT / DÖVRİ DÖVRÜ HESABAT DARMAN TƏHLÜKƏSİZLİĞİ / DÖVRİ DÖVRÜ HESABAT/ FARMAKOVİJİLANSannotasiya fundamental tibb üzrə elmi məqalə, elmi işin müəllifi - Olefir Yu.V., Romanov B.K., Alyautdin R.N., Lepaxin V.K., Krasheninnikov A.E.
Xülasə. 2018-ci il yanvarın 1-dən Rusiyada farmakovigilansa nəzarətə riskə əsaslanan yanaşmanın tətbiqi ilə əlaqədar olaraq, hesabatların düzgün hazırlanması və təqdim edilməsi baxımından dərman istehsalçılarının və istehsalçılarının məsuliyyəti artır. İşin məqsədi sistemin vəziyyətini qiymətləndirməkdir ekspress hesabat və Rusiya Federasiyasının və Avrasiya İqtisadi İttifaqının qanunvericiliyinin mövcud tələblərinə uyğun olaraq dərman vasitələrinin təhlükəsizliyinə dair dövri hesabatların verilməsi. Məqalədə farmakovigilans hesabat formalarının hazırlanmasına dair tövsiyələrə dair bir sıra nəşrlər davam etdirilir. Tibbi istifadə üçün dərman vasitələrinin qeydiyyat şəhadətnaməsi sahibləri üçün milli və beynəlxalq qanunvericiliyin mövcud normativ tələblərinə uyğun olaraq hesabat formalarının hazırlanması baxımından Rusiyada dərman təhlükəsizliyinə nəzarət sisteminin ayrı-ayrı elementlərinin vəziyyətinin qiymətləndirilməsinin nəticələri və dərman tərtibatçıları təqdim olunur. Nəticələr: Dövri hesabatların düzgün hazırlanması üçün tövsiyələr təklif olunur. Əlavə qiymətləndirmə tələb edən bir sıra problemlər, xüsusən də Rusiyada Dərmanların Təhlükəsizliyinə Nəzarət Regional Mərkəzləri sisteminin qeyri-qənaətbəxş vəziyyəti müəyyən edilmişdir. Məqalə klinik farmakoloqlara, farmakovigilans üzrə müvəkkillərə, farmakovigilans mütəxəssislərinə, tibb və əczaçılıq təşkilatlarının rəhbərlərinə və tibb sahəsində tədqiqatçılara ünvanlanıb.
Əlaqədar mövzular fundamental tibb üzrə elmi əsərlər, elmi işin müəllifi - Olefir Yu.V., Romanov B.K., Alyautdin R.N., Lepaxin V.K., Krasheninnikov A.E.
-
Dərman dövriyyəsi sahəsində mütəxəssislərin peşəkar maraqlarının əks olunması kimi təhsil ehtiyacları
2019 / Goloenko N.G., Yagudina R.I., Kulikov A.Yu., Serpik V.G., Protsenko M.V., Logvinyuk P.A. -
Dərman məhsulunun təhlükəsizliyinə dair dövri hesabatın hazırlanması
2018 / Romanov B.K., Alyautdin R.N., Qlagolev S.V., Polivanov V.A., Krasheninnikov A.E. -
Dərman vasitəsinin təhlükəsizliyinə dair dövri hesabatın standart forması
2017 / Romanov B.K., Alyautdin R.N., Darmostukova M.A., Qlagolev S.V., Polivanov V.A. -
Pediatrik praktikada həyəcan mesajları
2018 / Kutekhova G.V., Zhuravleva E.O., Darmostukova M.A., Snegireva I.I., Velts N.Yu., Alyautdin R.N., Shubnikova E.V. -
Valerian və korvalol preparatlarından istifadə edərkən mənfi reaksiyalar: spontan hesabatların təhlili
2018 / Morokhina S.L., Alyautdin R.N., Kaperko D.A., Şubnikova E.V., Snegireva I.I., Smirnova Yu.A. -
Marketinqdən sonrakı dövrdə qeydə alınmış dərmanların mənfi reaksiyaları haqqında
2019 / Şubnikova E.V., Darmostukova M.A., Bukatina T.M., Kaperko D.A., Velts N.Yu., Kazakov A.S., Snegireva I.I., Juravleva E.O., Kutexova G.V. - 2016 / Qlagolev S.V., Olefir Yu.V., Romanov B.K., Alyautdin R.N.
-
Klinik sınaqların təhlükəsizliyinə dair materialların təhlili və sintezinin nəticələri
2017 / Olefir Yu.V. -
Qeyri-steroid antiinflamatuar dərmanların istifadəsinin təhlükəsizliyi məsələsinə dair
2018 / Velts N.Yu., Bukatina T.M., Juravleva E.O., Kutexova G.V., Darmostukova M.A., Olefir Yu.V., Romanov B.K., Glagolev S.V., Polivanov V.A. -
Farmakovigilans üçün monitorinq ədəbiyyatı
2019 / Xudoşin A.G., Xu S., Romanov B.K.
2018-ci il yanvarın 1-dən Rusiyada tətbiq edilən farmakovigilans nəzarətinə risk əsaslı yanaşma dərman vasitələrinin istehsalçıları və inkişaf etdiricilərinin məsuliyyətini artırır. İşin məqsədi Rusiya Federasiyası və Avrasiya İqtisadi İttifaqının qanunvericiliyinin müvafiq tələblərinə uyğun olaraq dərman vasitələrinin təhlükəsizliyinə dair Ekspres hesabat və Dövri hesabat sistemini qiymətləndirməkdir. Məqalədə farmakovigilans üzrə hesabat formalarının hazırlanmasına dair tövsiyələrə dair bir sıra nəşrlər davam etdirilir. Məqalədə dərman vasitələrinin qeydiyyat şəhadətnaməsi sahibləri üçün milli və beynəlxalq qanunvericiliyin mövcud normativ tələblərinə uyğun olaraq hesabat formalarının hazırlanması baxımından Rusiyada dərman təhlükəsizliyinə nəzarət sisteminin elementlərinin vəziyyətinin qiymətləndirilməsinin nəticələri təqdim olunur. tibbi istifadə və dərmanların inkişaf etdiriciləri. Dövri hesabatların düzgün hazırlanması üçün tövsiyələr təklif olunur. Əlavə qiymətləndirmə tələb edən problemlərin sırası, xüsusən də Rusiyada dərman vasitələrinin təhlükəsizliyinə nəzarət edən regional mərkəzlər sisteminin vəziyyəti vurğulanır. Məqalə klinik farmakoloqlara, farmakovigil müvəkkillərinə, farmakovigilans mütəxəssislərinə, tibb və əczaçılıq təşkilatlarının rəhbərlərinə və tibb müəlliflərinə ünvanlanıb.
Elmi işin mətni "Rusiyada farmakovigilans hesabatının qiymətləndirilməsi" mövzusunda
ORİJİNAL MƏQALƏLƏR
https://doi.org/10.30895/2312-7821-2018-6-4-150-154
Rusiyada farmakovigilans hesabatının qiymətləndirilməsi
Yu. V. Olefir1, *B. K. Romanov1, R. N. Alyautdin1, V. K. Lepaxin1, A. E. Kraşeninnikov2, E. V. Şubnikova1
1 Rusiya Federasiyası Səhiyyə Nazirliyinin “Tibbi Məhsulların Ekspertizası Elmi Mərkəzi” Federal Dövlət Büdcə Müəssisəsi, Petrovski bulvarı, 8, bina 2, Moskva, 127051, Rusiya Federasiyası 2 Muxtar qeyri-kommersiya təşkilatı “Milli elm mərkəzi Farmakovigilans”, Bolşoy Bulvarı, 42, bina 1, Skolkovo İnnovasiya Mərkəzinin ərazisi, Moskva, 143026, Rusiya Federasiyası
Xülasə. 2018-ci il yanvarın 1-dən Rusiyada farmakovigilansa nəzarətə riskə əsaslanan yanaşmanın tətbiqi ilə əlaqədar olaraq, hesabatların düzgün hazırlanması və təqdim edilməsi baxımından dərman istehsalçılarının və istehsalçılarının məsuliyyəti artır. İşin məqsədi Rusiya Federasiyasının və Avrasiya İqtisadi İttifaqının qanunvericiliyinin mövcud tələblərinə uyğun olaraq təcili hesabat sisteminin vəziyyətini və dərman vasitələrinin təhlükəsizliyinə dair dövri hesabatları qiymətləndirməkdir. Məqalədə farmakovigilans hesabat formalarının hazırlanmasına dair tövsiyələrə dair bir sıra nəşrlər davam etdirilir. Rusiyada dərman təhlükəsizliyinə nəzarət sisteminin ayrı-ayrı elementlərinin vəziyyətinin tibbi istifadə üçün dərman vasitələrinin qeydiyyat şəhadətnaməsi sahibləri üçün milli və beynəlxalq qanunvericiliyin mövcud normativ tələblərinə uyğun olaraq hesabat formalarının hazırlanması baxımından qiymətləndirilməsinin nəticələri. dərman tərtibatçıları təqdim olunur. Nəticələr: Dövri hesabatların düzgün hazırlanması üçün tövsiyələr təklif olunur. Əlavə qiymətləndirmə tələb edən bir sıra problemlər, xüsusən də Rusiyada Dərmanların Təhlükəsizliyinə Nəzarət Regional Mərkəzləri sisteminin qeyri-qənaətbəxş vəziyyəti müəyyən edilmişdir. Məqalə klinik farmakoloqlara, farmakovigilans üzrə müvəkkillərə, farmakovigilans mütəxəssislərinə, tibb və əczaçılıq təşkilatlarının rəhbərlərinə və tibb sahəsində tədqiqatçılara ünvanlanıb.
Açar sözlər: ekspress hesabat; mesaj; xəbərdarlıq; mənfi hadisə; arzuolunmaz reaksiya; dövri hesabat; dərmanın təhlükəsizliyinə dair dövri hesabat; dərman vasitəsinin təhlükəsizliyinə dair dövri hesabat; uzaq maconadzor
Sitat üçün: Olefir YuV, Romanov BK, Alyautdin RN, Lepakhin VK, Krasheninnikov AE, Shubnikova EV. Rusiyada farmakovigilans hesabatının qiymətləndirilməsi. Farmakoterapiyanın təhlükəsizliyi və riskləri. 2018;6(4):150-154. https://doi.org/10.30895/2312-7821-2018-6-4-150-154
*Əlaqələndirici şəxs: Romanov Boris Konstantinoviç; [email protected]
Rusiyada Farmakovigilans Hesabatının Qiymətləndirilməsi
Yu. V. Olefir1, *B. K. Romanov1, R. N. Alyautdin1, V. K. Lepaxin1, A. E. Kraşeninnikov2, E. V. Şubnikova1
1 Dərman Məhsullarının Ekspert Qiymətləndirilməsi üzrə Elmi Mərkəz, 8/2 Petrovski Blvd, Moskva 127051, Rusiya Federasiyası 2 Müstəqil Qeyri-Kommersiya Təşkilatı "Milli Farmakovigilans Tədqiqat Mərkəzi", 42/1, Bolşoy Blvd, Moskva 143026, Rusiya Federasiyası
mücərrəd. 2018-ci il yanvarın 1-dən Rusiyada tətbiq edilən farmakovigilans nəzarətinə risk əsaslı yanaşma dərman vasitələrinin istehsalçıları və inkişaf etdiricilərinin məsuliyyətini artırır. İşin məqsədi Rusiya Federasiyası və Avrasiya İqtisadi İttifaqının qanunvericiliyinin müvafiq tələblərinə uyğun olaraq dərman vasitələrinin təhlükəsizliyinə dair Ekspres hesabat və Dövri hesabat sistemini qiymətləndirməkdir. Məqalədə farmakovigilans üzrə hesabat formalarının hazırlanmasına dair tövsiyələrə dair bir sıra nəşrlər davam etdirilir. Məqalədə dərman vasitələrinin qeydiyyat şəhadətnaməsi sahibləri üçün milli və beynəlxalq qanunvericiliyin mövcud normativ tələblərinə uyğun olaraq hesabat formalarının hazırlanması baxımından Rusiyada dərman təhlükəsizliyinə nəzarət sisteminin elementlərinin vəziyyətinin qiymətləndirilməsinin nəticələri təqdim olunur. tibbi istifadə və dərmanların inkişaf etdiriciləri. Dövri hesabatların düzgün hazırlanması üçün tövsiyələr təklif olunur. Əlavə qiymətləndirmə tələb edən problemlərin sırası, xüsusən də Rusiyada dərman vasitələrinin təhlükəsizliyinə nəzarət üçün regional mərkəzlər sisteminin vəziyyəti vurğulanır. Məqalə klinik farmakoloqlara, farmakovigilanslara ünvanlanıb
müvəkkilləri, farmakovigilans mütəxəssisləri, tibb və əczaçılıq təşkilatlarının rəhbərləri və tibb müəllifləri.
Açar sözlər: ekspress hesabat; mənfi hadisə; mənfi reaksiya; dövri hesabat; dövri təhlükəsizlik yeniləmə hesabatı; farmakovigilans
Sitat üçün: Olefir YuV, Romanov BK, Alyautdin RN, Lepakhin VK, Krasheninnikov AE, Shubnikova EV. Rusiyada farmakovigilans hesabatının qiymətləndirilməsi. "Təhlükəsizlik"
i risk farmakoterapii = Farmakoterapiyanın təhlükəsizliyi və riski. 2018;6(4):150-154. https://doi.org/10.30895/2312-7821-2018-6-4-150-154 *Əlaqələndirici şəxs: Boris K. Romanov; [email protected]
Rusiya Federasiyasının 1 yanvar 2018-ci il tarixindən etibarən farmakoloji nəzarət sahəsində nəzarət və nəzarət fəaliyyətlərinə risk əsaslı yanaşmanın tətbiqinə keçməsi, hesabatın kəmiyyət və keyfiyyət qiymətləndirilməsi daxil olmaqla, sənədli yoxlamaların sayını və əhəmiyyətini artırdı. , və bu hissədə risklərin minimuma endirilməsi dərman sisteminin təhlükəsizliyinin bütün subyektləri üçün aktual olmuşdur.
Dərman vasitəsinin təhlükəsizliyinə dair ekspress hesabatın və dövri hesabatın hazırlanması Roszdravnadzor-un 15.02.2017-ci il tarixli 1071 nömrəli “Farmakovigilansın həyata keçirilməsi Qaydasının təsdiq edilməsi haqqında” əmri əsasında və formada həyata keçirilir. Avrasiya İqtisadi Komissiyası Şurasının 11.03.2016-cı il tarixli, 87 nömrəli “Avrasiya İqtisadi İttifaqının yaxşı əczaçılıq təcrübəsi Qaydalarının təsdiq edilməsi haqqında”1 Qərarında nəzərdə tutulmuş müddətlərdə dərman vasitələrini hazırlayanlar (adından olan təşkilatlar) tərəfindən klinik sınaq keçirmək üçün icazə verilmiş və ya onlar tərəfindən icazə verilmişdir hüquqi şəxslər) və Rusiya Federasiyasında tibbi istifadə üçün qeydiyyatdan keçmiş bütün dərman vasitələrinin (dərman vasitələrinin) qeydiyyat şəhadətnamələrinin (DRU) sahibləri.
Hesabat formaları DRU və dərman tərtibatçıları tərəfindən tövsiyə olunan şəkildə - onları Roszdravnadzorun "Pharmaconadzor" federal məlumat bazasına (DRU üçün) və ya Roszdravnadzorun "MKILS" (Dərmanların klinik sınaqlarının monitorinqi) məlumat bazasına (dərman üçün) göndərməklə təqdim olunur. tərtibatçılar). Əgər kliniki sınaq zamanı xoşagəlməz hadisənin səbəbi qeydiyyatdan keçmiş dərman vasitəsinin istifadəsi olubsa, bu hadisə barədə təcili hesabat göndərilir.
1 Avrasiya İqtisadi Komissiyası Şurasının 2016-cı il 3 noyabr tarixli 87 nömrəli “Avrasiya İqtisadi İttifaqının yaxşı əczaçılıq təcrübəsi Qaydalarının təsdiq edilməsi haqqında” Qərarı. Buradan əldə etmək olar: http://docs. eaeunion.org/docs/ru-ru/01411948/cncd_21112016_87
Roszdravnadzorun Pharmaconadzor məlumat bazasına dərman hazırlayan.
Alternativ yol, işlənməkdə olan dərmanların klinik sınaqlarının təhlükəsizliyi ilə bağlı müstəqil etik komitələrə ekspress hesabat verən hallar istisna olmaqla, hesabatların digər verilənlər bazalarına göndərilməsidir.
İşin məqsədi Rusiya Federasiyasının və Avrasiya İqtisadi İttifaqının (EAEU) qanunvericiliyinin mövcud tələblərinə uyğun olaraq təcili hesabat sisteminin vəziyyətini və dərman təhlükəsizliyinə dair dövri hesabatları qiymətləndirməkdir.
Tədqiqatın məqsədləri: tənzimləyici təsirin qiymətləndirilməsinin aparılması; hesabat üçün məlumat mənbələrinin təhlili; tənzimləyicilər və sənaye tərəfindən düzəldici tədbirlərin qiymətləndirilməsi; düzgün hesabat üçün tövsiyələrin hazırlanmasının mümkünlüyünün qiymətləndirilməsi.
MATERİALLAR VƏ METODLAR
Tədqiqat materialları - əczaçılıq şirkətlərinin tibb və tənzimləmə bölmələrinin rəhbərləri arasında keçirilən sorğunun nəticələri; 01.09.2004-cü ildən 08.02.2018-ci il tarixədək Dərman Vasitələrinin Dövlət Reyestrində yerləşdirilmiş inzibati qərarlar, tibbi jurnalların müəllifləri arasında sorğunun nəticələri, habelə Rusiya Federasiyasının tənzimləyici orqanlarının normativ hüquqi aktları və daxili sənədləri. EAEU, dərmanların təhlükəsizliyinin qiymətləndirilməsi üsullarına dair yerli və xarici təlimatlar, elmi məqalələr, dərman təhlükəsizliyi üzrə federal məlumat bazaları.
Sistem təhlili metodlarından, rəy liderlərinin ekspert sorğularından, habelə metodlardan istifadə etməklə, farmakovigilansiya sahəsində mövcud qanunvericilik tələblərinin tibbi istifadə üçün dərman vasitələrinin dövriyyəsi ilə bağlı risklərə tənzimləyici təsirinin qiymətləndirilməsi məqsədilə informasiya-analitik araşdırmalar aparılıb. statistik məlumatların emalı.
NƏTİCƏLƏR VƏ MÜZAKİRƏ
Tənzimləmə təsirini qiymətləndirmək üçün 38 sənaye nümayəndəsi arasında sorğunun nəticələri və 164 inzibati qərarın təhlili qiymətləndirilib. Məlum olub ki, 2018-ci ilin ilk 9 ayında ən böyük çətinliklər DRU tərəfindən dövri olaraq dərman təhlükəsizliyi hesabatlarının (DSR) hazırlanması ilə bağlı yaranıb. Sorğuda iştirak edən DRU-ların yarısı (19 respondent) təqdim edilmiş PS-yə dair mənfi ekspert rəylərinin olduğunu qeyd etdi, onların yarıdan çoxu (12 respondent) yerli dərman istehsalçılarıdır. Tənzimləyicinin inzibati qərarlarının təhlilinin nəticələri fəal sənaye mənbələrinin üstünlük təşkil etdiyini göstərir - demək olar ki, bütün qərarlar ərizəçilərin məktubları və Nazirliyin "Tibbi Məhsulların Ekspertizası Elmi Mərkəzi" Federal Dövlət Büdcə Qurumunun məktubları əsasında hazırlanmışdır. Rusiya Federasiyasının Səhiyyə Nazirliyi (Rusiya Səhiyyə Nazirliyinin FSBI "NTsESMP").
Dərman istehsalçıları arasında aparılan sorğu göstərdi ki, bəzi təşkilatlar hazırlanmaqda olan dərmanların təhlükəsizliyinə dair illik hesabatların təqdim edilməsi üçün normativ tələblərə əməl etmir. Bu, yalnız qısamüddətli klinik tədqiqatlara aiddir, məsələn, bioekvivalentliyin qiymətləndirilməsi zamanı. Dərman hazırlayanlar tərəfindən tələb olunan hesabatların hazırlanması və təqdim edilməsi ilə bağlı başqa problem aşkar edilməmişdir.
Hesabat üçün məlumat mənbələrinin təhlili göstərdi ki, HPBS-də fayda-risk nisbətinin qiymətləndirilməsi üçün mühüm məlumat mənbəyi ixtisaslaşdırılmış mediada dərc olunan məqalələrdir. yan təsir Dərman vasitələrinin təhlükəsizliyi ilə bağlı xarici və beynəlxalq tənzimləyici və elmi təşkilatların dərman vasitələri və inzibati qərarları. Bu məlumatların keyfiyyətini qiymətləndirmək üçün dərman təhlükəsizliyi məsələlərində ixtisaslaşmış 4 tibbi jurnalın müəllifləri arasında sorğu keçirilib.
Sorğunun nəticələri tibbi jurnalların müəllifləri tərəfindən farmakovigilans sisteminin yüksək keyfiyyətli işləməsi üçün kifayət qədər tələb olunan minimum məlumat miqdarının yüksək səviyyədə başa düşüldüyünü göstərdi.
DRU üçün digər vacib məlumat mənbəyi kortəbii mesajlar sistemidir. Bu mesajlar Roszdravnadzorun Farmakonadzor məlumat bazasına müxtəlif kateqoriyalı respondentlər (klinik farmakoloqlar, əczaçılıq şirkətlərinin nümayəndələri, Roszdravnadzorun regional bölmələrinin nümayəndələri və s.) tərəfindən göndərilir. Ənənəvi olaraq, kortəbii hesabatlarda ən yüksək keyfiyyətli məlumat ixtisaslaşmış mütəxəssislərdən - Dərman Təhlükəsizliyinin Monitorinqi Regional Mərkəzlərinin (RMSC) klinik farmakoloqları və əczaçılarından gəlir.
2018-ci il iyulun 19-dan sentyabrın 21-dək RCMBLS əməkdaşları arasında aparılan sorğunun nəticələri göstərdi ki, Roszdravnadzor saytında2 siyahıya alınmış 61 RCMBLS-dən 25-nin e-poçt ünvanları dəyişdirilib, bir çox mərkəz artıq mövcud deyil, 3 mərkəz onlara 3 gün ərzində müraciətlərə cavab verib. və ya daha çox ay. RCMBLS-dən gələn spontan mesajların payı cüzidir. Rusiyada RCMBLS sisteminin hazırda faktiki olaraq məhv edildiyi qənaətinə gələ bilərik. Eyni zamanda, Rusiyanın müəyyən bölgələrindəki mərkəzlərin fəal işi çox yüksək keyfiyyət səviyyəsində həyata keçirilməyə davam edir ki, bu da dərman təhlükəsizliyi siqnalları ilə işləyərkən onlara etibar etməyə imkan verir.
Düzəliş tədbirlərinin qiymətləndirilməsi Roszdravnadzor-un farmakovigilans hesabat sistemini təkmilləşdirməyə yüksək dərəcədə hazır olduğunu göstərdi. Təşkilatın internet saytında təqdimat şəklində iki mühazirə yerləşdirilib, burada ekspert təşkilatının əməkdaşları risklərin qiymətləndirilməsi və HPBS-lərin hazırlanması ilə bağlı tövsiyələr veriblər.
İlk dəfə 2018-ci il oktyabrın 11-də Roszdravnadzor tərəfindən Beynəlxalq Əczaçılıq İstehsalçıları Assosiasiyasının dəstəyi və mütəxəssislərin iştirakı ilə keçirilən və aparıcı dünya səviyyəli mütəxəssislərin iştirakı ilə farmakoviqilasiya üzrə beynəlxalq konfransın Rusiya farmakovizatorluğu üçün əhəmiyyəti xüsusi qeyd olunur. Rusiya Səhiyyə Nazirliyinin "NTsESMP" Federal Dövlət Büdcə Təşkilatından və Rusiya və EAEU ölkələrinin digər ekspert təşkilatlarından. Konfransda 200-dən çox sənaye nümayəndəsi, ilk növbədə, farmakovigilans üzrə səlahiyyətli şəxslər iştirak ediblər.
2 http://www.roszdravnadzor.ru/drugs/monitpringlp/documents/42074
Dərman təhlükəsizliyi üzrə ekspress hesabatların və dövri hesabatların hazırlanması üçün normativ tələblərin qiymətləndirilməsi 2018-ci ildə heç bir dəyişikliyin olmadığını və əvvəllər hazırlanmış tövsiyələrin davamlı aktuallığını göstərir.
Dövri hesabatlar hazırlayarkən aşağıdakı tövsiyələrə əməl edilməlidir.
1. Hesabatın hazırlanması üçün son müddətlərin vaxtında qiymətləndirilməsinin zəruriliyi. Hesabat dövrünün bitməsinə bir neçə gün qalmış hazırlığa başlamaq tövsiyə olunur. Əvvəllər olduğu kimi, hazırlıq müddəti ifaçının fərdi ixtisasları (o cümlədən onun cari normativ tələbləri başa düşməsi, bütün lazımi məlumatları əldə etmək bacarığı və bu məlumatla işləmək üçün müvafiq metodları düzgün tətbiq etmək bacarığı), iş yükü ilə müəyyən edilir. , emal olunan materialın həcmi və xarakteri.
2. Dizaynın, bölmələrin adlarının, onların təqdim edilməsi qaydasının və məzmununun müvafiq cari normativ tələblərə (dəyişə bilər) uyğunluğunu yoxlamaq ehtiyacı.
3. Hesabat dövründə dərman vasitələrinin təhlükəsizliyinə dair məlumatların əvvəllər mövcud olan məlumatlara uyğunluğunun müəyyən edilməsi və tələb olunarsa, yeni məlumatlar əsasında qeydiyyat sənədlərinə dəyişikliklərin edilməsi barədə qərar qəbul edilməsi zərurəti.
4. Müəyyən edilmiş hesabat formasının bütün bölmələrinin rus dilində mövcud terminologiya kodifikatorundan və nəticədə fayda-risk nisbətini müəyyən etmək üçün müəyyən bir dərman üçün qeydə alınmış bütün əlamətlər üçün risk dərəcəsini qiymətləndirmək üçün universal təhlil metodlarından istifadə etməklə doldurulması ehtiyacı. .
NƏTİCƏ
Tədqiqatın nəticələri Rusiyanın təcili hesabat və dərman təhlükəsizliyinə dair dövri hesabat sisteminin hazırkı vəziyyətini qənaətbəxş kimi qiymətləndirməyə imkan verir. Əczaçılıq nəzarəti üzrə dövri hesabat formalarının hazırlanması üçün təklif olunan tövsiyələr Rusiya Federasiyası və EAEU qanunvericiliyinin mövcud tələblərinə cavab verir.
Təşəkkürlər İş Rusiya Səhiyyə Nazirliyinin “NTsESMP” Federal Dövlət Büdcə Müəssisəsində 15 oktyabr 2018-ci il tarixli 064.44.2018 nömrəli “Tibbi jurnalların müəlliflərinin sorğulanması” qrantı çərçivəsində həyata keçirilib. Dərman təhlükəsizliyinə dair dövri hesabatların hazırlanması üçün tövsiyələrin hazırlanması”.
Təşəkkürlər. Bu nəşrdə təqdim olunan məlumatlar Dərman Vasitələrinin Ekspertiza Qiymətləndirilməsi Elmi Mərkəzi tərəfindən dəstəklənib və dövlət tərəfindən maliyyələşdirilən tədqiqat layihəsinin (dövlət uçotu № 064.44.2018) bir hissəsi kimi həyata keçirilib.
Maraqların toqquşması. Müəlliflər bu məqalədə açıqlanmasını tələb edən maraqların toqquşması olmadığını bəyan etmirlər.
ƏDƏBİYYAT / ƏDƏBİYYAT
1. Snegireva II, Zatolochina KE, Ozeretskovsky NA, Romanov BK, Mironov AN. Rusiyada peyvəndlərin farmakovigilasiyası: hüquqi tənzimləmə, müasir mərhələdə inkişaf xüsusiyyətləri. Tibbi Məhsulların Ekspertizası Elmi Mərkəzinin Qəzeti. 2014;(4):27-31.
2. Makoveev AN, Berezina VS. Rusiya farmakovigilansı - 2016. Dərman vasitələrinin inkişafı və qeydiyyatı. 2015;(2):230-6.
3. Romanov BK, Alyautdin RN, Darmostukova MA, Glagolev SV, Polivanov VA. Dərman vasitəsinin təhlükəsizliyinə dair dövri hesabatın standart forması. Farmakoterapiyanın təhlükəsizliyi və riskləri. 2017;5(4):148-60.
4. Gildeeva GN, Yurkov VI. Rusiyada farmakovigilans: problemlər, perspektivlər və mövcud vəziyyət. J Farmakovigil. 2016;(4):206. https:// doi.org/10.4172/2329-6887.1000206
5. Kuznetsov EA, Tikhonov SA, Berezina VS. Əczaçılıq nəzarət sisteminin təşkili əczaçılıq şirkəti. Dərman vasitələrinin hazırlanması və qeydiyyatı. 2015;(4):172-80.
6. Gildeeva GN, Glagolev SV, Yurkov VI. Rusiya Federasiyasında dərman təhlükəsizliyinə nəzarət problemləri: farmakovigilans mütəxəssislərinin rolu. Roszdravnadzor bülleteni. 2016;(5):114-8.
Olefir Yuri Vitaliyeviç, dr med. Elmlər, Rusiya Səhiyyə Nazirliyinin "NTsESMP" Federal Dövlət Büdcə Təşkilatının baş direktoru. ORCID: http://orcid.org/0000-0001-7652-4642
Romanov Boris Konstantinoviç, tibb elmləri doktoru. Elmlər, Rusiya Səhiyyə Nazirliyinin "NTsESMP" Federal Dövlət Büdcə Təşkilatının elmi işlər üzrə baş direktorunun müavini. ORCID: http://orcid.org/0000-0001-5429-9528 Alyautdin Renad Nikolaevich, Dr. med. elmlər, prof., Rusiya Səhiyyə Nazirliyinin Federal Dövlət Büdcə Müəssisəsinin "NTsESMP" Dərman Təhlükəsizliyi Ekspertiza İdarəsinin rəhbəri. ORCID: http://orcid.org/0000-0002-4647-977X
Lepaxin Vladimir Konstantinoviç, Dr. Elmlər, prof., müxbir üzv. RAS, Rusiya Səhiyyə Nazirliyinin "NTsESMP" Federal Dövlət Büdcə Təşkilatının Dərmanların Təhlükəsizliyi Ekspertiza İdarəsinin baş elmi işçisi. ORCID: http://orcid.org/0000-0002-3706-7271
Krasheninnikov Anatoli Evgenievich, t.ü.f.d. əczaçılıq. Elmlər, “Milli Əczaçılıq Nəzarəti Mərkəzi” ANO-nun baş direktoru. ORCID: http://orcid.org/0000-0002-7791-6071 Şubnikova Elena Vladimirovna, t.ü.f.d. bal. Elmlər, Rusiya Səhiyyə Nazirliyinin "NTsESMP" Federal Dövlət Büdcə Qurumunun Dərman Təhlükəsizliyi Ekspertizası İdarəsinin Ekspert Təhlili Metodologiyası şöbəsinin baş analitiki. ORCID: http://orcid.org/0000-0002-2888-5993
Məqalə qəbul edilib 11.09.2018 Baxışdan sonra 26.11.2018 Dərc üçün qəbul edilib 26.11.2018
7. Murashko MA, Parhomenko DV, Asetskaya IL, Kosenko VV, Polivanov VA, Glagolev SV. Farmakovigilansın rolu və təcrübəsi Rusiya səhiyyəsi. Roszdravnadzor bülleteni. 2014;(3):54-61.
Yuri V. Olefir, MD, Dr. Sci. (med.), Dərman Məhsullarının Ekspertiza Qiymətləndirilməsi Elmi Mərkəzinin baş direktoru. ORCID: http://orcid.org/0000-0002-4647-977X
Boris K. Romanov, MD, Dr. Sci. (med.), Dərman Vasitələrinin Ekspertiza Qiymətləndirilməsi Elmi Mərkəzinin baş direktorunun elmi tədqiqatlar üzrə müavini. ORCID: http://orcid.org/0000-0001-5429-9528 Renad N. Alyautdin, MD, Dr. Sci. (Med.), Professor, Dərman vasitələrinin qiymətləndirilməsi şöbəsinin müdiri, Dərman vasitələrinin Ekspert Qiymətləndirilməsi Elmi Mərkəzinin Təhlükəsizliyi. ORCID: http://orcid.org/0000-0002-4647-977X
Vladimir K. Lepakhin, MD, Dr. Sci. (Med.), Professor, Rusiya Elmlər Akademiyasının müxbir üzvü, Dərman vasitələrinin qiymətləndirilməsi şöbəsinin baş elmi işçisi" Dərman Məhsullarının Ekspert Qiymətləndirilməsi Elmi Mərkəzinin Təhlükəsizliyi. ORCID: http://orcid.org /0000-0002-3706-7271 Anatoli E. Krasheninnikov, elmlər namizədi (Pharm.), Milli Farmakovigilans Tədqiqat Mərkəzinin ORCID: http://orcid.org/0000-0002-7791-6071
Elena V. Şubnikova, namizəd. Sci. (Med.), Dərman Vasitələrinin Qiymətləndirilməsi Şöbəsinin Ekspert Təhlili Metodologiyası Departamentinin Baş Analitiki” Dərman Vasitələrinin Ekspertiza Qiymətləndirilməsi Elmi Mərkəzinin Təhlükəsizliyi. ORCID: http://or-cid.org/0000-0002 -2888-5993
Əgər farmakovigilans xidmətinə mesaj göndərmək lazımdır tibbi istifadə GEROPHARM dərmanı ilə bağlı bir hadisə baş verdi:
- Dərmanın istifadəsi ilə əlaqəli ola biləcək mənfi reaksiyalar
- Dərman effektivliyinin olmaması
- Dərmanların qarşılıqlı təsiri dərmanın tibbi istifadəsi üçün təlimatlarda təsvir edilmir
- Saxta məhsulların aşkarlanması
- Dərmanın tibbi istifadəsində səhvlər
- Dərmanı istifadə edərkən həddindən artıq dozada
- Narkomaniya
- Dərmanın yanlış istifadəsi
- Tibbi cihazdan istifadə edərkən arzuolunmaz reaksiyanın inkişafı
Mesaj olsa belə göndərilməlidir
- Mənfi reaksiyanın bu xüsusi dərmanla əlaqəli olub olmadığına əmin deyilsiniz
- Bütün məlumatınız yoxdur
2. Mesajı necə göndərmək olar?
- Bu formanın bölmələrini sizdə olan məlumatlara uyğun olaraq mümkün qədər ətraflı doldurun.
- Mənfi reaksiyaların bir neçə halı haqqında məlumatınız varsa, onların hər biri üçün yeni formadan istifadə edin
- GEROPHARM farmakovigilans xidmətinə e-poçt, faks və ya poçt vasitəsilə mesaj göndərin.
- Doldurulmuş formanı GEROPHARM tibbi nümayəndəsi vasitəsilə də təqdim edə bilərsiniz
3. Mesajı nə vaxt göndərməliyəm?
- Məlumat sizə məlum olduqdan sonra mesaj mümkün qədər tez göndərilməlidir.
4. Doldurulmuş formanı hara və necə göndərmək olar?
5. Şəxsi məlumatların mühafizəsi
Xəstə məlumatları ciddi şəkildə məxfi saxlanılır. Bu formanın doldurulması fərdi məlumatların subyektinin GEROPHARM farmakovigilans xidməti tərəfindən emalına razılığı deməkdir. Hesabat verən şəxs haqqında məlumat ictimaiyyətə açıqlanmayacaq. Mesaj göndərilərkən başqa hal nəzərdə tutulmayıbsa, onlar Səhiyyədə Nəzarət üzrə Federal Xidmətə təqdim edilə bilər.
GEROPHARM farmakovigilans xidmətinin nümayəndəsi mesajda göstərilən məlumatları dəqiqləşdirmək üçün mesajı göndərən şəxslə əlaqə saxlaya bilər.
Hər hansı bir sualınız olarsa, GEROPHARM Qaynar Xəttinə zəng edin