IUPAC adı: 1 -(3R, 4S, 5R)-3,4-dihidroksi-5-(hidroksimetil)oksolan-2-il)pirimidin-2,4-dion
Digər adlar: uridin
Molekulyar Formula: C 9 H 12 N 2 O 6
Molar kütləsi: 244,20 q mol-1
Görünüş: Möhkəm
Sıxlıq: 0,99308 q/sm3
Ərimə nöqtəsi: 167,2 °C (333,0 °F)
Uridin, bir nukleozid, β-N1-qlikozid bağı vasitəsilə bir riboza halqasına (ribofuranoza kimi tanınır) bağlanmış urasil ehtiva edir. Dezoksiriboza halqasına birləşən urasil deoksiuridin əmələ gətirir. Uridin, pivədə çox miqdarda tapılan bir nukleotiddir və hüceyrə membranının sintezini artırmaq üçün, eləcə də digər nevroloji məqsədlər üçün istifadə olunur. Balıq yağı ilə gücləndirilmiş təsirləri ilə potensial koqnitiv gücləndirici xüsusiyyətlərə malikdir. Bilmək lazımdır Həmçinin tanınır: uridin difosfat (UDP), uridin monofosfat (UMP) Çeşid:
Pseudovitamin
Neotropik vasitə
Yaxşı birləşir:
Balıq yağı (xüsusilə dokosaheksaenoik turşu ilə, bilişsel performansa aid olduğu üçün)
Uridine: istifadə üçün təlimat
Uridinin dozası 500-1000 mq arasında dəyişir, nadir insan tədqiqatları bu diapazonun yuxarı ucunu istifadə edir. Uridini qida ilə qəbul edərkən ehtiyatlı olmaq tövsiyə olunur, lakin tələb olunmur.
Mənbələr və quruluş
Mənbələr
Uridin ribonuklein turşusunun (RNT) dörd əsas komponentindən biridir; digər üçü adenozin, guanin və sitidindir. Aşağıda RNT şəklində uridini olan qidalar verilmişdir. Bununla belə, bu formada uridin bioavailable deyil. Qaraciyərdə məhv edilir və mədə-bağırsaq traktının, və qida istehlakı qanda uridinin səviyyəsini artırmır. Ana südü və ya kommersiya uşaq formulası istehlak edən körpələrdə uridin monofosfat şəklində mövcuddur və bu uridinin mənbəyi həqiqətən bioavaildir və qan dövranına daxil olur. RNT ilə zəngin qidaların istehlakı qanda purinlərin (adenozin və quanozin) səviyyəsinin artmasına səbəb ola bilər. Purinlərin yüksək səviyyəsi sidik turşusu səviyyəsinin artmasına səbəb olur və pisləşə və ya gut kimi xəstəliklərin inkişafına səbəb ola bilər. Orta dərəcədə maya istehlakı, gündə təxminən 5 qram, minimum yan təsirlərlə yaxşılaşdırılmış sağlamlıq üçün adekvat uridin səviyyəsini təmin edəcəkdir.
Qeyd: Maya məhsullarının zülal mənbəyi kimi böyük miqdarda (gündə 50 q və ya daha çox) istehlak edildiyi təqdirdə tərkibindəki RNT-nin kimyəvi cəhətdən azaldılması təklif edilmişdir. Ancaq bu cür emal bahalıdır və nadir hallarda istifadə olunur.
Harvard tədqiqatçıları bildirirlər ki, uridin və EPA/DHA omeqa-3 yağ turşusu əlavələri siçovullarda antidepresan rolunu oynayır.
Saf formada uridin aşağıdakı qidalarda aşkar edilmişdir:
Əslində, pivə uridinin ən böyük mənbəyidir, öz növbəsində, əhəmiyyətli DNT və RNT tərkibi (ehtimal ki, uridinin tərkibini göstərir) (başqa cür qeyd edilmədiyi təqdirdə, quru çəkiyə nisbətən):
Qaraciyər (donuz və mal əti): mal ətində 2,12-2,3%, donuz ətində (RNT) 3,1-3,5%; mal ətində 1,7-2%, donuz ətində (DNT) 1,4-1,8%; hamısı quru çəki ilə bağlıdır
Pankreas, ən böyük RNT mənbəyi: 6,4-7,8% (donuz əti) və 7,4-10,2% (mal əti)
Limfa düyünləri, DNT-nin ən böyük mənbəyi: 6,7-7,0% (donuz əti) və 6,7-11,5% (mal əti)
Balıq: 0,17-0,47% (RNT) və 0,03-0,1% (DNT), siyənəkdə ən yüksək RNT tərkibi 1,53% təşkil edir.
Çörək mayası (6,62% RNT, 0,6% DNT)
göbələk; boletus 1,9-2,4% RNT, şampinonlar 2,05% RNT, şabalıd 2,1% RNT, hamısı az miqdarda (0,06-0,1%) DNT ehtiva edir.
Brokoli 2,06% RNT və 0,51% DNT
Yulaf 0,3% RNT, aşkar edilməyən DNT
Çin kələmində, ispanaqda və gül kələmində eyni miqdarda 1,5% RNT və 0,2-0,3% DNT var.
Cəfəri 0,81% RNT və 0,27% DNT
Orqan ətləri və təəccüblü şəkildə, xaç ağacı tərəvəzləri, ümumiyyətlə, RNT və DNT-də yüksəkdir, bu, 10 ml / kq-da pivə qəbulunun qanda uridinin səviyyəsini 1,8 dəfə artıra bilər ki, bu da uridinin oxşar dozası ilə eynidir (0,05 mq/kq); spirt tərkibi udulmaya təsir etmir və sidikdə uridinin səviyyəsi bərabər şəkildə artır. Uridin pivə içdikdən sonra sidik turşusu səviyyəsinin artmasına səbəb olmur və sidik turşusu sintezinin allopurinol tərəfindən inhibə edilməsi pivənin təsiri altında əldə edilən zərdabda uridinin səviyyəsinə təsir göstərmir.
Quruluş və xassələri
Bu formada ifşa olan uridine aşkar edilmişdir sulu məhlul ultrabənövşəyi radiasiya, dərhal parçalanır və fotohidratlara çevrilir. Ultrabənövşəyi radiasiyaya məruz qaldıqda sulu məhlulda qeyri-sabitdir
Qida qarşılıqlılığı
Dövrlərdə qidalanma(yalnız 1600-400 kkal şəkər; şirə pəhrizinə bərabərdir), plazma uridini aclıqdan sonra üç gün ərzində 36%-ə qədər azala bilər və bir gündən sonra 13% (əhəmiyyətli deyil) azalır. Bu nəticələr əvvəlki tədqiqatı təkrarlayır, oxşar nəticələr oruc zamanı dovşanlarda müşahidə edilir.
NucleoMaxX (Mitoknol)
Mitoknol, 36 qramlıq paketin 6 qramı nukleozidlər olmaqla, yüksək nukleozid tərkibinə (17%) malik, qamış şəkərindən əldə edilən xüsusi uridinin qarışığıdır. Bu kisələrdə 0,58 q uridin (1,61%) və 5,4 q (15%) 2′,3′,5′-tri-O-asetiluridin (TAU) var, strukturuna görə uridinə oxşardır; Hər iki molekulun çəkisi nəzərə alınarsa, hər bir paketdə təxminən 1,7 x 10-2 mol uridin var. Yalnız uridin və TAU mənbəyidir, sonuncusu uridinin daha yaxşı sorulduğu formasıdır (depo forması)
Uridin glikolitik yolda
Uridin qalaktozanın qlikolitik yolunda mühüm rol oynayır. Qalaktozanın metabolizması üçün katabolik proses yoxdur. Beləliklə, qalaktoza qlükoza çevrilir və ümumi qlükoza yolunda metabolizə olunur. Daxil olan qalaktoza qalaktoza-1-fosfata (Gal-1-P) çevrildikdən sonra, UDP (uridin di-fosfat) molekuluna birləşmiş qlükoza molekulu olan UDP-qlükoza ilə reaksiya verir. Bu proses qalaktoza-1-fosfat uridil transferaz fermenti tərəfindən kataliz edilir və UDP-ni qalaktoza molekuluna köçürür. Son nəticə UDP-qalaktoza molekulu və qlükoza-1-fosfat molekuludur. Bu proses qalaktoza molekulunun qlikolizinə davam edir.
Farmakologiya
Bioavailability və absorbsiya
Uridin ya asanlaşdırılmış diffuziya, ya da xüsusi uridin daşıyıcıları vasitəsilə bağırsaqdan sorulur. Məhdud absorbsiyaya görə, icazə verilən maksimum doza (göstəriləndən yüksək doza ishala səbəb olur) 12-15 q/m2 (orta boylu kişi üçün 20-25 q), serum səviyyəsini kəskin şəkildə 60-80 mikromol və ya 5 q/m2 (orta boylu kişi üçün 8,5 q), gündə üç dəfə hər 6 saatdan bir qəbul edilir, bu da serum konsentrasiyasını 50 mikromol səviyyəsində saxlayır; 5,8-9,9% bioloji həzm qabiliyyətini təmin edir. Uridinin udulmasının praktiki məhdudiyyətləri var, çünki yüksək dozalar ishala səbəb ola bilər, lakin bu məhdudiyyətlər standart dozadan xeyli yüksəkdir. 200 ml portağal suyu ilə götürülmüş NucleoMaxX markasının (36 q) bir "paket"inin tədqiqi müəyyən etdi ki, serum uridinin səviyyələri 80 dəqiqədən (Tmax) sonra 5,4-5,8µM-dən 152+/-29,2µM-ə (Cmax) qədər artıb. yüksək fərdlərarası dəyişkənlik ilə Cmax 116-dan 212 mikromol. Bu araşdırma həmçinin 8 və 24 saatda serum konsentrasiyaları müvafiq olaraq 19,3+/-4,7µM və 7,5+/-1,6µM-ə düşməklə ilkin yarımxaricolma dövrü 2 saat və terminal yarımxaricolma dövrü 11,4 saat aşkar edilmişdir. Bu tədqiqat daha sonra 80 dəqiqədə (Tmax) oxşar yüksək Cmax dəyərləri (150,9 mikromol) verən əlaqəli farmakokinetik tədqiqatda təkrarlandı, lakin müşahidə olunan yarımxaricolma dövrü 3,4 saat və sidikdə orta konsentrasiya∞ 620,8+/- təşkil etdi. 140,5 mikromol; hər iki tədqiqatda qadınlarda uridinin yüksək konsentrasiyası qeyd edildi, bu, parçalanmadan sonra yox olan bədən çəkisindəki fərqlərlə əlaqələndirilir və bərabərləşdirməyə səbəb olur. Mitoknolun sidikinin tərkibinə təsiri yoxlanılmış tək uridinlə müqayisə edildikdə, uridinin səbəb olduğu konsentrasiyanı üstələyən Mitoknolun əldə etdiyi konsentrasiyanın 4 dəfə artması aşkar edilmişdir. Mitoknolun artan bioavailability, sadəcə olaraq, yüksək triasetiluridin (TAU) tərkibinə görə ola bilər, çünki TAU patentində iddia edildiyi kimi, lipofilliyi və passiv diffuziyasına görə ekvimolekulyar miqdarda uridindən 7 dəfə daha çox bioavailliyə malikdir. Bağırsaq və plazma esterazları ilə uridinə parçalanır, lakin uridin fosforilazaya davamlıdır. Mitoknol mədə-bağırsaq traktından istifadə etmədən yüksək serum uridinin konsentrasiyasına nail olmaq lazım olduğu hallarda istifadə edilə bilər. yan təsirlər, yüksək bioloji həzm qabiliyyətinə görə
Daxili tənzimləmə
Serum uridinin səviyyəsi istirahətdə 3-8 mikromol arasında dəyişir. Qırmızı qan hüceyrələri P450 sisteminin bir hissəsi olan uridin difosfat qlükoza fermentini ehtiva edir; zərurət yaranarsa, uridinin tərkibi tükəndikdə bədəndə təmiz uridin və qlükoza təmin etmək üçün bu ferment parçalana bilər.
Neyrologiya (mexanizmlər)
Hərəkat
Uridinin qan-beyin baryerini keçdiyi məlumdur və iki daşıyıcıdan biri tərəfindən qəbul edilir, bir sinfi tarazlıq adlanır (SLC29 ailəsi; məsələn, ENT1, ENT2 və ENT3 daşıyıcıları) aşağı yaxınlıq (100-) 800 mikromolyar diapazon) və natriumdan asılı olmayan, yüksək yaxınlıqlı (1-50 mikromolyar) aktiv daşıyıcı olan natriumdan müstəqil və konsentrasiyalı (SLC28 ailəsi, ENT4-dən, həmçinin CNT1, 2 və 3-dən ibarətdir).
Fosfolipidlər
Uridin Kennedi dövründə fosfatidilkolinin sintezində qida mühiti rolunu oynayır (həmçinin sitidin difosfat xolin yolu kimi tanınır; fosfatidiletanolamin də bu yolla istehsal olunur). Bu üsulda xolin kinaz xolini fosfokolinə kataliz edir, prosesdə bir ATP molekulunu istehlak edir, cüzi bir yaxınlığa malikdir (beləliklə, əksər hüceyrə xolin dərhal fosfokolinə çevrilir) və bu fosfokolinin (parçalanması) istehsalının yeganə mümkün yolu olmasa da. sfinqomielin də fosfokolin istehsal edir), bu, Kennedi dövrü vasitəsilə fosfokolinin sintezində ən qabaqcıl yol və ilk addımdır, fosfokolinin konsentrasiyası kolinin qəbulunun artması ilə birbaşa təsirlənir. Digər zonalarda fosfokolin sitidiltransferaza sitidin trifosfatı sitidin difosfat xoline plus pirofosfata çevirir (xolin mənbəyi kimi əvvəllər yaradılmış fosfokolindən istifadə etməklə). Bu mərhələ Kennedi dövrəsində ən yavaş və sürət məhduddur, lakin onun fəaliyyəti bütün fosfokolin sintezini müəyyən edir. Tipik olaraq, hüceyrə kulturalarında yüksək fosfokolin və aşağı sitidin difosfat xolin olur, bu mərhələdə sürət həddi sitidin trifosfatın mövcudluğu ilə müəyyən edilir. Bu ferment beyin fosfolipidləri tərəfindən də mənfi şəkildə tənzimlənir və bunlar fosfolipid homeostazına vasitəçilik edən və artıq fosfolipid sintezinin qarşısını alan əsas mexanizmlərdir. Nəhayət, xolin fosfotransferaza (oxşar abbreviaturaya malik olan karnitin palmitoiltransferaza ilə qarışdırılmamalıdır) fosfokolini sitidin difosfat xolindən diasigliserola nəql edir. Həmçinin, sitidin difosfat kolin və sitidin difosfat etanolamin (və xüsusilə sonuncu) üçün ikili spesifikliyə malik olan, fosfokolini diasiqliserinə bağışlayan, nəticədə fosfolin-etanolamin fosfotransferaza da iştirak edir fat etanolamin əvəzinə fosfatidiletanolamin yaradır) . Bu ferment uridin ilə inkubasiya ilə stimullaşdırılmır, lakin sinir böyümə faktoru (NGF) tərəfindən stimullaşdırılır. Uridin və sitidin Kennedi dövrü ilə fosfolipidlərə çevrilir, yuxarıdakı dövr CCT fermentindən dərhal sonra məhdudlaşır. Fermentin sitidin üzərində hərəkət etməsini təmin etmək sürəti təyin edir. Uridin, sitidin vasitəsilə dolayı yolla sitidin difosfat kolinin sintez olunduğu qida mühiti kimi istifadə olunur. Sitidinin təmin edilməsi (uridindən sintez olunur) yuxarıda göstərilən prosesdə sürət məhduddur, kifayət qədər xolin konsentrasiyası olan hüceyrələrə və ya beyin dilimlərinə əlavə sitidinin verilməsi sitidin difosfat kolinin sintezini sürətləndirir. Uridin əvvəlcə uridin trifosfata (UTP), sonra isə canlı modeldə təsdiqlənən sitidin trifosfata çevrilərək sitidinə çevrilərək oxşar xüsusiyyət nümayiş etdirdi. Uridin 5 mikromolyar UTP istehsal edərkən, in vitroda sitidin difosfat kolinin maksimal 50 mikromol sintezini stimullaşdırır; Uridindən sitidin difosfat kolinin istehsalı in vivo olaraq uridinin oral tətbiqi ilə təsdiq edilmişdir. Hüceyrə mədəniyyətlərinə uridin və ya sitidinin əlavə edilməsi hüceyrələrdə sitidinin səviyyəsini artıracaq və sürət həddini aşaraq fosfolipidlərin istehsalına gətirib çıxaracaq. Müdaxilə baxımından, bir həftə ərzində gündə bir dəfə 500 mq uridin qəbul edən sağlam kişilərdə aparılan bir araşdırma, fosfatidilkolinin artması ilə, ilk növbədə, ümumi beyin fosfoetanolamin səviyyələrində (7,17%) artım səbəbiylə ümumi beyin fosfomonoester səviyyələrində (6,32%) artım olduğunu bildirdi. uridin qrupunda statistik əhəmiyyətə çatmadı. Fosfoetanolamin səviyyəsinin artması sitidin difosfat xoline görə digər sahələrdə aşkar edilmişdir, lakin sonuncu həmişə fosfoetanolamin artımı ilə müşayiət olunmur. Fosfatidilkolinə gəldikdə, böyümənin uğursuzluğunun fosfolipid membranlarında fosfatidilkolinin sürətli yığılması ilə əlaqəli olduğu fərz edilmişdir; fərziyyə, uridin və ya uridin ön dərmanları ilə fosfatidilkolinin konsentrasiyalarının azaldığını qeyd edən əvvəlki tədqiqatla bağlıdır. Uridinin ağızdan qəbulu sağlam insanlarda beyin fosfolipid prekursorlarının, xüsusən də fosfatidiletanolamin səviyyəsini artırır. Fosfatidilkolinin artımını istisna etmək mümkün olmasa da, insanlarda bu, etibarlı şəkildə aşkar edilməmişdir.
P2 reseptorları
P2 reseptorları hüceyrədənkənar purinlərə və pirimidinlərə (məsələn, ATP) cavab verən və punerjik neyrotransmissiya kimi tanınan reseptorların metasinifləridir. Bu reseptor sinfi strukturuna görə adenozin reseptorlarına bənzəyir (onlar adətən eyni adlanırlar) və P2Y və P2X siniflərinə bölünür (bunlar P2Y reseptorlarının G-zülal birləşməsi, P2X isə liqand olması ilə fərqlənir) -qapılı ion kanalları). Uridin P2 reseptorlarının, xüsusən də P2Y yarımsinifinin agonistidir, bunlar səkkiz tanınmış insan P2Y reseptorunu (1,2,4,6 və 11-14) və məməli olmayan reseptorların qalan hissəsini təşkil edir, fosforlanmış uridinə yaxınlıq var. ilk növbədə P2Y2 reseptorları üçün və daha az dərəcədə P2Y4, P2Y6 və P2Y14 ilə. Sinir sistemi həmçinin sidiklə əlaqəsi olmayan yeddi P2X reseptoru ilə təmsil olunur. Uridinin təsir edə biləcəyi öz reseptorları var, yəni P2 reseptorları, burada P2Y2, P2Y4, P2Y6 və P2Y14-ə daha çox təsir göstərir. Fosfolipid sintezi üçün xammal kimi istifadə edilmədikdə, uridin punerjik reseptorlar vasitəsilə yeni bir nörotransmitter kimi çıxış edir, P2Y2 reseptorları inteqrinlərlə qarşılıqlı əlaqəni və nəzarət reseptorlarının böyüməsini təşviq edən struktur elementlərə malikdir və bu reseptorların aktivləşməsi sinir artımı faktorunun aktivləşməsinə səbəb olur. /tropomyozin reseptor kinaz A və əsasən neyroprotektivdir.
Sinaps
Uridin dendrit membranlarının tərkib hissəsi olan beyin fosfatidilkolinin səviyyəsini artıraraq sinaptik funksiyaya faydalı təsir göstərir. Alzheimer xəstəliyində olduğu kimi, sinaptik funksiyanın azalmasından və ya tənzimlənməsindən əziyyət çəkən insanlara faydası olduğu güman edilir, burada sinaptik funksiyanın azalması neyron sinapslara və dendritik tikələrə toksik təsir göstərən ümumi beta-amiloid birləşmələrinin nəticəsidir. Fosfatidilkolini təmin etməklə uridin, ehtimal ki, sinaptik funksiyaya kömək edə bilən membranların və dendritlərin meydana gəlməsini təşviq edir. Uridinin təsiri altında sinaptik konstruksiyanı araşdıran tədqiqatlar, sinaptik funksiyanın kəmiyyətini müəyyən etməkdə çətinlik çəkdiyinə görə dendritik tikələrə baxmağa meylli olmuşdur və dendritlərin 90%-nin sinaps meydana gətirdiyinə görə dendritik tikanlar ən etibarlı biomarkerdir. Heyvanlara uridin, xolin və omeqa-3 yağ turşularının ( balıq yağı) sinaptik formalaşma və funksiyanın artmasına gətirib çıxardı və bir qrup insanda (n=221) inkişaflar nümayiş etdirdi. yüngül xəstəlik Alzheimer.
Akson böyüməsi
Purinlər və pirimidinlər neyronlarda hüceyrə diferensiasiyasını artırır, uridin öz reseptoru P2Y2-yə təsiri ilə onun reseptor tropomiyozin reseptor kinaz A (neyron böyüməsini artırmaq üçün geniş şəkildə məlumdur) vasitəsilə sinir böyümə faktoru siqnalını aktivləşdirərək neyronların differensiasiyasının artmasına və cücərməsinə səbəb olur. P2Y2 reseptorunun çıxarılması tropomiyozin reseptor kinaz A vasitəsilə müvafiq sinir artım faktoru siqnalının qarşısını alır, iki reseptor koimmunopresipitasiyada olduğu kimi bir-birinə təsir edir. Bu mənada P2Y2 agonistləri, P2Y2 agonisti uridin (trifosfat) ilə aşkar edildiyi kimi, amilə neyronların həssaslığına görə neyron proliferasiyasını artıraraq sinir böyümə faktorunun siqnalını artırır. P2Y2 reseptorunun aktivləşdirilməsi öz reseptoru (tropomiyozin reseptor kinaz A) vasitəsilə sinir böyümə faktorunun təsirini təşviq edir və nəticədə P2Y2 reseptor agonistlərinin amillə bağlı neyron artımını artırmasına gətirib çıxarır. 6 həftə, lakin 1 həftə deyil, qocalmış siçovullara 330 mq/kq (1 mmol/kq) uridinin verilməsi neyrofilament -70 (+82%) və neyrofilament-M (+121%) səviyyəsini artırdı, aksonal böyümədə iştirak edən iki sitoskeletal zülal və əvvəllər aksonal artım aşkar edildikdə uridin tərəfindən diferensiallaşdırılmış PC12 neyron hüceyrələrində sinir artım faktoru ilə in vitro induksiya edilmiş biomarkerlər kimi istifadə edilmişdir. Qeyd etmək lazımdır ki, in vitro tədqiqat uridinin aksonal böyüməni artırmaq üçün P2Y reseptoru vasitəsilə hərəkət edə biləcəyini göstərdi.
Katexolamin
Yaşlı siçovulların 2,5% disodium uridin (500 mq/kq və ya 330 mq/kq uridin, insan ekvivalenti təxminən 50 mq/kq) ilə əlavə edilmiş qocalmış siçovulların pəhrizi siçovulların neyron dilimlərində istirahət dopamin səviyyələrinə təsir etməmişdir, lakin K+-nı artırmışdır. 1 və 6 həftəlik administrasiya zamanı DOPAC və ya HVA konsentrasiyasına təsir etmədən fəaliyyət potensialında müvəqqəti azalma fərqi olmadan dopaminin orta səviyyəsini 11,6-20,5% artırdı. Uridin əlavəsi ümumi dopamin səviyyələrinə əhəmiyyətli dərəcədə təsir etmədən aktivləşdirilmiş neyronlardan salınan dopamin səviyyəsini artırır.
İdrak prosesi və idrak
Bir açıq etiketli araşdırma istifadə edərək ticarət adı Cognitex (50 mq uridin 5"-monofosfat, 600 mq alfa-gliserilfosforilxolin, 100 mq fosfaditilserin, 50 mq pregnenolon, 20 mq vinposetin və digərləri ilə güclü şəkildə qarışdırılır), 2 həftəlik qısamüddətli yaddaşı yaxşılaşdırır, tanınma, 10 həftədən çox qəbuldan sonra daha da artan xatırlama, diqqət və təşkilatçılıq qabiliyyətləri.
Alzheimer xəstəliyi
Uridin, Alzheimer xəstəliyində zəifləmiş sinaptik əlaqələri qorumaqla Alzheimer xəstəliyinin müalicəsində kömək edə bilər. Sinaptik proliferasiyanı təşviq edərək, uridin Alzheimer xəstəliyi üçün terapevtik olaraq istifadə edilə bilər. Bir araşdırma sürətlənmiş β-amiloid istehsalı (və beləliklə, Alzheimer xəstəliyinə meylli) olan siçovullarda Alzheimer xəstəliyinin simptomlarında əhəmiyyətli dərəcədə yaxşılaşdığını qeyd etdi, lakin digər qida maddələrinin istifadəsini təmin etmək üçün böyük ölçüdə çaşqınlıq yarandı. uridinin təsiri. Bu günə qədər uridinə dair eksperimental məlumatlar qeyri-müəyyəndir və uridinin effektivliyini qiymətləndirməyə imkan vermir.
Bipolyar pozğunluq
Açıq etiketli bir araşdırmada 6 həftəlik uridindən sonra bipolyar pozğunluq uşaqlarda gündə iki dəfə 500 mq (cəmi 1000 mq) ilkin göstərici ilə müqayisədə depressiya əlamətlərinin yaxşılaşması ilə əlaqəli olduğu qeyd edildi (Uşaqların Depressiya Qiymətləndirmə Şkalası üzrə orta göstərici 65,6-dan bir həftə ərzində effektivliklə 27,2-yə qədər); manik simptomlar qiymətləndirilməmişdir. Triasetiluridin (TAU) yetkinlərdə bipolyar pozğunluğun öyrənilməsində istifadə edilmişdir, 6 həftə ərzində gündə 18 q və depressiv simptomlarda əhəmiyyətli yaxşılaşma qeyd edilmişdir.
Ürək-damar sisteminin vəziyyəti
Ürək toxuması
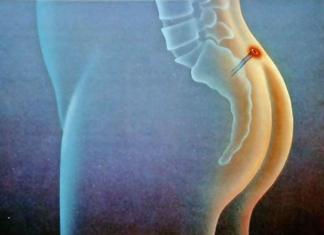
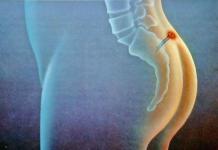
Uridin miyokard işemiyası zamanı dərhal kardioprotektiv təsir göstərməyə qadirdir, onun əvvəlcədən yüklənməsi mitoxondrial kalium kanallarının bloklanması ilə aradan qaldırılır (5-hidroksidekanoat vasitəsilə); Bu o deməkdir ki, uridinin əvvəlcədən yüklənməsi enerji metabolitlərinin (ATP, kreatin fosfat və uridin) səviyyəsini qoruyur və lipidlərin peroksidləşməsini daha da azaldır.
Piy kütləsi və piylənmə
Lipodistrofiya
Lipodistrofiya piy kütləsinin lokallaşdırılmış itkisidir və adətən əks transkriptazın nukleozid inhibitorları ilə HİV terapiyası zamanı müşahidə olunur. IN çoxmərkəzli tədqiqat uridin 24 həftədən sonra ətraflarda yağ artımı (lipodistrofiyanın normallaşmasının son əlaməti kimi görünür) ilə əlaqələndirildi, lakin təsir 48 həftədən çox davam etmədi; uridin yaxşı tolere edildi və virusoloji reaksiyaya mənfi təsir göstərmədi. Bu uğursuz nəticələr, NucleoMaxX (dərmanın ticarət adı) kimi uridinin mitoxondrial RNT-yə faydalı təsir göstərdiyi, lakin mitoxondrial DNT-yə mənfi təsir göstərdiyi və ətrafların piyinə heç bir təsiri olmadığı ikiqat kor tədqiqatda təkrarlandı; bütün bunlar sistematik iltihabın artması ilə müşayiət olundu (interleykin-6 və C-reaktiv protein), başqa bir araşdırma oxşar bir iş rejimi ilə yağ kütləsində əhəmiyyətli irəliləyişləri təsdiqləsə də. Standart HİV müalicəsi alan insanlarda lipodistrofiya ilə bağlı qarışıq nəticələr var.
Xərçənglə qarşılıqlı əlaqə
Pankreas xərçəngi
P2Y2 reseptorunun uridin trifosfatla aktivləşdirilməsi selektiv reseptor agonisti tərəfindən təqlid edilən və protein kinaz B-nin protein kinaz C-dən asılı aktivləşməsi ilə vasitəçilik edilən pankreas xərçəngi hüceyrə xətti PANC-1-in proliferasiyasını artırır.
Estetik tibb
Saç
Saç böyüməsinin erkən anagen mərhələsində, digər nukleotidlərə (məsələn, timidin və sitidin kimi) uzanan in vitro istirahət mərhələsi (telogen) ilə müqayisədə dermal papilla hüceyrələrində və saç matrisi hüceyrələrində uridinin yığılmasında artım qeyd edilmişdir; güman edilir ki, bu, saç hüceyrələrinin spontan böyüməsi şəraitində RNT və DNT sintezinin artan sürətini göstərir. Bu günə qədər uridinin yığılmasının bu vəziyyətdə sürətin məhdudlaşdırılmasına səbəb olub-olmaması ilə bağlı heç bir araşdırma yoxdur və ya ekzogen uridinin DNT sintezi üçün yetişdirici zəmin rolunu oynaması qəti deyil. Uridin böyümə fazasında (anagen) saç hüceyrələrində toplanır, lakin yuxarıda qeyd edildiyi kimi uridinin DNT/RNT sintezi üçün qida mühiti kimi istifadə edilib-edilməməsi və ya uridinin qəbulunun məqsədəuyğun olub-olmaması müəyyən edilməmişdir P2Y1 və P2Y2 reseptorları (ikincisi uridinin hədəfidir) anagen zamanı saç hüceyrələrində görünür, P2Y2 reseptorları saçın xarici intequmentinin/nüvəsinin kənarında canlı hüceyrələrdə və epiteldə P2Y1 reseptorları ifadə edilir. kök qabığı və ampul; P2X5 reseptorları epitelial kök qabığının və dibinin içərisində və xaricində tapıldı, P2X7 reseptorları isə aşkar edilmədi. üzərində P2Y2 reseptorları aşkar edilmişdir erkən mərhələ, və artıq inkişaf etmiş saç papillasında yoxdur və uridinin keratinositlərin yayılmasını stimullaşdıran bu reseptorun agonisti kimi roluna görə, uridinin saç hüceyrələrinin diferensiasiyasını stimullaşdıra biləcəyi fərz edilir. Nəzəri cəhətdən mümkündür, lakin praktikada sübut olunmamışdır ki, uridinin P2Y2 reseptoru vasitəsilə böyümə fazasının (anagen) başlanğıcında saç hüceyrələrini fərqləndirə bilər.
Qida maddələri ilə qarşılıqlı əlaqə
Xolin
Kolin və uridinin neyron funksiyasına təsiri var və şifahi olaraq qəbul edilən xolin siçovulların və insanların beynində fosfokolinin səviyyəsini artıra bilər, serum xolin səviyyələrində 3-6% artım beyin fosfokolinin səviyyəsinin 10-22% artması ilə nəticələnir. Uridinin qəbulu beyində sitidin difosfat xolin səviyyəsini artırır.
Dokosaheksanoik turşu
İstifadə olunmuş ədəbiyyat siyahısı:
Almeida C və başqaları. 1H NMR spektroskopiyası ilə pivənin tərkibi: dəmləmə yerinin təsiri və istehsal tarixi. J Agric Food Chem. (2006)
Thorell L, Sjöberg LB, Hernell O. İnsan südündəki nukleotidlər: yeni doğulmuş körpənin mənbələri və metabolizmi. Pediatrik Res. (1996)
Inokuchi T, et al. Allopurinolun purin əsaslarının və uridinin plazma konsentrasiyasının pivə ilə bağlı artmasına təsiri. Nukleozidlər Nukleotidlər Nuklein turşuları. (2008)
Shetlar MD, Hom K, Venditto VJ. Uridin, 2"-Deoksiuridin və 2"-Deoksisitidinin Neytral pH-da Aminlərlə Fotohidrat Vasitəçiliyi Reaksiyaları. Photochem Photobiol. (2013)
Eells JT, Spector R, Huntoon S. Yetkin dovşan serebrospinal maye və plazmada nukleozid və oksipurin homeostazı. J Neyrochem. (1984)
Kəskin miokard işemiyası və koronar axının işemikdən sonrakı bərpası ürəyin elektrik sabitliyinin pozulması ilə müşayiət olunur ki, bu da erkən işemik və ya reperfuzion aritmiyaların (ekstrasistoliya, mədəcik taxikardiyası və ya ventrilyasiya) inkişafında ifadə edilir. Bu cür ritm pozğunluqlarının əsas səbəblərindən biri işemik və ya reperfuziya edilmiş miokardda K+, Na+ və Ca 2+ ionlarının balanssızlığıdır. Bu ionların hüceyrədaxili və hüceyrədənkənar konsentrasiyalarının dəyişməsi böyük ölçüdə sarkolemma (Na+, K+ nasos, Ca 2+ nasosu, ATP-dən asılı K+ kanalları) vasitəsilə ion daşıma sistemlərinin disfunksiyası ilə əlaqədardır. əməliyyatı qlikoliz prosesi zamanı əmələ gələn ATP-nin nisbətən kiçik bir hissəsi ilə təmin edilir.
Miokard işemiyası zamanı anaerob qlikolizin qısa müddətli aktivləşməsindən sonra, ilk növbədə, qlükozanın işemik toxumaya daxil ola bilməməsi və ürəkdə qlikogen ehtiyatlarının sürətlə tükənməsi ilə əlaqədar onun yatırılması müşahidə olunur. Artıq işemiyanın 5-10-cu dəqiqəsində miokardda qlikogenin səviyyəsi 50-75% azalır və sonrakı reperfuziya zamanı bərpa olunmur. İşemiya zamanı qlikogen ehtiyatının azalması aritmiya ehtimalını artıran amillərdən biridir.
Glikogen resintezi aktivatorlarının istifadəsi ritm pozğunluqlarının qarşısının alınması üçün müəyyən perspektivlər açır. kəskin ürək böhranı miokard, trombolitik dərmanların qəbulu, ekstrakorporal dövriyyə, koronar angioplastika və s. Belə aktivatorlar uridin nukleozidləri və onun fosfor efirləri ola bilər - uridin-5"-monofosfat (UMP), uridin-5"-difosfat (UDP), uridin-5"-trifosfat (UTP). Ekzogen uridin kardiomiositlərə aktiv şəkildə nəql olunur, ardıcıl olaraq UMP, UDP, UTP və qlikogen sintezi üçün birbaşa substrat olan uridin-5"-difosfoqlükozaya çevrilir. Uridinin uridin birləşmələrinin hüceyrədaxili hovuzuna daxil olma dərəcəsi koronar cərəyanın azalması ilə əhəmiyyətli dərəcədə artır. Ekzogen nukleotidlər də ya uridinə fosforilasiya edildikdən sonra, ya da birbaşa, məsələn, Mg 2+ ionlarının iştirakı ilə ürək əzələsinə daxil edilə bilər.
Tədqiqatın məqsədi uridinin, onun mono-, di- və trifosfatının sol mədəciyin miokardının regional işemiyası və sonrakı reperfuziyası zamanı, həmçinin total işemiyadan sonra ürəyin reperfuziyası zamanı mədəcik aritmiyalarının şiddətinə təsirini öyrənməkdən ibarət idi.
MATERİAL VƏ METODLAR
İş ağ qeyri-xətti erkək siçovulların (heyvan çəkisi 250-280 q) Langendorff-perfused ürəkləri üzərində aparılmışdır. Siçovullar efir buxarı ilə anesteziya edildi və sonra parçalandı. sinə, ürək çıxarıldı, 4°C-yə qədər soyudulmuş Krebs-Henseleit məhlulu ilə yuyuldu və Krebs-Henseleit məhlulu ilə perfuziya üçün sistemə qoşuldu (mmol/l-də tərkibi: NaCl - 118,0; KCl - 4,7; CaCl 2 - 2,5). KH 2 PO 4 - 1,2 Na-EDTA - 0,5 pH 7,4), 37 ° C-də 5% CO 2 qarışığı və 97 sm təzyiqdə; sütun. Ürək dərəcəsinin 15 dəqiqəlik sabitləşməsi dövründən sonra sol mədəciyin regional işemiyası sol atrial əlavənin aşağı kənarı səviyyəsində sol koronar arteriyanın bağlanması və ya perfusatın tədarükü dayandırılaraq ümumi işemiya ilə simulyasiya edilmişdir. 30 dəqiqəlik işemiyadan sonra hər iki halda koronar axın bərpa olundu və 30 dəqiqə ərzində reperfuziya aparıldı.
Ritm pozğunluqları monitorinq rejimində bipolyar elektroqrafiyadan istifadə etməklə qeydə alınmış, mədəcik ekstrasistollarının (ES) sayı, mədəcik taxikardiyası (VT) və mədəcik fibrilasiyası (VF) dövrlərinin müddəti qiymətləndirilmişdir. Nəzarət qrupundakı heyvanların ürəkləri yalnız eksperimental qruplarda Krebs-Henseleit məhlulu ilə perfuza edildi, perfuzata uridin, UMP, UDP və ya UTP (50 μmol/l; Reanal, Macarıstan) əlavə edildi. Hər qrupda 8 heyvanın ürəklərindən istifadə edilmişdir. Statistik təhlil üçün birtərəfli ANOVA testindən istifadə edilmişdir (Microcal Origin 3.5 proqramı). Nəzarət və eksperimental qruplardakı dəyərlər arasındakı fərq p ehtimal dəyərlərində əhəmiyyətli hesab edildi<0,05.
NƏTİCƏLƏR VƏ MÜZAKİRƏ
Nəzarət. Sol koronar arteriyanın tıxanması işemiyanın 2-3-cü dəqiqəsində baş verən və 20-25-ci dəqiqədə dayanan erkən aritmiyaların (cədvəl) inkişafına gətirib çıxardı. Ligatura çıxarıldıqdan 4-5 dəqiqə sonra yenidən reperfuziya dövrünün sonuna qədər davam edən ritm pozğunluqları qeyd edildi. Ümumi işemiya halında, ürək döyüntüləri yox olana qədər perfusatın tədarükü dayandırıldıqdan sonra ilk 2 dəqiqə ərzində yalnız tək ES qeyd edildi. Koronar axının bərpasından 3-4 dəqiqə sonra reperfuziyanın 25-27-ci dəqiqəsində dayanan əsasən ES və VF şəklində ritm pozğunluqları da müşahidə edildi.
| Regional işemiya, 30 dəq. | Reperfuziya 30 dəq. |
Ümumi işemiya, 30 dəq. | Reperfuziya 30 dəq. |
|||||
| Tezlik | n və ya san. | Tezlik | n və ya san. | Tezlik | n və ya san. | Tezlik | n və ya san. | |
| Nəzarət | ||||||||
| ES | 100 | 674±98 | 100 | 212±15 | 50 | 27±3 | 88 | 268±19 |
| ZhT | 88 | 240±28 | 88 | 40±10 | 0 | 0±0 | 50 | 21±4 |
| VF | 75 | 320±57 | 88 | 373±37 | 0 | 0±0 | 75 | 163±13 |
| Uridin | ||||||||
| ES | 88 | 147±10* | 100 | 95±11* | 63 | 20±4 | 75 | 105±12* |
| ZhT | 50 | 37±6* | 0* | 0±0* | 0 | 0±0 | 0* | 0±0* |
| VF | 50 | 40±5* | 63 | 67±9* | 0 | 0±0 | 0* | 0±0* |
| UMF | ||||||||
| ES | 75 | 162±38* | 88 | 80±7* | 75 | 16±5 | 38* | 32±4* |
| ZhT | 50 | 29±4* | 0* | 0±0* | 0 | 0±0 | 0* | 0±0* |
| VF | 0* | 0±0* | 50 | 55±12* | 0 | 0±0 | 25* | 8±3* |
| UDF | ||||||||
| ES | 88 | 119±54* | 100 | 202±17 | 50 | 18±6 | 88 | 159±18* |
| ZhT | 75 | 105±13* | 75 | 84±11* | 0 | 0±0 | 38 | 20±6 |
| VF | 63 | 56±8* | 75 | 305±21 | 0 | 0±0 | 50 | 148±10 |
| UTF | ||||||||
| ES | 50 | 84±9* | 100 | 265±24* | 63 | 30±8 | 100 | 353±22* |
| ZhT | 38 | 25±2* | 100 | 94±9* | 0 | 0±0 | 75 | 49±14* |
| VF | 0* | 0±0* | 88 | 207±12* | 0 | 0±0 | 75 | 195±12* |
|
Qeyd. * - nəzarət qrupundan fərqlər statistik cəhətdən əhəmiyyətlidir (s<0,05). |
||||||||
Uridin və UMF. Koronar arteriyanın tıxanmasından sonra 30 dəqiqə ərzində ürəklərə uridin və ya UMF olan bir məhlul vurulduqda, mədəcik aritmiyalarının tezliyində azalma (UMF, VF-dən istifadə edilən təcrübədə baş vermədi) və digərləri ilə müqayisədə əhəmiyyətli dərəcədə azaldı. nəzarət qrupu, onların şiddətinin azalması. Ligatura çıxarıldıqdan sonra reperfuziya dövründə dərmanların sonrakı tətbiqi VT-nin yaranmasının qarşısını aldı, ES sayının 2 dəfədən çox azalmasına, VF tezliyinin azalmasına kömək etdi və müddəti təxminən 5 dəfə azaldıldı. . Uridin və UMF-nin oxşar təsiri 30 dəqiqəlik ümumi işemiyadan sonra ürəklərin reperfuziyası zamanı müşahidə edilmişdir (cədvəl).
Kəskin işemiya və ya miokardın postişemik reperfuziyası zamanı erkən aritmiyaların patogenezində aparıcı rolu kardiyomiyosit membranlarının hər iki tərəfində ionların paylanmasının pozulması oynayır. Sarkolemmanın ATP-dən asılı K+ kanallarının (K ATP kanalları) rolu xüsusilə qeyd olunur. Bu kanalların aktivləşməsi hüceyrədaxili subsarkolemmal ATP səviyyəsinin 3-4 mmol/l-dən aşağı düşdüyü və K+ ionlarının kardiomiositlərdən intensiv şəkildə ayrılması, membranın depolarizasiyası, fəaliyyət potensialının amplitudasının və müddətinin azalması ilə müşayiət olunduqda baş verir. həmçinin repolarizasiya dərəcəsi.
Bu dəyişikliklər ürək əzələsində avtomatizmin, həyəcanlılığın və keçiriciliyin pozulmasına gətirib çıxarır ki, bu da həm yenidən daxil olma mexanizmi ilə, həm də elektrik aktivliyinin heterotopik ocaqlarının formalaşması ilə əlaqədar aritmiyaların inkişafına şərait yaradır. K ATP kanal blokatoru, antidiyabetik preparat olan qlibenklamid, miokard işemiyası zamanı aritmiyaların inkişafının qarşısını alır. İonların tarazlığının pozulması sarkolemmanın Na + ,K + -ATPase və Ca 2+ -ATPase aktivliyinin azalması ilə asanlaşdırılır, bunun üçün substratı da qlikoliz zamanı əmələ gələn ATP olur.
İon paylanması pozulmuş işemik reperfuziya zamanı kəskinləşir ki, bu da K+ ionlarının hüceyrədənkənar boşluqdan yuyulması, konsentrasiya qradiyenti boyunca zədələnmiş membranlardan daxil olan kardiyomiyositlərdə Na+ və Ca 2+ ionlarının toplanması, habelə əvvəllər işemik miokardın kifayət qədər qlükoza axınına baxmayaraq, ATP səviyyəsinin qeyri-adekvat bərpası.
Uridin və UMF-nin antiaritmik təsiri yəqin ki, onların miokard qlikogeninin resintezində, glikogenolizin aktivləşdirilməsində və ion daşıma sistemlərinin fəaliyyətini normallaşdırmaq üçün zəruri olan ATP-nin glikolitik fraksiyasının formalaşmasında iştirakı ilə əlaqələndirilir. Bundan əlavə, uridin və UMP katabolizminin məhsulu pantotenik turşunun bir parçası şəklində asetil-KoA-nın bir hissəsi olan -alanindir, buna görə uridin birləşmələrinin metabolitləri ürəkdə redoks proseslərinin aktivləşməsinə kömək edə bilər. Ekzogen UMP defosforilləşdikdə, yerli nukleozidlə eyni təsirə malik olan kardiyomiyositlərə daşına bilən uridin əmələ gəlir.
UDF və UTF. Uridin di- və trifosfat da regional işemiyada antiaritmik təsir göstərmişdir, hətta uridinin təsirindən bir qədər üstün olmuşdur (cədvəl). Hər iki birləşmə, bir tərəfdən, miokard tərəfindən tutulan uridinə qismən fosforilləşir, digər tərəfdən, qan damarlarının endotelinin purin (pirimidin) P 2U reseptorlarına təsir edərək, damarların əmələ gəlməsinə səbəb olan vazodilatasiyaya səbəb olur. rolunu azot oksidi (NO) yerinə yetirən endotel rahatlaşdırıcı faktor (EDRF). Nəticədə, bu birləşmələrin antianginal təsiri infarkt sahəsinin azalması və işemiyanın aritmogen təsirinin zəifləməsi şəklində özünü göstərə bilər.
Post-işemik reperfuziya zamanı fərqli bir vəziyyət müşahidə edildi. UDP və xüsusən də UTP regional və ya total işemiyadan sonra koronar axının bərpasında proaritmogen təsir göstərmişdir. Bəlkə də onların səbəb olduğu koronar dilatasiya əvvəllər işemik miokardın hiperoksigenləşməsinə və aritmogen aktivliyə malik lizofosfogliseridlərin əmələ gəlməsi ilə lipid peroksidləşməsinin aktivləşməsinə kömək edir. Bənzər bir təsir eksperimental miokard işemiyası zamanı mədəcik aritmiyalarının qarşısını alan, lakin post-işemik reperfuziyanın aritmogen təsirini gücləndirən aktiv koronar dilator adenozin tərəfindən həyata keçirilir.
Kardiyomiyositlərin səthində damar endotelindən başqa P 2U reseptorları da mövcuddur. Onların həyəcanlanması sarkolemmanın fosfolipaz C-nin aktivləşməsinə və inozitol-1, 4, 5-trifosfat səviyyəsinin artmasına səbəb olur, bu da hüceyrədaxili Ca 2+ miqdarının artması ilə müşayiət olunur və iz depolarizasiyasının meydana gəlməsinə kömək edir. və əvvəllər işemik miokard toxumasında avtomatizmi tetikler.
ƏDƏBİYYAT
1. Eliseev V.V., Sapronov N.S. Adenozin və miokard funksiyaları. - Sankt-Peterburq: "Lan" nəşriyyatı, 2000. - 160 s.
2. Eliseev V.V., Slobodskaya V.V., İlyin G.I. və başqaları. Riboksin, uridin, uridin-5"-monofosfat və quanosinin eksperimental miokard distrofiyasına təsiri // Chem.-Pharm. Jurnal. - 1985. - N 6. - S. 694-696.
3. Meerson F.Z. Stressin və ürəyin işemik zədələnməsinin patogenezi və qarşısının alınması. - M.: Nauka, 1984. - 272 s.
4. Olbinskaya L.I., Litvitsky P.F. Koronar və miokard çatışmazlığı. - M.: Tibb, 1986. - 272 s.
5. Sperelakis N. (Sperelakis N.) Yavaş fəaliyyət potensialı və miokard hüceyrələrinin yavaş kanallarının xüsusiyyətləri // Ürəyin fiziologiyası və patofizyolojisi. - T. 1. - Per. ingilis dilindən / Ed. N. Sperelakis. - M.: Tibb, 1990. - S. 241-277.
6. Gödecke S., Decking U.K.M., Gödecke A., et al. Siçovul P2u reseptorunun klonlaşdırılması və onun koronar vazodilatasiyada potensial rolu // Am. J. Fiziol. - 1996. - Cild. 270, №. 2. - P. C570-C577.
7. Aussedat J., Ray A., Rossi A. Normal və işemik perfused siçovul ürəyində uridinin birləşdirilməsi // Mol. Fiziol. - 1984. - Cild. 6. - S. 247-256.
8. Aussedat J., Verdetti J., Grably S., et al. Nucleotides uridiliques et glycogеne cardiaques: effet de l"administration d"uridine et de ribose chez le rat // J. Physiol. (Paris). - 1982. - Cild. 78. - S. 331-336.
9. Chang K., Hanaoka K., Kumada M., et al. Molekulyar klonlaşdırma və yeni bir P 2 nukleotid reseptorunun funksional təhlili // J. Biol. Kimya. - 1995. - Cild. 270. - Yox. 44. - S. 26152-26158.
10. Froldi G., Paridolfo L., Chinellato A., et al. ATP və UTP-nin siçovul qulaqcıqlarına ikili təsiri: hansı növ reseptorlar iştirak edir? // Naunyn-Schmiedebergs tağı. Farmakol. - 1994. - Cild. 349. - S. 381-386.
11. Janse M.J., Wit A.L. Miokard işemiyası və infarkt nəticəsində yaranan mədəcik aritmiyalarının elektrofizioloji mexanizmləri // Fiziol. Rev. - 1989. - Cild. 69. - N 4. - S.1049-1169.
12. Kirsch G.E., Codina J., Birnbaumer L., et al. ATP-həssas K + -kanallarının siçovul mədəcik miyositlərində G zülalları ilə A1 reseptorlarına qoşulması // Am. J. Fiziol. - 1990. - Cild. 259. - P. H820-H826.
13. Neely J., Grotyohann L.W. İşemik miokardın zədələnməsində qlikolitik məhsulların rolu. Adenozin trifosfat səviyyələrinin dissosiasiyası və reperfuziya edilmiş işemik ürəklərin funksiyasının bərpası // Circ. Res., 1984. - Cild 55, No. 6. - S. 816-824.
14. Opie L.H. ATP-həssas kalium kanalının tənzimlənməsi ilə işemiyanın modulyasiyası // Kardiovask. Narkotik Ther. - 1993. - Cild. 7, Əlavə. 3. - S. 507-513.
15. Ralevic V., Burnstock G. Purinlərin və pirimidinlərin siçovul mezenterik arterial yatağına təsiri // Circ. Res. - 1991. - Cild. 69. - S. 1583-1590.
16. Rovetto M.J. Miokard nukleotidlərinin nəqli // Ann. Rev. Fiziol. - 1985. - Cild. 47. - S. 605-616.
17. Taegtmeyer H., Roberts A.F.C., Raine A.E.G. Reperfused ürək əzələsində enerji mübadiləsi: metabolik funksiyanın qaytarılması ilə əlaqələndirilir // J. Amer. Col. Kardiol. - 1985. - Cild. 6. - Xeyr. 4. - S. 864-870.
18. Wilde A.A. K + ATP-kanalının açılması və aritmogenez // J. Cardiovasc. Farmakol. - 1994. - Cild. 24, Əlavə. 4. - S. S35-S40.
AMP, GMP və IMP onların sintezinin əsas reaksiyalarını maneə törədir. İki ferment: PRDF sintetaza və amidofosforiboziltransferaza yalnız AMP və GMP konsentrasiyasının eyni vaxtda artması ilə inhibə edilir, adenilosusinat sintetaza və IMP dehidrogenazanın fəaliyyəti isə yalnız metabolik proseslərin hər bir şöbəsində əmələ gələn son məhsulun miqdarının artması ilə azalır. cığır. AMP IMP-nin adenilosuksinata çevrilməsini, GMP isə IMP-nin ksantozin-5"-monofosfata (KMP) çevrilməsini maneə törədir, beləliklə adenil və guanil nukleotidlərinin balanslaşdırılmış tərkibini təmin edir.
Purin nukleotidlərinin sintezi üçün "ehtiyat" yollar sadə prekursorlardan əsas sintez yolu nuklein turşularını substratlarla tam təmin edə bilmədiyi zaman toxumaların aktiv böyüməsi dövrlərində əhəmiyyətli rol oynayır (Şəkil 10.31). Eyni zamanda, aktivlik artır:
hipoksantin-guanin fosforiboziltransferaza(HGPRT), azotlu əsasların: hipoksantin və guaninin nüvəyə çevrilməsini katalizləyir.
Hipoksantin |
||
kleotidlər - fosforiboza donoru kimi PRDF istifadə edən IMP və GMP;
adenin və PRDP-dən AMP sintez edən adenin fosforiboziltransferaza (AFRT);
adenozini daşıyaraq AMP-yə çevirən adenozin kinaz (AKase). ATP-nin γ-fosfat qalığı ribozun 5"-hidroksil qrupuna
kleosid
Purin nukleotidlərinin katabolizmi. Hiperurikemiya və gut
İnsanlarda purin nukleotidlərinin katabolizmi əmələ gəlməsi ilə başa çatır sidik turşusu. Başlanğıcda, nukleotidlər fosfataz və ya nukleotidazaların kataliz etdiyi reaksiyalarda hidrolitik olaraq fosfat qalıqlarını itirirlər. Adenozin dezaminasiya olunur adenozin deaminaza inozinin əmələ gəlməsi ilə. Purin nukleozid fosforilaz nukleozidləri sərbəst əsaslara və riboza-1-fosfata qədər parçalayır. Sonra ksantin oksidaz- protez qrupuna dəmir ionları (Fe3+), molibden və FAD daxil olan aerob oksidoreduktaza azotlu əsasları sidik turşusuna çevirir. ferment qaraciyər və bağırsaqlarda əhəmiyyətli miqdarda aşkar və molekulyar oksigen (Şəkil. 10.32) ilə purines oksidləşir. Urik turşusu insan orqanizmindən əsasən sidiklə, bəziləri isə nəcislə xaric olur. Zəif bir turşudur və bioloji mayelərdə zülallarla kompleksdə və ya monosodium duzu - urat şəklində ayrılmamış formada olur. Normalda qan zərdabında onun konsentrasiyası 0,15-0,47 mmol/l və ya 3-7 mq/dl təşkil edir. Gündəlik bədəndən 0,4-0,6 q sidik turşusu və urat xaric olunur.
Purin katabolizminin ümumi pozulması qan plazmasında sidik turşusunun konsentrasiyası normadan artıq olduqda baş verən hiperurikemiyadır. Bu maddənin zəif həll olması səbəbindən, hiperurikemiya fonunda, gut inkişaf edir - sidik turşusu və urat kristallarının artikulyar qığırdaqda, bağlarda və yumşaq toxumalarda gut düyünləri və ya tofi meydana gəlməsi ilə iltihaba səbəb olan bir xəstəlikdir. oynaqlar və nefropatiya. Gut dünya əhalisinin 0,3-1,7%-ni əhatə edir. Kişilərin zərdabında urat səviyyəsi qadınlardan iki dəfə yüksəkdir, ona görə də onlar qadınlardan 20 dəfə tez-tez gutdan əziyyət çəkirlər. Xəstəlik genetik olaraq təyin olunur və səbəb olur:
- PRDF sintetazasının hiperaktivasiyası və ya fermentin son sintez məhsulları tərəfindən inhibə edilməsinə qarşı müqaviməti ilə əlaqəli qüsurlar;
– purinlərin təkrar emalını təmin edən hipoksantin guanin fosforiboziltransferaza fəaliyyətinin qismən itirilməsi.
Hipoksantin-guanin fosforiboziltransferaza fəaliyyətinin tam itirilməsi ilə hiperurikemiyanın ağır forması - sindrom inkişaf edir.

Bölmə 10. Azot tərkibli birləşmələrin mübadiləsi |
|||||
Adenozin |
Quanozin |
||||
H3PO4 |
|||||
H3PO4 |
|||||
Riboza 1-fosfat |
|||||
Hipoksantin |
|||||
H2O + O2 |
H2O2H2O |
||||
H2 O2 |
|||||
Sidik turşusu |
|||||
düyü. 10.32. Purin nukleotidlərinin katabolizmi:
1 - nukleotidaza və ya fosfataza; 2 - adenozin deaminaza;
3 - purin nukleosid fosforilaz; 4 - guanaza; 5 - ksantin oksidaz
Nevroloji və zehni anormallıqların müşahidə edildiyi Lesha-Nyhan. Xəstəlik X xromosomu ilə əlaqəli resessiv bir əlamət kimi miras alınır və yalnız oğlanlarda baş verir.
Gut, hipoksantinin struktur analoqu olan allopurinol ilə müalicə olunur. Ksantin oksidaz preparatı oksipurinola oksidləşdirir, o, fermentin aktiv mərkəzinə möhkəm bağlanır və hipoksantin mərhələsində purinlərin katabolizmini dayandırır ki, bu da orqanizm mayelərində sidik turşusundan 10 dəfə çox həll olunur.
Pirimidin nukleotidlərinin biosintezi və katabolizmi. Orotasiduriya
Azotlu əsasın riboza-5-fosfat qalığı üzərində əmələ gəldiyi purin nukleotidlərinin sintezindən fərqli olaraq, pirimidin halqası əvvəlcə sadə prekursorlardan: glutamin, aspartat və CO2-dən yığılır. Sonra PRDP ilə qarşılıqlı əlaqədə olur və uridin-5"-monofosfata çevrilir - UMP (şəkil 10.33).

Bioloji kimya |
|||||||||||||||||
HCO3- |
|||||||||||||||||
Uridin-5"-monofosfat |
|||||||||||||||||
Qlutamat |
|||||||||||||||||
Karbamoil fosfat |
|||||||||||||||||
COO- |
|||||||||||||||||
COO- |
Orotidin 5"-monofosfat |
||||||||||||||||
Karbamoil aspartat |
|||||||||||||||||
COO-NAD+ |
NADH + H+ O C |
COO- |
|||||||||||||||
4 Orotate
Dihidroorotat
Amid qrupu
N 1 6 5
2 3 4
düyü. 10.33. Pirimidin halqasının atomlarının mənşəyi və UMP sintezi:
I - KAD fermenti: 1 - karbamoilfosfat sintetaza P; 2 - aspartat transkarbamoylaza; 3 - dihidroorotaza; 4 - Dihidroorotat dehidrogenaz;
II - UMP sintaza: 5 - orotat fosforiboziltransferaza, 6 - OMP dekarboksilaza

UMP sintezi hüceyrələrin sitozolunda baş verir və ikisi çoxfunksiyalı olan 3 ferment tərəfindən kataliz olunan 6 mərhələni əhatə edir. Birinci mərhələdə 2 ATP molekulundan istifadə edərək Gln və CO2-dən karbamoil fosfat sintez edilir. Asp karbamoil fosfata əlavə edildikdə və H2O çıxarıldıqda siklik birləşmə - ilk çoxfunksiyalı zülalın - CAD fermentinin məhsulu olan dihidroorotat əmələ gəlir. KAD adı fərdi katalitik domenlərin malik olduğu fermentativ fəaliyyətlərin ilk hərflərindən ibarətdir:
karbamoilfosfat sintetaza P (CPS P), aspartat transkarbamoylaza və dihidroorotaza . Dihidroorotat daha da oksidləşir orotat NAD-dan asılı dihidroorotat dehidrogenazın təsiri altında və ikinci bifunksional fermentin iştirakı ilə - UMP sintazaları UMF-yə çevrilir.
UMP UTP-ni iki mərhələdə formalaşdırır:
birinci mərhələ UMP kinaz, UMP + ATP → UDP + ADP tərəfindən katalizlənir,
ikincisi isə geniş substrat spesifikliyinə malik NDP kinazdır UDP + ATP → UTP + ADP,
CTP, ATP-nin enerjisindən istifadə edərək, urasilin keto qrupunu Gln-in amid qrupu ilə əvəz edən CTP sintetazasının təsiri altında UTP-dən əmələ gəlir:
UTP + Glu + ATP → CTP + Glu + ADP + H3 PO4.
Pirimidin nukleotidlərinin sintezinin tənzimlənməsi mənfi əks əlaqə mexanizmi vasitəsilə allosterik şəkildə həyata keçirilir:
– UTP tərkibindəki CPS P-nin fəaliyyətini maneə törədir KAD fermenti;
– UMP və CMF ikinci çoxfunksiyalı fermentin fəaliyyətini boğur - UMP sintazaları;
– CTP-nin yığılması CTP sintetazasının fəaliyyətini azaldır.
Pirimidin nukleotidlərinin sintezində ehtiyat yollar purin nukleotidlərinin sintezində olduğu kimi əhəmiyyətli rol oynamır, baxmayaraq ki, hüceyrələrdə aşağıdakılar olur:
pirimidin fosforiboziltransferaza, katalizator reaksiyası: pirimidin + PRDP → pirimidin monofosfat + H 4 R 2 O 7 (U və ya C) (UMF və ya CMF), uridin kinaz, nukleozidin nukleotidə çevrilməsi:
Uridin + ATP → UMP + ADP, və uridin fosforilaz, nukleozid deqradasiya reaksiyasını geri qaytara bilir:
urasil + riboza-1-fosfat → uridin + H3 PO4.
Katabolizm zamanı sitidil nukleotidləri hidrolitik olaraq amin qrupunu itirir və UMP-yə çevrilirlər. Qeyri-üzvi fosfat UMP və dTMP-dən nukleotidaz və ya fosfataz və fosforilazların iştirakı ilə ribozadan istifadə edərək ayrıldıqda, azot əsasları - urasil və timin qalır. Hər iki heterosikl NADPH-dən asılı dihidropirimidin dehidrogenazın iştirakı ilə hidrogenləşməyə və dihidrourasildən β-ureidopropion turşusunu və dihidrotim turşusundan β-ureidopropion turşusunu əmələ gətirmək üçün hidrolitik parçalanmaya məruz qala bilər.

on - β-ureidobutirik turşular. Ureid törəmələrinin sonrakı hidrolitik parçalanması CO2, NH4 və β-alanin və ya β-aminobutirik turşunun əmələ gəlməsi ilə başa çatır.
Pirimidin nukleotid mübadiləsinin pozğunluqları arasında yalnız bir nadir irsi xəstəlik təsvir edilmişdir - ikinci çoxfunksiyalı fermentin - UMP sintazasının genində mutasiya nəticəsində baş verən orotasiduriya. Bu zaman orotatın UMP-yə çevrilməsi pozulur, böyük miqdarda orotat (gündə 1,5 q-a qədər) sidikdə ifraz olunur. Pirimidin nukleotidlərinin çatışmazlığı inkişaf edir. Bu xəstəliyin müalicəsi üçün uridin və ya sitidin gündə 0,5-1 q dozada istifadə olunur, bu, pozulmuş reaksiyadan yan keçərək, nukleozid kinaz tərəfindən UMP və ya CMP-yə çevrilir.
Dezoksiribonukleotidlərin əmələ gəlməsi
Tipik olaraq, dezoksiribonukleotidlərin hüceyrədaxili konsentrasiyası çox aşağıdır, lakin hüceyrə dövrünün S mərhələsində o, DNT sintezini substratlarla təmin edərək artır. Dezoksiribonukleotidlərin əmələ gəlməsində iki ferment kompleksi iştirak edir: ribonukleotid reduktaza Və timidilat sintaza.
Bütün ribonukleotidlərin deoksi törəmələrinə reduksiyası ribonukleotid reduktaza kompleksi tərəfindən kataliz edilir. ribonukleotid reduktaza, zülalın azaldılması - tioredoksin və ferment tioredoksin reduktaza, NADPH-nin köməyi ilə tioredoksin regenerasiyasında iştirak edir (Şəkil 10.34).
Ribonukleotid reduktaza, fəaliyyəti fərdi dNTP-lərin konsentrasiyasından asılı olan allosterik bir fermentdir və dATP bütün ribonukleotidlərin reduksiyasının inhibitorudur. Bu vəziyyət ağır formaların baş verməsini izah edir immunçatışmazlıqlar purin katabolizmi fermentlərinin aktivliyinin azalması ilə: adenozin deaminaza və ya purin nukleozid fosforilaza(Şəkil 10.32). Bu fermentlərin çatışmazlığı B və T limfositlərində dATP və dGTP-nin yığılmasına gətirib çıxarır ki, bu da ribonukleotid reduktazı allosterik şəkildə inhibə edir və DNT prekursorlarını məhrum edir. DNT sintezi azalır və hüceyrələr bölünməyi dayandırır.
Timidil nukleotidlərinin sintezi timidilat sintaza kompleksi tərəfindən kataliz edilir. timidilat sintaza, bir karbonlu radikalın dUMP molekuluna daxil edilməsini kataliz edərək, dihidrofolat reduktaza, NADPH-nin iştirakı ilə H2-folatın H4-folata azalmasının təmin edilməsi və serin oksimetiltransferaza, N5 N10 -metilen-H4 -folatın əmələ gəlməsi ilə Serin hidroksimetil qrupunun H4 -folata köçürülməsini həyata keçirmək (Şəkil 10.35). İnsan bədənində dUMP dCDP-dən defosforilasiya və sonradan hidrolitik deaminasiya yolu ilə əmələ gəlir.
"Ehtiyat" sintez marşrutları arasında aşağıdakılar xüsusi əhəmiyyət kəsb edir:
timin fosforilaz, timini timidinə çevirir: Timin + Dezoksiriboza-1-fosfat → Timidin + H3 PO4 və
timidinin fosforlaşmasını kataliz edən timidin kinaz. Timidin + ATP → dTMP + ADP.

Ribonükleotid |
|||
nukleozid- |
reduktaza |
Deoksinukleozid- |
|
difosfatlar |
difosfatlar |
||
(NDF) |
(dNDF) |
||
Tioredoksin |
Tioredoksin |
||
NADP+ |
NADPH + H+ |
||
Tioredoksin
reduktaza
düyü. 10.34. Ribonükleozid difosfatların deoksi törəmələrinə azaldılması.
NDP şəklində ribonukleotidlər üçün azaldıcı agent tioredoksindir, bu reaksiya zamanı sulfhidril qrupları oksidləşir. Oksidləşmiş tioredoksin, NADPH-nin iştirakı ilə tioredoksin reduktaza tərəfindən azaldılır.
N 5,N 10 - metilen-H 2 - folat
H4 - fol turşusu
Serin-
hidroksimetiltransferaza
NADPH + H+
düyü. 10.35. Timidin-5"-monofosfatın sintezi.
Timidilat sintaza yalnız N5 N10-metilen-H4-folatın metilen qrupunu dUMP-nin pirimidin əsasının 5-ci mövqeyinə köçürmür, həm də onu H4-folatdan iki hidrogen atomu alaraq, metil radikalına qədər azaldır, buna görə də ehtiyatları artırır. N5 N10-metilen H4-folat daha iki fermentin işini tələb edir: dihidrofolat reduktaza və serinoksimetiltransferaza

Antiviral və antitümör dərmanlar kimi nukleotid sintezi inhibitorlarının istifadəsi
Azotlu əsasların, nukleozidlərin və nukleotidlərin analoqları dərman preparatları kimi tibbi praktikada geniş istifadə olunur (Cədvəl 10.3). Onlar bacarar:
– nukleotidlərin və ya nuklein turşularının sintezində iştirak edən müəyyən fermentləri maneə törədir;
– artan RNT və ya DNT zəncirlərində iştirak etmək və zəncirlərin böyüməsini dayandırmaq.
Cədvəl 10.3
Bəzi antitümör və antiviral dərmanlar
Əlaqələr |
Fəaliyyət mexanizmi |
Tətbiq sahəsi |
||||||||||||||
5-fluorourasil |
Ribo- və deoksiribona çevrilir. |
möhkəm |
||||||||||||||
timidini inhibə edən kleotidlər |
şişlər |
|||||||||||||||
lat sintaza və RNT zəncirinin böyüməsi |
Mədə-bağırsaq traktının, süd vəzilərinin |
|||||||||||||||
meşələr, ağciyərlər və s. |
||||||||||||||||
Metotreksat |
Fol turşusunun struktur analoqu, |
Kimyaterapiya |
||||||||||||||
dihidrofolat reduktazını inhibə edir, |
||||||||||||||||
purin nukleotidlərinin sintezini pozur və |
||||||||||||||||
dUMP-nin dTMP-yə çevrilməsi |
||||||||||||||||
Tioquanin |
Antimetabolit, DNT sintezini pozur və |
Kəskin leykozun müalicəsi |
||||||||||||||
şiş hüceyrələrində mitoz |
keçi və xroniki |
|||||||||||||||
miyeloid lösemi |
||||||||||||||||
Asiklovir |
Müvafiq NTF-ə çevrilir |
herpes |
||||||||||||||
(asiklo-guanozin) |
və viral DNT sintezini dayandırır |
infeksiyalar |
||||||||||||||
Sidovudin |
ilə bədən hüceyrələrində fosforlanmışdır |
|||||||||||||||
(timidin analoqu) metabolik yollarda ümumi ara məhsulların olması; ümumi metabolitlər vasitəsilə maddələrin qarşılıqlı çevrilməsi imkanı; ümumi koenzimlərin istifadəsi; katabolizmin ümumi yolunun və enerjinin buraxılması və istifadəsi üçün vahid sistemin (tənəffüs zənciri) mövcudluğu; oxşar tənzimləmə mexanizmlərindən istifadə etməklə. Şəkildə. Şəkil 11.1 əvvəlki fəsillərdə təsvir olunan karbohidratların, zülalların və yağların əsas metabolik yollarının ümumi diaqramını təqdim edir. 11.1. Metabolik yolların kompartmentallaşdırılması və tənzimlənməsi Metabolik proseslərin hüceyrələrin ayrı-ayrı bölmələrinə bölünməsi maddələr mübadiləsinə nəzarətdə mühüm rol oynayır (Cədvəl 11.1). Cədvəl 11.1 Əsas metabolik yolların bölmələri
| ||||||||||||||||
Bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsinin müalicəsində polifarmasiya problemi effektivliyin və təhlükəsizliyin optimal balansının yüksək tələblərinə cavab verən innovativ dərmanların tədqiqini aktuallaşdırır. Bu dərmanlara nukleotidlər daxildir.
Tədqiqatın məqsədi: bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsi üçün Keltican ® kompleksinin istifadəsinin effektivliyini və təhlükəsizliyini qiymətləndirmək.
Material və üsullar: xəstələr iki qrupa bölündü: 1-ci qrupa bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsindən əziyyət çəkən 20 xəstə (10 qadın və 10 kişi, orta yaş - 44,6±0,84 il) daxil idi. narkotik Keltican ® kompleksi (1 kapsul 1 dəfə/gün yeməklə) 20 gün ərzində; 2-ci qrupa kürək nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsindən əziyyət çəkən 30 xəstə (15 qadın və 15 kişi, orta yaş 46,5±1,34 il) kompleks prosedurlar qəbul etmişdir. Terapiyanın effektivliyi 20 günlük müalicədən sonra və 90 günlük müşahidədən sonra klinik və psixometrik tədqiqat metodlarından istifadə etməklə qiymətləndirilmişdir.
nəticələr: tədqiqat 20 günlük terapiya və 90 günlük müşahidədən sonra nəzarət qrupu ilə müqayisədə Keltican ® kompleksi ilə müalicə qrupunda ağrı intensivliyində əhəmiyyətli azalma aşkar etdi. Bel bölgəsində xroniki qeyri-spesifik ağrıların şiddətlənməsi üçün Keltican ® kompleksini qəbul edən bir qrup xəstədə təhlükəsizliyi qiymətləndirərkən, dərmanın təhlükəsizliyini göstərən heç bir mənfi dərman reaksiyası halı müşahidə edilməmişdir.
Nəticə: Keltican ® kompleksini qəbul edərkən ağrı sindromunun şiddəti əhəmiyyətli dərəcədə azalır və həyat keyfiyyəti yaxşılaşır, bu da Keltican ® kompleksini bu kateqoriyalı xəstələr üçün köməkçi terapiya kimi tövsiyə etməyə imkan verir.
Açar sözlər: nukleotidlər, Keltican ® kompleksi, xroniki bel ağrısı, köməkçi terapiya.
Sitat üçün: Raçin A.P., Şarov M.N., Vygovskaya S.N., Nuvaxova M.B., Voropaev A.A., Tarasova L.Yu. Bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsi üçün uridin monofosfat kompleks preparatının istifadəsi təcrübəsi // RMZh. 2017. № 24. S. 1812-1817
Xroniki qeyri-spesifik bel ağrılarının şiddətlənməsində kompleks uridin monofosfat preparatının istifadəsi təcrübəsi
Rachin A.P. 1, Şarov M.N. 2, Vygovskaya S.N. 1, Nüvaxova M.B. 1, Voropayev A.A. 1, Tarasova L.Yu. 1
1 Milli Tibbi Tədqiqat Reabilitasiya və Balneologiya Mərkəzi, Moskva
2 A.I. adına Moskva Dövlət Tibb və Stomatoloji Universiteti. Evdokimov
Xroniki qeyri-spesifik bel ağrılarının kəskinləşməsinin polipraqmasiyası şəraitində optimal effektivlik və təhlükəsizlik nisbətinin yüksək tələblərinə cavab verən innovativ dərmanların, o cümlədən nukleotid terapiyası preparatlarının tədqiqi problemi aktuallaşır.
Tədqiqatın məqsədi xroniki qeyri-spesifik bel ağrılarının şiddətlənməsində Keltikan ® kompleksinin istifadəsinin effektivliyini və təhlükəsizliyini qiymətləndirmək idi.
Xəstələr və Metodlar: xəstələr iki qrupa bölündü: 1 qrup - xroniki qeyri-spesifik bel ağrısının kəskinləşməsindən əziyyət çəkən 20 xəstə (10 qadın və 10 kişi, orta yaş 44,6 ± 0,84 il) Keltican ® kompleksinin təyin edilməsi ilə birlikdə prosedurlar kompleksi aldı. 1 kapsul gündə 1 dəfə yemək zamanı) 20 gün ərzində. 2-ci qrupa xroniki qeyri-spesifik bel ağrılarının kəskinləşməsindən əziyyət çəkən, kompleks prosedurlar qəbul edən 30 xəstə (15 qadın və 15 kişi, orta yaş 46,5 ± 1,34 il) daxildir. Terapiyanın effektivliyi 20 günlük müalicədən sonra və 90 günlük müşahidədən sonra tədqiqatın klinik və psixometrik metodları ilə qiymətləndirilmişdir.
Nəticələr: müqayisə edilən qruplarda ağrı intensivliyinin tədqiqi "Keltikan ® kompleksi" qrupunda "Nəzarət" qrupu ilə müqayisədə 20 günlük terapiya və 90 günlük müşahidədən sonra bu parametrin əhəmiyyətli dərəcədə azaldığını aşkar etdi. Xroniki qeyri-spesifik bel ağrılarının kəskinləşməsi zamanı Keltikan ® kompleksini qəbul edən xəstələr qrupunda onun təhlükəsizliyini sübut edən heç bir mənfi dərman reaksiyası müşahidə edilməmişdir.
Nəticə: Keltikan ® kompleksinin istifadəsi ağrı sindromunu əhəmiyyətli dərəcədə azaldır və həyat keyfiyyətini yaxşılaşdırır, bu da Keltican ® kompleksini bu kateqoriya xəstələr üçün köməkçi terapiya kimi tövsiyə etməyə imkan verir.
Açar sözlər: nukleotidlər, Keltikan ® kompleksi, xroniki bel ağrısı, köməkçi terapiya.
Sitat üçün: Raçin A.P., Şarov M.N., Vygovskaya S.N. və b. Xroniki qeyri-spesifik bel ağrısının şiddətlənməsində kompleks uridin monofosfat preparatının istifadəsi təcrübəsi // RMJ. 2017. No 24. S. 1812–1817.
Məqalədə bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsi üçün kompleks preparat uridin monofosfatın (Keltican kompleksi) istifadəsi üzrə tədqiqatın nəticələri təqdim olunur. Dərmanın qəbulunun ağrının şiddətini əhəmiyyətli dərəcədə azaltdığı və həyat keyfiyyətini yaxşılaşdırdığı göstərilmişdir ki, bu da Keltican kompleksini köməkçi terapiya kimi tövsiyə etməyə imkan verir.
Xroniki ağrı sindromu vacib bir cari fənlərarası problemdir. Bu vəziyyətin tibbi-sosial əhəmiyyəti əhali arasında baş və bel ağrılarının yüksək yayılması, yaş artdıqca yayılmasının artması və yuxusuzluq və anksiyete-depressiv pozğunluqlar da daxil olmaqla yanaşı xəstəliklərin olması ilə müəyyən edilir.
Son onilliklərdə əczaçılıq bazarında qeyri-spesifik, tez-tez təkrarlanan bel ağrısı üçün istifadə edilən çoxlu sayda dərman peyda oldu. Eyni zamanda, qeyri-steroid antiinflamatuar dərmanlar dorsalji üçün ənənəvi olaraq istifadə olunan dərmanlar olaraq qalır. Eyni zamanda, bel ağrısı olan xəstələrin təxminən 40% -i adekvat ağrı kəsici almır, polifarmasiyadan və dərmana mənfi reaksiyaların yüksək tezliyindən əziyyət çəkir, bu da belə müalicəni əsassız edir. Belə bir vəziyyətdə, effektivlik və təhlükəsizlik optimal balansının yüksək tələblərinə cavab verən, nukleotid terapiyası dərmanlarını ehtiva edən innovativ dərmanların öyrənilməsinin aktuallığı artır.
Nukleotidlər metabolik proseslərdə əsas rol oynayan, enerjinin qorunmasında və müəyyən molekul qruplarının ötürülməsində iştirak edən, həmçinin hüceyrədaxili siqnal zülalları kimi fəaliyyət göstərən aşağı molekulyar struktur elementləridir. Bundan əlavə, nukleotidlər nuklein turşularının, xüsusilə DNT və RNT-nin vacib komponentləridir.
Nukleotid uridin monofosfat bütün əsas pirimidin nukleotidlərinin neyron sintezində böyük rol oynayır. Membran vasitəsilə neyrona nüfuz edərək, nukleotid tez bir zamanda sinir toxumasının təmirinə daha aydın metabolik təsir göstərən di- və trifosfat nukleotidlərinə çevrilir. Beləliklə, biokimyəvi proseslər vasitəsilə bədənə xaricdən daxil olan uridin monofosfat daha sonrakı nukleotidlərə metabolizə olunur ki, onlar da maddələr mübadiləsinə və reparativ proseslərə daxil olurlar.
Uridin monofosfat (50 mq) Keltican ® kompleksinin əsas komponentidir. Keltican ® kompleksinə nukleotiddən əlavə vitamin B12 (3 mkq) və fol turşusu (400 mkq) da daxildir.
Vitamin B12 müxtəlif metabolik reaksiyalar üçün vacib bir koenzimdir. Siyanokobalamin purin və pirimidin nuklein əsaslarının, nuklein turşularının və zülalların sintezi mərhələlərində iştirak edir.
Fol turşusu bir çox katalitik reaksiyalarda, xüsusilə zülal və nuklein turşularının mübadiləsində, xüsusən purin, DNT və müxtəlif amin turşularının sintezində koenzim kimi çıxış edir və neyrotransmitterlərin, fosfolipidlərin və hemoglobinin biosintezində iştirak edir. . Beləliklə, Keltican ® kompleksi sinir toxumasının təmiri üçün zəruri olan elementlərin xarici mənbəyidir.
Keltican ® kompleksi sinir toxumasının lipidlərin və zülalların sintezi və ya istifadəsi üçün artan ehtiyacını ödəyərək sinir regenerasiyasını təşviq edir. Tərkibindəki uridin monofosfat sinir toxumasının hüceyrələrində (DNT və RNT sintezi) transkripsiya və tərcümə proseslərini aktivləşdirir. Nəticədə hüceyrə bölünməsi, maddələr mübadiləsi və periferik sinirlərin bərpası stimullaşdırılır. Bundan əlavə, uridin monofosfat Schwann hüceyrələrinin aksona miqrasiya/yapışmasının mürəkkəb prosesini idarə edən hüceyrədaxili və hüceyrədankənar siqnalların aktivləşdirilməsi prosesində əsas rol oynayır.
Bu tədqiqatın məqsədi: bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsi üçün Keltican ® kompleksinin istifadəsinin effektivliyini və təhlükəsizliyini qiymətləndirmək.
Material və üsullar
Tədqiqata daxil olan bütün xəstələr iki qrupa randomizə edilib:1-ci qrup (Keltikan ® kompleksi) – bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsindən əziyyət çəkən 20 xəstə (10 qadın və 10 kişi, orta yaş – 44,6±0,84 il), prosedurlar kompleksi: masaj (No12 ) , istifadə edərək biofeedback ilə fiziki terapiya Dr. Wollf (No 12), interferensiya vakuum terapiyası (No 8), iki kameralı jakuzi vannaları (No 8) Keltican ® kompleksi ilə birlikdə (1 kapsul gündə 1 dəfə yeməklə birlikdə) 20 gün ərzində. Gecikmiş ziyarət - terapiyanın başlanmasından 90 gün;
2-ci qrup (nəzarət) - bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsindən əziyyət çəkən 30 xəstə (15 qadın və 15 kişi, orta yaş - 46,5±1,34 il), bir sıra proseduralar qəbul etmişlər: masaj (No12), istifadə edərək biofeedback ilə fiziki terapiya Dr. Wollf (No 12), interferensiya vakuum terapiyası (No 8), iki kameralı jakuzi vannaları (No 8) sinir sistemi pozğunluqları olan xəstələr üçün tibbi reabilitasiya şöbəsində 20 gün qalma müddətində. Gecikmiş ziyarət - terapiyanın başlanmasından 90 gün.
Xəstələr təsadüfi nömrələr cədvəlindən istifadə edərək qruplara bölündülər. Müalicənin başlanması zamanı müqayisə edilən qruplar arasında yaş, dorsalji tarixinin orta müddəti və son kəskinləşmə müddətində statistik əhəmiyyətli fərqlər aşkar edilməmişdir.
Tədqiqatda aşağıdakı qiymətləndirmə metodlarından istifadə edilmişdir:
– klinik, nevroloji və anamnestik tədqiqat;
– vizual analoq şkalası (VAS);
- hərtərəfli ağrı anketi;
– Bel Ağrısında Əlillik üçün Oswester Ağrı Anketi.
Terapiyanın effektivliyi Keltican ® kompleksi ilə 20 günlük müalicədən və 90 günlük müşahidədən sonra klinik və psixometrik tədqiqat metodlarından istifadə etməklə qiymətləndirilmişdir.
Xəstə və tədqiqatçı tədqiqat preparatının effektivliyini və dözümlülüyünü aşağıdakı parametrlərə və dərəcələrə görə qiymətləndirdilər: effektivlik - çox yaxşı, yaxşı, qənaətbəxş, təsirsiz; dözümlülük – çox yaxşı, yaxşı, qənaətbəxş, zəif.
Hər səfərdə həyati əlamətlərin qiymətləndirilməsi ilə ümumi müayinə aparıldı. Fərdi uçot vərəqəsinə cari sağlamlıq vəziyyəti haqqında məlumatlar daxil edilib.
Statistik təhlil. Alınan nəticələr təsviri və müqayisəli statistikadan istifadə etməklə işlənmişdir. Təhlil olunan bütün göstəricilər üçün dəyişənin növündən asılı olaraq təsviri statistika aparılmışdır: kəmiyyət dəyişənləri təhlil edilərkən orta hesab, standart kənarlaşma, minimum və maksimum qiymət, keyfiyyət dəyişənləri təhlil edilərkən isə ümumi göstəricinin tezliyi və payı (faizlə) müəyyən edilmişdi. Statistik təhlil, Windows 7 üçün Statgraphics Centurion statistik proqram paketindən istifadə edərək parametrik t-testləri və Fisher və ya qeyri-parametrik Wilcoxon və Kolmogorov-Smirnov testlərindən istifadə etməklə nümunə populyasiyasının paylanmasından asılı olaraq həyata keçirilmişdir. Bütün statistik testlər iki dəfə tərəfli statistik əhəmiyyət səviyyəsi (p) 0,05 .
Tədqiqat nəticələri
Tədqiqatımızın nəticələri göstərdi ki, bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsindən əziyyət çəkən xəstələrdə müalicəyə başlamazdan əvvəl 1-ci və 2-ci müqayisəli qruplarda əhəmiyyətli fərqlər yox idi. ağrı intensivliyi, VAS-dan istifadə etməklə qiymətləndirilmiş və müvafiq olaraq 46,0±1,14 və 46,3±1,18 bal təşkil etmişdir.20 gün ərzində Keltican ® kompleksi (yeməklə birlikdə gündə 1 kapsul) ilə birlikdə prosedurlar dəstini qəbul edən 1-ci qrup xəstələrdə (Keltican ® kompleksi, n=20), biz müalicədən sonra ağrı intensivliyinin əhəmiyyətli dərəcədə azaldığını göstərən məlumatlar əldə etdik. 26,3±1,54 bal təşkil edən 20 günlük terapiya, həmçinin terapiyanın başlanmasından 90 gün sonra bu göstəricinin əhəmiyyətli sabitliyi (13,7±1,33 bal). Güclü ağrının oxşar etibarlı dinamikası nəzarət qrupunda qeyd edildi və 20 günlük müalicədən və terapiyanın başlanğıcından 90 günlük müşahidədən sonra müvafiq olaraq 31,5±1,63 və 17,6±1,68 bal təşkil etdi.
Eyni zamanda vurğulamaq lazımdır ki, müqayisə edilən qruplarda ağrı intensivliyinin ətraflı təhlili zamanı Keltican ® kompleks qrupunda 20 günlük terapiyadan sonra və 90 gündən sonra nəzarət qrupu ilə müqayisədə bu parametrdə əhəmiyyətli azalma müəyyən etdik. müşahidənin (Şəkil 1).
Keltican ® kompleksinin bel nahiyəsində xroniki qeyri-spesifik ağrıların şiddətlənməsindən əziyyət çəkən xəstələrdə ağrının intensivliyini azaltmaqda etibarlı effektivliyi haqqında, prosedurlar kompleksini qəbul edən nəzarət qrupu ilə müqayisədə.
Tədqiqatımız göstərdi ki, bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsindən əziyyət çəkən xəstələrdə və 1-ci və 2-ci müqayisəli qruplarda müalicə başlamazdan əvvəl heç bir ciddi fərq yox idi. subyektiv ağrı qiymətləndirməsi ilə, təhlili şifahi şkala üzrə aparılmış və göstərici müvafiq olaraq 2,5±0,15 və 2,5±0,19 bal olmuşdur.
1-ci qrup xəstələrdə (Keltican ® kompleksi, n=20) 20 günlük terapiyadan sonra ağrının subyektiv qiymətləndirilməsinin əhəmiyyətli dərəcədə azaldığını göstərən məlumatlar əldə etdik ki, bu da 1,6±0,12 bal təşkil etdi, həmçinin əhəmiyyətli sabitlik bu göstərici terapiyanın başlanmasından 90 gün sonra (1,1±0,11 bal). Ağrının subyektiv qiymətləndirilməsi parametrinin oxşar etibarlı dinamikası müqayisə edilən nəzarət qrupunda qeyd edildi və
Müalicənin 20 günü və terapiyanın başlanmasından 90 günlük müşahidə müvafiq olaraq 1,9±0,17 və 1,6±0,15 bal təşkil etmişdir. Bununla birlikdə, müqayisə edilən qruplarda ağrının subyektiv qiymətləndirilməsinin ətraflı təhlilində, Keltican ® kompleks qrupunda 20 günlük terapiyadan və 90 günlük müşahidədən sonra nəzarət qrupu ilə müqayisədə bu parametrdə əhəmiyyətli bir azalma müəyyən etdik (Şəkil 2). 2). 
Beləliklə, əldə edilən məlumatlar, bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsindən əziyyət çəkən xəstələrdə ağrının subyektiv qiymətləndirilməsini və bu parametrin sabitliyini azaltmaqda Keltican ® kompleksinin əhəmiyyətli effektivliyini göstərir. nəzarət qrupu.
Müalicə başlamazdan əvvəl 1-ci və 2-ci müqayisə qruplarında bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsindən əziyyət çəkən xəstələrdə parametrdə əhəmiyyətli fərqlərin olmadığını nümayiş etdirdik. hərtərəfli ağrı anketi(ağrının xəstələrin həyat keyfiyyətinə təsirini əks etdirir - Müəllif qeydi) və şkala üzrə ümumi bal müvafiq olaraq 87,0±2,46 və 87,3±2,74 olmuşdur.
1-ci qrup xəstələrdə (Keltican ® kompleksi, n=20) 46,5±2,67 təşkil edən hərtərəfli ağrı anketi üzrə ümumi balın əhəmiyyətli dərəcədə azaldığını, həmçinin 90-dan sonra bu göstəricinin əhəmiyyətli sabitliyini göstərən məlumatlar əldə etdik. terapiyanın başlanmasından günlər (27,4±2,76 bal). Hərtərəfli ağrı anketindəki ümumi balın oxşar etibarlı dinamikası müqayisə edilən nəzarət qrupunda qeyd edildi və 20 günlük müalicədən və terapiyanın başlanğıcından 90 günlük müşahidədən sonra müvafiq olaraq 54,2 ± 2,36 və 33,6 ± 3,14 bal təşkil etdi. Bununla birlikdə, müqayisə edilən qruplarda ağrının həyat keyfiyyətinə təsirini əks etdirən hərtərəfli ağrı anketindəki ümumi balın ətraflı təhlilində biz Keltican ® kompleks qrupunda nəzarətlə müqayisədə bu parametrdə əhəmiyyətli bir azalma müəyyən etdik. qrup 20 günlük terapiyadan sonra və 90 günlük müşahidədən sonra (Şəkil 3). 
Beləliklə, əldə edilən məlumatlar göstərir
bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsindən əziyyət çəkən xəstələrin həyat keyfiyyətinə ağrının təsirini azaltmaqda Keltican ® kompleksinin etibarlı effektivliyi haqqında prosedurlar kompleksi alan xəstələr qrupu.
Tədqiqatımızın nəticələri göstərdi ki, bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsindən əziyyət çəkən xəstələrdə müalicə başlamazdan əvvəl 1-ci və 2-ci müqayisəli qruplarda əhəmiyyətli fərqlər yox idi. əlillik haqqında Oswestry şkalası üzrə, göstərici isə müvafiq olaraq 36,0±0,24 və 36,2±0,23 bal təşkil etmişdir.
1-ci qrup xəstələrdə (Keltican ® kompleksi, n=20) Oswestry sorğusuna uyğun olaraq həyat fəaliyyətinin əhəmiyyətli dərəcədə yaxşılaşdığını göstərən məlumatlar əldə etdik (ağrının həyatın müxtəlif sahələrinə mənfi təsirinin azaldılması nəticələrinə əsasən). 20 gün terapiya; bu göstərici 17,3±1,12 bal, həmçinin terapiyanın başlanmasından 90 gün sonra bu göstəricinin əhəmiyyətli sabitliyi (8,6±0,71 bal) olmuşdur. Həyat fəaliyyətinin yaxşılaşması parametrinin oxşar əhəmiyyətli dinamikası müqayisə edilən qrupda da qeyd edildi və müalicənin 20 günü və terapiyanın başlanğıcından 90 günlük müşahidədən sonra müvafiq olaraq 21,4 ± 1,17 və 12,7 ± 0,89 bal təşkil etdi.
Nəzərə almaq lazımdır ki, əldə edilmiş məlumatların ətraflı təhlilindən sonra biz Keltican ® kompleks qrupunda 20 günlük terapiya və 90 günlük müşahidədən sonra nəzarət qrupu ilə müqayisədə bu göstəricidə əhəmiyyətli irəliləyiş müəyyən etdik (Şəkil 4). 
Beləliklə, əldə edilən məlumatlar göstərir
bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsindən əziyyət çəkən xəstələrdə həyat fəaliyyətinin yaxşılaşdırılmasında Keltican ® kompleksinin etibarlı effektivliyi haqqında (ağrının həyatın müxtəlif sahələrinə mənfi təsirinin azaldılması nəticələrinə əsasən). prosedurlar kompleksi alan xəstələr qrupu.
Qiymətləndirərkən təhlükəsizlik Bel bölgəsində xroniki qeyri-spesifik ağrıların kəskinləşməsi üçün Keltican ® kompleksini qəbul edən xəstələr qrupunda Keltican ® kompleksinin dərmanı, onun təhlükəsizliyini göstərən heç bir mənfi dərman reaksiyası halı müşahidə edilməmişdir.
nəticələr
Əldə edilən məlumatları təhlil edərkən aşağıdakı nəticələri tərtib etdik.1. Keçirilən müqayisəli klinik və psixoloji təhlil statistik cəhətdən etibarlı şəkildə Keltican ® kompleksinin bel nahiyəsində xroniki qeyri-spesifik ağrıların şiddətlənməsində effektivliyini sübut etdi.
2. Bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsindən əziyyət çəkən xəstələrin tibbi reabilitasiyası zamanı Keltican ® kompleksinin farmakoloji korreksiyaya daxil edilməsi tövsiyə olunur.
3. Bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsi üçün Keltican ® kompleksi yüksək təhlükəsizlik profilinə malikdir.
4. Keltican ® kompleksi bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsindən əziyyət çəkən xəstələrin həyat keyfiyyətini əhəmiyyətli dərəcədə yaxşılaşdırır, bunu Oswestry və Rolland-Morris şkalası üzrə yaxşılaşdırılmış ballar sübut edir.
5. Bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsi üçün Keltican ® kompleksi preparatını istifadə edərkən, əldə edilmiş nəticələrin sabitliyi (ağrının aşağı subyektiv qiymətləndirilməsi və həyati parametrlərdə yaxşılaşma) 90 günlük müşahidədən sonra etibarlı şəkildə qorunub saxlanılmışdır ki, bu da təsdiq edilmişdir. şifahi miqyasda və Oswestry sorğusunda göstəricilərin yaxşılaşdırılması ilə.
Nəhayət Qeyd etmək lazımdır ki, fizioloji pirimidin nukleotidlərinin istifadəsi bel nahiyəsində xroniki qeyri-spesifik ağrıların kəskinləşməsinin müalicəsində haqlı olaraq perspektivli istiqamətlərdən biri hesab olunur. Keltican ® kompleksini qəbul edərkən sinir toxumasının regenerasiyası güclənir, sinir impulslarının ötürülməsi prosesləri normallaşır, ağrı sindromunun şiddəti əhəmiyyətli dərəcədə azalır və həyat keyfiyyəti yaxşılaşır, bu da Keltican ® kompleksini tövsiyə etməyə imkan verir. xəstələrin bu kateqoriyası üçün analjezik terapiyaya əlavə olaraq.
Ədəbiyyat
1. Raçin A.P., Anisimova S.Yu. Dorsopatiya: praktiki həkim üçün təcili problem // RMJ. 2012. T.20. № 19. səh.964–967.
2. Raçin A.P., Yakunin K.A., Demeşko A.V. Miyofasiyal ağrı sindromu. Ser. “Tibbdə aktual problemlər”. M., 2009.
3. Rachin A.P. Xroniki baş ağrısının formalaşmasının nümunələri (klinik, psixofizioloji və sosial amillər), terapiyanın optimallaşdırılması, proqnoz və qarşısının alınması. dis. ...Dr. Sci. adına PMGMU. ONLAR. Seçenov. M., 2007.
4. Rachin A.P., Yudelson Ya.B. Uşaqlarda xroniki gündəlik baş ağrısı // Z. nevrologii i psihiatrii im № 83–85.
5. Rachin A.P., Yudelson Ya.B., Sergeev A.V. Xroniki gərginlikli baş ağrısı prosesində beynin funksional xüsusiyyətləri (P300 potensialının dinamikasına görə) // Patogenez. 2005. № 1. S.48.
6. Yudelson Ya.B., Rachin A.P. Uşaqlarda və yeniyetmələrdə gərginlik baş ağrılarının xüsusiyyətləri // Müasir pediatriya məsələləri. 2003. T.2. № 5. S.51.
7. Yudelson Ya.B., Rachin A.P. Uşaqlarda və yeniyetmələrdə gərginlik baş ağrılarının klinik və psixoloji xüsusiyyətləri // Nevroloji jurnal. 2003. № 5. səh. 32–35.
8. Raçin A.P., Sergeev A.V. Persen: narahatlıq pozğunluqları və yuxu pozğunluqları üçün istifadə imkanları // Farmateka. 2008. № 8. S.29–32.
9. Raçin A.P., Mixaylova E.V. Depressiya və narahatlıq vəziyyətləri. Ser. "Tibb mütəxəssisinin kitabxanası." Psixiatriya. Nevrologiya. Ümumi tibbi təcrübə. M., 2010.
10. Rachin A.P. Yuxu pozğunluqlarının müalicəsi: təsnifat və analitik yanaşmalar // Poliklinik həkiminin məlumat kitabı. 2007. № 6. səh.64–68.
11. Rachin A.P., Yudelson Ya.B. Osteoartritin müalicəsi üçün sübuta əsaslanan farmakoanalitik // Pharmateka. 2007. № 19. 81-dən.
12. Yudelson Ya.B., Rachin A.P., Beloqorokhov O.O. Dorsalji üçün neyrodiklovit dərmanının istifadəsinin effektivliyi və təhlükəsizliyi // Farmateka. 2008. № 20. səh.132–136.
13. Karelov A.E., Zaxarov D.A., Lebedinski K.M., Semenov D.A. Anesteziologiyada yeni texnologiyalar: purin analjeziyası // Vestnik Sankt-Peterburq. un-ta. 2008. № 11 (1). səh.77–82.
14. Salter M.W., Henry J.L. Adenozin 5'-monofosfat və adenozin 5'-trifosfatın pişik onurğa dorsal buynuzunda funksional olaraq müəyyən edilmiş vahidlərə təsiri. Adenozin 5'-trifosfatın nosiseptiv və qeyri-nosiseptiv vahidlərə diferensial təsirinin sübutu // Neurosci. 1985. Cild. 15. S.815–825.
15. Phyllis J.W., Kirkpatrick J.R. Adenozinin və müxtəlif nukleozidlərin və nukleotidlərin təcrid olunmuş toad onurğa beyninə təsiri // Gen. Farmakol. 1978. Cild. 9. S.239–247.