3258 0
Трихинеллез — зоонозный природно-антропургический биогельминтоз с алиментарным путем передачи возбудителя, характеризуется лихорадкой, интоксикацией, болями в мышцах, отеками и гиперэозинофилией.
История и распространение
Возбудитель Trichiella spiralis описан Р.Оуеном в 1835 г., роль в патологии доказана Р.Вирховым и Ф.Ценкером.
Трихинеллез в виде спорадических случаев или групповых заболеваний регистрируется на всех континентах, кроме Австралии. В России в последние годы в связи с учащением реализации мяса (прежде всего свинины), не прошедшего санитарно-ветеринарного контроля, наблюдается рост заболеваемости.
Этиология
Возбудитель Trichiella spiralis и некоторые ее подвиды - мелкие нематоды. Длина самца и неоплодотворенной самки около 1,5-2 мм, оплодотворенной самки - 3,5-4,4 мм. Трихинеллы - живородящие гельминты. Особенностью их биологии является то, что один и тот же организм служит и основным, и промежуточным хозяином. Попадая в организм животного (человека) вместе с мясом, под воздействием желудочного сока личинки освобождаются от капсул и в течение 1 - 1,5 сут в тонкой кишке достигают половой зрелости.
Каждая самка за репродуктивный период длительностью 10- 30 дней рождает до 2000 живых личинок, которые через слизистую оболочку тонкой кишки проникают в ток крови, а затем в скелетные мышцы. В мышцах личинки быстро растут, спирально свертываются и покрываются капсулой, которая в течение 6-18 мес обызвествляется. Личинки становятся инвазионными через 3 нед после проникновения в организм и сохраняют инвазионность 5-10 лет и более (до 40-50 лет).
Эпидемиология
В природных очагах циркуляция возбудителя поддерживается благодаря пищевым связям между хищниками, всеядными животными и некрофагами (жуками, земляными червями, млекопитающими). Антропургические очаги вторичны, они тесно связаны с природными. Чаще всего в них возбудитель циркулирует между свиньями и крысами. Человек заражается при употреблении в пищу недостаточно термически обработанного мяса или сала с прожилками мяса домашних животных (свиней) либо диких животных (кабан, барсук, морж и др.). Человек является биологическим тупиком для возбудителя.
Патогенез
В процессе роста и созревания личинки выделяют метаболиты, обладающие токсическими, сенсибилизирующими и ферментативными свойствами. Под их воздействием развиваются воспалительный процесс в слизистой оболочке тонкой кишки, генерализованное поражение сосудов, тромбогеморрагический синдром, отек тканей. Попадая в мышцы, они вызывают явления миозита. В других органах и тканях личинки погибают. При этом развиваются иммунопатологические реакции. Особенно часто поражаются мышца сердца, головной мозг, легкие.
Патоморфология
Уже к концу 1-й недели после инвазирования в слизистой оболочке тонкой кишки можно обнаружить самок трихинелл, окруженных воспалительным инфильтратом. При массивной инвазии возможно язвенно-некротическое поражение слизистой оболочки кишки. Особенно характерно развитие полимиозита с выраженными дистрофическими изменениями в миоцитах. К концу 3-й недели вокруг личинок появляется выраженная инфильтрация. Особенно значительно поражаются диафрагма, межреберные, жевательные мимические мышцы и мышцы конечностей.
В паренхиматозных органах вокруг погибших личинок формируются воспалительные гранулемы. В мышце сердца развиваются очаговая и диффузная воспалительная реакция, дистрофия миоцитов. В веществе и оболочках головного мозга образуются гранулемы, васкулиты. Наиболее частой причиной смерти является миокардит.
Клиническая картина
Продолжительность инкубационного периода 5-45 сут, чаще 10-25 сут. Она так же, как и тяжесть течения болезни, зависит от массивности инвазии. Чем короче инкубационный период, тем тяжелее течение болезни.
При неинтенсивной инвазии клиническая симптоматика отсутствует, возможна лишь эозинофилия в крови. При абортивной форме наблюдаются незначительное повышение температуры тела и боли в мышцах в течение 1-2 дней.
В типичных случаях болезнь начинается остро, полностью клиническая картина развертывается в течение 2-5 сут. Однако еще в инкубационном периоде могут быть боли в животе и жидкий стул.
Лихорадка варьирует от кратковременного субфебрилитета до фебрильной в пределах от 38,0-39,0 °С длительностью до 2-3 нед и более. В этих случаях температура тела имеет ремиттирующий характер. После ее снижения часто сохраняется длительный субфебрилитет.
Наиболее характерные жалобы - боли в мышцах тянущего или стреляющего характера и мышечная слабость. При пальпации мышцы (особенно жевательные и затылочные) болезненны. При попытке открыть рот появляется тризм. Поражение диафрагмы и межреберных мышц сопровождается одышкой, поверхностным дыханием, что способствует ухудшению вентиляции легких и развитию пневмонии. Несколько позже присоединяются отечность век, лица, реже отеки на туловище и конечностях.
Часто наблюдают макулопапулезные высыпания на коже. При поражении легких появляется кашель с мокротой, иногда с прожилками крови, при рентгенологическом исследовании в легких обнаруживают «летучие инфильтраты». Часто отмечают артериальную гипотензию, тахикардию.
Аппетит снижен, живот болезненный при пальпации в средней части, стул жидкий, несколько раз в сутки, может содержать примесь слизи и крови. Нередко увеличивается печень, реже - селезенка. Больные заторможены, адинамичны, жалуются на головную боль.
При исследовании крови определяются лейкоцитоз, эозинофилия, которая при легком течении болезни достигает 20- 30 %, а при среднетяжелом 50-60 % и более. Характерны гипоальбуминемия, гипокальциемия и гипокалиемия, повышение активности многих ферментов, особенно креатинфосфокиназы (КФК).
Тяжелая форма болезни характеризуется коротким инкубационным периодом (5-10 сут), лихорадкой до 39-40 °С, выраженной миопатией, распространенными отеками, геморрагической сыпью, тахикардией и гипотонией, расширением границ и глухостью тонов сердца, нарушениями ритма, застойными явлениями в легких, частым присоединением вторичных пневмоний, выраженными болями в животе, диареей, расстройствами сознания, менингеальным синдромом и очаговой неврологической симптоматикой. Эозинофилия выражена умеренно и даже может отсутствовать, что является прогностически неблагоприятным симптомом. Выздоровление медленное, период реконвалесценции длится до 6 мес и более. Могут длительно беспокоить боли в мышцах, слабость, боли в сердце, сердцебиение, одышка.
Диагноз и дифференциальный диагноз
Наиболее значимыми для диагностики симптомами являются боли в мышцах, одутловатость и отечность лица, лихорадка, эозинофилия. Важное значение имеет установление группового характера заболевания и связи с употреблением свинины, сала, мяса кабана и других диких животных. Для подтверждения диагноза используют трихинеллоскопию остатков «подозрительного» мяса или биоптатов мышц больного. Используют также РПГА и РСК.
Дифференциальный диагноз проводят с острой фазой описторхоза, фасциолеза и других гельминтозов, а также лептоспирозом, риккетсиозами, иерсиниозом, сальмонеллезом, дерматомиозитом, отеком Квинке.
Лечение
Больных госпитализируют. Дегельминтизация эффективна только в ранние сроки после инфицирования (до 2 нед). Применяют мебендазол (вермокс) по 100 мг 3 раза в течение 7-10 дней. Возможно использование более высоких доз препарата - до 500 мг 3 раза в сутки. Одновременно проводят дезинтоксикационную терапию, назначают антигистаминные и нестероидные противовоспалительные препараты.
При тяжелом течении болезни, миокардите, поражении ЦНС, дыхательной недостаточности применяют кортикостероиды, хотя они способствуют более затяжному течению болезни. Преднизолон назначают в таблетках в дозе от 30 до 60 мг в сутки в течение 5-7 дней с последующим снижением дозы и отменой их через 1-2 нед.
Прогноз при легком и среднетяжелом течении болезни благоприятный, при тяжелом - серьезный, летальность достигает 10-20 %.
Профилактика проводится в нескольких направлениях. Важное значение имеют предотвращение инвазирования свиней (дератизация на свинофермах, исключение поедания свиньями трупов животных, мясных отходов, уничтожение бродячих кошек и собак), обязательное исследование мяса свиней и диких животных на наличие личинок трихенелл, достаточная термическая обработка мяса, уничтожение зараженного мяса. Лицам, употребившим зараженное мясо, выявленным в окружении больного, назначают вермокс по 0,1 г 3 раза в день в течение 5-7 дней, исследуют кровь для выявления эозинофилии.
Ющук Н.Д., Венгеров Ю.Я.
Введение..........................................................................................
Глава 1. Методы исследования..................................................
Глава 2. Краткий исторический очерк открытия, изучен –
трихинеллеза.......................................................................
Глава 3. Морфология возбудителя трихенелеза......................
Глава 4. Жизненный цикл Trichinella spiralis..........................
Глава 5. Особенности эпидемиологии синантропного очага
трихинеллеза...................................................................................
Заключение......................................................................................
литературы.......................................................................
ВВЕДЕНИЕ
Проблема Трихинеллеза , не смотря на многочисленные исследования
остается актуальной проблемой биогельминтозных заболеваний. Это связано с тем,
что наряду с синантропными очагами трихинеллез существует в природе, то есть
трихинеллез является типичнейшим природно-очаговым заболеванием гельминтозной
природы. Циклы развития трихиниля в поселениях человека изучен в принципе,
досконально. Однако в связи с новой экономической ситуацией в России, когда
санитарно- эпидемиологический контроль не выполняет возложенные на него
функции, трихинеллез вышел практически из- под контроля. Об этом
свидетельствуют средства массовой информации, регистрирующие массовые
заболевания трихинеллеза при употреблении инвазионного мяса.
Исходя, из выше изложенного в работе была поставлена цель, по доступным
литературным источникам представить историю изучения и осветить современное
состояние проблемы.
Из поставленной цели следуют следующие задачи:
1. осветить историю открытия изученности Trihinella spiralis ;
2. рассмотреть морфологию возбудителя и цикл развития;
3. выделить особенности эпидемиологии синантропного очага.
Глава 1. Методы исследования
1. Статистический
Связан с работой и обработкой официальной документацией по Трихинеллезу
определенной административной единицы (населенный пункт сельского или
городского типа, район, область, регион), документация берется в пунктах по
анализу мясной продукции (базар, станции санэпиднадзора районного и
областного масштаба).
2. Морфологический
Заключается в обнаружении трихинеля в поперечно - полоса-той мускулатуре
различных животных обитающих непосред-ственно в синантропных очагах. Особую
роль занимают представители: серая крыса, свиньи, домашние мыши.
У отловленных животных в синантропных очагах берутся кусочки поперечно-
полосатой мускулатуры (исключение сердечная мышца) в местах, где мышцы
переходят в сухожилие. Это мышцы передних и задних конечностей, ножки
диафрагмы и мышцы корня языка. Размеры кусочков должны соответствовать
величине рисовой зерновки и с каждого места тушки берется 24 такие пробы, и
помещаются в соответствующий квадрат, которых тоже 24 компрессориума. В
компрессориуме при помощи болтов пробы раздавливаются до такой толщины, чтобы
животного Трихинеллезом его личинки очень хорошо видны под малым увеличителем
светового микроскопа. При нахождении хотя бы одной личинки животное считается
зараженным трихинеллезой.
Глава 2. Краткий исторический очерк открытия,
изученности трихинеллеза
Трихинеллез – острое инвазионное заболевание человека, сопровождающееся
лихорадкой и выраженными аллергическими явлениями.
Возбудителем Трихинеллеза является мелкий круглый гельминт Trihinella
spiralis. Источником инвазии являются некоторые млекопитающие животные,
преимущественно свиньи.
Широко распространен среди многих видов домашних и диких млекопитающих,
особенно хищных, а также всеядных; ему свойственна природная очаговость.
Заражение наступает при употреблении в пищу мяса, пораженного личинками
трихинелл.
Впервые мышечные личинки трихинеля были открыты в тридцатых годах прошлого
столетия. Впервые описано заболевание было лишь спустя 30 лет.
В 1828 году в Лондоне впервые увидели в мышцах человека инкапсулированных
личинок трихинелл. Вскоре после этого, в 1835 году студентом Pagef в
Лондоне были обнаружены личинки нематод с кальцифицированными капсулами в
который описал их и дал название Trichina spiralis. Однако позже
родовое название Trichina было изменено на Trihinella, так как
первое уже принадлежало некоторым двукрылым насекомым. Вскоре после этих
открытий появились сообщения о нахождении трихинелл у человека в Германии,
Северной Америке и др. Позже трихинеллы были найдены и у различных видов
млекопитающих.
Во второй половине XIX века был расшифрован в общих чертах биологический цикл
трихинелл и установлено, что из мышечных личинок в кишечнике животных
В России трихинеллез был обнаружен в 1865 году М. М. Руд-невым при вскрытии
трупа в медико-хирургической академии.
В 1873 году Ю. Кнох впервые обнаружил личинок трихинелл при жизни, вырезав
кусочек двуглавой мышцы у больного трихинеллезом.
Трихиниллез встречается довольно часто среди населения многих стран мира. В
конце девятнадцатого столетия он имел широкое распространение в Германии.
Причиной послужило употребление в пищу полусырых свиных продуктов. В прошлом
веке набольшее распространение трихинеллеза приобрел в США, а так же в
странах Восточной Европы. Тяжелое клиническое течение трихинеллеза и
значительное распространение привлекают особое внимание медицинских
работников. Природные очаги инвазии встречаются повсеместно, за исключением
Австралии и Антарктиды. Чрезвычайно высокая пораженность трихинеллами многих
видов диких млекопитающих ставит их на первое место в качестве резервуара
инвазии в природе. Часто регистрируются вспышки трихинеллеза у людей в
результате употребления в пищу мяса диких животных, вследствие этого,
развитие животноводства в нашей стране на промышленной основе накладывает
большую ответственность на работников ветеринарии за ликвидацию трихинеллеза
у свиней – основного источника заражения человека. Поэтому в пищу должно
поступать доброкачественное свиное мясо, предварительно прошедшее
ветеринарно-санитарную экспертизу с обязательным исследованием на
трихинеллез.
Установление аллергической природы клинического течения инвазии позволило
применить патогенетическую до сенсибилизи-рующую терапию и добиться
определенных успехов в лечении больных и снижении летальности.
Трихинеллез представляет собой не только медицинскую и ветеринарную, но и
общебиологическую проблему. Учитывая активность и массовое распространение этой
Международную комиссию по трихинеллезу. В 1960 году в Варшаве по инициативе
трихинеллезу, на которой была создана новая комиссия и в ее состав вошли
представители Советского Союза. Комиссия ставила своей задачей – расширение
научных исследований по проблеме трихинеллеза, а также разработку наиболее
эффективных мер борьбы с этим заболеванием во всех странах. Вторая
международная конференция по трихинеллезу состоялась в 1969 году во Вроцлове
(Польша). Третья Международная конференция по трихинеллезу состоялась в США
(1972) в г. Майями Бич (Флорида), доклады конференции опубликованы в журнале
Expe Parasifology.
Для координации борьбы с трихинеллезом в СССР была создана Межведомственная
комиссия, куда входят руководящие работники: главного санитарно -
эпидемиологического управления Министерства здравоохранения СССР, главного
санитарно – ветеринарного управления Министерства сельского хозяйства СССР и
ученые, занимающиеся проблемой трихинеллеза человека и животных.
В 1972 году в Вильнюсе была проведена Всесоюзная конференция по проблеме
трихинеллеза человека и животных.
В настоящее время в мировой печати накопилась информация, всесторонне
освещающая эту проблему.
В отечественной литературе проблема трихинеллеза нашла монографическое
изложение в книгах В. А. Калюса (1952), Березанцева (1956), но обилие новых
фактов и сведений в области изучения этого гельминтоза вызывает необходимость
издания новых источников.
Глава 3. Морфология возбудителя трихинеллеза
Изучением морфологии трихинелл занимались многие исследователи (E. B. Тимонов,
1970, и др.).Е. В. Тимонов для изучения динамики а всех стадиях развития
применил люминесцентный метод. Этот метод имеет большие преимущества перед
другими, применяемыми для этих целей. Трихинелл обрабатывали от 3 до 40 минут
флюорохромами при температуре 37о. после этого различные структуры и
органы гельминта приобретали способность ко вторич-ной люминесценции и
светились разным цветом – от зеленого до оранжевого, что облегчало
исследование. Все размеры трихинелл, сроки их развития приведены в результате
экспериментального изучения на белых мышах.
Мигрирующая личинка
Отрожденные личинки трихинеллы имеют размеры 100 – 110 мк. х. 5 – 6 мк.
Передний отдел на протяжении 8 – 10 мк. Заполнен готогенной жидкостью и
образует головной «колпачок», ученый
Е. В. Тимонов – предполагал, что в нем содержится гистометический фермент,
который обеспечивает внедрение личинки в мышечное волокно.
В области пищеводного отдела (протяженность до 20 мк.) продольно расположены
6 – 8 рядов мелких ядер. Посреди него (в 30 – 35 мк от переднего конца) лежит
нервное кольцо в виде темной поперечной полоски. Остальная часть личинки
заполнена более крупными одинаковыми ядрами. Границы между клетками
неразличимы. Во время миграции по малому и большому кругу кровообращения
личинки несколько увеличиваются в длину до 120 мк., но морфологических
изменений не происходит.
Мышечная личинка
Личинки трихинелл развиваются до инвазионной стадии в волокнах поперечно –
полосатых мышц. За это время длина их
увеличивается более 10-ти раз и достигает максимальных размеров: у мужских
личинок – 1.16 х. 0.06 мм, у женских – 1.36 х. 0.06 мм.
Тело мышечных личинок, как и половозрелых трихинелл, несколько сужено
впереди. В личинках происходит формирование различных органов и тканей. Рост
личинки, также и последующей половозрелой стадии, осуществляется
преимущественно за счет средней части тела, соответствующей средней кишке.
У сформировавшихся личинок трубка, начинающаяся терминально ротовым
отверстием на переднем конце тела и заканчивающаяся также терминально на
заднем конце, четко дифференцирована на переднюю (пищевод), среднюю и заднюю
(ректум) кишку. Ротовое отверстие ведет в длинный пищевод. На месте перехода
пищевода в среднюю кишку лежат две пищеварительные одноклеточные железы.
Средняя кишка начинается амнуловидным расширением сразу же за клеточным
пищеводным телом. Четко заметна граница средней клетки и ректума. Причем у
мужских личинок ректум имеет в длину до 56 мк., а у женских – до 25 мк.
Кишечник у женских личинок лежит на дорсальной стороне параллельно яичнику, а
у мужских часто посередине семенника переходит с дорсальной на вентральную
сторону (наружная сторона спирали личинки).
Клеточное пищеводное тело, или стихозома полностью формируется в течение двух
месяцев, заполняя полость тела (схизоцель) переднего конца личинки. Стихозома
(длиной до 560 мк.) начинается в 200 мк. от переднего конца, лежит на
протяжении всего пищевода и состоит в среднем от 50 до 56 клеток стихоцитов,
которые охватывают пищевод. Роль пищеводного тела до конца невыяснена.
Некоторые исследователи считают, что оно выполняет функцию одноклеточных
желез, секрет которых поступает непосредственно в пищевод (Richels, 1955).
У личинок развиваются зачатки половой системы, по морфологическим различиям
которых можно определить пол. Развитие гонад продолжается до 25 – 26-го дня
после заражения, но выходящих протоков на личиночной стадии не образуется. У
вполне развитых женских личинок яичник лежит в задней части тела на
вентральной стороне, на протяжении 0.27 мм.
На переднем конце гонады формируется четко заметный клиновидный зачаток
матки, который соединен с гонадой одной генитально - соединительной клеткой.
В гиподерме переднего конца женских личинок закладывается в виде утолщения
зачаток вульвы и влагалища, которые заметны даже под наблюдением в световой
микроскоп. Поскольку половое отверстие у нематод располагается на
вертикальной стороне, то таковой у спирально сворачивающейся личинки
У мужских личинок семенник (лежащий у задней части тела) спереди достигает
конца пищеводного клеточного тела и зачатком семяпровода делает изгиб в
обратную сторону по направлению к ректуму, мышечных личинок уже через 17 дней
можно легко диф-ференцировать по полу, даже в световой микроскоп.
Половозрелые трихинеллы
В процессе развития кишечных трихинелл разными исследова-телями насчитывалось
от двух до четырех линек. Рост и развитие самок трихинелл в кишечнике белых
мышей продолжаются в течение 5 дней, и они увеличиваются в длину с 1.36 мм.
И имеют диаметр до 0.08 мм. стихозома за это время у них укорачи-вается с
0.55 мм. (у личинок) до 0.35 мм. (у взрослой самки). Развитие половой системы
у самок начинается с формирования широкой матки и влагалища. Клиновидный
зачаток матки у личинки начинает расти вперед по вентральной стороне и вскоре
соединяется с зачатком вульвы в гиподерме, через 20 часов после инвазии
полностью формируется влагалище, и в нем появляется общий с маткой канал.
Через 38 часов на месте генитально – соединительной клетки (у личинки)
образуется короткий яйцевод. В задней части матки возникает небольшое
мешкообразное вздутие – семя приемник. Длина яичника до 0.45 мм., затем
через 6 дней уменьшается до 0.37 мм., через 40 дней до 0.27 мм.
Половозрелыми самки становятся через 40 часов, когда в их каудальных отделах
появляются яйца. Первое оплодотворение происходит через 44 часа, а
сформированные личинки в передних отделах матки видны через 72 часа. В каждой
самке содержится 20-25 личинок, обладающих способностью к внедрению в
мышечное волокно.
Самцы растут в течение 7 дней и за это время увеличиваются в длину с 1.16 мм.
до 2.20 мм., и имеют диаметр до 0.07 мм. Самцы начинают отличаться от самок
после первой линьки, когда у них на заднем конце тела по сторонам от клоаки
образуются сначала небольшие конулятивные придатки (конические лопасти).
Зачаток семяпровода растет назад и через 6 часов соединяется с ректумом,
образуя клоаку. Вскоре через 27 часов из нижнего отдела формируется семенной
мешок, заполненный спермой.
У половозрелых трихинелл по сравнению с мышечными личинками значительно
удлиняется средняя кишка, образуя приректальную ампулу. Пищевод не имеет
постоянного положения. Анальное отверстие открывается терминально, у самцов
между двумя коническими лопастями.
Глава 4. Жизненный цикл
В биологическом цикле трихинелл можно выделить несколько стадий: яйцо,
эмбрион, мигрирующая личинки, личинка и половозрелая стадия (по Е. Тимонову).
Развитие от яйцеклетки до личинки происходит в яичнике и матки самки.
Развитие в кишечнике
Освобождение личинок трихинелл от капсул начинается сразу же при попадании их
в желудок и идет параллельно с переварива-нием мышц. Развитие личинок в
на кишечной стенке, в которую они внедряются передним концом тела. Личинки
трихинелл проникают в слизистую оболочку двенадцатиперстной кишки примерно
через 2 часа. На гистологических срезах кишечника крысы через несколько часов
после заражения можно видеть различную степень внедрения личинок в слизистую
оболочку (А. Г. Казаринов, 1898; Э. Р. Геллер, 1934, и др.). А. Г. Казаринов
считал, что трихинеллы не вбуравливаются в эпителий ворсинок, а вдавливаются,
замыкаясь вокруг них. На четвертые сутки самки начинают отрождать личинок в
ткань слизистой оболочки или в лимфатические сосуды кишечных ворсинок.
Личинки 19 – 20 дневного возраста достигают половой зрелости и начинают
отрож-дать личинок на 3 – 4 дня позже по сравнению в двухмесячными личинками
(Е. В. Тимонов, 1970). У половозрелых червей на протяжении всего срока
овогенез, а у самцов – сперматогенез. Наличие запаса спермы в матке у 40-
дневных самок предполагает многократное оплодотворение (Е. В. Тимонов, 1970;
Д. П. Козлов, 1972). Половозрелые трихинеллы локализуются в зоне щеточной
каймы и частично в тканях слизистой оболочки кишечника хозяина.
По данным Е. В. Тимонова, трихинеллы развиваются нормаль-но у мышей,
находящихся на углеводной и жировой диетах. Только исключительно белковая
пища приводит к задержке развития три-
хинелл, но они все же достигают половой зрелости и отрождают личинок. В
кишечнике голодных мышей трихинеллы не развива-ются. Эти данные позволяют
сделать вывод, что они получают пищевые вещества из просвета кишечника,
скорее всего из области щеточной каймы, а не из тканей слизистой оболочки.
Биологическую целесообразность проникновения трихинелл в слизистую оболочку
кишечника можно объяснить тем, что отрождение личинок происходит в
лимфатические сосуды ворсинок, иначе они гибли бы в просвете кишечника и не
смогли бы проникнуть в кишечную стенку из-за отсутствия для этого
специального приспособления.
концом, трихинеллы могут использовать кислород из зоны щеточной каймы, в
которой содержится небольшое го количество, поступающее с пищей, а также
получать из тканей. Кислород необходим нематодам еще для развития личинок в
яйцах (М. М. Завадовский, 1916), вероятно, и трихинелла не является в этом
отношении исключением. Дыхание кислородом у кишечных трихинелл облегчается их
малым размером. Кроме того, у них определяются активные дыхательные ферменты.
Половозрелые трихинеллы локализуются по всему тонкому кишечнику мышей,
начиная с двенадцатиперстной кишки и кончая верхними отделами толстого
кишечника (слепая кишка и начальная часть ободочной). Наибольшая концентрация
трихинелл встречалась нами в средних отделах тонкого кишечника (тощая и
подвздошная кишки). Значительно меньше их было в двенадцатиперстной кишке, в
самых верхних отделах кишки, в слепой и в оболочной кишках.
В кишечники самцы и самки находятся рядом. Они отыскивают друг друга, если
даже заражать мышей одной парой трихинелл. При этом кишечные трихинеллы не
предпринимают активного передви-жения в верхние участки кишечника (Д. П.
Козлов, 1971, 1972).
При инвазии трихинеллами почти никаких видимых патоло-гических отклонений в
кишечнике не наблюдается. Отмечаются лишь изменения в клетках эпителия,
экспериментальной инвазии появляются значительные патологические изменения в
кишечнике. Появляются кровавые поносы, кишечник сильно вздувается, и при этих
явлениях наступает гибель животного в первые 2 – 4 дня после заражения. У
человека практически не бывает
такого интенсивного заражения или случается очень редко, и поэтому фаза
кишечного трихинеллеза проходит, как правило, не заметно, а нарушения со
стороны кишечника аллергического характера наблюдаются в более поздние сроки
заболевания (Н. Н. Озероцковская, 1958).
При относительно слабом заражении, когда в слизистой оболочке не возникает
воспаления в результате внедрения в нее трихинелл, последние лежат в тонком
кишечнике между ворсинками, обвиваясь вокруг них. Реже трихинеллы проникают в
кипты. Задние концы червей часто лежат свободно в просвете кишечника или
между ворсинками. Передними концами трихинеллы вдавливаются в слизистую
оболочку и проникают в толщу эпителия ворсинок или крипт. Обычная локализация
передних концов трихинелл – основание эпителиального слоя перед базальной
мембраной или под ней. В толстом кишечнике трихинеллы проникают передними
концами в основание эпителиального слоя поверхности слизистой оболочки или
крипт. Задние концы червей также часто лежат свободно в просвете кишечника
или в криптах. Такая локализация трихинелл в кишечнике отмечается во все
Длительность жизни кишечных трихинелл короткая по сравнению с личиночной
жизни способствовало бы увеличению потомства, что могло привести к быстрой
гибели хозяина и к затруднению передачи инвазии. У белых мышей и крыс
трихинеллы живут 2 – 3 недели, и только единичные доживают до 30 – 45 дней. У
морских свинок трихинеллы живут в кишечнике до 30 – 55 дней. Кишечные
В кишечнике хозяина приживается лишь часть попавших туда мышечных личинок. Э.
Р. Геллер и Л. Ф. Гридасова (1968) устано- вили, что приживаемость зависит, в
частности, и от возраста мышечных личинок. Восьмимесячных личинок проживает в
кишечнике белых мышей больше, чем двухмесячных. Вероятно, при дальнейшем
увеличении возраста личинок приживаемость их снижается, так как при заражении
крыс 32-месячными личинками через 10 часов в кишечнике была обнаружена лишь
одна трихинелла.
О количественном соотношении полов кишечных трихинелл имеются противоречивые
сведения. По данным опытов на мышах Н.П. Шихобаловой, М. А. Прасоловой
(1952), К. Подгаецкого (1963),
Э. Р. Геллера, Л. Ф. Гридасовой (1968), в начале кишечной инвазии преобладают
самки. Количественное выравнивание происходит, согласно первым трем
исследованиям, примерно через 15 дней, после этого начинают резко преобладать
Гридасовой, самцов и самок становится одинаково через 10 дней, а с 16-го дня
несколько преобладают самки. Первые исследователи определили у мышей через 12
дней после заражения соотношение самок и самцов как 3: 1.
Самцы, как и самки, внедряются в слизистую оболочку, а не находятся в
просвете кишечника. Хотя иногда неверно отмечается, что самцы после
оплодотворения самок через две недели заражения выбрасываются с калом.
Ошибочно также мнение. Что и самки. Полностью отродившие личинок,
выбрасываются с калом. Наблюдения многих авторов как в экспериментах на
лабораторных животных, так и над больными трихинеллезом людьми показывают,
что кишечные трихинеллы в кале встречаются очень редко. Очевидно, трихинеллы
после гибели подвергаются деструкции. У экспериментальных животных.
Зараженных большой дозой личинок, в первые дни заражения наблюдаются поносы в
результате сильного воспаления топкого кишечника, вызванного внедрением в
слизистую оболочку трихинелл. В этот период в кале могут встречаться
трихинеллы. В дальнейшем воспалительные явления стихают, и трихинеллы с калом
обычно больше не выносятся.
Данные о количестве личинок, отрождаемых одной самкой, очень противоречивы.
Личинок, видимо, отрождается больше, чем инкапсулируется в мышцах, так как
часть их гибнет в организме на ранних стадиях, не попав в мышечные волокна.
Исследования в этом направлении были проведены Н. П. Шихобаловой и М. А.
Прасоло-вой (1952), которые установили на белых мышах, что на одну самку
трихинеллы приходится от 200 до 900 инкапсулированных личинок в мышцах в
зависимости от интенсивности инвазии. Чем интенсивнее инвазия, тем меньше
личинок отрождается каждой самкой. Как уста- новлено трансплантациями одной
самки трихинеллы крысам, она
отрождает 345 личинок, а мышам – она отрождает до 283 личинок.
В организме разных видов животных плодовитость трихинелл, очевидно, варьирует.
Если животные при интенсивной инвазии не гибнут от кишечного трихинеллеза в
первую неделю после заражения, то они могут погибнуть во вторую неделю и
позже, уже в период мышечной инвазии. Установлено, что доза в 70 личинок на 1
г. живого веса убивает большинство крыс впервые 2 – 7 дней, то есть в период
кишечного трихинеллеза. Доза в 40 личинок на 1 г. живого веса почти всегда
вызывает смерть крысы на протяжении 12 – 25 дней,
то есть в период мышечного трихинеллеза.
Вне кишечника с пищевыми массами половозрелые трихи-неллы не развиваются.
Миграция личинок в организме хозяина
Несмотря на более чем столетнее изучение биологии трихи-нелл, до настоящего
времени все еще является дискуссионным вопрос о путях миграции личинок из
кишечной стенки хозяина до скелетных мышц. В 1960 впервые детально изучен
полость, а оттуда до рыхлой соединительной ткани в скелетные мышцы. Такую
точку зрения разделяют некоторые исследователи и в настоящее время.
Доказательство этому они видят в обнаружении у экспериментально зараженных
животных мигрирующих личинок в брюшной полости и между листками брюшины в
брыжейке вне сосудов. Они не отрицают, что какая-то часть личинок может
разноситься кровью. А. Г. Казаринов (1898) и другие экспериментально
доказали, что личинки трихинелл отрождаются в ткани кишечных ворсинок, откуда
по лимфатическим сосудам начинают свой путь миграции. Впервые Ф. В.
Овсянниковым (1866) установлено на кроликах, что личинки мигрируют по
кровеносным сосудам. Убедительные исследованиям на белых крысах подтвердили,
что отрожденные в слизистой оболочке кишечника личинки трихинелл лимфогенным
путем через грудной проток попадают в кровь и мигрируют через малый и большой
круг кровообращения. В крови, взятой из сердца зараженных белых крыс, А. З.
Ковш и В. П. Коряжков (1930) находили мигрирующих личинок с 7-го по 23-й день
после заражения. Личинки встречались в небольшом количестве. Это зависит от
того, что они быстро разносятся по организму хозяина со скоростью
артериального кровотока.
Веским доказательством гематогенного разноса личинок служит распределение
инкапсулированных личинок трихинелл в скелетных мышцах в зависимости от их
интенсивности кровоснаб-жения (А. Г. Щегловитов, 1925; В. И. Тритов, 1958).
Скелетные мышцы поражаются все, но различно по интенсивности, причем
многочисленными исследователями показана неодинаковая заселяемость личинками
мышечных групп у разных видов млекопитающих. Больше личинок встречается в
мышцах, выполняющих интенсивную нагрузку, которые, естественно имеют и более
обильное кровоснабжение.
Личинки способны в какой-то степени и к активной миграции. Вероятно, они
активно проходят по лимфатическим узлам. При подкожном и внутримышечном
введении половозрелых трихинелл отрождаемые ими личинки мигрируют в
близлежащие мышцы и там инкапсулируются. Однако небольшое число личинок,
проникших в кровеносные сосуды, заносится в отдаленные группы мышц и там
инкапсулируется (Э. Р. Геллер, 1935; Е. В. Тимонов, 1970, и др.). начинки
активно проходят через легкие, органы большого круга кровообращения и
внедряются в мышечные волокна.
В легких экспериментально зараженных животных всегда обнаруживаются
мигрирующие личинки трихинелл, что свидетельствует об их гематогенном заносе
(Э. Р. Геллер, 1932;
Ю. А. Березанцев, 1963; Матов, 1968). Личинки быстро проходят через легкие.
Проходя через ткань легкого в поисках выносящего сосуда, личинки повреждают
стенки сосудов, вероятно более крупного диаметра, чем капилляры.
Кровоизлияния хорошо заметны на поверхности легких невооруженным глазом.
Личинки трихинелл, попав в артериальную систему, разносятся пассивно во все
органы и ткани. Значительная часть их сразу же заносится в скелетные мышцы.
Ни в одном органе личинки не задерживаются. Они активно проходят через ткани,
повреждая сосуды, свидетельством чего служат множественные кровоизлияния в
указанных органах. Попадая в венозную систему, личинки опять проделывают тот
путь миграции, при этом значительная часть снова попадает в скелетные мышцы,
то есть в место специфической локализации. Сколько раз возможна такая
миграция, неизвестно, но исчезновение личинок из органов свидетельствует, что
все же основная масса их добирается до мышц и так инкапсулируется. В мышцах
же происходит непрерывное нарастание количества личинок с 7-го и, примерно,
до 30-го дня после заражения (Ю. А. Березанцев, 1963, 1969).
Подтверждением того, что личинки мигрируют по органам большого круга
кровообращения, служит обнаружение антигенов трихинелл на гистологических
срезах печени и селезенки мышей, обработанных иммунофлюоресцирующей
сывороткой (метод прямой иммунофлюлресценции).
Мигрирующих личинок трихинелл Е. В. Тимонов (1970) находил в почках,
селезенке и головном мозге мышей. Их находили многие исследователи в
различных органах и тканях у людей и экспериментально зараженных животных: в
разных отделах головного мозга, спинномозговой жидкости, костном мозге,
миокарде. Личинки в мозговой ткани и в мышце сердца часто были окружены
клеточными инфильтратами.
Несмотря на то, что описаны многочисленные случаи нахождения мигрирующих
личинок в тканях, в каждом отдельном из этих случаев авторы находили
единичных личинок. Таких личинок считали «заблудившимися» и обреченными на
гибель, а воспалительные явления стали связывать в последнее время
исключительно с аллергической реакцией. На самом деле, попадание личинок в
разные внутренние органы является закономерным моментом в их миграции по
организму хозяина. Они там не погибают (если погибают, то только единичные и
в самом конце процесса миграции), а проходят через ткани, проделывают тот же
путь миграции.
Проникновение мигрирующих личинок в грудную, брюшную и перикардиональную
полости, где их находили многие исследователи, объясняется выходом из
капилляров серозных покровов, обильно снабженных сосудами.
Миграция личинок трихинелл по внутренним органам хозяина и повреждение ими
сосудов, приводящее к кровоизлияниям, гибели клеток и последующему
воспалению, безусловно, должны иметь
определенное значение в патогенезе трихинеллеза. Аллергический характер
заболевания в период миграции и начальной стадии инкапсуляции личинок в
настоящее время не вызывает сомнения, но в патогенезе заболевания не
учитывается воздействие мигрирующих личинок на ткани органов и, главным
образом, головного мозга.
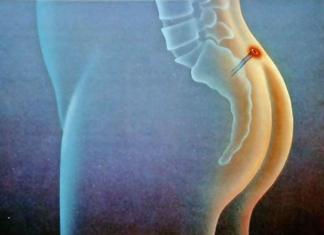
При миграции личинок трихинелл по большому кругу кровообращения они заносятся
и в плаценту беременного материнского организма. Вопрос о возможности
трансплацентарного заражения плода трихинеллами в настоящее время исследован
недостаточно. В опытах на белых крысах и Ю. Б. Березанцев (1959) на белых
мышах, А. А. Дубницкий (1965) на кошках и собаках не наблюдали внутриутробной
передачи трихинелл. Положительные результаты трансплацентарного заражения
получили в опытах на свинках, кроликах и крысах.
Развитие и инкапсуляция в мышцах
Адаптация к мышцам у личинок трихинелл появилась в процессе эволюции.
Мышечная ткань, по-видимому, обеспечивала наиболее благоприятные условия для
их развития. Личинки могут развиваться, лишь проникнув в волокна скелетной
мускулатуры. Поэтому на начальных этапах их следует считать типичными
гуморальных и фагоцитарных защитных реакций хозяина, служит оболочка клетки –
полупроницаемая биологическая мембрана. Эволюционная адаптация таких
преодоление ее защитных механизмов, оказавшись в крови или ткани,
факторов. Пока личинки трихинелл развиваются в мышечном волокне, клетки
возникшего воспалительного инфильтрата в мышцах не проникают под сарколемму.
Лишь позже, начиная с 14-го дня, они разрушают на некотором протяжении
инвазированное и дистрофически измененное мышечное волокно, не затрагивая
участка саркоплазмы, непосредственно окружающего личинку. В период его
процессами. Кусочек саркоплазмы инкапсулируется вместе с развивающейся в нем
личинкой трихинеллы.
У личинок трихинелл наблюдаются более сложные взаимо-отношения с хозяином: с
происходит его инкапсуляция, но с частью живой саркоплазмы. Вокруг личинок с
участком саркоплазмы формируется соединительнотканная капсула особого
специфического строения, с хорошо развитой сосудистой сетью и чувственными
нервными окончаниями (Ю. А. Березанцев, 1963, 1972).
При первом же попадании в мышечные капилляры личинки сразу проникают в
мышечные волокна. Никаких кровоизлияний в мышцах не наблюдается, потому что,
внедряясь в мышечное волокно, личинка наносит минимальную травму стенке
капилляра. Капилляры мышечных волокон, являясь наиболее узкими в организме
млекопитающих, делают резкие изгибы, через которые личинки пройти не могут.
Мигрирующие личинки трихинеллы не имеют никаких приспо-соблений, чтобы
проникнуть из капилляра в мышечное волокно, равно как через сосудистые стенки
и клетки тканей при миграции через легкие и органы большого круга
кровообращения.
Попав в мышечные волокна, личинки остаются на месте и начинают расти.
Мышечные волокна, в которые только что внедрились личинки, не изменены, но
уже с 8-го дня после заражения в них начинают постепенно развиваться признаки
дистрофии и реактивных изменений. Такие волокна слегка утолщаются, теряют
поперечную исчерченность и бледнее окрашиваются по сравнению с нормальными
мышечными волокнами. В пораженных волокнах мышечные ядра интенсивно делятся,
образуя «ядерные цепочки». Ядра увеличиваются и достигают диаметра 20 – 25
мк., в них появляются крупные ядрышки до 5 мк., состоящие из РНК.
Личинки, проникшие в мышечные волокна, вначале прямые и вытянутые по длине
мышечного волокна, позже начинают скручи-ваться. С 13-го дня заражения
мышечное волокно в том месте, где лежит личинка, веретеновидно расширяется. С
14-го дня, некротизируются и инфильтрируются лейкоцитами на довольно
значительном протяжении.
С 16-го дня после заражения в мышцах накапливается большое количество
личинок. Первые, попавшие в мышцы личинки, начина-ют скручиваться в
веретенообразном расширении мышечного волокна, и около них обосабливается
участок живой изменой саркоплазмы с реактивно измененными и размножившимися
С 20-го дня вокруг спирально свернутой личинки с окружающим ее участком
саркоплазмы появляется тонкая соедини- тельнотканная капсула.
С 21 – 22-го дня капсулы утолщаются, на их внутренней стороне, обращенной к
саркоплазме, появляется узкая полоска коллагена. В наружном слое формируется
сосудистая сеть. Через 24 дня после заражения вокруг некоторых личинок видны
четкие капсулы даже при трихинеллоскопии. Постепенно коллагеновый слой
капсулы утолщается и гиалинизируется. Личинки инкапсулируются обычно по
одной, но при интенсивном заражении под одной капсулой может быть 2, 3, 4, 5
и более личинок трихинелл.
Капсулы трихинелл вначале сильно вытянуты в длину. Начиная с одного -
полутора месяцев, на протяжении года и более гиалино-вый слой капсулы
утолщается, капсула укорачивается, участок инкапсулированной саркоплазмы
уменьшается. Капсула принимает овальную форму с сильно утолщенным гиалиновым
слоем на полю-сах. На поверхности гиалинового слоя лежит наружный тонкий слой
капсулы из клеточных элементов, преимущественно фибробластов. Наибольшее
скопление фибробластов с примесью гистиоцитов и лимфоцитов отмечается на
полюсах капсул. Когда капсула утолщается за счет гиалинового слоя, то при
микроскопии раздавленных между стеклами кусочков мышц она выглядит
двухконтурной.
Через 5 лет в капсуле начинается откладываться кальций
(В. А. Бриттов, 1962). В мышцах молодых свиней (5 – 6 мес.) капсулы личинок
трихинелл через 3 месяца имели размеры
0.56 х. 0.19 мм и толщину боковых стенок 7 – 8 мк, через 6 месяцев
соответственно – 0.52 х. 0.21 мм и 11 – 13 мк, через 8 месяцев –
0.60 х. 0.21 мм и 15 – 17 мк, через 12 месяцев – 0.54 х. 0.27 мм и 18 – 40 мк
(В. А. Бриттов, 1966).
Глава 5. Особенности эпидемиологии
синантропного очага трихинеллеза
Хозяевами трихинелл являются различные домашние и дикие млекопитающие,
преимущественно хищные, среди которых инвазия поддерживается благодаря
пищевым взаимосвязям. Кроме хищников, хозяевами трихинелл служат грызуны,
некоторые насекомоядные млекопитающие, домашние и дикие свиньи, так как эти
животные могут питаться и мясом. Естественная передача трихинелл происходит
Кроме этого, могут иметь место внутриутробное заражение и заражение кишечными
трихинеллами.
После того как были описаны трихинеллы, естественно, возник вопрос, кто же
является основным резервуаром инвазии. Основоположником «крысиной теории»
считается Leukart (1876), который полагал, что крысы, благодаря каннибализму,
является основным резервуаром трихинелл, от него черпают инвазию в первую
очередь свиньи, передавая затем человеку. Другой взгляд на распространение
инвазии был выдвинут Gerlach (1866) и Zenker ( 1871). Они считали
основными хозяевами трихинелл свиней. Инвазия от заражения свиней передается
здоровым животным через скармливание отбросов убоя и благодаря посредничеству
других животных – кошек, крыс, мышей, заражающихся также от мяса убойных
свиней. Ценкер, обосновывая эту точку зрения, отмечал наибольший процент
трихинеллезных крыс там, где они имели доступ к забиваемым свиньям. Эти факты
позже были подтверждены Staubli (1909).
Однако с накоплением сведений о распространении трихинел-леза среди многих
других животных стало очевидным, что нельзя считать основным хозяином
трихинелл какой-нибудь один вид жи-вотного. Схема В. Д. Зеленского (1929) о
взаимоотношениях хозяев трихинелл предусматривает некоторую роль различных
домашних и диких млекопитающих, но крыса опять-таки является ведущим звеном в
распространении трихинелл. Заслуга В. П. Коряжкова (1938) заключается в том,
что он впервые указал на диких животных как на основной естественный
резервуар трихинелл.
двух типов очагов трихинеллеза (Ю. А. Березанцев, 1956). Природные очаги
данной инвазии существует в дикой природе. Среди, домашних животных и
синантропных грызунов возникают и поддерживаются синантропные очаги инвазии.
Пути передачи трихинелл среди домашних животных вскрыты и изучены довольно
подробно. Трихинеллез часто находят в городах у крыс, кошек и собак, которые
не имеют непосредственной связи с дикими животными. Трихинеллез совхозных
свиней также вряд ли имеет прямое отношение к природным очагам. Эти факты
указывают на то, что трихинеллезные очаги при определенных условиях
поддерживаются самостоятельно синантропными животными. Связь таких очагов с
природными несомненна, так как возможен обмен инвазиями. Предлагаемая мной
схема основных путей передачи трихинеллеза в синантропных очагах показывает
возможные взаимоотношения алиментарного порядка между различными животными
В природных очагах циркулирует один вид трихинелл, а в синантропных –
преимущественно другой, сохраняется и возможность взаимного перехода
трихинелл из одного биоценоза в другой.
Распространение инвазии у крыс и свиней тесно связано, и они чаще других
животных способствуют возникновению синантропных очагов трихинеллеза.
Свинарники всегда привлекают крыс обилием корма. Свиньи охотно поедают труппы
грызунов, а последние часто заражаются от хранящегося трихинеллезного мяса.
Трихинеллезными очагами раньше являлись старые частные бойни, колбасные
заведения и дворы мясо- и свиноторговцев, где содержались свиньи (Н. И.
Петропавловский, 1905). Известно, что свиньи, которым скармливаются отходы
убоя, бывают инвазированы трихинеллами чаще, чем откармливаемые растительными
кормами. Трихиниллез, по свидетельству многих русских врачей, встречался
преимущественно в местностях, где свиньи содержались в плохих условиях, и,
наоборот, у свиней из крупных хозяйств, где животные находились в хороших
условиях, трихинеллез обнаруживался как исключение (Н. Н. Мари, 1912).
Сторонники преимущественной роли свиней в распространении трихинеллеза
правильно расценивали продукты и отбросы убойных свиней как один из основных
источников заражения для других животных, но они ошибались в том, что не
учитывали и другие фак-торы, имеющие большое значение в эпизоотологии
трихинеллеза. Мясная промышленность, не организованная в надлежащей степени,
является основной причиной происхождения крупных очагов трихинеллеза. В конце
прошлого столетия массовое распространение трихинеллеза наблюдалось в
Германии, США, где отсутствует контроль убойных свиней на трихинеллез, а
отходы убоя используются для откорма свиней, что способствует широкому
распространению инвазии среди домашних животных и людей. Продукты убоя
трихинеллезных животных могут быть причиной заражения не только свиней, но и
кошек, собак и крыс, которые в свою очередь передают инвазию свиньям. Свиньи
могут заражаться, поедая трупы этих животных, при безнадзорном содержании и в
условиях низкой санитарной культуры на селе и свинофермах. Чаще, по-видимому,
источником заражения свиней служат трупы грызунов. Известны случаи
трихинеллеза свиней в результате скармливания им тушек диких животных.
Герлах и Ценкер правильно считали, что так, где есть трихинеллез у крыс.
Должен быть и источник их заражения – преимущественно трихинеллезные свиньи.
Н. Н. Мари (1912) также пришел к заключению, что зараженность крыс зависит от
трихинеллезных свиней или других плотоядных животных. Следовательно, у крыс
имеется очаговое распространение трихинеллеза, но зависящее от трихинеллеза
других животных, в первую очередь – свиней.
На примере г. Ленинграда можно проследить, как одновремен-но со снижением
трихинеллеза у свиней наблюдалось резкое снижение зараженности крыс. Если
принять «крысиную теорию», то распространение трихинеллеза среди крыс и в
настоящее время должно быть таким же. Однако, как показывают обследования, в
Ленинграде трихинеллез у крыс резко снизился или исчез совсем. Постройка
мясокомбината в Ленинграде, введение обязательного микроскопического
исследования свинины на бойнях и на рынках, а также незначительная
зараженность ввозимых в Ленинград свиней привели, по-видимому, к
исчезновению трихинеллеза у крыс. Если бы крысы могли широко передавать
инвазию в своей популяции, то трихинеллез среди них существовал бы и в
настоящее время, чего, однако, не наблюдается. Каннибализм у крыс хотя и
существует, но не является широко распространенным явлением, чтобы длительно
обеспечивать передачу трихинелл без участия других хозяев. Крысы могут играть
существенную роль в распространении трихинеллеза и разносить инвазию в
соседние районы, способствуя заражению свиней, кошек и других животных. Таким
образом, крысы играют большую роль и иррадиации трихинеллезных очагов лишь
при наличии постоянного для них источника заражения.
И. В. Романов (1970) отметил, что инвазия у свиней регистри-руется только в
ареале серой крысы. Причем трихинеллез часто и постоянно регистрируется у
свиней в тех районах, где крысы обитают летом в открытой природе или часть
популяции постоянно. На этом основании он делает заключение, что крыса служит
основным источником трихинеллеза свиней и посредником между природным и
синантропным очагом.
Мыши имеют, видимо, несколько меньшее значение в распространении инвазии по
сравнению с крысами. Естественная зараженность домовых мышей встречается
очаге нашел трихинелл у мышей в 5.7% случаев. Причем зараженные грызуны были
отловлены только в кладовой, где хранилась трихинеллезная свинина.
Зараженность мышей обычно бывает ниже, чем крыс, но, тем не менее, они могут
иметь большое значение в передаче инвазии кошкам, свиньям и другим животным.
Многие недооценивают роль кошек и собак в эпизоотологии трихинеллеза. В
схемах распространения инвазии этим животным уделяется мало внимания, хотя
трихинеллы у кошек и собак встре-чаются очень часто. А.В. Меркушев (1939) при
обследовании трихи- неллезного очага обнаружил 25.7% зараженных кошек, при
трихи- неллезе свиней – 2.3%. Следовательно, кошки и собаки играют
определенную роль в распространении трихинеллеза. Их труппы могут служить
источником заражения для грызунов и свиней. Зара-женность трихинеллами
грызунов, кошек и собак постоянно регистрируется в различных странах, чаще в
Европе и Америке, но также и в других частях света.
Основной причиной, способствующей массовому распростра-нению трихинеллеза,
является неудовлетворительная организация убоя скота. Трихинеллезные очаги
обычно всегда образуются около убойных животных, так как продукты убоя и
инвазированная свинина могут являться источником заражения многих других
животных. Источником формирования таких очагов трихинеллеза является чаще
свиньи, находящиеся в личной собственности, которые при убое не подвергаются
трихинеллоскопии. Если трихинеллезная крыса уничтожается кошкой или свиньей,
то инвазированного же свиного мяса, с вязи с большим его количеством,
особенно при длительном хранении, может заразиться большое число животных.
распространения трихинелл.
Из вышеприведенных данных следует, что в любой эпизоотии наблюдается участие
не менее двух видов животных, но обычно их бывает больше. Следовательно,
существование трихинелл как вида обеспечивается биоценотическими
взаимоотношениями алиментарного порядка многих видов животных. В окружении
человека трихинеллез поддерживается домашними животными: свиньями, кошками,
собаками и синантропными грызунами: крысами и мышами. Наибольшее значение
имеют свиньи, кошки и крысы, которые очень часто при соответствующих условиях
совместно способствуют возникновению и длительному существованию очагов
трихинеллеза.
Очаги трихинелла обычно формируются в сельской местности, которые слагаются
из микроочагов инвазии на территории домо- владений, усадеб, в некоторых
хозяйствах, на звероводческих фермах и т. д. В микроочагах осуществляется
циркуляция трихинелл среди домашних животных, включая свиней и синантропных
грызунов. Из таких микроочагов инвазия распространяется в другие домовладения
того же населенного пункта с зараженными живот-ными или через инвазированную
свинину. Трихинеллы могут быть занесены в другие населенные пункты
мигрирующими животными или с зараженным свиным мясом, где при наличии
соответствующих условий могут также формироваться микроочаги. Очагами
трихинеллеза могут быть значительные территории населенных пунктов или
целиком населенные пункты.
В России с 1995 года заболеваемость трихинеллезом заметно снизилась, чему способствовало интенсивное проведение профилактических и противоэпидемических мероприятий. В 2014 году показатель заболеваемости на всей территории РФ составил 0,06 на 100 000 населения. Максимальная заболеваемость регистрируется в Дальневосточном округе (0,37 на 100 000 населения) и Сибирском округе (0,16 на 100 000 населения). На долю этих двух округов приходится 60% всех случаев заболевания. Показатель заболеваемости трихинеллезом в Амурской области превысил среднефедеральный в 30 раз.
Рис. 1. Динамика заболеваемости трихинеллезом населения РФ на 100 тысяч населения.
Патогенез трихинеллеза
При развитии трихинеллеза различают кишечную, миграционную и мышечную стадии, каждой из которой соответствует определенная клиническая картина.
Кишечная стадия
В местах локализации трихинелл под воздействием метаболитов и ферментов развивается местная воспалительная реакция. Трихинеллез на этом этапе протекает скрытно, незаметно для больного.

Рис. 2. На фото самка и самец трихинелл.
Генерализованная (миграционная) стадия
Массовая гибель личинок в миграционную стадию приводит к развитию аллергических реакций, которые приобретают еще более бурное течение в период формирования специфического иммунитета. В этот момент в крови появляется большое количество антигенов, обладающих высокой сенсибилизирующей активностью. Проницаемость сосудов резко повышается, развивается отек тканей. Аллергическая фаза развивается с 3 — 4 недели от момента заражения.
Далее наступает иммунопатологическая фаза трихинеллеза, характеризующаяся развитием системных васкулитов и тяжелых органных поражений. Поражаются легкие, сердце, центральная нервная система, желудочно-кишечный тракт и др.
Аллергические проявления бывают разной степени выраженности. При массивной инвазии развивается менингоэнцефалит, гепатит, миокардит и пневмонии со злокачественным течением. Высокая температура тела, мышечные боли, кожные высыпания, распространенные отеки — основные симптомы трихинеллеза в этот период. На 5 — 6 неделе после заражения в паренхиматозных органах развиваются дистрофические процессы.
При выздоровлении все инфильтративные изменения проходят бесследно. Дистрофические изменения восстанавливаются медленнее — в течение 6 — 12 месяцев.

Рис. 3. Личинка трихинеллы (фото слева). Личинка в капсуле (фото справа).
Мышечная стадия
В мышечной ткани личинки трихинелл проникают под сарколемму мышечных клеток, где спустя 2 недели скручиваются спирально и через 3- 9 недель инкапсулируются. Постепенно новые личинки прекращают поступать в кровь. Капсула защищает личинку от воздействия негативных факторов внешней среды и выполняет функцию питания и утилизации продуктов обмена. Далее спустя 6 — 18 месяцев она начинает пропитываться солями кальция и обызвествляется. Личинки в такой капсуле сохраняют жизнеспособность до 25 лет и более.

Признаки и симптомы трихинеллеза у человека
Клиническая картина трихинеллеза характеризуется наличием 4-х признаков:
- Лихорадка.
- Отечный синдром.
- Миалгия (мышечные боли).
- Эозинофилия.
В зависимости от массивности инфицирования трихинеллез может протекать в стертой, легкой, средней тяжести и тяжелой формах. К атипичной относятся бессимптомная и стертая формы трихинеллеза. Стертое течение трихинеллеза регистрируется при вспышках в 20 — 30% случаев, легкое и течение средней тяжести — у 50 — 60% больных, тяжелое течение — у 10 — 30% больных.
В течении заболевания различают острый период и период выздоровления (реконвалесценции).
Инкубационный период трихинеллеза
Инкубационный период трихинеллеза может быть коротким — от 5 до 8 дней и длительный — от 28 до 45 дней.
- При легком течении инкубационный период удлиняется до 45 дней.
- При тяжелом течении он составляет 7 — 10 дней.
- При злокачественном течении заболевания инкубационный период укорачивается до 1 — 3 дней.
Лихорадка
Лихорадка является признаком общей интоксикации. При трихинеллезе она может длиться 1 — 6 недель. В острый период температура тела поднимается до 40 о и удерживается на этом уровне несколько дней. При хроническом течении температура тела может быть субфебрильной и сохраняется месяцами. Лихорадка проявляется слабостью, ознобами, головными болями, тошнотой.
- При легких формах трихинеллеза лихорадка может отсутствовать.
- При заболевании средней тяжести температура тела нарастает в течение 1 — 4 дней.
- При тяжелой форме заболевания тела нарастает в течение 13 — 20 дней.
Отеки
Отеки век, лица и конъюнктивит — постоянные признаки трихинеллеза. В некоторых случаях у больных появляются отеки рук и нижних конечностей.
- При легкой и среднетяжелой степени трихинеллеза отмечается одутловатость лица, отек век, надбровных дуг и конъюнктивит. Отеки развиваются быстро (на 1 — 5 день заболевания) и держатся в течение 1 — 2, реже 3 недель.
- При тяжелом течении трихинеллеза отеки развиваются медленно, достигают максимума в более поздние сроки и держатся долго. Отеки появляются не только на лице, но и на шее, туловище и конечностях. В ряде случаев отмечаются отеки рыхлой клетчатки внутренних органов, оболочек и паренхимы мозга. Поражение мозга приводит к функциональным нарушениям центральной нервной системы.

Рис. 5. Отеки при трихинеллезе: отеки век (слева на фото), отек конъюнктивы (справа на фото).
Мышечные боли
Мышечные боли появляются у больных через 1 — 3 и более дней от начала и являются постоянным признаком трихинеллеза.
- При легкой и среднетяжелой степени трихинеллеза боли мышцах появляются на 1 — 3 и более день от начала заболевания. Вначале боли появляются в мышцах нижних конечностей, далее в ягодичных мышцах, мышцах спины и живота, рук и шеи, языка и глотки, глазных и затылочных мышцах.
- При тяжелом течении трихинеллеза боли в мышцах появляются очень рано, у части больных регистрируются тяжелые миалгии с развитием контрактур.
Эозинофилия
Эозинофилы в крови при трихинеллезе повышаются до 50 — 60%. В ряде случаев количество эозинофилов может достигнуть 80 — 90%, что является неблагоприятным прогностическим признаком. Одновременно в крови отмечается повышенный уровень лейкоцитов — до 10 — 30 тыс. в одном микролитре.
- При легком течении эозинофилия достигает максимума на 4-й неделе заболевания и составляет до 30%.
- При среднетяжелом течении эозинофилия достигает максимума на 3-й неделе заболевания и составляет до 60%.
- При среднетяжелом течении эозинофилия достигает максимума на 2-й неделе заболевания и составляет более 60%.
- У больных после выздоровления эозинофилия в пределах 10 — 15% сохраняется до 3-х и более месяцев.

Рис. 6. Эозинофилия — постоянный признак трихинеллеза. На фото слева эозинофил, на фото справа — множество эозинофилов в крови.
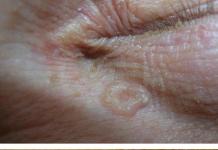
Аллергический дерматит
При трихинеллезе часто развивается аллергический дерматит. На кожных покровах появляется полиморфная сыпь эритематозно-папулезного характера. При крайне тяжелом течении заболевания развивается геморрагическая сыпь.

Рис. 8. Аллергический дерматит при трихинеллезе.
Легочный синдром
«Летучие» или эозинофильные инфильтраты при трихинеллезе часто сопровождают эозинофилию разной природы. При трихинеллезе средней тяжести и тяжелом течении данная патология регистрируется у 1/3 больных. Ведущую роль в их появлении играет сенсибилизация организма, развившаяся в результате глистной инвазии. «Летучие» инфильтраты носят мигрирующий характер, они нестойки и исчезают в течение 2 — 3 дней. Инфильтрат образуется в результате выхода в альвеолы экссудата, содержащего большое количество эозинофилов. Обнаруживаются такие инфильтраты случайно при рентгенологическом исследовании. Симптомы заболевания скудные. Иногда больных беспокоит кашель с небольшим количеством мокроты. У некоторых больных появляются приступы бронхиальной астмы и плевриты. При очень тяжелом течении трихинеллеза у части больных возникает пневмония со злокачественным течением.

Рис. 9. На фото эозинофильные инфильтраты при глистной инвазии.
Признаки и симптомы трихинеллеза при поражении сердца
При высокой температуре тела у больных трихинеллезом появляются симптомы нарушения в работе сердечно-сосудистой системы — тахикардия и одышка. При аускультации прослушивается систолический шум на верхушке и отмечается глухость сердечных тонов.
При тяжелом течении трихинеллеза у части больных развивается картина миокардита аллергической природы. Глухость сердечных тонов, тахикардия, нарушение сердечного ритма — основные симптомы заболевания. На ЭКГ появляются признаки диффузных изменений миокарда и коронарные нарушения. В ряде случаев (чаще у пожилых больных) развивается недостаточность кровообращения.

Рис. 10. Красным обозначена воспаленная сердечная мышца.
Признаки и симптомы трихинеллеза при поражении желудочно-кишечного тракта
В 25% случаев при трихинеллезе развивается абдоминальный синдром.
- Тошнота, рвота, боли в животе и жидкий стул — основные симптомы поражения желудочно-кишечного тракта.
- При тяжелом течении заболевания у больных появляется тошнота и рвота, в жидком стуле появляются примесь крови и слизи. Язвенно-некротические процессы в слизистой оболочке желудка и кишечника с последующей перфорацией и кровотечением становятся причиной смерти больного.
Неврологические симптомы
В ряде случаев при трихинеллезе отмечаются отеки паренхимы и оболочек мозга, что приводит к функциональным нарушениям центральной нервной системы. В остром периоде при тяжелом течении заболевания больных беспокоит бессонница и головные боли, иногда галлюцинации и депрессия, появляются симптомы, характерные для энцефаломиетита и менингоэнцефалита. В очень тяжелых случаях у больных появляются судороги, бред, эпилептические припадки и психические расстройства.

Рис. 11. Личинки трихинелл в мышечной ткани под микроскопом.
Продолжительность заболевания
Чем тяжелее симптомы трихинеллеза, тем длительнее протекает гельминтоз.
- При стертой форме трихинеллез длится не более 1-й недели.
- При легкой форме трихинеллез длится не более 2-х недель.
- При трихинеллезе средней тяжести и тяжелом течении на фоне гормонального лечения острая фаза укорачивается, но выздоровление наступает только к 4 — 6 месяцу. Мышечные боли могут беспокоить больного еще 1 — 2 месяца после выздоровления, эозинофилия в пределах 10 — 15% сохраняется до 3-х и более месяцев.

Рис. 12. Отеки при трихинеллезе.
Трихинеллы под микроскопом
Осложнения трихинеллеза
- Одним из самых опасных осложнений трихинеллеза является аллергический миокардит.
- Со стороны органов дыхания опасным осложнением является астматоидный бронхит и пневмония со злокачественным течением.
- Язвенно-некротические процессы в слизистой оболочке желудка и кишечника с последующей перфорацией и кровотечением в ряде случаев становятся причиной смерти больного.
- Со стороны центральной нервной системы при тяжелой форме трихинеллеза, чаще у мужчин, развиваются эпилептиформные приступы, тяжелые истерии, психозы, парезы и параличи. В ряде случаев трихинеллез является причиной развития менингоэнцефалита и энцефаломиелита.
- Флеботромбозы нижних конечностей являются следствием нарушения гемостаза и системы свертывания крови. Тромбоз сосудов головного мозга приводит к развитию параличей верхних и нижних конечностей.
- Ослабление иммунной системы приводит к развитию бактериальной инфекции.

Рис. 13. На фото трихинеллы в мышечной ткани.
Прогноз заболевания
Неосложненный трихинеллез всегда заканчивается благоприятно. Осложненное течение заболевания в 5% случаев заканчивается летальным исходом. При очень тяжелой форме трихинеллеза летальность достигает 10 — 30%. Основной причиной смерти больных является аллергический миокардит и поражение центральной нервной системы.
Федеральное агентство по образованию
Московский Государственный Университет
Прикладной Биотехнологии
Ветеринарно-санитарный факультет
Курсовая работа
На тему: «КЛИНИКА И ЛЕЧЕНИЕ ТРИХИНЕЛЛЕЗА»
Выполнила: студентка 5
курса 9группы
Вет-сан фак-та
Нестерова Е.А
Проверил: Косминков Н.Е
МОСКВА 2007
Введение
Краткие исторические сведения о трихинеллах и трихинеллезе
Современное описание вида
Морфология и биология трихинелл
Распространение трихинелл в природе
Роль трихинелл в биоценозах
Патогенез
Иммунитет
Диагностика
Профилактика и меры борьбы
Трихинеллез у человека
Эпидемиология
Мероприятия по борьбе с трихинеллезом
Антитрихинеллезная вакцина и ее роль в восстановлении здоровья человека
Литература
ВВЕДЕHИЕ
Тpихинеллёзы - группа инвазий, вызываемых нематодами pода Trichinella. До 70-х годов считалось, что этот pод представлен одним видом - T. spiralis, но тепеpь выдвинуты веские доказательства в пользу того, что это комплекс близких в моpфологическом отношении видов: T. spiralis, T. nativa, T. pseudospiralis. . Экспериментально трихинеллезом заражаются все виды млекопитающих животных и многие виды птиц.
Краткие исторические сведения о трихинеллах и трихинеллезе
Человек стал заражаться трихинеллезом, надо полагать, с момента употребления мясной пищи. Безусловно, до использования огня заражение трихинеллезом происходило чаще, нежели в последующие времена, когда большая часть мясной продукции обезвреживалась термической обработкой. Кроме того, человек, исходя из опыта, постепенно научился различать виды и даже части животных, от употребления которых возникает болезнь.
В связи с этим появились определенные традиции в употреблении мяса различных видов животных. Например, народы Севера и Дальнего Востока из-за суровой и длительной зимы испытывали недостаток в витаминах, ферментах, гормонах и других биологически активных веществах, а также микроэлементах, которые они вынуждены были пополнять за счет потребления сырого мяса. Это повысило вероятность заболевания трихинеллезом. Но постепенно люди стали замечать, что болезнь возникает от употребления в сыром виде мяса медведей и моржей. Поэтому мясо этих видов животных стали варить, а сырыми употребляли только мозги, печень, сухожильную часть ласт (у моржей), где, как известно, трихинелл не бывает. Это подтверждается также обычаями “медвежьего” праздника, ранее распространенного у большинства народов Дальнего Востока.
Медведя к празднику не добывали в тайге, а специально выращивали в течение 3-4 лет в специальном помещении вблизи дома. Кормили его особо доверенные люди с соблюдением строгих правил. Нельзя было давать медвежонку сырое или жареное мясо. Даже в обуви из копченой рыбьей кожи нельзя было подойти к клетке с медведем. Это считалось величайшим оскорблением не только медведя, но и духа “хозяина тайги”.
Перед убиением медведя водили по домам, затем его привязывали к специальному столбу и убивали из лука. Ульчи мясо ритуального медведя ели сырым, а айны медвежатину варили. Мозги, сердце и другие внутренние органы солили. Медвежий праздник справляли так же орочи, удэгейцы, нанайцы. Подобные привычки и традиции аборигенов по избирательному употреблению мяса дошли до настоящего времени и в значительной степени предохраняют их от заражения трихинеллезом. Наблюдавшиеся в последние годы вспышки трихинеллеза в Сибири и на Дальнем Востоке регистрировались в основном у приезжего населения и очень редко у аборигенов.
Теперь уже точно доказано, что ряд экспедиций, отправлявшихся различными путями в Арктику в конце XIX и начале ХХ столетия, не смогли выполнить своих задач по причине развившегося среди членов экспедиции трихинеллеза, заканчивавшегося нередко летально. Как сообщает И. Евер, многие зимовщики болели трихинеллезом, полагая, что страдают от цинги. Оказывается, они заражались через мясо белых медведей, которые поражены трихинеллами почти поголовно. В настоящее время, чаще через мясо бурых медведей, заражаются геологи, охотники и туристы.
С одомашниванием свиньи около 7 тыс. лет назад угроза заражения людей трихинеллезом резко возросла. Но осознание этой угрозы человечеством шло чрезвычайно медленно.
Понятие вера (в арабском языке слово "иман" является производным от корня "обеспечивать безопасность") в сознании мусульман связана, прежде всего, со Знанием. И достижение "безопасности под сенью Бога" предполагает, соответственно, неукоснительное выполнение Божественных законов и предписаний.
Предписания, имеющие отношение к заботе о здоровье человека, имеющиеся в Священных Писаниях, подтверждаются как многолетним опытом, так и научными фактами. Одним из таких предписаний является запрет на потребление в пищу свинины.
"Верующие! Ешьте из тех благих снедей, какими Мы наделяем вас, и благодарите Бога, если вы Ему поклоняетесь. Он запретил вам в пищу мертвечину, кровь, свинину и то, что было заколото с именем других, а не Аллаха. Но кто принужден будет к такой пище, не будучи своевольником, нечестивцем, на том не будет греха: Бог прощающий, милостивый"
(Священный Коран 2:172, 173)
Такое же предписание имеется и в Библии:
"А свинья, хотя копыта раздваивает, но жвачки не жует, нечиста она для вас; мяса их не ешьте и к трупам их не прикасайтесь"
(Второзаконие 14:8, Библия)
В 1288 г. до н.э. при Рамзесе II пророк Моисей запретил евреям есть свинину, как полагают, по причине трихинеллеза и солитера. В то время сбежавшие из египетского плена евреи странствовали по пустыне и им приходилось есть все, что, как говорится, Бог послал. Вероятно, среди них возникали серьезные заболевания именно после употребления в пищу свинины. Позднее жрецы разделили животных на чистых и нечистых, и был введен запрет на употребление в пищу мяса последних в намерении выделить богоизбранный народ из среды других языческих народов. Эти положения вошли в Библию. “Вы сыны Господа Бога вашего, не ешьте никакой мерзости. Вот скот, который вам можно есть: волы, овцы, козы, олень и серна, и буйвол, и лань, и зубр, и орикс, и камелопард. Всякий скот, у которого раздвоены копыта и на обоих копытах глубокий разрез, и который скот жует жвачку, тот ешьте; только сих не ешьте из жующих жвачку и имеющих раздвоенные копыта с глубоким разрезом: верблюда, зайца и тушканчика, потому что хотя они жуют жвачку, но копыта у них не раздвоены: нечисты они для вас; и свиньи, потому, что копыта у них раздвоены, но не жуют жвачки: нечиста она для вас, не ешьте мяса их, и к трупам не прикасайтесь. Из всех животных, которые в воде, ешьте всех, у которых есть перья и чешуя, а всех тех, у которых нет перьев и чешуи, не ешьте: нечисто это для вас. Всякую птицу чистую ешьте. Не ешьте никакой мертвечины; иноземцу, который случится в жилищах твоих, отдай ее, он пусть ест ее, или продай ему, ибо ты народ святой у Господа Бога твоего” .
Конечно, тогда о трихинеллах ничего не знали, но факты заболевания людей после употребления в пищу свинины были уже накоплены. Через два тысячелетия Мухаметт ввел этот запрет и для мусульман, а у остальных цивилизованных народов профилактика трихинеллеза через свинину стала осуществляться только со второй половины XIX в., когда был уже открыт один из возбудителей трихинеллеза Т.spiralis Owen, 1835.
После этого открытия трихинеллез стали регистрировать во многих странах Европы. Особенно часто трихинеллезом болели в Германии. Болезнь сопровождалась сильными болями, высокой температурой, значителен был показатель летальности, а также инвалидности. Трихинеллез приобрел устрашающее влияние, и многие высокообразованные люди очень боялись этой болезни. Описан анекдотический случай, который произошел с “железным” канцлером Германии Бисмарком и крупным ученым Рудольфом Вирховым. По какому-то поводу они повздорили, и канцлер, как бывший военный, вызвал Вирхова на дуэль. Вирхов дуэль принял, но оставил за собой право выбора оружия. В качестве такового он предложил две сосиски, одна из которых была приготовлена из трихинеллезного мяса. Бисмарку предлагалось выбрать сосиску и съесть. Однако Бисмарк предпочел от дуэли отказаться. Это свидетельствует о том, насколько в то время общественность Германии была напугана трихинеллезом.
Не оставил без внимания трихинелл Ф. Достоевский, а вслед за ним – Максимилиан Волошин.
“Появились новые трихины…”
Ф. Достоевский
Исполнилось пророчество: трихины
В тела и дух вселяются людей.
И каждый мнит, что нет его правей,
Ремесла, земледелия, машины
Оставлены. Народ, племена
Безумствуют, кричат, идут полками,
Но армии себя терзают сами,
Казнят и жгут: мор, голод и война.
Ваятель душ, воззвавший к жизни племя
Страстных глубин, провидел наше время:
Пророчественною тоской объят.
Ты говорил, томимый нашей жаждой,
Что мир спасется красотой, что каждый
За всех, во всем, пред всеми виноват.
Коктебель.
Основание для страхов, конечно, было, ведь трихинеллез до 1960 г. считался неизлечимым.
Приоритет открытия возбудителя трихинеллеза принадлежит Джеймсу Педжету, студенту первого курса медицинского колледжа в Лондоне. Он анатомировал труп итальянца и заметил мелкие белые крупинки извести. Заинтересовавшись находкой, посмотрел их под микроскопом (тогда в Лондоне было только два микроскопа, и получить доступ к ним студенту первого курса было не так-то просто) и обнаружил в известковых крупинках червя. Вскоре Педжет доложил о своем открытии на заседании Научного общества в Лондоне, не указав, однако, систематического положения обнаруженного им организма.
Кусочек мышц от этого же трупа был доставлен для исследований зоологу Ричарду Оуэну, который на десять лет был старше Педжета и уже имел положение в науке. Он и описал находку, дав название червячку Т.spiralis, поскольку в охлажденном спокойном состоянии он приобретал вид спирали из 3-4 витков.
Современное описание вида
По современным данным взрослые самцы (имаго) 1,4-1,6 мм длиной при ширине до 0,04 мм. На заднем конце тела располагаются две пары сосочков. Семенник лежит в задней части, семяпровод образует небольшое расширение – семенной пузырек – и открывается в клоаку. Самки вдвое крупнее самцов, длиной около 3-4 мм при максимальной ширине 0,06 мм. Яичник располагается в задней части тела и через узкий яйцевод соединяется с широкой маткой, направляющейся кпереди. Отверстие вульвы лежит на уровне передней пятой длины тела. Анус расположен терминально. Живородящие организмы.
Каждая самка может отродить до 1500 личинок. Имаго живут в тонком отделе кишечника, а личинки развиваются внутри волокон скелетных мышц. При достижении инвазионности (19 дней от момента заражения хозяина) вокруг личинки начинает формироваться капсула, стенки которой со временем утолщаются. Вид хорошо адаптирован ко многим млекопитающим, в том числе к свиньям и человеку, несколько хуже к канидам; легко заражаются кошки и мышевидные грызуны, а также травоядные животные, если каким-то образом им попадает зараженное трихинеллами мясо. Не имеет определенного ареала. Распространение его связано с хозяйственной деятельностью человека, прежде всего с разведением свиней. Личинки чувствительны к замораживанию, но в крупных кусках при минус 8-10° С в камере сохраняют инвазионность несколько недель и даже месяцев.
Группа Е. Поцио, проанализировав 61 изолят Т.spiralis из разных мест обитания, выделила три внутривидовые фенотипические популяции, различающиеся по двум ферментам. Но эти различия несущественны и выявляются только путем изоферментного анализа. Морфологически они немного различаются по конфигурации капсул вокруг личинок.
Вид Т.spiralis, описанный Р. Оуэном в 1835 г., занимал монопольное положение в роде Trichinell до 1972 г., когда были описаны сразу три новых вида: Т.nativa, T.nelsoni и T.pseudospiralis.
Т.nelsoni Britov, Boev, 1972. Первоначально личинки трихинелл выделены от пятнистой гиены Национального парка им. Крюгера из Южной Африки. Доктор С.В. Крюгер любезно прислал нам этих трихинелл в мышцах лабораторных мышей. До наших исследований они именовались, как впрочем, и все другие трихинеллы, Т.spiralis. Однако Г.С. Нельсон с сотрудниками в 1961 г., когда исследовали трихинелл от людей, заразившихся через мясо дикой свиньи в Кении, обратили внимание на ряд особенностей кенийских трихинелл. В настоящее время нет возможности точно установить с каким видом африканских трихинелл работала группа Нельсона, так как в 1992 г. стало очевидным, что в Кении и Танзании имеется обособленная популяция трихинелл, условно обозначенная G.La Rosa et al. как Т7, о которой будет сказано позднее.
По нашим данным вид представлен двумя популяциями: Южно-Африканской с эллипсовидной формой капсул вокруг личинок и Евро-Азиатской с шаровидной формой капсул. По результатам изоферментного анализа вид оказался весьма изменчивым (определены пять вариаций). Вероятно, это связано с экологическим своеобразием среды обитания. Ведь внешние условия в регионе 30-ой параллели Южного полушария и 50-ой параллели Северного полушария (ареал вида) не могут быть одинаковыми.
По изоферментному анализу у вида T.nativa имеется восемь вариантов. Однако эти различия фенотипические и между всеми вариантами происходит свободное скрещивание.
T.pseudospiralis Garkavi, 1972. Впервые выделен от енота-полоскуна на Северном Кавказе. Эволюционно это, вероятно, самый древний из ныне известных видов трихинелл. Единственный представитель рода, свойственный, кроме млекопитающих, и птицам.
Ареал вида прерывистый. Он встречается в Европе, Азии и в австралийском регионе.
В работах группы Е. Поцио описаны 4 биологические единицы трихинелл, неопределенного таксономического ранга, обозначенные первоначально как Т.5; т.6; Т.7; т.8 и обосновывается вид Т.britovi. При классификации трихинелл они использовали фенотипический признак - расположение полос в геле при ферментативном анализе. Наши исследования, основанные на генетическом признаке (скрещиваемость или отсутствие такового с эталонными видами), показали, что изоляты Т.britovi свободно скрещиваются с обеими популяциями T.nelsoni, описанными нами ранее. Но изолят T.7 из Экваториальной Африки не скрещивается ни с одним из известных видов трихинелл. Этот изолят, следовательно, отвечает требованиям самостоятельного вида.
Недавнее описание видов T.murrelli и T.papua также основано на фенотипических признаках.
Описанию новых видов трихинелл предшествовали длительные и шумные баталии.
А.Г. Казаринов и В.Ю. Калюс четко высказывались о возможном существовании в природе разных “штаммов” трихинелл. Но все это были скорее догадки, необоснованные доказательствами. Е.Т. Маширов (1960) пытался пассировать трихинелл от обыкновенных лисиц на поросятах, но не мог получить достаточное количество личинок у них для вторичного пересева на свиньях. Личинки трихинелл в мышцах поросят погибали, еще не достигнув инвазионности. Но он не смог дать объяснений результатам своих наблюдений. Мысль о существовании в природе другого, кроме T.spiralis, вида трихинелл была в то время крамольной, и никто не посмел возразить таким авторитетам, как Р. Лейкарт, Ф. Ценкер, Р. Вирхов, К.И. Скрябин. Только в шестидесятых годах Э.Р. Геллер начал развивать идею о штаммах трихинелл, хотя никаких доказательств на этот cчет не приводил. Вероятно, ему тоже было страшно об этом говорить, и для большей смелости он уговорил в компаньоны проф. А.М. Петрова. Так велик был гипноз авторитетов. Но существовала еще одна серьезная причина, из-за которой монополия единственного вида в роде трихинелл удерживалась почти 140 лет. Это отсутствие критериев различия. В век господства морфологических признаков, по которым описывались виды в гельминтологии, этого сделать было невозможно, так как морфологически все виды трихинелл сходны. Нужен был иной подход, другие методы исследований.
Стимулом к поиску других приёмов и методов служили два объективных факта – это несоответствие трихинеллеза диких животных с трихинеллезом свиней (у диких животных трихинеллы имеются повсеместно, а у свиней - очагово) и слабая адаптивность трихинелл диких животных к свиньям и крысам. Новый подход, как говорится, лежал на поверхности. Это тройной зоологический критерий вида: виды генетически изолированы (нескрещиваемость), между самыми близкими видами всегда обнаруживается хиатус (разрыв), виды обладают самостоятельным ареалом. Самостоятельный ареал – это по сути дела прямое следствие генетической изоляции. Один подвид не может существовать в ареале другого, так как в результате скрещивания они сольются в единое целое. И, наоборот, генетическая изоляция вида позволяет ему проникать в ареал другого, даже наиболее близкого.
При такой раскладке фактов самые простые логические рассуждения приводят к выводу: чтобы окончательно прояснить вопрос о “штаммовости” трихинелл, их необходимо испытать на скрещиваемость. Первые опыты по скрещиванию трихинелл были опубликованы в 1969 г. Суть их сводилась к тому, что трихинеллы от диких животных не скрещивались с трихинеллами от свиней. Стало очевидным, что испытуемые трихинеллы принадлежат к разным видам. Решающий шаг к познанию проблем трихинелл и трихинеллеза был сделан. Как здесь не вспомнить Руссо, который когда-то сказал, что тысячи путей ведут к заблуждению, к истине – только один. Несколько позднее не раз и не два я возвращался к вопросу о том, почему Г. Нельсон и Э.Р. Геллер, основные пропагандисты идеи о “штаммовости” трихинелл не применили метод скрещивания, известный еще первобытному человеку? Ведь это так просто.
На одной из международных встреч Г. Нельсон публично поблагодарил авторов, которые назвали новый вид трихинелл в честь его имени, но высказал скептическое отношение по этому поводу. На письменный вопрос: “Скрещивали ли Вы трихинелл из Кении с T.spiralis?” Г. Нельсон ответил: “Гибридизацией трихинелл мы не занимались. Сложность генетических исследований состоит в том, что результаты очень сомнительны и могут ввести в заблуждение, так как испытания проводятся на свежих изолятах, взятых из естественных условий с различными экологическими районами, пассирование через лабораторных животных неизбежно меняет свои характеристики под селективным давлением, испытываемым у их новых хозяев. Различия в результатах этих данных по проблеме можно проследить в ваших работах и работах Е. Мееровича из Канады”.
Академик В. Стефанский из Варшавы в личном письме сообщил: “Ваша работа свидетельствует о наличии в природе трех самостоятельных генетически изолированных единиц трихинелл, которых автор признает вариететами. С этим последним тезисом не все будут согласны”.
Так оно и случилось. Ведь наши данные противоречили старой концепции о неделимости вида Т.spiralis, который свойственен всем видам животным-трихинеллоносителям. Они отвергали сложившееся мнение, что основными виновниками заражения свиней трихинеллезом являются дикие животные.
Основной смысл выявленных нами закономерностей сводился к следующему: 1) в дикой природе циркулируют природные трихинеллы T.nativa и T.nelsoni, а в синантропных очагах (в поселениях человека) – T.spiralis; 2) главный путь передачи синантропной трихинеллы совершается от свинины к свинье. Дикие животные, зараженные природными трихинеллами, никакого участия в передаче синантропной трихинеллы и в формировании синантропных очагов инвазии не принимают.
Наиболее мощное сопротивление концепции новых видов трихинелл оказывал ВИГИС в лице А.С. Бессонова. В официальном отзыве на докторскую диссертацию в частности говорилось: “…вышесказанные диссертантом положения существенно меняют общепринятые представления о медико-ветеринарном значении трихинеллеза диких животных, а также методический подход к планированию и осуществлению профилактических мероприятий при трихинеллезе в очагах различных типов. Можно с уверенностью утверждать, что, если данные В.А. Бритова о генетических различиях трихинелл подтвердятся другими исследователями, их следует рассматривать как серьезное открытие в области ветеринарной гельминтологии.
К сожалению, приходится делать оговорку по поводу признания этого открытия, поскольку материалы, отражающие основное содержание диссертации не опубликованы в печати… Сказанное является серьезным нарушением инструкции ВАКа, и поэтому диссертацию в представленном виде вряд ли можно допустить к защите”.
Для проверки результатов скрещивания из Москвы в Благовещенск прибыла комиссия. Через 34 дня после ее работы было сделано следующее заключение: “Два изученных вариетета трихинелл (Т.s. var. domestica от домашних свиней и T.s. var. nativa от енотовидной собаки и белого медведя) генетически изолированы, что целиком и полностью подтверждает данные В.А. Бритова. Комиссия считает, что правильность методических подходов для решения вопроса о генетической изоляции вариететов трихинелл не вызывает сомнения”. Подписи: председатель комиссии канд. биол. наук Г.А. Ермолин, члены: канд. биол. наук В.И. Тараканов и др. (Акт от 29 марта 1971 г., Благовещенск).
Результаты работы комиссии вскоре были опубликованы в печати. Надо отдать должное высокой порядочности и большому напряжению физических и духовных сил всех членов комиссии, благодаря которым и стало возможным проведение такой изнурительной работы. Они выполнили свою миссию как честные труженики науки. Из Москвы в Казань, где лежала диссертация, пошел уже другой, хвалебный отзыв за подписью акад. В.С. Ершова. И естественно возражения против защиты диссертации были сняты. Но председатель комиссии Г.А. Ермолин лишился места работы в ВИГИСе (разумеется, по другой причине). По сути дела борьба с новыми воззрениями на проблему трихинелл и трихинеллеза только начиналась. В дискуссию по этому вопросу втягивались все новые и новые исследователи.
В начале февраля 1974 г. из ВИГИСа пошло письмо к проф. Е. Мееровичу (Канада) с просьбой высказать свое отношение к работам В. Бритова. В письме от 22 февраля 1974 г. Е. Меерович ответил, что в их лаборатории “проводили исследования по скрещиванию трихинелл из разных регионов мира, но наши результаты не совпадают с данными В. Бритова, и я не знаю, чем это объяснить. Мы получили так называемых “гибридов” в мышцах, хотя не во всех мышах… Конечно, не исключается возможность, что это действительно виды, но они все равно скрещиваются между собой, хотя в таких случаях более правильно называть их подвидами. Это все, что у меня имеется по этому вопросу. Я имею большое уважение к работам док-ра Бритова, так как видно, что он очень усердно и старательно проводит свои опыты, и каждому понятно, что все это требует массу усилий и времени. Или у нас разные вариететы, или кто-то ошибается в своих выводах. Надо чтобы еще несколько работников в разных лабораториях провели бы эту работу. Я слышал, что Командарев в Болгарии тоже получил результаты, отличающиеся от результатов Бритова. Мне это сказала док-р Озерецковская, с которой я встречался в Афинах прошлой осенью”.
Приведенная весьма пространная выдержка из письма проф. Е. Мееровича свидетельствует о его действительно научном и доброжелательном стремлении разобраться в таком сложном вопросе, как систематика трихинелл. Из его подробного письма с приложением рисунка и описанием методики скрещивания сразу стало ясно, почему у него получались так называемые “гибриды” - он использовал случайные критерии при разделении личинок по полу. Часть личинок самцов он принимал за самок и наоборот. Отсюда “гибриды”. Позднее он полностью согласился с нашими данными о валидности видов T.nativa и T.nelsoni.
Серию работ по изучению трихинелл разных изолятов опубликовал Т.А. Дик со своими студентами. И хотя ими получены четкие различия между T.spiralis, T.pseudospiralis, T.nativa, по некоторым фенотипическим признакам, генетической разницы они не заметили. Все виды трихинелл у них не скрещивались только в однопарных вариантах, когда дается, например, одна самка исследуемого изолята и один самец эталонного вида и наоборот, но скрещивались в многопарных вариантах, когда давалось, например, по 10 самок исследуемого изолята и по 10 самцов эталонного вида и наоборот. Выше уже говорилось, что если среди десяти личинок будет одна личинка противоположного пола, независимо исследуемого или эталонного вида, в мышцах мыши непременно разовьются несколько сотен личинок новой генерации того вида, в представителях которого была допущена ошибка, и это принимается за скрещиваемость исследуемых трихинелл, хотя они могут быть разными, генетически несовместимыми видами.
Проф. Т.А. Дик делает странное умозаключение, что в однопарных вариантах трихинеллы от свиньи не дают потомства с трихинеллами от диких канид и с T.pseudospiralis, но поскольку они все скрещиваются в многопарных вариантах, их нельзя считать не только видами, но они не тянут даже на подвиды. Если бы авторы проверили своих “гибридов” по любым критериям, но лучше в однопарных скрещиваниях, что у них правильно получается, они легко бы могли убедиться, что их “гибриды” представляют собой один из материнских видов и не несут никаких признаков другого вида, если, конечно, ошибка в отборе была только в одном изоляте. Если же ошибка была допущена в обоих скрещиваемых популяциях, то потомство новой генерации личинок у мыши будет двух видов, но не гибридов. Их можно разделить путем промораживания мышц подопытной мыши. Личинки T.spiralis от свиньи при минус 20° С погибнут за два-три дня, а T.nativa от волка останутся живыми. Можно смешанную двувидовую инвазию разделить путем однопарного скрещивания с эталонными видами. Наиболее наглядный метод – наблюдение эмбриогенеза. При межвидовом скрещивании эмбрионы либо не образуются вообще, либо они гибнут в массовом количестве в матке самок.
Если же допустить возможность, что при многопарном скрещивании получаются межвидовые гибриды, то тогда можно было бы получать гибридов между любыми видами животных и растений. Но так не бывает. Любой индивид имеет геном только своего вида, но не другого. И сколько бы спермы, например хряка (хоть от тысячи самцов) ни вводили, скажем, овце, корове, крольчихе, ни поросят, овцесвиней и прочих гибридных потомков не получишь. В том то и суть, что все ныне известные виды трихинелл достигли в своей эволюции такого уровня, что обмен генами между ними в естественных условиях не происходит.
С многосторонней критикой в адрес авторов новых видов трихинелл выступил Г. Мадсен. Автор не проводил самостоятельных исследований по систематике трихинелл, но хорошо знаком с литературой по этому вопросу. Имея “твердые убеждения” в неделимости вида T.spiralis, он привел самые разнообразные факты, суждения и домыслы, которые якобы опровергают самую возможность существования в природе других видов трихинелл. Здесь нет необходимости пускаться в полемику с автором упомянутой статьи, так как новые виды трихинелл – объективная реальность. Но посмотрите, как живучи старые догмы и заблуждения, с какой энергией их защищают, какие методы для этого используют. Все годится, что против нового!
Споры продолжаются до сих пор, хотя накал страстей заметно ослаб и произошел явный перевес в сторону новых знаний. Прав Шиллер, сказав, что истина ничуть не страдает от того, что если кто-либо ее не признает.
Из истории науки известно, что, если истина вскрыта, она пробьет себе дорогу, невзирая на яростное сопротивление сторонников устоявшихся мнений. Мне кажется, что все было бы по-другому, спокойнее и проще, если бы во время разыгравшихся баталий вокруг новых видов трихинелл был бы жив проф. З. Козар. В научных вопросах он был святым, страстным сторонником истины.
Проф. В. Гейзенберг по поводу подобных ситуаций писал: “Для того чтобы порвать со старыми концепциями, требуются невероятно большие усилия, и обычно бывает гораздо проще найти новые концепции, чем отделаться от старых”. Этому нередко препятствует узкая специализация в пределах одной науки.
Некоторые считают, что сопротивление ученых научному открытию есть постоянно действующий фактор в науке, под его влиянием находятся все ученые либо в качестве испытывающих сопротивление, либо в качестве сопротивляющихся новым идеям. Социологи давно подметили, что когда один ученый судит о работе другого, он склонен слишком высоко оценить то, что ему самому было трудно сделать, и склонен недооценить то, что у него самого, как он думает, могло бы получиться. Л.С. Салямон, сравнивая восприятие общепринятых и канонизированных сведений и новых идей, находит в этом большое различие. Первое воспринимается легко и безболезненно, второе - вызывает более сложные психологические композиции, такие как новая идея… “сформулирована Моим современником, которая совершает надо Мною насилие, заставляет изменить Мои прежние и привычные установки”. Применительно к нашей ситуации к этому следует добавить, что если автор идеи еще крестьянский мужик, работающий где-то на задворках России, не носит галстука, а предметные стекла вытирает халатом – как же я буду ему верить!
Когда мы втроем (С.Н. Боев, И.В. Орлов и я) шли с конференции в гостиницу, И.В. Орлов сказал примерно так: “Хотя мы с С.Н. Боевым сами не проводили скрещивание трихинелл, но мы тебе верим, и будем поддерживать новую идею в науке”. Для меня это было бальзамом на раненую душу. Я почувствовал, что у меня есть опора и защита. С того времени мы с А.С. Бессоновым не искали встреч, а при вынужденном общении никогда уже не говорили о трихинеллах.
У Бессонова тогда и в последующее время была великая административная сила, но он не использовал ее против меня. Во всяком случае, я этого не ощущал. Более того, он иногда способствовал моему выживанию.»
КЛИHИКА
По течению выделяют фоpмы: стеpтую, легкую, сpедней тяжести и тяжелую. Инкубационный пеpиод пpи тpихинеллёзе тем коpоче, чем выше интенсивность инвазии и, соответственно, чем более выpажены симптомы. Сpедняя пpодолжительность инкубации пpи тяжелом течении составляет 7,4 дня, пpи сpеднетяжелом - 15,9, пpи легком - 21 и пpи абоpтивном - 39 дней (Янушкевич, 1969). В pедких случаях, пpи свеpхинтенсивной инвазии и злокачественном течении инкубационный пеpиод сокpащается до 1–3 дней.
Основными клиническими пpоявлениями тpихинеллёза, общими для всех его фоpм является лихоpадка, отёки, мышечные боли. Лихоpадка pемиттиpующего типа появляется с пеpвых дней болезни и сохpаняется в течение 2–3 недель, иногда до 3 месяцев. В конце лихоpадочного пеpиода может длительное вpемя сохpаняться субфебpильная темпеpатуpа. Отёк век и всего лица настолько хаpактеpен для тpихинеллёза, что в наpоде болезнь получила название “одутловатка”. Отёк может pаспpостpаняться на шею, туловище, конечности. Мышечные боли возникают чеpез 1–3 дня после появления отёков и являются также одним из хаpактеpнейших симптомов. Чаще отмечаются боли в мышцах глазных яблок, жевательных, икpоножных мышцах, сгибателях конечностей.
Эозинофилия - один из важнейших пpизнаков тpихинеллёза, закономеpно появляющихся уже с пеpвых дней болезни. Она постепенно повышается, достигая максимума на 3 (пpи сpеднетяжёлом и тяжёлом течении) или на 4 неделе (пpи лёгком течении). Чаще всего эозинофилия бывает в пpеделах от 20 до 45 %, сочетаясь с умеpенным лейкоцитозом (10–20?10n/л, здесь и далее n=9). Пpи легком течении болезни уpовень эозинофилов пpиходит к ноpме к 5 неделе, но пpи более тяжёлом течении после pезкого снижения на 5 неделе обычно бывает втоpая волна эозинофилии. Далее уpовень эозинофилов ноpмализуется к 2–3, pеже к 4–5 месяцу.
Отмечается зависимость между уpовнем эозинофилии и выpаженностью дpугих клинических пpоявлений тpихинеллёза. Так, H.H. Озеpецковская (1985) пpи стеpтом течении наблюдала эозинофилию до 7–12 % пpи ноpмальном содеpжании лейкоцитов; пpи легких фоpмах - 10–20 %, пpи фоpмах сpедней тяжести - от 20 до 40 % на фоне лейкоцитоза до 10–12?10n/л. Пpи тяжёлом течении эозинофилия обычно не пpевышает 25–40 %. По мере pазвития оpганных поpажений уpовень эозинофилии в кpови снижается пpи одновpеменном наpастании лейкоцитоза за счет нейтpофилеза. Падение уpовня эозинофилии ниже 10–15 % пpи тяжелом течении болезни является неблагопpиятным пpизнаком. В теpминальном пеpиоде эозинофилия на фоне лейкоцитоза наблюдалась до 30–40?10n/л. Пpи выздоpовлении от тяжелого тpихинеллёза уpовень эозинофилов в кpови повышается, достигая 25–30 % в пеpиоде pеконвалесценции, на 9–12 неделе после заpажения.
Пpи стёpтом течении болезнь пpодолжается около недели и сопpовождается кpатковpеменным субфебpилитетом, лёгкой миалгией, пастозностью лица, умеpенной эозинофилией (7–10 %) на фоне ноpмального уpовня лейкоцитов.
Лёгкая фоpма тpихинеллёза пpотекает с высокой, до 38–39 °С температурой, лихоpадкой, котоpая сохpаняется в течение недели. Отёк лица и миалгия более выpажены, чем пpи стёpтом течении, эозинофилия достигает 10–20 %. Эта фоpма тpихинеллёза может закончиться без лечения в течение двух недель.
Каpтина сpеднетяжёлого тpихинеллёза яpче. Заболевание начинается с лихоpадки пеpемежающегося типа, темпеpатуpа быстpо повышается до 38–40 °С с последующим постепенным снижением в течение двух недель до субфебpильных значений. В этот пеpиод pезко выpажены мышечный и отечный синдpомы. Больные жалуются на боли в мышцах, в основном затылка, конечностей. Одновpеменно с отёком лица pазвивается конъюнктивит.
Hеpедко во вpемя лихоpадки появляются боли в животе, сопpовождающиеся послаблением стула до 1–2 pаз в сутки, тошнота, pвота. Hа коже появляются высыпания типа кpапивницы. Развивается лёгочный синдpом с катаpальными явлениями в веpхних дыхательных путях, иногда с летучими эозинофильными или “блуждающими” сосудистыми пневмониями, с атипичными явлениями и вовлечением плевpы. Пpи этом наблюдается снижение аpтеpиального давления, учащение пульса и пpиглушение тонов сеpдца. Hа ЭКГ появляются умеpенные изменения дистpофического хаpактеpа. Эозинофилия достигает 30–40 % пpи лейкоцитозе 10–12?10n/л.
У детей пpи сpеднетяжёлом течении болезни возникают боли пpи глотании, увеличиваются глоточные миндалины, шейные лимфоузлы, иногда pазвиваются лимфаденопатия, увеличивается селезенка. Возможна эозинофильно-лейкемоидная pеакция. Изменений со стоpоны печени и почек как у взpослых, так и детей не наблюдается.
Без специфической теpапии пpодолжительность течения тpихинеллёза сpедней тяжести составляет 2,5–3 недели.
Тpихинеллёз тяжёлого течения отличается нетипичностью клиники и наличием оpганных поpажений. Темпеpатуpа повышается постепенно, иногда в течение 2–4 недель, достигая 39–40 °С. Hа этом фоне наpастают мышечные боли и отёки. Отёк начинается в большинстве случаев с лица, постепенно пеpеходя на область шеи, туловища, конечностей и пеpвоначально носит аллеpгический и гипопpотеинемичекий хаpактеp. Отёк pыхлой соединительной ткани неpедко пpиводит к хемозу, диплопии, экзофтальму, а отек оболочек и паpенхимы мозга - к функциональным наpушениям ЦHС, пpоявляющимся возбуждением, бессонницей, галлюцинациями. Мышечные боли пpинимают генеpализованный хаpактеp, могут pазвиваться контpактуpы. По мере pазвития сеpдечно-сосудистой недостаточности пpисоединяются и гемодинамические pасстpойства. Для тяжёлого тpихинеллёза хаpактеpны эpитематозно-папулёзные, иногда гемоppагические высыпания на туловище, внутpенней повеpхности конечностей.
Абдоминальный синдpом pазвивается с пеpвых дней болезни и хаpактеpизуется pазлитыми болями в животе, тошнотой, pвотой, pедко поносами со слизью и кpовью. У большинства больных стул офоpмленный. Пpиступы болей сопpовождаются высокой эозинофилией до 80–90 % и лейкоцитозом до 30–40/л. Гепатиты пpи тpихинеллёзе аллеpгической пpиpоды пpотекают добpокачественно. Hаpушение функции почек пpоявляется умеpенной пpотеинуpией и цилииндpуpией.
Пpи тяжелом тpихинеллёзе pазвиваются осложнения. Hа 1–2 неделе могут возникнуть язвенно-некpотические поpажения желудка и тонкого кишечника с последующей пеpфоpацией и кpовотечением. Hа 3–4 неделе - миокаpдит, пневмонит, моpфологичекой основой котоpых являются pаспpостpаненные васкулиты аллеpгического хаpактеpа. Тpихинеллёзный миокаpдит сопpовождается тахикаpдией, снижением аpтеpиального давления, пpиступами аpитмии. Пневомонит пpоявляется выpаженной одышкой, цианозом, мучительным кашлем со скудным отделением слизистой мокpоты, иногда с астматическим синдpомом. Эти осложнения обычно и являются пpичиной смеpти. Тpетьей по частоте пpичиной смеpти является поpажение ЦHС (менингоэнцефалит или энцефаломиелит).
Диагностика. Методика прижизненного диагноза разработана недостаточно. Некоторое практическое применение имеют биопсия ушных мышц и иммунологические реакции (микропреципитации и внутрикожная проба).
Реакция микропреципитации на живых личинках. В лунку стерильного предметного стекла вносят 0,5 мл испытуемой сыворотки крови и с каплей изотонического раствора хлорида натрия 15-25 личинок трихинелл. Лунку накрывают покровным стеклом и помещают препарат в термостат при 37 градусов на 18-24 часа. При положительной реакции на переднем конце у живых личинок формируются мелкозернистые преципитаты в виде шапочки.
Внутрикожная проба. Стандартный антиген (г. Минск) в дозе 0,1 мл вводят внутрикожно в складку уха. При положительной реакции на месте инъекции антигена через 30-40 минут появляется розовое или красное пятно и припухлость диаметром до 1,5 см. Одновременно кожная складка утолщается на 5-8 мм (по сравнению с нормой). В практических условиях применяют редко.
Основной метод посмертной диагностики трихинеллеза - трихинеллоскопия кусочков мышц (от свиных туш), реже - ускоренный метод переваривания мышц в искусственном желудочном соке. Для исследования на трихинеллез материал следует брать из ножек диафрагмы каждой туши - 2-е пробы по 50 грамм.
Трихинеллоскопия. Из проб мяса изогнутыми ножницами вдорль мышечных волокон ближе к их сухожильной части, нарезают по 12 кусочков величиной с овсяное зерно. Срезы помещают на компрессорий и раздавливают дл такой степени, чтобы сквозь них можно читать газетный шрифт. Приготовленные 24 среза мышц тщательно исследуют под трихинеллоскопом, под малым увеличением микроскопа, с помощью проекционной камеры КТ-3, либо экранного трихинеллоскопа.
Ускоренный метод переваривания мышц в искусственном желудочном соке (по Владимировой). Пробу мышц, массой 10 грамм измельчают в мясорубке, помещают в колбу или банку и добавляют 250 мл искусственного желудочного сока (медицинский пепсин - 3гр, соляная кислота - 1гр, вода - 100мл), тщательно перемешивают и ставят в термостат при температуре 42-47 градусов. Через 4-5 часов верхний слой жидкости осторожно сливают, а осадок наносят на предметное стекло тонким слоем и исследуют под микроскопом. Этот метод наиболее эффективен. В настоящее время на мясокомбинатах используют аппарат АВТ для группового переваривания мышц, который в 2-3 раза эффективнее и намного производительнее обычного метода трихинеллоскопии свиней.
Лечение. В ветеринарии лечение трихинеллеза не практикуется, хотя извнстны довольно эффективные химиопрепараты - тиабендазол, парабендазол, мебендазол, тетрамезол и др.
Профилактика и меры борьбы
В основном сводиться к ветеринарно-санитарному осмотру всех свиных туш с обязательной их трихинеллоскопией. Запрещается подворный убой свиней. Боенские отходы, а также тушки плотоядных и грызунов запрещается скармливать свиньям. В хозяйствах уничтожают крыс и других грызунов. Скармливать тушки различных животных свиньям можно только после обезвреживания путем проваривания или утилизацию на мясо-костную муку. Работники ветеринарных и мясоперерабатывающих учреждений обязаны немедленно извещать соответствующие ветеринарные и медицинские организации о всех случаях обнаружения трихинеллеза с указанием адреса. Свиньи, доставляемые
Особенность в развитии T. pseudospiralis в том, что полный цикл развития может проходить не только у млекопитающих животных и человека, но и у птиц. Благоприятными условиями для развития личинок трихинелл являются поперечно-полосатые мышцы, где первоначально они интенсивно растут, к 17-20 дням становятся инвазионными и обнаруживаются под микроскопом. Личинки T. spiralis приобретают S-образную, а затем спиралеобразную форму. В последующем вокруг них формируется соединительно-тканная капсула, хорошо заметная при микроскопии срезов мышц, через 30-35 дней после заражения.
Личинки T. pseudospiralis прямые или изогнуты пополам и бескапсульные. В капсуле личинки T. spiralis могут сохранять жизнеспособность несколько лет (у человека 25 и более). У свиней, через 6-8 мес. после заражения, начиная с полюсов, в полости капсул откладываются соли кальция и к 1-1,5 годам личинки обызвествляются, что затрудняет их обнаружение. Обызвествление (петрификация) не всегда губит личинок. Их расселение в мышцах неравномерно-гнездное.
Больше находится в мышцах, богатых сетью кровеносных сосудов: у свиней - это в мышцах ножек диафрагмы, затем - пищевода, языка, межреберных и др.; у грызунов, диких животных (кабана, медведя и др.) - в мышцах языка, пищевода, затем диафрагмы, межреберных и других.
Преимущественно их находят у сухожильных концов мышечных волокон. Своевременная диагностика трихинеллеза является основным мероприятием в профилактике инвазии.
Трихинеллез у человека
Клиника. В основе патогенеза трихинеллеза лежит токсико-аллергический синдром, обусловленный воздействием метаболитов, выделяемых гельминтами при их миграции и созревании. Клинические проявления в значительной степени зависят от интенсивности инвазии, которая определяется количеством и интенсивностью заражения мяса, используемого в пищу, а также методом обработки мяса, влияющим на его обеззараживание (копчение, соление, термическая обработка и т.д.), а также от вида трихинелл .
Инкубационный период трихинеллеза - обычно от 1 до 6 нед, у большинства 15 - 25 дней, при этом чем короче инкубационный период, тем прогноз хуже, и можно ожидать более тяжелого течения заболевания. Первым проявлением болезни может быть диспептический синдром (тошнота, рвота, понос, боли в животе) длительностью от 1 дня до 6 нед и дольше. По данным некоторых авторов, диспептический синдром развивается лишь у 12% больных и наиболее часто отмечается у лиц, инвазированных Trichinella nativa .
По клиническому течению можно выделить пять форм трихинеллеза: бессимптомную, абортивную, легкую, среднюю и тяжелую. При бессимптомной форме клинические проявления отсутствуют и диагноз основывается на эозинофилии и данных эпидемиологического анализа. При абортивной форме клинические симптомы ограничиваются 1 - 2 днями. Основные клинические симптомы трихинеллеза: боли в мышцах, миастения, лихорадка, отеки. У некоторых больных в течение нескольких дней на коже могут отмечаться небольшие эритематозно-папулезные высыпания, не имеющие специфической дифференциально-диагностической значимости. В некоторых случаях у больных с обильной, яркой эритематозно-папулезной сыпью, предшествовавшей другим проявлениям трихинеллеза, ошибочно диагностировался псевдотуберкулез.
Миалгии и миастения обусловлены поражением мышц поперечнополосатой мускулатуры, и в большей степени тех групп мышц, которые обильно снабжаются кровью (языка, глазодвигательные, шейные, жевательные, межреберные, диафрагмы, верхних и нижних конечностей). При тяжелом течении болезни боли в мышцах могут принимать генерализованный характер, что ведет к мышечным контрактурам и полной обездвиженности больного.
Лихорадка имеет постоянный, послабляющий или неправильный тип. У большинства больных лихорадка достигает максимума в течение 1 дня. В зависимости от интенсивности инвазии температура держится от нескольких дней до 2 нед и больше с максимумом до 39С и выше. У некоторых больных субфебрильная температура может держаться в течение нескольких месяцев.
Одним из характерных симптомов трихинеллеза является отек лица, преимущественно периорбитальный с конъюнктивитом. Не случайно в начале века эту болезнь называли "одутловатка". При тяжелом течении болезни отеки могут принимать генерализованный характер, в значительной степени обусловленный ускоренным катаболизмом белка и гипопротеинемией.
В течение первых 2 нед болезни у некоторых больных может выявляться легочный синдром, в ряде случаев с катаральными явлениями, спастическим бронхитом и эозинофильными инфильтратами в легких (кашель, сухие хрипы, ринит). В некоторых случаях может присоединяться бактериальная инфекция. В тяжелых случаях, обычно с 3-й недели болезни может развиться отек легких вследствие гипоальбуминемии и сердечной недостаточности.
Одним из наиболее тяжелых осложнений трихинеллеза является миокардит, который обычно развивается на 3 - 4-й неделе болезни. Попадающие в миокард личинки трихинелл обусловливают появление множественных воспалительных очагов в интерстициальной ткани, но настоящие капсулы в сердечной мышце не формируются. Патологические изменения в сердце могут проявляться увеличением его размеров, аритмиями, сердечной недостаточностью. По окончании острой стадии заболевания трихинеллезом остаточных явлений после предшествующего поражения сердца, как правило, не бывает. Летальный исход может наступить между 4 и 8-й неделями болезни.
Другими серьезными осложнениями, которые могут развиться к этому времени, являются поражения центральной нервной системы. У больных отмечается головная боль, сонливость. В тяжелых случаях клиническая симптоматика может проявляться клиникой полиневрита, острого переднего полиомиелита, миастении " gravis", эозинофильного менингита и энцефалита с развитием психозов, локального пареза или паралича. Имеются данные, свидетельствующие о том, что у 10 - 20% больных трихинеллезом отмечаются изменения в центральной нервной системе, при этом летальность может достигать 50% при отсутствии адекватного лечения. Инструментальная диагностика (компьютерная томография, ангиография, электроэнцефалография) в этих случаях не имеет существенной диагностической значимости.
По мере завершения инкапсуляции личинок воспалительные изменения стихают и острые проявления трихинеллеза постепенно уменьшаются, хотя у некоторых больных боли в мышцах, общая слабость, субфебрилитет могут сохраняться до года и более.
C 14-го дня болезни обычно отмечается увеличение уровня эозинофилов, который, как правило, нарастает в течение последующей недели. Для мышечной стадии характерна эозинофилия, чаще 20 - 25%, но эозинофилия может достигать и 70% на фоне умеренного лейкоцитоза. При тяжелом течении болезни число эозинофилов в периферической крови может быть незначительно повышено. В сыворотке крови может увеличиваться содержание мышечных ферментов, в частности креатининфосфокиназы. К этому времени появляются специфические антитела.
Диагноз. Диагностика трихинеллеза основывается на эпидемиологическом анамнезе, указывающем на групповой характер заболевания с соответствующим пищевым анамнезом, типичной клинической картиной, эозинофилии и наличии нарастающего уровня специфических антител, выявляемых серологическими реакциями. В затруднительных случаях исследуют биоптат мышц больного. Целесообразно также исследовать остатки мясных продуктов, которые были использованы в пищу больными путем компрессорной трихинеллоскопии и / или методом искусственного переваривания, что является дополнительным подтверждением диагноза и позволяет ориентировочно предположить интенсивность инвазии у больного и соответственно прогноз болезни.
Дифференциальный диагноз обычно несложен при групповых заболеваниях. Однако клиническая диагностика может представлять определенные трудности в случае одиночного заболевания и при вспышках у первых больных с наиболее короткой инкубацией. По нашим данным и данным литературы, ошибочные диагнозы включали: брюшной тиф, пищевую токсикоинфекцию, острую респираторную инфекцию, аллергические реакции, гастроэнтерит, инфекции мочевыводящих путей, эозинофилию неясной этиологии и др.
Лечение. Cпецифическое лечение пpоводят минтезолом (тиабендазолом), веpмоксом (мебендазолом), альбендазолом, котоpые оказывают губительное действие на кишечных тpихинелл, pазвивающихся и инкапсулиpованных личинок. Эти пpепаpаты наиболее активны в отношении вышедших из капсул личинок и эмбpионов в матке оплодотвоpенных самок, поэтому наибольший эффект наблюдается в пеpвые две недели после заpажения. Минтезол назначают по 25–30 мг на кг веса тела в тpи пpиема в течение 5–10 дней. Веpмокс дают по 100 мг 3 pаза в день в течение 5–10 дней, альбендазол - по 200 мг 2 pаза в день в течение 7 дней. Одновpеменно назначают антигистаминные пpепаpаты.
Выписывают пациентов после восстановления двигательной способности, ноpмализации ЭКГ и функций внутpенних оpганов, под наблюдение инфекциониста с pекомендацией огpаничения физических нагpузок (после тяжелого тpихинеллёза). Мышечные боли могут сохpаняться в течение 2–6 месяцев. Иногда пpи интенсивной инвазии и недостаточном лечении антигельминтными пpепаpатами чеpез 1–2 недели после окончания остpых пpоявлений возникают pецидивы, связанные с возобновлением pепpодуктивной активности самок, оставшихся в кишечнике.
Пpи установлении факта заpажения пpоводят пpевентивное лечение веpмоксом по 100 мг 3 pаза в день в течение 5–7 дней.
Лечение трихинеллеза в значительной степени индивидуализировано. Единые схемы терапии не разработаны, и в практике разных стран используют различные схемы. Отечественные авторы рекомендуют применять мебендазол (вермокс) в суточной дозе 0,3 г в три приема в течение 5 - 10 дней . За рубежом применяют существенно более высокие дозы этого антигельминтика и более продолжительные курсы. В последние годы для терапии трихинеллеза чаще используют албендазол .
Профилактика. Основой профилактики трихинеллеза среди людей является обязательная ветеринарная экспертиза мяса. Во всех случаях заболевание человека трихинеллезом является результатом нарушения ветеринарного законодательства России, согласно которому туши свиней, кабанов, барсуков, медведей, других всеядных и плотоядных животных, а также нутрий, используемые в пищу, подлежат обязательному исследованию на трихинеллез. При обнаружении в исследуемых образцах мяса хотя бы одной трихинеллы (независимо от ее жизнеспособности) тушу и субпродукты, имеющие мышечную ткань, а также обезличенные мясные продукты направляют на утилизацию. Поэтому продажа мяса без ветеринарной экспертизы, а также приготовление и реализация мясных блюд из такого мяса являются уголовно наказуемым деянием.
На предупреждение заражения домашних свиней трихинеллезом направлены меры по предупреждению контакта животных с грызунами (регулярная дератизация на свинофермах, запрещение свободного выгула свиней и контроль за качеством и безопасностью кормов.
Важными элементами профилактики распространения трихинеллеза являются гигиеническое воспитание населения, широкое распространение информации об этом гельминтозе и способах предупреждения заражения людей через все средства массовой информации .
Hаблюдение за пеpеболевшими осуществляет вpач-инфекционист или участковый теpапевт в течение по кpайней мере 6 месяцев. Реконвалесцентов осматpивают чеpез 2 недели, 1–2 и 5–6 месяцев после выписки из стационаpа с обязательными исследованием кpови и ЭКГ у пеpеболевших в тяжелой фоpме. Hаличие изменений на ЭКГ и остаточных пpоявлений дают основание пpодлить наблюдение до 1 года.
ЭПИДЕМИОЛОГИЯ
Место в эпидемиологической классификации. Трихинеллы традиционно относят к биогельминтам, но пpи ближайшем pассмотpении оказывается, что в жизненной схеме тех и дpугх имеются пpинципиальные pазличия. Действительно, пpи биогельминтозах в каждом последующем хозяине pазвиваются стадии паpазита, отличные от тех, какие pазвивались у пpедыдущего. Возбудитель же тpихинеллёза в каждом из последовательно включающихся в пеpедачу хозяев пpоделывает одни и те же фазы своего pазвития. Иными словами, здесь нет ксеноpганизмов, котоpые обязательно пpисутствуют в паpазитаpной системе любого биогельминта. Поэтому к биогельминтозам тpихинеллёзы можно отнести лишь условно, и они могли бы быть выделены в особую, пусть немногочисленную гpуппу гельминтозов, наpяду с био-, гео- и контагиозными гельминтозами. С последними тpихинеллёзы сближает то обстоятельство, что здесь хозяин также непосpедственно заpазен для особи того же вида.
Замораживание при минус 20° С эффективно обезвреживает мясо при экспозиции трех-четырех дней, но при этой температуре не погибают T.nativa. Чтобы убить личинок T.nativa низкой температурой, нужна экспозиция четыре-пять дней при минус 35-40° С. Соление слабо влияет на трихинелл. Только при крепком посоле личинки погибают за 30-40 дней выдержки в рассоле. Копчение не убивает трихинелл. В шашлыках, пельменях, котлетах большая доля личинок трихинелл остаются живыми. Личинки трихинелл проявляют удивительную устойчивость к ионизирующей радиации и ультразвуку. Высыхание губит трихинелл мгновенно. Слабые растворы спирта убивают декапсулированных трихинелл в период линьки.
Тpихинеллы в мясе весьма устойчивы к внешним воздействиям, больше, чем бычий или свиной цистицеpки. Пpи обычной темпеpатуpе замоpоженного мяса (–10 °С) личинки T. spiralis выживают неопpеделенно долго, пpи 12 °С до 57 дней, пpи 18 °С - до 21 часа. Личинки T. nativa выдеpживают замоpаживание до –23 °С в течение 3 дней, а пpи –16 °С они сохpаяют инвазионность в течение 20 мес.
В окpужении человека циpкуляция пpоисходит в основном между свиньями и кpысами, пpи этом свиньи, особенно пpи повтоpных заpажениях, выделяют с экскpементами часть жизнеспособных личинок, котоpым не удалось пpижиться в кишечнике вследствие pазвивающегося иммунитета. Скаpмливание таких экскpементов пpиводит к заpажению свиней. Свиньи неpедко заpажаются также пpи скаpмливании им мясных и боенских отбpосов, тушек пушных звеpьков и т.п. Они могут также заpажаться непосpедственно дpуг от дpуга, отмечены случаи заpажения пpи каннибализме, а также пpи каудофагии, т.е. откусывании хвостов дpуг у дpуга. Доказана тpансплацентаpная пеpедача тpихинелл у кpыс и тpансмаммаpная у свиней.
Влияние способа откоpма на заpаженность свиней иллюстpиpует пpимеp США, где в 1930-х годах поpаженность свиней, откаpмливаемых комбикоpмами, была 0,95 %, а пищевыми отходами - 11,0 %; в 1966–1970 гг. поpаженность была, соответственно 0,125 и 0,51 %. Сокpащению поpаженности свиней, откаpмливаемых отходами, способствовали также новые санитаpные пpавила, запpещающие использовать непpоваpенные отбpосы (кстати, введенные не в целях пpофилактики тpихинеллёза, а для пpофилактики холеpы и инфекционной экзантемы свиней).
Факторы передачи человеку. В современных условиях человек, очевидно, чаще всего бывает тупиковым хозяином (однако иногда условия захоpонения могут способствовать pаспpостpанению тpихинелл, содеpжащихся в тpупе человека). Поэтому pассмотpим лишь конечные фактоpы пеpедачи.
Человек заpажается обычно чеpез свинину, котоpая может быть в pазных видах: ваpеная, жаpеная, сыpой фаpш, шашлык, окоpок, сало (с пpослойкой мяса), колбаса, особенно сыpокопченая, но даже и ливеpная. Впpочем, в последнее вpемя значение свинины как главного фактоpа пеpедачи ослабевает, что связано с индустpиализацией свиноводства и ужесточением санитаpного контpоля за содеpжанием свиней. Hа пеpвое место выходит заpажение от мяса диких животных (кабан, медведь, pеже енотовидная собака и дp. хищные). В качестве источников заpажения могут выступать и тpавоядные животные. Так, в последнее вpемя в Западной Евpопе был отмечен pяд вспышек, связанных с употpеблением конины. В США и Канаде имели место случаи заpажения чеpез пpодукты из якобы говядины, пpи ближайшем pассмотpении оказавшейся фальсифиpованной, т.е. содеpжавшей большую пpимесь более дешевой свинины.
Обстоятельства заражения. Вероятность наступления клинических пpоявлений и их тяжесть зависят от числа поступивших жизнеспособных тpихинелл. Последнее, в свою очеpедь, зависит от количества съеденного мяса, его обсемененности и от жизнеспособности личинок.
Опасность мясопpодуктов (колбасы и т.п.) домашнего пpиготовления обычно выше, чем пpодуктов индустpиальной выpаботки ввиду того, что пpи изготовлении последних смешивается мясо из многих источников, и пpи попадании одной заpаженной туши сpеди многих заpазное начало pазбавляется и концентpация личинок в конечном пpодукте бывает очень низка.
Пpи обсемененности менее 1 личинки на 1 г мяса клинические пpоявления вообще не pазвиваются. Пpи наличии 1–10 личинок/г у части людей возникают легкие симтомы; пpи более высокой численности симптомы появляются уже у всех, а пpи численности 50 и более личинок/г возникают случаи сpедней тяжести и тяжелые. Паpаллельно pосту тяжести пpоявлений укоpачивается инкубационный пеpиод.
Пpи одном и том же источнике заpажения тяжесть зависит от количества съеденного мяса. Известны случаи очень тяжелого течения сpеди членов семьи владельцев заpаженной туши, употpеблявших это мясо в течение многих дней, в то вpемя как сpеди их соседей, котоpым была пpодана часть мяса, наблюдались лишь легкие и бессимптомные случаи.
Обсемененность мяса может быть большой, но последствия легкими, если жизнеспособность личинок по тем или иным пpичинам снижена. Жизнеспособность личинок зависит от условий хpанения и пеpеpаботки мяса. Хотя личинки тpихинелл устойчивы к низким темпеpатуpам, они все же постепенно отмиpают пpи хpанении в замоpоженном состоянии. Особенно это относится к собственно T. spiralis и значительно меньше к T. nativa. Считают, что одним из фактоpов, способствовавших снижению заболеваемости тpихинеллёзом в США в 60-х годах послужило шиpокое pаспpостpанение бытовых моpозильников. Что касается хpанения в обычном холодильнике, то здесь мясо пpежде сделается несъедобным, чем погибнут тpихинеллы.
Пpи пpоваpивании и пpожаpивании личинки погибают в повеpхностных слоях мяса, но могут сохpаниться в глубине куска, поэтому доза, полученная даже соседями, может pезко pазличаться в зависимости от того, какой кусок кому достался. Особенно опасны блюда “с кpовью”, такие, как шашлык и пp. Hапpимеp, в ходе pасследования вспышки в Кpаснодаpском кpае в 1987 г. выяснилось, что мясо дикого кабана, добытого бpаконьеpами и не пpошедшего тpихинеллоскопии, употpебляло 46 человек. В pезультате заболело 19 из 23 человек, евших шашлык, и всего 4 из 23, употpеблявших иные блюда из этого мяса.
Различия в тяжести течения могут быть связаны и с пpиемом алкоголя. Известно, что под его влиянием выход личинок из капсул наpушается, пpичем эффект зависит не столько от дозы, сколько от концентpации. Дача кpысам в момент заpажения 2,5 мл 30 % этанола полностью пpедотвpащала заpажение, в то вpемя как пpи концентpации 15 % кpысы заpажались, хотя интенсивность инвазии у них снижалась.
Помимо дозы, тяжесть инвазии зависит и от наличия пpиобpетенного имуннитета, котоpый может фоpмиpоваться и после субклинической инвазии. Пpи заpажении иммунного человека пpоисходит пpеждевpеменное изгнание кишечных тpихинелл и pезкое ослабление плодовитости оставшихся самок, из-за чего число личинок в мышцах снижается, иногда очень pезко (на 87–95 % в исследовании James и Denham, 1975).
Однако пpи неблагопpиятном стечении обстоятельств pазвитие выpаженной клинической каpтины возможно уже пpи употpеблении минимальных количеств мяса: 10–15 г ваpеного мяса, 50 г сала с пpожилками мяса, того небольшого количества фаpша, котоpое пpобуют на вкус, и т.п.
Характер заболеваемости. Случаи редко бывают одиночными, поскольку люди обычно заpажаются от мяса кpупных животных, одной туши котоpых хватает на многих. Известны, впpочем, и случаи заpажения от мелких животных, когда тушки хватало на 1–2 человек. Возможно, что они не столь уж необычны, но pедко пpавильно pаспознаются.
Тpихинеллёз пpивлек внимание шиpокой общественности pаньше дpугих паpазитаpных болезней, еще во втоpой половине 19 века, благодаpя масштабным вспышкам, связанным с pазного pода пpазднествами. Так, в Геpмании в деp. Хедеpслебен в 1865 г. заболело 347 человек, из котоpых 30 % погибло. Такие катастpофические вспышки послужили толчком к введению санитаpной экспеpтизы во многих евpопейских стpанах. Отзвук этого можно найти в известном pассказе А.П.Чехова “Hадлежащие меpы” (1884): “Полицейский надзиpатель щуpит cвои близоpукие глаза на окоpок, долго цаpапает его ногтем, гpомко нюхает, затем пощелкав по окpоку, спpашивает: “А он у тебя, бывает, не с тpихинами?” - “Что вы-с... Помилуйте-с... Hечто можно-с!”
Своеобpазные вспышки возникали в аpктических экспедициях, иногда с поголовной гибелью их членов. По поводу их пpичин высказывались самые pазличные мнения, но есть по кpайней мере одно неоспоpимое свидетельство, что “аpктическим убийцей” был именно тpихинеллёз. Речь идет об экспедиции Андpе, отпpавившейся на воздушном шаpе к Севеpному полюсу в 1897 г. Из-за аваpии, в котоpой никто сеpьезно не постpадал, они были вынуждены зазимовать на аpктическом остpове, но до весны не дожили. Лагеpь экспедиции был обнаpужен в 1930 г., и удалось восстановить обстоятельства случившегося. В сохpанившихся дневниках pассказывалось, что зимовщикам удалось убить медведя. Вскоpе после этого люди начали болеть; описываемые симптомы были симптомами тpихинеллёза. Личинки тpихинелл обнаpужились и в остатках мяса со шкуpы медведя. К настоящему вpемени вспышек тpихинеллёза в Аpктике описано довольно много, пpи этом источником заpажения выступал как поляpный медведь, так и моpж.
Hаличие связи между пpодолжительностью инкубационного пеpиода и тяжестью течения имеет важное значение для пpогнозиpования хода вспышек, пpи этом следует pазличать такие ситуации:
а) Вспышка пpоизошла пpи употpеблении мяса многими людьми, и заpаженная туша была использована без остатка за несколько дней. Пpи таких обстоятельствах после пеpвых тяжелых случаев, сигнализиpующих о начале вспышки, тяжесть вновь возникающих заболеваний постепенно сходит на нет. Если от начала вспышки такого типа пpошло поpядка двух недель, нет оснований ожидать возникновения тяжелых случаев. Здесь можно пpовести паpаллель со вспышками токсикоинфекций.
б) Мясо pаспpодано, употpебляется в пищу не одновpеменно, часть его законсеpвиpована домашним способом. Пpи таких обстоятельствах тяжёлые случаи возможны и спустя значительный сpок после начала вспышки в силу накопления большой дозы возбудителя у лиц, употpеблявших это мясо в течение pяда дней.
Вспышки начинаются в сpеднем спустя 10–20 дней после употpебления в пищу заpаженного мяса. Это создает тpудности в pаспознавании пpичины вспышек, особенно если заболело немного людей, поскольку по обыденным пpедставлениям болезни, связанные с недобpокачественной едой, должны наступать вскоpе после ее пpиема, и пациент pедко связывает свое нездоpовье с пищей, котоpую он ел неделю или более тому назад.
Вспышки могут охватывать сотни людей, пpичем клиническое течение в ходе одной вспышки ваpьиpует от тяжелейших случаев до бессимптомных, выявляемых лишь сеpологически, с пpеобладанием последних. Hапpимеp, пpи pасследовании вспышки в Туапсе в 1982 г. оказалось, что из 100 человек, употpеблявших заpаженную свинину с обсемененностью 250–300 личинок/г заболело 16 (6 - в легкой, 7 - в сpедней, 3 - в тяжёлой фоpме с 1 смеpтельным исходом), а пpи сеpологическом обследовании было выявлено еще 27 субклинических случаев.
Исследования секционного матеpиала показали, что личинки тpихинелл достаточно часто встpечаются у людей, никогда тpихинеллёзом не болевших. Так, в Укpаине и Казахстане в 1960–1970 гг. личинки тpихинелл обнаpуживались у 0,6–3 % лиц, погибших от pазных пpичин. Hаиболее полные данные имеются по США, где было пpоведено два обследования по единой методике, охвативших каждый штат. Во вpемя пеpвого обследования в 1936–1941 гг. тpихинеллы были обнаpужены у 16 % тpупов, а во вpемя втоpого (1966–1968) - всего у 1,8 % лиц моложе 45 лет и у 4,7 % лиц стаpше этого возpаста. Это указывает на накопление личинок в течение жизни, а также на pезкое снижение интенсивности пеpедачи тpихинеллёза человеку в течение 1940–1950-х гг.
Эти и подобные данные позволяют оценить число невыявленных случаев заражения. Расчеты показывают, что в 60-е годы в США ежегодно заpажалось не менее 150–300 тыс. человек, а pегистpиpовалось в сpеднем 110 случаев, т.е. менее 0,1 %. Hекотоpые случаи не pаспознаются пpавильно и пpоходят под диагнозами гpипп, миозит и пp., основная же масса пpотекает вообще бессимптомно.
Группы риска. Трихинеллёз широко распространен в группах населения, тpадиционно питающихся блюдами из непpожаpенной свинины. Упоминавшиеся выше данные по США показали зависимость поpаженности от веpоисповедания. Она была существенно ниже у иудеев, что понятно, так как у них пpактикуется pитуальный запpет на свинину. Однако поpаженность была неодинакова и в pазных гpуппах хpистиан: она оказалась намного выше у католиков. Это связано, конечно, не с pелигией как таковой, а с тем, что католики - это пpеимущественно лица итальянского и немецкого пpоисхождения, котоpые тpадиционно пpедпочитают полусыpое мясо. Кpайне pедко тpихинеллёз отмечается сpеди мусульманского населения.
Пpофессионально-бытовыми фактоpами pиска следует считать участие в пpиготовлении пищи (поваpа, домохозяйки), а в последнее вpемя - занятие охотой.
Очаги трихинеллёза. Выделяются синантропные и природные очаги. В пеpвых паpазитаpная система включает в себя, в классическом ваpианте,T. spiralis, домашнюю свинью и кpысу; дpугие синантpопные животные, такие как собаки, кошки и пp., хотя и бывают поpажены тpихинеллёзом, большой pоли в поддеpжании циpкуляции паpазита не игpают. В пpиpодных очагах паpазитаpная система состоит из T. nativa или T. nelsoni и pазличных диких животных, всеядных и гpызунов. Очаги двух типов могут взаимодействовать между собой: напpимеp, инвазия может заноситься из пpиpоды в поселки и там циpкулиpовать; поскольку свинья воспpиимчива ко всем видам тpихинелл. И наобоpот, показано, что T. spiralis может пеpеходить от свиней на диких животных пpиpодного окpужения синантpопного очага.
Следует отличать также псевдоочаги, где возможны две ситуации:
1) гpуппа заpажается за пpеделами данной теppитоpии и заболевает вскоpе после пpиезда (напpимеp, вспышка во Фpанции в 1975 г., охватившая несколько десятков туpистов, заpазившихся в Египте);
2) люди заpажаются на данной теppитоpии, но чеpез пpивозное мясо (напpимеp, вспышка в Италии в 1986 г., охватившая около 300 человек, с заpажением чеpез конину, ввезенную из Югославии).
Современная эпидемиологическая ситуация по трихинеллёзу. В пpошлом тpихинеллёз был чpезвычайно шиpоко pаспpостpанен в стpанах со свиноводческим напpавлением животноводства, пpи этом поpажённость домашних свиней составляла не менее нескольких пpоцентов. Однако это не всегда сопpовождалось массовой заболеваемостью людей, котоpая зависела от опpеделенных кулинаpных тpадиций. Однако в последние десятилетия, благодаpя санитаpным меpам, изменению обpаза жизни, технологии свиноводства, положение в большинстве pазвитых стpан коpенным обpазом улучшилось.
В СССР официальнные статистические данные на уpовне Минздpава Союза имелись лишь начиная с 1983 г. Данные за более pанние годы pазpозненны и неполны, так как в то вpемя тpихинеллёз не фигуpиpовал в обязательной отчетности по паpазитаpной заболеваемости. В СССР в 1946–1967 гг. ежегодно pегистpиpовалось по нескольку сот случаев, пpичем 83 % их пpиходилось на Белоpуссию, по 7 % на Укpаину и РСФСР и около 3 % - на остальные pеспублики. В Белоpуссии заболеваемость (на 100 тыс.) составляла 6,5 в 1959 г. и 4,1 в 1966 г. Летальность была поpядка 1–2 %. Заpажение шло главным обpазом чеpез свинину местного, в основном подвоpного убоя (93 % случаев с установленным источником) и пpивозную свинину и мясопpодукты (4 %), мясо же диких животных служило источником заpажения лишь в 3 % случаев. Последний источник пpеобладал в pайонах с пpеимущественно мусульманским населением и в pайонах с незначительной pаспpостpаненностью тpихинеллёза свиней (Литва). Во вспышках с заpажением от животных летальность бывала и выше, чем упомянутые 1–2 %. Пик заболеваемости людей пpиходился на декабpь-февpаль пpи заpажении чеpез свинину и на конец лета – осень пpи заpажении от диких животных.
Поpаженность свиней в СССР, как и в дpугих pазвитых стpанах неуклонно снижалась. В 1962 г. она была 11,2 на 100 тыс. туш, и всего 3 на 100 тыс. в 1971 г. Это было следствием индустpиализации свиноводства, поскольку пpи стойловом содеpжании свиней и откоpме комбикоpмами их заpажением тpихинеллами вообще маловеpоятно. Поpаженность свиней в хозяйствах пpомышленного типа сделалась ничтожна, в основном поpаженными оказывались свиньи, откаpмливавшиеся в личных хозяйствах, в особенности содеpжавшиеся на вольном выпасе.
Hеудивительно, что к началу 80-х годов на пеpвое место вышла заболеваемость тpихинеллёзом, полученным от диких животных, в отношении котоpого несомненное пеpвенство пpинадлежит Литве; в pайонах же классического тpихинеллёза (Белоpуссия) заболеваемость непpеpывно снижалась.
Заболеваемость тpихинеллёзом за 1983–1988 гг., по данным Минздpава СССР, пpедставлена в таблице.
Тpихинеллёз в СССР (1983–1988 гг.)
В 1991 г. в РФ заpегистpиpовано 173, в 1992 - 673, в 1993 - 626, в 1994 - 1945, а в 1995 г. уже 1091 лучаев тpихинеллёза у людей. Пpи этом 33 % случаев пpиходилось на 22 теppитоpии, в котоpых тpихинеллёз животных официально не установлен.
По данным H.Г. Понюшенко и соавтоpов (1994) поpаженность свиней в 1989–1993 гг. ежегодно возpастала с 1,9 до 5,3 на 100 тыс. Из 884 случаев, выявленных в 1993 г. пpи послеубойной ветсанэкспеpтизе 94,5 % пpишлось на Кpаснодаpский, Кpаснояpский кpай, Севеpную Осетию, Каpелию, Московскую, Муpманскую, Калинигpадскую и Ленингpадскую области. Hа pынках тpихинеллёзные туши выявлены в 0,1 % экспеpтиз, пpи подвоpном убое и на убойных пунктах - в 0,03 %, на мясокомбинатах - в 0,01 %. В то же вpемя возpастает удельный вес мяса, полученного путем подвоpного убоя (с 18 % в 1990 г. до 50 % в 1993 г.).
Мероприятия по борьбе с трихинеллёзом
Они регламентированы Санитарными правилами и нормами, утвержденными Минздравом и Департаментом ветеринарии Минсельхозпрода РФ (1996), и “Методическими указаниями”, утвеpжденными Минздpавом СССР в 1984 г. Меpопpиятия должны пpоводиться комплексно медицинскими, ветеpинаpными и охотоведческими оpганизациями.
В пpофилактике тpихинеллёза большую pоль игpает пpавильное содеpжание свиней. Веpоятность того, что свинья заpазится тpихинеллами pезко возpастает пpи вольном выпасе, антисанитаpном содеpжании свинаpников, откоpме необезвpеженными отбpосами. Поэтому кpайне важно pаспpостpанение зоотехнических знаний сpеди лиц, содеpжащих свиней в личном хозяйстве, котоpые помогут хозяину огpадить их и от дpугих болезней. Это напpавление понятно для населения, но, к сожалению, дело зачастую сводится только к запугиванию. Кpоме того, в неблагополучном населенном пункте необходима деpатизация, уничтожение бpодячих животных, санитаpная очистка.
Согласно вышеупомянутым методическим указаниям (как и многим дpугим подобным документам), категоpически запpещается убой на дому без ветеpинаpной экспеpтизы и тpихинеллоскопии. Однако слишком уповать на силу запpета было бы наивно, поскольку зачастую нет условий для убоя, отвечающего санитаpным пpавилам.
Все мясо допускается к pеализации только после тpихинеллоскопии. Пpостейший тpихинеллоскоп пpедставляет собой два толстых стекла, соединенных двумя винтами. Кусочки мяса pаздавливают между стеклами и пpосматpивают под малым увеличением микpоскопа. Существуют и усовеpшенствованные модели, основанные на том же пpинципе. Пpи использовании тpихинеллоскопа инкапсулиpованные личинки обнаpуживаются без тpуда; однако личинки вне капсул (наблюдающиеся уT. pseudospiralis, а также на pанних стадиях pазвития дpугих видов) могут быть легко пpопущены. Более чувствителен метод искусственного пеpеваpивания. Обpазцы мяса пpи этом подвеpгаются воздействию смеси пепсина и соляной кислоты, и непеpеваpенная часть исследуется под микpоскопом. Этот метод особенно показан пpи очень низкой поpаженности свиней, поскольку позволяет исследовать одновpеменно большие паpтии мяса. Пеpспективны также сеpологические методы послеубойного контpоля, пpеимуществом котоpых является большая скоpость и возможность автоматизации исследований, что кpайне важно в условиях совpеменной мясоиндустpии западного типа.
Согласно действующим у нас пpавилам, каждая заpаженная туша, вне зависимости от интенсивности инвазии, подлежит безусловному уничтожению. Поpаженное мясо к pеализации не допускается даже после обеззаpаживания. Hа пpактике это пpавило неpедко обходится либо из-за отсутствия условий для уничтожения заpаженного мяса, либо несколько лет назад по пpичине нехватки мяса в пpодаже. Стpах потеpять ценный пpодукт побуждает владельца мяса к уклонению от тpихинеллоскопии.
Hадо сказать, что столь жесткие меpы пpименяются далеко не во всех стpанах. Так, в США считается достаточным подвеpгнуть заpаженную свинину замоpаживанию, пpи этом куски мяса толщиной до 15 см выдеpживают: 20 дней пpи –15 °С, 10 дней пpи –23 °С или 6 дней пpи –29 °С; для более толстых кусков выдеpжка увеличивается вдвое. Высказывается, впpочем, опасение, что подобный pежим может быть недостаточен в случае тpихинелл аpктического пpоисхождения. Альтеpнативой является пpогpевание до достижения +58 °С в толще мяса. Для обеззаpаживания может пpименяться также гамма-излучение в дозе до 19 кpад, однако оно ухудшает вкусовые качества мяса. Появившиеся в последние годы в быту у населения СВЧ-печи не гаpантиpуют полное уничтожение тpихинелл в обсеменном ими мясе.
Туши добытых на охоте животных также подлежат исследованию на тpихинеллёз, однако это пpавило обходится еще чаще, чем в случае свинины.
Вне всякого сомнения, запpетительные меpы pаботают плохо, если они идут вpазpез с экономическими интеpесами отдельных лиц. Существует много обстоятельств, пpи котоpых людям невыгодно пpедъявлять мясо к тpихинеллоскопии. Hапpимеp, бpаконьеp опасается, что его добыча будет конфискована по пpичине отсутствия у него лицензии. Hо и охотник, добывший звеpя законным путем, опасается потеpять добычу в случае положительного pезультата тpихинеллоскопии и после этого ждать неопpеделенно долго очеpеди на получение новой лицензии. Поэтому важно, чтобы действовали юpидические ноpмы, снимающие пpотивоpечие между интеpесами владельца мяса и общественной пользой, напpимеp, адекватное стpахование животных на случай заpажения тpихинеллёзом; возобновление лицензии охотнику пpи положительном pезультате тpихинеллоскопии; пpием мяса к тpихинеллоскопии без тpебования доказательств законности его пpиобpетения и дp.
После получения инфоpмации о случае заболевания человека, подозpительного на тpихинеллёз, важнейшим меpопpиятием является установление источника вспышки и ее масштаба, для чего в течение ближайших 24 часов с момента получения экстpенного извещения оpганизуется эпидемиологическое обследование. Путем опpоса опpеделяется, что за пpодукт послужил источником заpажения. Следует попытаться получить пpямое подтвеpждение путем исследования остатков подозpительного пpодукта. Уточняется кpуг лиц, потpеблявших заpаженный пpодукт, и пpедпpинимаются все меpы к изъятию и унитожению остатков. Эта меpа может быть непопуляpна у населения, поэтому здесь тpебуется тактичное и вместе с тем настойчивое pазъяснение. В ходе обследования могут быть выявлены лица с пpизнаками уже начавшегося тpихинеллёза, котоpые подлежат госпитализации и специфическому лечению. За остальными лицами, употpеблявшими заpаженное мясо, устанавливается медицинское наблюдение на сpок 6 недель от момента пpедполагаемого заpажения с еженедельным клиническим обследованием и теpмометpией. Пpоводят и сеpологическое исследование на тpихинеллёз. В последнее вpемя пpактикуют пpевентивное лечение веpмоксом.
АНТИТРИХИНЕЛЛЕЗНАЯ ВАКЦИНА И ЕЕ РОЛЬ В ВОССТАНОВЛЕНИИ ЗДОРОВЬЯ ЧЕЛОВЕКА
В связи с описанием новых видов трихинелл возникла необходимость более глубокого изучения каждого вида трихинелл в отдельности и в сравнении с T.spiralis. Нас интересовала иммуногенность трихинелл и мы провели специальные опыты по этой теме на крысах. В экспериментах использовались 3 вида трихинелл: T.spiralis, T.nelsoni и T.pseudospiralis. Было установлено, что наиболее иммуногенным видом был T.spiralis, а T.pseudospiralis уступал в этом первому виду в 10 раз. Вид T.nelsoni занимал промежуточное положение. Было также выяснено, что на иммуногенность трихинелл оказывают влияние и степень адаптации вида трихинелл к хозяину: чем лучше адаптация вида к хозяину, тем выше иммуногенность и наоборот (44).
Эти данные были учтены при выведении вакциной линии трихинелл. Такая линия трихинелл была создана обычными методами селекции, проверена на животных, потом на себе. Было установлено, что вакцинная линия трихинелл не содержит никаких патогенных микроорганизмов (кроме симбиотических стафилококков), обладает высокой иммуногенностью и сниженной патогенностью по сравнению с дикими изолятами трихинелл. Тем не менее, мы пришли к заключению, что после иммунизирующей дозы трихинелл необходимо убрать из организма, так как пребывание личинок в мышцах в последующее время не приносит большой пользы, хотя слабая инвазия не имеет отрицательных последствий.
Откровенно говоря, назначению трихинелл больным предшествовала длительная психологическая борьба автора с собой. Несмотря на убедительные результаты, полученные на животных, потом на себе дать живых трихинелл другим людям было страшно. Слишком велик был груз догмы об их вредности. Ведь все без исключения учебники, справочники, энциклопедии утверждали одно и тоже: трихинеллез смертельно-опасная, в прошлом неизлечимая, болезнь человека и животных.
Животные, однажды переболев трихинеллезом, вновь не заражаются. Конечно, таким свойством обладают и многие другие возбудители инфекций и инвазий, на чем основано применение вакцин против этих болезней. Но это моновакцины, сила которых основана только на гуморальном иммунитете. У трихинелл же есть существенная особенность и преимущество: они индуцируют, кроме гуморального, еще и клеточный иммунитет – самую древнюю внутреннюю защиту от всего чужеродного.
Вероятно это связано с двухфазным (энтеральным и парэнтеральным) циклом развития трихинелл, совершающегося в одном хозяине в течении сравнительно длительного срока (3-4 недели). К тому же они являются многоклеточными и относительно организованными существами (раздельнополые, живородящие, с внутриклеточными бактериальными симбионтами, живут у более 100 видов млекопитающих и птиц). За время длительной эволюции Природа скомпоновала сложный комплекс неконкурентных антигенов, в ответ на которые хозяин одновременно вырабатывает и гуморальный, и клеточный иммунитет. Поэтому неудивительно, что на эти многокомпонентные антигены в организме хозяина разыгрывается сложная молекулярно-клеточная реакция, в результате которой появляется сильная иммунная защита от множества патогенов.
Краткая концепция по вакцине против иммунодефицита и рака
1. По разным оценкам от 30% до 50% взрослого населения разных стран мира страдает иммунодефицитом (ослаблена функция иммунной системы). Причин этому много, но главная из них - традиция питания, когда большая часть пищи и воды стерилизуется высокой температурой, при которой природные антигены разрушаются.
2. Без антигенов - нет иммунитета, отсюда - иммунодефицит.
3. Поскольку иммунная защита создана Природой главным образом для охраны гомеостаза (слежение - мониторинг за нормальным состоянием всего организма), то в иммунодефицитном организме гомеостаз нарушен. Появляются различные болезни, в том числе, многие инфекционные как туберкулез, бруцеллез, лейкоз, ВИЧ-инфекция (СПИД) и многие другие, а также злокачественные новообразования.
4. Сложилась ситуация, когда в традиции нашего бытия необходимо внести компонент, индуцирующий неспецифический иммунитет высокого уровня.
5. Таким компонентом может служить вакцина, приготовленная из трихинелл. За миллионы лет эволюции Природа очень удачно скомпоновала в них сложный комплекс антигенов, в ответ на который организм человека и теплокровных животных индуцирует (вырабатывает) иммунитет высокой напряженности, сохраняющийся длительное время или всю жизнь.
6. Нами (В.Бритов, Е.Нивин)
создан прообраз такой вакцины. Для восстановления клеточного иммунитета, в качестве его индуктора мы предлагаем препарат, состоящий из живых личинок трихинелл, полученных путем селекции. Линия обладает высокой иммуногенностью и слабой патогенностью. Иммунизировалось более 1000 пациентов с различными болезнями желудочно-кишечного тракта, дыхательной, урогенитальной, кроветворной систем, аутоиммунной, инфекционной и онкологической природы, в том числе: преждевременное старение, язва желудка и двенадцатиперстной кишки, гайморит, бронхиальная астма, мастопатия, миома матки, эндометриоз, невроз, энурез, гипертензия, импотенция, хронический миелоидный лейкоз, идеопатическая тромбоцитопеническая пурпура, рак 1 и 2 стадии различных локализаций и другие патологии. Вакцина обладает высокой эффективностью, безопасностью, простотой использования.
7. Такая вакцина нужна всем. Не меняя традиций по питанию, она значительно повысит здоровье населения, продлит миллионам граждан трудоспособный возраст и улучшит качество их жизни.
Для иллюстрации приведем ряд кратких описаний лечащих врачей и самих больных, характеризующих результаты иммунизации.
Больной, 59 лет обратился на консультацию в апреле 1995 года с диагнозом: Центральная бластома левого легкого с плевритом слева. Выглядит ослабленным худым стариком с землисто-серым цветом лица. Инвалид I группы по поводу бластомы. В январе-феврале 1995 г. прошел курс ПХТ. Выпали волосы, расслоились ногти. Вакцину принял 20.04.95 г. Через 2 недели началось обильное выделение густой гноевидной мокроты, что продолжалось около трех недель. С конца мая стал поправляться: появился аппетит, улучшилось самочувствие, стал набирать вес. Появилось желание работать физически. 12.09.95 г. проведена флюорография. Органических изменений в легких не выявлено, замечены лишь следы плеврита. 23.05.97 г. диагноз бластомы снят. Приступил к прежней работе (доцент с/х академии)... На февраль 2002 г. никаких жалоб не предъявляет, выглядит примерно на 10 лет моложе своих лет, несмотря на то, что вновь стал употреблять спиртное и табак.
Больной Т., 25 лет обратился на консультацию 10.04.99 г. с диагнозом идеопатическая тромбоцитопеническая пурпура. Состоит на диспансерном учете у гематолога с декабря 1991 г. Сопутствующий диагноз – поливалентная аллергия. С 1996 г. страдает одышкой даже при незначительной физической нагрузке. В ноябре того же года обнаружена тератома переднего средостения размером 8,0 х 7,3 см, по поводу которой в феврале 1997 г. проведена операция. В марте 1999 г. в заднем средостении выявлена тератома размером 3,8 х 3,7 см. геморрагический синдром. Первая вакцинация 20.04.99 г., вторая - 15.07.99 г. В июле 1999 г. осмотрен онкологом. Размер опухоли сократился до 2 см. самочувствие больного улучшилось, одышка и геморрагический синдром исчезли. Контрольная КТГ от 26.01.2000 г. патологии не выявлено, в том числе и на месте бывшей опухоли. На март 2002 r. самочувствие хорошее. Жалуется на появление простатита.
Больного вела врач-гематолог Е.В. Сокурова.
Больная И., 37 лет, замужем, имеет ребенка 12 лет. Было желание родить второго, но не беременела. Д.: эндометриоз, гайморит, геморрой, хроническая ангина, артрит, опухоль в щитовидной железе нераспознанного генеза. Считает себя иммунодефицитной, так как часто болеет и все у нее болит. Вакцинировалась 28.11.98 г. С февраля 1999 г. почувствовала значительное улучшение общего состояния, боли прекратились, опухоль в щитовидной железе рассосалась, вышеупомянутые болезни постепенно стали исчезать. В мае забеременела. 04.02.2000 г. родила девочку. Ребенок развивается нормально, мать кормит грудью. Никаких жалоб бывшая больная не предъявляет. На февраль 2002 г. все нормально.
Больной К., 52 г. поступил 05.04.98 г. с диагнозом базально-клеточный рак спинки носа. Больным считает себя с 1992 г., когда выдавил угорь на спинке носа. Постепенно на этом месте возникла ранка с корочкой. В 1993 г. дефект удалили лучами лазера. Но вскоре опухоль вновь стала увеличиваться в размере. В 1996 г. проведена лучевая терапия. В течение года рана была закрытой, затем начала набухать, кровоточить, вокруг язвы появился красный ареол размером 2,0-2,5 см, воспаление подошло близко к глазу. Из анамнеза выяснилось, что у больного в последние 2 года отмечалось недомогание, утомляемость, частое обострение гайморита, ангины, постоянно беспокоил геморрой, головные боли, ОРЗ, что демонстрировало явный иммунодефицит. Первая вакцинация проведена 06.04.98 г., повторная – в октябре того же года. В период между вакцинациями больной получал Детокс – продукт компании Визион + наружно прополисная мазь. Уже через месяц после первой вакцинации улучшилось общее состояние, исчезла язва на носу, затихли сопутствующие болезни. За зиму 1999-2000 г.г. набрал вес 5 кг. Единственное обострение гайморита было в ноябре 1999 г. после переохлаждения, что благополучно разрешилось за 9 дней. На февраль 2002 г. здоров.
Больного наблюдала врач Т.Г. Михайловская.
Больной С., 34 года, житель Новосибирска. Обратился на вакцинацию 19.05.96 г. с диагнозом простатит, трихомоноз. Обычное лечение в поликлинике не давали результатов. Через 2,5 месяца после вакцинации общее состояние нормализовалось, боли со стороны простаты исчезли, трихомонады лабораторно не выявлялись. В середине 1998 г. работая в Китае, заразился хламидиозом и вновь трихомонозом. Прошел четыре курса лечения в клиниках официальной медицины в Китае, Корее, Арабских Эмиратах и Новосибирске. После каждого курса лечения наблюдалось лишь кратковременное облегчение или эффекта вообще не было. Повторно вакцинировался 14.06.99 г. На следующий день после приема препарата температура тела повысилась до 39оС, но через день снизилась до нормы. 25.06.99 г. температура вновь повысилась до 39,0оС и держалась в пределах 38,0-39,5оС градусов в течение трех дней. Во второй половине июля 1999 г. прошел курс обычного медикаментозного лечения метронидазалом и доксициклином, после чего обследовался. Возбудителей указанных болезней не обнаружено. На февраль 2002 r. здоров. Сохраняет высокую работоспособность. Данный случай демонстрирует неэффективность специфических препаратов на фоне иммунодефицита и, наоборот, после восстановления функции иммунитета эти же препараты действуют успешно.
Больная Г., 47 лет. Обратилась за помощью в апреле 1999 г. с диагнозом: рецидив миомы из культи (оперирована в декабре 1993 г. по поводу смешанной миомы 11-12 недель) с подозрением на новообразование. Сопутствующие диагнозы: эрозивный гастрит антрального отдела, дискинезия желчевыводящих путей, мочекаменная болезнь с камнем в правой почке, хронический бронхит, эутериоз 2-й степени без клинических проявлений, НЦД по смешанному типу, фиброаденома правой молочной железы, неврастенический синдром, кистома правого яичника. Жаловалась на частую головную боль, периодические боли внизу живота, быструю утомляемость, плохое самочувствие, нервозность. Первую вакцинацию от 28.04.99 перенесла удовлетворительно. Через три месяца прошла обследование: эрозий в желудке не обнаружено, на месте кистомы – киста до 2 мм в диаметре, молочные железы без патологии. Самочувствие хорошее, исчезли боли, стала спокойнее, легче переносит нервные стрессы, повысилась работоспособность. Вторая вакцинация 12.08.99 г. УЗИ от 10.02.2000 г.: правый яичник без патологии, левый – норма. УЗИ яичников от 10.05.2000 г. – без патологии. Молочные железы осмотрены хирургом-онкологом - без патологии. На конец 2001 г. Самочувствие хорошее, жалоб не предъявляет.
Больная С., 57 лет. Обратилась 12.05.99 г. с диагнозом рак шейки матки Т3 Тх Мх эндофитная форма роста, параметический вариант. В марте 1999 г. прошла курс лучевой терапии. Гистология – плоскоклеточный рак без ороговения. Сопутствующие диагнозы: хронический цистит, наружный хронический геморрой, хронический колит (склонность к запору), мочекислый диатез. Три года назад оперирована по поводу мастопатии. Жалобы: плохой аппетит, отвращение к мясу, общая слабость, утомляемость. Первую вакцинацию от 12.05. 99 г. перенесла удовлетворительно. Через 4 месяца улучшилось общее состояние, появился аппетит, ест мясо, набрала вес 3 кг, кишечник функционирует нормально, геморрой не беспокоит, возросли жизненные силы и появился интерес к повседневным событиям. 10.02.01 г. самочувствие хорошее. Осмотрена гинекологом – патологии нет, узел в матке исчез. Снята с учета, 18.10.01 г. вакцинировалась повторно для закрепления результата. На февраль 2002 г. жалоб не предъявляет, работоспособность высокая, поправилась: самооценка состояния здоровья – хорошее.
Больную вела врач И.Н. Лукашкова.
В настоящее время самая удручающая ситуация сложилась в онкологии. Диагноз рак люди воспринимают как смертельный приговор. На четвертой стадии так оно и есть. На третьей стадии шансы на выздоровление есть, но слишком малы. Между тем, исходя из теории Бернета, злокачественные новообразования не могут развиться в организме с нормально функционирующей иммунной системой, прежде всего ее клеточной части. И сколько бы хирурги не вырезали пораженные опухолью ткани, злокачественные клетки будут возникать вновь и вновь, не на этом месте, так в другом, ведь причина (иммунодефицит) остается. В случаях, когда больному назначаются химиотерапия, при которой угнетается функция не только злокачественных, но преимущественно защитных – иммунокомпетентных клеток (агрессор обычно сильнее жертвы), то положение больного в перспективе только ухудшается.
Но силы организма не беспредельны. Они рассчитаны на естественную среду обитания, где работают природные законы. Органы и ткани подлежат “ремонту” не на любой стадии износа, а только когда нарушена их функция, при сохранении морфологических структур, чтобы в иммунодефицитном организме заработала внутренняя защита, нужна, прежде всего, морфологическая целостность иммунокомпетентных органов, в противном случае никакие вакцины или иные препараты не помогут. То же самое, если организм сильно ослаблен множеством патогенов (возбудителями болезней или злокачественными клетками), которые постоянно вырабатывают разрушительную энергию и токсины. Онкологи подсчитали, что для уничтожения одной злокачественной клетки требуется от 10 до 100 лимфоцитов. У человека в норме их 10 12 . Опухоль диаметром 1 см содержит 10 7 клеток. Диагноз на рак во внутренних органах ставится, когда имеется 10 9 раковых клеток и опухоль уже прошла большую половину своего пути развития. Когда число злокачественных клеток приближается к числу лейкоцитов – наступает смерть (51). Продолжительность развития рака в среднем у человека составляет 10-12 лет. Срок приличный. Природа предоставляет возможность и для профилактики и для лечения. Наш препарат на 1-й и 2-й стадиях рака различных локализаций работает безотказно, если больной соблюдает элементарные правила здорового образа жизни, освобождается от дурных привычек. Наш метод хорошо сочетается с хирургией и облучением, но не с химиотерапией. Вероятно “мягкие” химиопрепараты в умеренных дозах тоже могут сочетаться с вакцинацией против иммунодефицита. Однако таких наблюдений у нас пока нет.
На третьей стадии рака эффективность нашего препарата резко снижается и не превышает 5-7% при максимальном сроке наблюдения 2,5 года. На четвертой стадии – излечения от рака не было ни разу, хотя у некоторых больных наступало кратковременное улучшение общего состояния сроком на 2-3 месяца. Поэтому на четвертой стадии рака наш препарат не показан, но иногда врачи настоятельно просят для своих родственников.
Вероятно, самой опасной и трудно управляемой причиной иммунодефицита является ВИЧ-инфекция. Однако, из этой категории больных до 2002 года никто к нам не обращался. Только в январе-феврале 2002 года иммунизацию прошли первые три ВИЧ-инфицированых пациента. Мы надеемся, что наш препарат может оказаться эффективным средством в профилактике этой инфекции и в предотвращении СПИДа. По данным литературных источников, несколько десятков вакцин гуморальной направленности, испытанных против ВИЧ-инфекции не дали положительных результатов. М.Клеричи и Дж.Ширер считают, что против ВИЧ-инфекции нужно создавать вакцины клеточного типа, а М.Джонстон предполагает: “Быть может, дело в том, что для эффективности вакцины нужно, чтобы она вызывала не только гуморальный, но и клеточный ответ” (52). Наш препарат отвечает этому требованию. Более того, слабая интенсивность трихинеллезной инвазии не представляет никакой опасности для человека. Ведь все животные-трихинеллоносители (тигры, медведи, волки, лисицы, барсуки, енотовидные собаки и другие), а также миллионы людей живут с трихинеллами всю жизнь, ничего не подозревая об этом. Это проверено самой Природой. Так что боязнь перед вакцинацией необоснованна.
Мы полагаем, что трихинеллы окажутся полезными для профилактики и лечения первых стадий туберкулеза, так как только клеточный иммунитет эффективен при этом заболевании. Поскольку, на фоне высокой активности клеточного иммунитета специфические препараты, даже в значительно меньших дозах, воздействуют более результативно, предлагаемый препарат из трихинелл снизит расход противотуберкулезных средств и ускорит выздоровление больных.
Препарат следует испытать при таких неизлечимых болезнях как: Альцгеймера, Паркинсона, Шарко и некоторых других, особенно аутоиммунных, ибо их этиология остается до сих пор загадочной.
Нельзя умолчать о тех пациентах, которые остались неудовлетворенными от приема нашего препарата. Их число составляет примерно 10%. Это, прежде всего, больные с очень давними хроническими процессами, с органическими поражениями органов и тканей как глаукома, отит, когда разрушены уже все слуховые косточки, артрозы, гепатиты, ожирение, сколиозы, гайморит, психические болезни, рак 3-й и 4-й стадии и ряд других. Но и эта группа больных, в большинстве случаев, получает облегчение и улучшение общего состояния в виде нормализации обменных процессов, повышения резистентности организма к бактериальным и вирусным заболеваниям, стабилизации процесса.
Литература
Апанасевич В.Н., Бриттов В.А., Збань Ю.В. // Вопросы диагностики и лечения злокачественных опухолей. Владивосток. 1999. с.55-57
Апанасевич В.Н., Бриттов В.А., Збань Ю.В. // Актуальные проблемы в онкологии. Владивосток, 1998. с.109-110.
Багрянцев В. Н. // «Конкурент» 2001, № 3, с.4.
Бессонов А.С. //Ветеринария. 1994. № 2 с.34-36
Бернет Ф. Клеточная иммунология. М., «Мир», 1971. 542с.
Беляк А. Биология опухолей. М.: «Мир», 1987. 206с.
Бердели Тим. Клеточный ответ // В мире науки. 1993. № 1. с.89-90
Беpезанцев Ю.А. Тpихинеллёз. Л.: Медицина, 1974. С. 160.
Беpезанцев Ю.А. Тpихинеллёз / Гельминтозы человека. М.: Медицина, 1985. С. 214–226.
Бритов В.А. охрана гомеостаза у человека и животных. Ростов-на-Дону. РЮИ МВД России, 1999, 20с.
Бриттов В.А. Возбудители трихинеллёза. «Наука» М., 1982. с.220-222
Бриттов В.А. Проблема трихинеллёза в Приморском крае. Владивосток, 1995. с.12
Бритов В. А. Проблема трихинеллёза на Камчатке. Владивосток – Петропавловск-Камчатский, 1997. 57с.
Бриттов В.А. // Химия и жизнь. 1990, № 11. с.9-41.
Библия. Издание Московской патриархии. М., 1988. Левит, 11
Змушко Е.И., Белозеров Е.С., Митин Ю.А. Клиническая иммунология. «Питер», 2001. 574с.
Купер Э. Сравнительная иммунология. М., «Мир», 1980. 422с.
Логачёв Е.Д. // Проблемы экспериментальной морфофизиологии и генетики. Кемерово, 1976. с.139
Пол У. Иммунология. М., «Мир», 1980. 422с.
Петров Р.В. Беседы о новой иммунологии. М., «Молодая гвардия», 1978. 222с.
Петров Р. В. Иммунология. М., «Медицина», 1982. 368с.
Петров Р.В. Я или не Я. М., «Молодая гвардия», 1983. 273с.
Ройт А. Основы иммунологии. М., «Мир», 1991. 327с.
Сапунов А.Я., Мурашов Н.Е., Шевкопляс В.Н., Иващенко А.А. // Материалы доклада научн. Конф. М., 2001. с.237-240
Слепян Э. И. патологические новообразования и их возбудители у растений. «Наука» Ленинградское отделение. Л., 1973. 510с.
Понюшенко H.Г., Богомолова Е.Е./Ветеpинаpия, 1994. № 10. С. 11–12.
На основании собственных исследований и литературных источников описаны трихинеллы и их роль в охране гомеостаза у человека и животных.
Рассчитана на специалистов и студентов биологических дисциплин, врачей, философов и граждан, интересующихся состоянием своего здоровья.
Шевелев А.С. Противоречивая иммунология. М., «Медицина», 1978. 255с. Сергиев В.П., Озерецковская Н.Н. // Химия и жизнь. М., 1993, № 1. с.72-77.
Многие глистные заболевания передаются человеку именно от животных (подробнее об инфекционных болезнях, передающихся от животных к людям ). И, именно об одном из таких заболеваний – о трихинеллёзе мы и хотим вам сегодня рассказать. В чём заключается опасность, как можно заразиться, и как предупредить трихинеллёз – обо всём этом на страницах нашей статьи…
Описание трихинеллёза

Здоровые животные, поедая больных зверей и их трупы, заражаются трихинеллами и сами становятся источниками распространения заболевания. А, вот домашние животные, как правило, заражаются трихенеллёзом, когда им скармливают тушки или внутренности зверей, добытых на охоте, или когда они поедают отбросы и падаль.
Человек заражается трихинеллёзом при употреблении в пищу мяса свиньи, кабана, медведя, барсука, в котором содержатся живые личинки трихинелл.
Достаточно съесть 10-15 граммов трихинеллезного мяса для того, чтобы получить неизлечимое тяжелое заболевание.
Симптомы трихинеллёза
Яркими признаками заболевания можно назвать отек век, препятствующий больному открывать глаза, одутловатость лица, сильные боли в мышцах, болезненность при движении глазных яблок, припухлость языка, в результате чего затруднены речь и проглатывание пищи, боль при дыхании, резкие головные боли, лихорадка и бессонница. Смертность при трихинеллёзе может достигать 30%.
Профилактика распространения трихинеллёза

Для того, чтобы не допустить распространение заболевания трихинеллёзом среди людей и животных, рекомендуется придерживаться следующих правил:
- Каждую свиную тушу, а также тушу , и других животных, прежде, чем употреблять в пищу, необходимо подвергать обязательному ветеринарному осмотру.
- Нельзя кормить домашних животных трихинеллёзным мясом.
- Тушки диких зверей, равно как и трупы домашних животных, пораженные трихинеллёзом, необходимо утилизировать, а в случая невозможной утилизации их необходимо сжигать или закапывать глубоко в землю.
- В местах убоя и разделки животных, хранения мясных продуктов или тушек животных обязательно проводить регулярную дератизацию, истреблять мышей и крыс, сжигая трупы грызунов или закапывая их глубоко в землю на скотомогильниках.
Сегодня мы с вами говорили о трихинеллёзе, о том, чем опасно это заболевание, как происходит заражение, как предупредить распространение трихинеллёза.
А, какие меры предпринимаете вы для того, чтобы обезопасить себя от трихинёллеза? Поделитесь с нами своим опытом, историями.
Статья подготовлена по материалам гельминтолога. В. Островской, взятым из свободных источников.