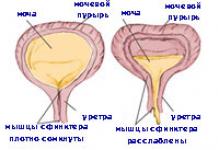
Antinukleārās antivielas (ANA, ANA, antinukleārās antivielas, antinukleārais faktors-ANF) - NIF metode uz HEp-2 šūnu līnijas ar luminiscences veida noteikšanu.- autoimūno saistaudu slimību indikators. ANA ir autoantivielu grupa pret proteīniem un citiem komponentiem (ieskaitot DNS), kas atrodami šūnu kodolos. Galvenās lietošanas indikācijas: diagnozes izslēgšana - sistēmiskā sarkanā vilkēde (tiek uzskatīts, ka ANA parādās 90% SLE gadījumu, citiem vārdiem sakot, negatīvs rezultāts ar aptuveni 90% varbūtību izslēdz SLE diagnozi), diferenciāldiagnoze sistēmiskas kolagenozes (sistēmiskā sarkanā vilkēde, sklerodermija, mezglains periarterīts, dermatomiozīts), hronisks aktīvs hepatīts.
Līdz šim ir aprakstītas vairāk nekā 200 ANA šķirnes, kas vērstas pret nukleīnskābēm, histoniem, kodolmembrānas proteīniem, spliceosomu komponentiem, ribonukleoroproteīniem, nukleolāriem un centromēru proteīniem. Tajā pašā laikā tie bojā saistaudus, kas veicināja antinukleārā faktora noteikšanas ieviešanu kā sistēmisku saistaudu slimību testu. Termins “pretnukleārais faktors” attiecas uz testu antinukleāro antivielu noteikšanai, izmantojot netiešās imunofluorescences metodi.
Viena no metodēm antinukleārā faktora (pretnukleāro antivielu) noteikšanai asinīs ir netiešās imunofluorescences metode, uzklājot pacienta serumu uz nepārtrauktas cilvēka šūnu līnijas HEp-2 (cilvēka epitēlija karcinoma hep-2 balsenes šūnām) audu šūnām. līnija, kas satur dažādus kodola antigēnus), izmantojot marķētu konjugātu ar cilvēka antivielām. Kā substrātus var izmantot arī citas cilvēka šūnu līnijas, taču to labās morfoloģijas un kultivēšanas vienkāršības dēļ Hep-2 ir kļuvis par vispārpieņemtu netiešās imunofluorescences substrātu. ANF noteikšanas metodi Tan izstrādāja 1982. gadā, par substrātu izmantojot cilvēka nepārtraukto epitēlija šūnu līniju HEp-2. Šī šūnu līnija, kas iegūta no cilvēka balsenes adenokarcinomas, ir liela poliploīda nekeratinizējoša plakanšūna, kas uz stikla veido monoslāni. Pacienta serumu inkubē ar audu substrātu, un antinukleārās antivielas no pacienta seruma (ja tādas ir) saistās ar attiecīgajiem kodola antigēniem. Autoantivielu saistīšanās vietas tiek noteiktas, izmantojot ar fluoresceīnu iezīmētu anti-cilvēka antiserumu. Reakcijas rezultātus novērtē ar mikroskopiju, izmantojot luminiscējošu mikroskopu, un vizuāli novērtē saistīto antivielu luminiscences raksturu. Starp HEp-2 priekšrocībām (salīdzinājumā ar dzīvnieku audu krio sekcijām) var atzīmēt augsto šūnu dalīšanās biežumu, kas ļauj noteikt antivielas pret antigēniem, kas ekspresēti tikai šūnu dalīšanās laikā, un audu šūnu matricas neesamību, kas apgrūtina konkrētas luminiscences vizualizāciju, salīdzinot ar histoloģiskām sekcijām. Dažu slimību, piemēram, SLE, sistēmiskās sklerodermijas (sistēmiskās sklerozes) un dažu infekciju gadījumā pacienta imūnsistēma uztver savu audu šūnu kodolus (kodolproteīnus) kā svešus un ražo pret tiem antivielas (pretnukleārās antivielas - AHA). Tajā pašā laikā tie bojā saistaudus, kas veicināja antinukleārā faktora noteikšanas ieviešanu kā sistēmisku saistaudu slimību testu.
Interpretējot datus, jāņem vērā, ka AHA spektrā ir liela autoantivielu grupa pret DNS, nukleoproteīniem, histoniem, kodola ribonukleoproteīniem un citiem kodolkomponentiem. Tādējādi testa mērķis ir noteikt dažādas antivielas pret kodolu un citoplazmas komponentiem, kas pirmo reizi tika atklāti SLE. Tālāk diagnostikas kritēriji Pārbaude tika paplašināta, jo šīs antivielas tika atklātas citās saistaudu slimībās.
Skrīninga testos kopējās ANA noteikšanai parasti izmanto šādu antigēnu komplektu, kas ir galvenie autoimūno saistaudu slimību marķieri: SS-A (Ro), SS-B (La), BNP70, Sm, RNP/Sm, J01, centromērs B.
Galvenie antigēni, ko izmanto mūsdienu komplektos IgG klases kodola antivielu noteikšanai, ir attēloti ar šādu komplektu:
- SS-A (Ro) - kodola ribonukleoproteīni (polipeptīdi). Antivielas pret tām biežāk tiek konstatētas sistēmiskās sklerodermijas (60% gadījumu), Sjogrena sindroma (līdz 70% gadījumu) un SLE (līdz 30% gadījumu). Tiek uzskatīts, ka, ja šīs antivielas tiek konstatētas grūtnieču asinīs, tas liecina par jaundzimušo lupus līdzīga sindroma (jaundzimušo vilkēdes sindroma) rašanās riska palielināšanos jaundzimušajam bērnam. Šīs mātes antivielas šķērso placentu un izraisa augļa bojājumus, izraisot hemolītisko anēmiju un trombocitopēniju. Nopietnas sekas ir bērna sirds vadīšanas sistēmas bojājumi (līdz pastāvīgai sirds stimulācijai). Tika atzīmēts, ka sievietēm, kurām grūtniecības laikā bija ievērojams šo antivielu titrs, bez acīmredzama klīniskās pazīmes, pēc tam attīstās jebkura autoimūna slimība, tostarp SLE.
- SS-B (La) - kodolproteīni. Antivielas pret tām tiek konstatētas līdz 60% gadījumu ar Sjogrena sindromu un 15% gadījumu ar SLE.
- Scl-70 ir enzīma proteīns, kas iesaistīts nukleīnskābju metabolismā (topoizomerāze-1). Antivielas pret šo proteīnu ir visspecifiskākās sistēmiskai sklerodermijai (līdz 70% gadījumu).
- Divpavedienu DNS ir dabiska DNS. Antivielas pret DNS ir visspecifiskākās SLE gadījumā (līdz 80% gadījumu), un tās praktiski nav nosakāmas reimatoīdā artrīta un sklerodermijas gadījumā.
- RNP/Sm - RNP/Sm antigēnu komplekss sastāv no U1-ribonukleoproteīniem: U1-68, U1-A, U1-C, U5, U6; un arī no Sm-polipeptīdiem: SmA | , SmB | B, SmD, SmE, SmF, SmG. Antivielas, kas veidojas pret šiem antigēniem, ir visspecifiskākās jauktām saistaudu slimībām – t.i. ja Jums ir sklerodermijas simptomi, reimatoīdais artrīts, SLE, polimiozīts (apmēram 95% gadījumu) un mazākā mērā SLE (līdz 30% gadījumu).
- Jo-1 ir aminoacilpārneses RNS sintetāzes enzīms. Autoantivielas pret šo proteīnu ir diagnostiski nozīmīgas miozīta (polimiozīta/dermatomiozīta) gadījumā.
- CENP-B (Centromere) - Anti-Centromer antivielu noteikšanai (Anti-Centromer B), ar mērķi diagnosticēt CREST sindromu (šis sindroms ir ādas pārkaļķošanās, Reino sindroma, barības vada motorikas traucējumu, sklerodaktilijas, telangiektāzijas kombinācija). CREST sindroms attiecas uz sistēmiskās sklerozes (sistēmiskās sklerozes) variantu. Šīs antivielas pacientiem norāda uz labvēlīgu sistēmiskas sklerodermijas gaitu un norāda uz nelieliem iekšējo orgānu bojājumiem.
- Hep-2 šūnas ir cilvēka balsenes epitēlija karcinomas šūnas no Hep-2 līnijas, kas satur daudz dažādu kodolantigēnu, tostarp SS-A (Ro) antigēnu un centromēru antigēnus. Antivielas pret Hep-2 tiek konstatētas pacientiem ar polimiozītu un dermatomiozītu līdz pat 90% gadījumu.
- Mitohondriji (PDC) - PDC - piruvāta dehidrogenāzes komplekss. Liela antimitohondriju antivielu grupa ir autoantivielas, kas veidojas pret piruvāta dehidrogenāzes kompleksa enzīmiem, kas atrodas šūnu mitohondrijās un ir iesaistītas piruvāta oksidatīvajā dekarboksilācijā.
ANA bieži tiek konstatētas žults cirozes gadījumā.
AHA parasti neiekļūst dzīvās šūnās un tāpēc ir nekaitīgas. Bet dažreiz tie veido antigēnu-antivielu kompleksus, kas izraisa audu bojājumus (kā SLE gadījumā, nieru bojājumus). Tā kā patoloģiskajā procesā ir iesaistīti daudzi orgāni, AHA noteikšanas diagnostiskā vērtība ir maza un analīzes rezultāti tikai daļēji apstiprina klīniskos datus.
Papildus reimatiskajām slimībām ANA tiek konstatēti arī hroniska aktīva hepatīta gadījumā līdz pat 50% gadījumu. Izskats (zemi titri) ir iespējams, ja iekaisuma slimības, onkoloģijas un vīrusu infekcijas.
- Pretkodolu antivielu noteikšanas salīdzinošais biežums.
Slimība un stāvoklis Noteikšanas biežums, % SCR 95-100 Lupoīds hepatīts (jauns nosaukums - hronisks autoimūns hepatīts) 70 -80% Felty sindroms (Felty. 1924) - reimatoīdais artrīts + splenomegālija + neitropēnija + leikopēnija + limfadenopātija. 95-100 Sistēmiskā sklerodermija 75-80 Zāļu izraisīts vilkēdes sindroms (hidralazīns, prokainamīds, izoniazīds) Apmēram 50 Šegrena sindroms (Autoimūns sistēmisks saistaudu bojājums. Raksturīga eksokrīno dziedzeru, galvenokārt siekalu un asaru, iesaistīšanās patoloģiskajā procesā un hroniska progresējoša gaita). 40-75 SLE slimnieka klīniski veseli radinieki Apmēram 25 Diskoidālā sarkanā vilkēde 15-50 Hronisks juvenīlais artrīts, reimatoīdais artrīts 15-30 Nodosa periarterīts 15-25 Dermatomiozīts un polimiozīts 10-30 Reimatisms Ap 5 Reino sindroms 15-20
Pamatojoties uz antivielām un nosakot to koncentrāciju asins plazmā, tiek diagnosticēti daudzi ķermeņa stāvokļi. Viens no indikatoriem ir antinukleārais faktors, kas ar savu nosaukumu apvieno dažādu veidu antivielu grupu, kas vērsta pret šūnu komponentiem. Kad šāds faktors tiek identificēts, ir jēga runāt par autoimūnu slimību, īpaši sistēmisku sarkano vilkēdi.
Lai gan tests ir universāls, lai noteiktu daudzas sistēmiskas ķermeņa patoloģijas, jo īpaši tādu nopietnu slimību kā sarkanā vilkēde, ar to ir saistītas dažas interesantas pazīmes. To sāka izmantot kopš 1957. gada, bet tehnika kļuva plaši izplatīta tikai no pagājušā gadsimta 80. gadu beigām. Ir vērts atzīmēt, ka implantu klātbūtne krūtīs palielina antinukleāro antivielu titru, ko novēro no 5% līdz 55% no visiem gadījumiem sievietēm.
Kas viņi ir?
Antivielu kompleksu, kas ietver antinukleāro faktoru, attēlo vairāk nekā 200 indikatori, visbiežāk tie ir G klases imūnglobulīni, retos gadījumos IgM un IgA. Tie parādās patoloģijās, kurām raksturīgs bojājuma autoimūns vai reimatisks raksturs, ko izraisa imūnsistēmas tolerances traucējumi pret saviem audiem.
Dažos apstākļos imūnsistēma visus savus spēkus virza nevis uz cīņu pret svešiem faktoriem, bet pret saviem audiem un šūnām, kam parasti nevajadzētu notikt. Tolerance pret noteiktām šūnām, uz kurām ir vērsta agresija, tiek salauzta, un attīstās autoimūna slimība. Antivielas, kas rodas slimības procesa laikā, jeb kompleksus sauc par autoimūnām.
Daudziem cilvēkiem ir neliels autoantivielu daudzums, taču tas nav slimības pazīme. Tikai nopietns imūnsistēmas darbības traucējums var izraisīt autoantivielu līmeņa paaugstināšanos, tas ir iemesls, lai veiktu atbilstošu diagnozi. Bet tas joprojām ir jāpapildina ar citiem pētījumiem, jo īpaši ar asinīm, urīnu, kā arī klīniskām izpausmēm.
Personai, kas cieš no sistēmiskas sarkanās vilkēdes, ANF palielinās pat pirms pirmo simptomu parādīšanās. No visiem pacientiem 95% ir paaugstināts antinukleārais faktors asinīs, ko papildina slimības simptomi, kas, savukārt, apstiprina diagnozi.
Faktora rašanās mehānisms
Ir vairāki iemesli, kas veicina slimības attīstību cilvēkiem. Viss notiek noteiktā secībā:
- Saules ultravioletā starojuma ietekmē āda tiek uzsākti iepriekš ģenētiski ieprogrammētas šūnu nāves procesi, ko sauc par apoptozi. Tā ir normāla organisma reakcija, tomēr sistēmiskas dabas slimību gadījumā limfocīti sāk intensīvi migrēt.
- Iepriekš nepieejamie, neredzamie šūnu komponenti kļūst pieejami imūnsistēmai, jo īpaši šūnu membrāna, nukleoli, histoni, kodola membrāna un citi. Viņi kļūst kaili, un makrofāgi, tā vietā, lai pārstrādātu šādu materiālu, pārraida informāciju tālāk, provocējot ķermeņa imūnreakciju.
- B-limfocīti reaģē uz makrofāgu doto signālu, veidojot antinukleāras antivielas, kas mijiedarbojas ar atbilstošo antigēnu, veidojot kompleksu.
- Kompleksi tiek nogulsnēti uz orgānu un audu membrānām, tas notiek bagātīgi uz asinsvadu sieniņas no iekšpuses vai tiek aktivizēta vietēja imūnreakcija.
- Bojājumi pasliktina orgānu darbību.

Analīze, indikācijas
Ir vairākas norādes, kad tiek noteikts antinukleāro antivielu tests. Pirmkārt, ir aizdomas par sistēmiskās sarkanās vilkēdes, Sjogrena sindroma attīstību. Ja tāds ir sistēmiska slimība, ārstam ir aizdomas par ko citu, piemēram, uz sarkanās vilkēdes fona var veidoties antifosfolipīdu sindroms.
Simptomi un kad veikt pārbaudi
Vienmēr ir simptomi, kuru parādīšanās brīdina cilvēku un piespiež viņu veikt pārbaudi. Ārstam jāorientē pacients, ja ir:
- Artrīts, kas izpaužas kā locītavas iekaisums, ar sāpēm, pietūkumu, kustību traucējumiem, ādas apsārtumu virs tās un paaugstinātu temperatūru.
- Nenāktu par ļaunu izmeklējums uz perikardītu un pleirītu, kuru cēlonis nav zināms.
- Nieru bojājumi, kas saistīti ar imūnsistēmas traucējumiem, izmaiņu parādīšanos urīna analīzēs, jo īpaši olbaltumvielās, asinīs.
- Vēl viena indikācija ir anēmijas hemolītiskais variants, kurā sarkanās asins šūnas tiek iznīcinātas lielos daudzumos, palielinās bilirubīna līmenis asinīs un urīna analīzes.
- Indikācija ir trombocītu un neitrofilu līmeņa pazemināšanās leikocītu formulā.
- Izpausmes uz ādas izsitumu, sabiezējumu veidā, kas rodas pēc saules iedarbības.
- Reino sindroms, kurā roku un kāju pirksti periodiski maina krāsu. Tie kļūst bāli, zili vai sarkani, jutīgums ir traucēts, sāpes satrauc.
- Indikācija ir neraksturīgi simptomi no neiroloģijas vai psihiatrijas.
- Ja temperatūra paaugstinās, rodas nogurums, samazinās ķermeņa svars, palielinās limfmezgli.

Pētījumu veidi
Ir divas metodes, kas ļauj noteikt antinukleārās antivielas asinīs. Pirmo sauc par netiešo imunofluorescences mikroskopiju. Viņas šūnu līnija tika iegūta no adenokarcinomas balsenes. Ja ir antinukleāras antivielas, tās saistās ar specifiskiem antigēniem, pēc tam tiek pievienoti tagi, kas var spīdēt noteiktā gaismas spektrā. Zem mikroskopa kļūst iespējams noteikt mirdzuma intensitāti un veidu.
Šī metode ir atzīta par labāko antinukleāro antivielu līmeņa noteikšanai. Tam ir cits nosaukums - lupus teststrēmeles.
Pētījuma rezultāts ir titrs vai maksimālais asins atšķaidījums, kas piešķir spīdumu. Ja rezultāts ir pozitīvs, tiek aprakstīts mirdzuma veids. Titrs palielinās ar lielu antivielu uzkrāšanos. Zemu titru var uzskatīt par negatīvu rezultātu, savukārt augsts titrs var liecināt par antinukleāro antivielu koncentrācijas palielināšanos.
Otrā diagnostikas iespēja ir enzīmu imūnanalīze. Tās būtība ir tāda, ka antivielas, kas atrodas asinīs, nonāk saskarē ar atbilstošo antigēnu, kā rezultātā šķīdums maina savu krāsu.
Ir vērts atzīmēt, ka pozitīvs testa rezultāts nav 100% diagnoze. Tas ir signāls, ka nepieciešama papildu pārbaude, kas palīdzēs identificēt slimību agrīnā periodā un nozīmēt ārstēšanu. Ja antinukleāro faktoru tests ir negatīvs, mēs varam runāt par to pilnīgu neesamību, taču nav izslēgta aizdomas par autoimūnu patoloģiju.
Obligāti jāveic asins analīzes dažādi rādītāji. Taču der atcerēties, ka rezultātus var ietekmēt noteiktu medikamentu lietošana, kā arī akūtu vai hroniskas slimības. Speciālists vienmēr palīdzēs izprast visas smalkumus, pēc tam noteiks diagnozi un ieteiks, kā rīkoties tālāk.
Antinukleārais faktors HEp-2 šūnu līnijā (ANF) ir tests antinukleāro antivielu noteikšanai ar netiešo imunofluorescenci.
Sistēmiskās sarkanās vilkēdes (SLE) un citu sistēmisku reimatisko slimību gadījumā imūnā atbilde ir vērsta pret nukleoproteīna antigēniem, t.i. nukleīnskābju un olbaltumvielu kompleksi. Šie endogēnie nukleoproteīnu kompleksi veidojas epitēlija šūnu apoptozes procesā un atgādina svešas vīrusu daļiņas. Apoptozes procesu paātrināšana ultravioletā starojuma ietekmē, vīrusu infekcijas Un zāles, izraisa autoimūnas reakcijas SLE gadījumā. Apoptozes laikā galvenie antivielu antigēni kondensējas apoptotiskos ķermeņos, kas kļūst par autoantivielu mērķiem. Pašlaik ir aprakstīti aptuveni 200 veidu antivielu pret nukleoproteīniem un riboproteīniem. nukleīnskābes, ko sauc par antinukleārajām antivielām. Autoimūno slimību gadījumā autoantivielām pret kodola antigēniem nav tiešas citotoksiskas iedarbības uz cilvēka šūnām, tomēr imūnkomplekss spēj izraisīt imunoloģisku iekaisumu, īpaši vietās, kur asinsvadi ir īpaši plāni, tostarp nierēs, ādā, centrālajā nervu sistēmā. locītavu sinovijā un pleirā.
Antinukleārā faktora (ANF) testēšana ir galvenā antinukleāro antivielu noteikšanas metode, kas ļauj noteikt autoantivielas pret nukleīnskābēm (dsDNS, ssDNS, RNS), ribonukleoproteīniem, kā arī lielāko daļu konformācijas un nešķīstošo antigēnu.
Antinukleārās antivielas tiek noteiktas, saistoties ar nepārtrauktas cilvēka epitēlija šūnu līnijas (HEp-2) intracelulārajiem antigēniem. HEp-2 šūnu kodols un citoplazma satur visus cilvēka organismam raksturīgos antigēnus, kas ļauj vienā testā noteikt visas galvenās antinukleārās antivielas. Vadošie Eiropas (EASIgroup2010) un Amerikas eksperti (ACRANATaskforce2008) kā zelta standartu pretnukleāro antivielu noteikšanai iesaka izmantot HEp2 šūnu līnijas netiešās imunofluorescences metodi. Antinukleāro antivielu antigēnu daudzveidības dēļ ne visus tos var attīrīt vai sintezēt, lai tos izmantotu enzīmu imūnanalīzēs antinukleāro antivielu noteikšanai.
ANF pozitivitāte uz HEp-2 šūnu līniju tiek novērota sistēmiskās sarkanās vilkēdes (SLE), sistēmisku reimatisko slimību un daudzu autoimūno slimību gadījumā, kas padara to par universālu testu pacientu ar autoimūnu patoloģiju izmeklēšanā. Pozitīvs ANF rezultāts tiek novērots vairāk nekā 90% pacientu ar difūzām saistaudu slimībām, piemēram, sistēmisku sarkano vilkēdi un ādas formasšī slimība, sklerodermija un tās šķirnes, jaukta saistaudu slimība, Sjogrena sindroms. ANF noteikšanai ir liela nozīme juvenilā reimatoīdā artrīta un autoimūno aknu slimību diagnostikā. Šīs autoantivielu saimes pārstāvjus var atrast dažādu citu autoimūnu (tiroidīts, diabēts), infekciozo (vīrusu hepatītu), iekaisuma un onkoloģiskās slimības. ANF sastopamība sasniedz 1–3% klīniski veseliem cilvēkiem un nedaudz palielinās cilvēkiem, kas vecāki par 65 gadiem. Personām ar augstu ANF titru ir paaugstināts autoimūnu slimību attīstības risks.
Indikācijas:
- Sistēmiskā sarkanā vilkēde.
- Subakūta ādas vilkēde un citi ādas vilkēdes veidi.
- Jaukta saistaudu slimība.
- Šegrena sindroms un ar to saistītās slimības.
- Difūza un lokalizēta sklerodermija, CREST sindroms.
- Iekaisīgas miopātijas (polimiozīts un dermatomiozīts).
- Juvenīls hronisks artrīts.
- Autoimūns hepatīts.
- Primārā biliārā ciroze un sklerozējošais holangīts.
- Polineuropatija un mielīts.
Asinis ieteicams ziedot no rīta, no pulksten 8 līdz 12. Asinis tiek ņemtas tukšā dūšā vai 4-6 stundas pēc pēdējās ēdienreizes. Ir atļauts dzert ūdeni bez gāzes un cukura. Pārbaudes priekšvakarā jāizvairās no pārtikas pārslodzes.
Rezultātu interpretācija
Mērvienības: titrs.
Atsauces vērtības:<1:160 (отрицательно).
ANF noteikšanas rezultāts ir titrs, kas ir seruma galīgā atšķaidījuma vērtība, kurā saglabājas ievērojama kodola fluorescence. Jo lielāks ir frakcijas saucējs, jo lielāks ir seruma atšķaidījums, jo vairāk antivielu pacienta serumā. Augsti seruma atšķaidīšanas titri atspoguļo augstu autoantivielu afinitāti un koncentrāciju.
Augsta līmeņa noteikšana (1/640 un vairāk) norāda uz lielu sistēmiskas reimatiskas slimības vai autoimūnas aknu slimības iespējamību un prasa rūpīgu klīnisku, laboratorisku un instrumentālu izmeklēšanu. Paaugstināta antinukleāro faktoru titru trūkums ievērojami samazina sistēmisku autoimūnu slimību iespējamību.
Zemos titros (līdz 1/160) antinukleāro faktoru var novērot 1–2% veselu cilvēku un pacientu ar sistēmiskām slimībām radiniekiem. Pozitīvo titru biežums populācijā nedaudz palielinās līdz ar vecumu. Zems antinukleāro antivielu titri var rasties daudzu autoimūnu, infekcijas un onkoloģisko slimību gadījumā. Augstu antinukleāro antivielu titru trūkums ievērojami samazina sistēmiskā reimatiskā procesa iespējamību, un to var izmantot, lai izslēgtu, nevis apstiprinātu diagnozi.
Sistēmiskas reimatiskas slimības
Antinukleārais faktors (ANF) un luminiscences veids
Antinukleārā faktora (ANF) noteikšana ir galvenā antinukleāro antivielu noteikšanas metode, kas ļauj noteikt lielāko daļu antinukleāro antivielu veidu, tai skaitā autoantivielas pret nukleīnskābēm (dsDNS, ssDNS, RNS), konformācijas un nešķīstošus antigēnus. ANF noteikšanas rezultāts ir autoantivielu klātbūtne diagnostikas titrā, seruma atšķaidījuma galīgais titrs, kas atspoguļo autoantivielu afinitāti un koncentrāciju, kā arī šūnas kodola luminiscences veidu. (pārbaude 01.02.15.005). Konkrētas tehnikas īpašības galvenokārt ir atkarīgas no substrāta izvēles, kas var atšķirties no kriozes (žurku aknām vai nierēm) līdz kultivētām proliferējošām šūnu līnijām (Hep2, Kb, HeLa), kā arī no audu fiksācijas metodes, kas var ietekmēt vairāku kodola antigēnu ANA saglabāšana.
Antinukleāro antivielu noteikšanas testu izstrādes vēsture:
Divdesmitā gadsimta sākums - "hialīna ķermeņi" leikocītu citoplazmā
1948 Hargraves, Richmond, Morton - metode LE šūnu noteikšanai in vitro ilgstošas leikēmijas inkubācijas laikā no SLE pacientiem
1951. gads Lī, Maikls, Vurals — atklāj seruma faktoru, kas stimulē limfocītu kodolu fagocitozi ar perifēro asiņu leikocītiem.
1957 Holoborovs, Veirs, Džonsons izmantoja Coons 1950. gadā izstrādāto netiešo imunofluorescences metodi, lai noteiktu ANF cilvēka aknu kriozes daļās.
1961. gads Beks - izmantoti laboratorijas dzīvnieku audi
1982. gads Tan - tika izmantota cilvēka nepārtrauktā šūnu līnija HEp-2, šis tests kļuva par zelta standartu ANA noteikšanai
1958. gads Džonss - atklāja Šegrena sindroma pacientu asinīs faktoru, kas spēj izgulsnēt šūnu kodolu ekstraktus, kas kalpoja par stimulu, lai aprakstītu lielāko daļu antinukleāro antivielu šķirņu.
Netiešā imunofluorescence uz nepārtrauktas šūnu līnijas Hep2
Metodi ANF noteikšanai izstrādāja Tan (1982), kurš kā substrātu izmantoja cilvēka nepārtraukto epitēlija šūnu līniju HEp-2 (ATCC atsauces nr. CCL-23). Šī šūnu līnija, kas iegūta no cilvēka balsenes adenokarcinomas, ir liela poliploīda nekeratinizējoša plakanšūna, kas veido monoslāni uz plastmasas un stikla.
Attēlā: HEp-2 šūnu līnijas šūnas, iekrāsotas ar hematoloģisko krāsvielu.
Šīs līnijas salīdzinošā nepretenciozitāte, lielie kodoli un visu cilvēka antigēnu klātbūtne padarīja netiešās imunofluorescences metodi, izmantojot nepārtraukto šūnu līniju HEp-2, par galveno metodi ANF noteikšanai. Angļu valodas literatūrā šai metodei nav vienota nosaukuma. Vienotības trūkums nomenklatūrā ir radījis neskaidrības laboratorijas izmeklējumu nosaukumos. Dažreiz terminu “pretnukleārās antivielas” imunoloģiskās laboratorijas lieto, lai apzīmētu testus, kuru pamatā ir enzīmu imūnanalīzes un imūnķīmiskās analīzes metodes, kā arī imunofluorescences metodi. Krievu valodas literatūrā mēs uzskatām par nepieciešamu saglabāt šī indikatora vietējo nosaukumu - “antinukleārais faktors” (ANF), lai atšķirtu imunofluorescējošo metodi no citiem ANA noteikšanas testiem.
Ir nepieciešams identificēt IgG klases ANF, jo citu imūnglobulīnu klašu ANF noteikšanai nav neatkarīgas diagnostikas vērtības. Pacienta seruma standarta atšķaidījumus inkubē ar audu substrātu, ļaujot antinukleārajām antivielām no pacienta seruma saistīties ar atbilstošiem kodola mērķiem. Pēc tam autoantivielu saistīšanās vietas nosaka, izmantojot ar fluoresceīnu iezīmētu anti-cilvēka antiserumu.

Lai gan kā substrātus var izmantot citas cilvēka šūnu līnijas, to labās morfoloģijas un kultivēšanas vienkāršības dēļ Hep-2 ir kļuvis par vispārpieņemtu netiešās imunofluorescences substrātu. Tā lietošana uzlabo testa jutību spilgtas fluorescences dēļ pat ar ievērojamu pacienta seruma atšķaidījumu, un lielais, ar eihromatīnu bagātais kodols ļauj precīzi aprakstīt fluorescences veidu. Turklāt Hep-2 šūnu līnijas izmantošana atvieglo Ro/SS-A antivielu noteikšanu, kā arī antivielu noteikšanu pret nukleolārajiem antigēniem, kas ir slikti, izmantojot laboratorijas dzīvnieku audu kriosekcijas. Citas HEp-2 priekšrocības ietver augstu šūnu dalīšanās biežumu, kas ļauj noteikt antivielas pret antigēniem, kas ekspresēti tikai šūnu dalīšanās laikā, un audu šūnu matricas neesamību, kas apgrūtina specifiskas luminiscences vizualizāciju salīdzinājumā ar histoloģisko. sadaļas.
Antinukleāro faktoru titri
ANF titrs ir definēts kā pēdējais pacienta seruma atšķaidījums, kam ir skaidra šūnu kodolu fluorescence. Izmantojot laboratorijas dzīvnieku audus, diagnostiskais ANF titrs ir 1:8-1:10, savukārt, izmantojot HEp-2 šūnu līniju, ieteicams lietot sākotnējo titru 1:80. Šajā gadījumā normālie ANF titri ir mazāki par 1:160.
Lietojot titrus, kas mazāki par 1:160, vāji pozitīvu rezultātu biežums klīniski veseliem indivīdiem būs ne vairāk kā 5%, un tajā pašā laikā pacientiem ar difūzām saistaudu slimībām neļaus palaist garām nozīmīgus ANA titrus.
Lai noteiktu galīgo titru, parasti tiek izmantota titrēšana ar x2 soļiem (1:160-1:320 - 1:640 - 1:1280 - 1:2560 - 1:5120 utt. Var izmantot arī rupjāku titrēšanu. Uz fona reimatisko slimību saasināšanās gadījumā parasti tiek novēroti ANF titri, kas pārsniedz 1:640, un remisijas laikā titri samazinās līdz 1:160-1:320.
Ir ieteikumi ANF identificēšanas rezultātu vērtēšanai, norādot saturu “krustiņos”. Tas ļauj laboratorijām ietaupīt reaģentus un samazināt darbaspēka izmaksas pētniecībai. Šajā gadījumā galīgā titra noteikšana nav iespējama. Jāņem vērā, ka galīgais titrs ir svarīgāks par substrātam saistīto autoantivielu daudzumu, jo tas ir tieši saistīts ar to mijiedarbības afinitāti ar antigēnu. Visiem pozitīvajiem pacientiem vēlams noteikt galīgo titru, kas ļauj noskaidrot augstas afinitātes autoantivielu klātbūtni serumā, kas ir ciešāk saistītas ar procesa aktivitāti.
Antinukleārā faktora kodola luminiscences veids
Jau pirmajā netiešās imunofluorescences klīniskās izmantošanas pieredzē, lai noteiktu ANF, izmantojot laboratorijas audu kriosekcijas, tika atzīmēts, ka pacientu ar autoimūnām slimībām serums šūnu kodolus “iekrāso” atšķirīgi, kas izraisīja atsevišķu kodolstruktūru selektīvu luminiscenci. Šīs parādības noskaidrošana noveda pie tā saukto kodola “luminiscences veidu” apraksta imunofluorescences testā. Tas ir saistīts ar faktu, ka katram ANA veidam ir specifiski šūnu mērķi, kā rezultātā šūnas kodola, kodola un citoplazmas luminiscences veids atspoguļo ANA mijiedarbību pacienta serumā ar antigēnu saturošām struktūrām iekšpusē. šūna. Luminiscences veids ir atkarīgs no specifisku autoantivielu klātbūtnes pacienta asins serumā, uz kuru pamata var izdarīt provizorisku secinājumu par ANA veidiem, kas atrodas šajā serumā. Tomēr laboratorijas dzīvnieku audu histoloģisko sekciju izmantošana neļauj droši noteikt luminiscences veidu. Tajā pašā laikā nepārtrauktu šūnu līniju, piemēram, Hep-2, izmantošana ļauj aprakstīt ievērojamu skaitu kodola un citoplazmas krāsošanas variantu. Ir trīs galvenās antigēnu grupas, pret kurām antivielu klātbūtne nosaka dažādus luminiscences veidus:

Šūnas kodola luminiscences veids ievērojami palielina ANF identificēšanas informācijas saturu, un tāpēc, nosakot šo indikatoru, tas regulāri jānosaka. HEp-2 šūnu izmantošana ļauj raksturot vairāk nekā 20 dažādus kodolkrāsojuma variantus, kas ir atkarīgi no pētāmajā serumā esošo ANA spektra. Tomēr praktiskai laboratorijai pietiek nošķirt 6 galvenās iespējas autoantivielu saistīšanai ar antigēnu saturošām šūnu struktūrām.

Ir viendabīgi, perifēri, granulēti (mazi/lieli), nukleolāri, centromēri un citoplazmas kodolluminiscences veidi. Katram luminiscences veidam ir ļoti raksturīgas iezīmes, kas ļauj atšķirt vienu variantu no otra, kā arī antigēnu kopumu, ar kuriem reaģē autoantivielas pacientu serumos. Luminiscences veidu apraksts sniedz vērtīgu klīnisko informāciju pats par sevi, turklāt luminiscences veids var liecināt par noteiktu laboratorisko izmeklējumu nepieciešamību nākotnē.

Plkst viendabīgs tips spīdēt autoantivielas reaģē ar tiem antigēniem, kas izkliedēti izkliedēti kodolā, t.i. ir daļa no hromatīna. Parasti, kad tiek atklāts homogēns luminiscences veids, sadalošās šūnās kondensētās hromosomas ir spilgti iekrāsotas. Galvenās hromatīna struktūrvienības ir nukleosomas – DNS un histonu kompleksi. Tādējādi homogēnais luminiscences veids liecina par antivielu klātbūtni pret nukleozomām, dsDNS un antivielām pret histoniem. Tas rodas pacientiem ar SLE un zāļu izraisītu vilkēdi, kā arī pacientiem ar sklerodermiju. Parasti augsta ANF titra noteikšana ar homogēnu luminiscences veidu norāda uz SLE diagnozi.
Perifērijas tips mirdzums bieži tiek izolēts atsevišķi, lai gan tas ir homogēna mirdzuma veids. Tā noteikšana ir šūnu fiksācijas artefakts, kas noved pie hromatīna pārdales kodolā uz perifēriju. Ir svarīgi atšķirt perifēro luminiscences veidu no kodola membrānas iekrāsošanās, kas tiek novērota autoimūnu aknu slimību gadījumā. Perifērais luminiscences veids tiek konstatēts pacientiem ar antivielām pret divpavedienu DNS, un tas tiek konstatēts galvenokārt pacientiem ar SLE.
Granulēts veids ir visizplatītākā un tajā pašā laikā nespecifiskākā. Dažreiz šāda veida mirdzumu krievu literatūrā sauc par “raibu” vai “sietu”. Nosaukums “granulēts” precīzāk atspoguļo šo parādību, jo šajā gadījumā autoantivielas reaģē ar granulām kodolā, kas ir supramolekulārie nukleoproteīnu kompleksi. Šādi proteīnu un nukleīnskābju kompleksi kodolā veic vairākas funkcijas, kas nepieciešamas normālai šūnas funkcionēšanai. Šādi kompleksi jo īpaši ietver spliceosomas, kas veic mRNS pēctranskripcijas pārkārtošanos, kas nepieciešama proteīnu sintēzei uz ribosomām. Sastāvā ir daudz dažādu nukleoproteīnu, kas nosaka antigēnu mērķu daudzveidību, nosakot granulētu luminiscences veidu. Galvenie autoantigēni, antivielas, pret kurām tiek vizualizēta granulētā luminiscences forma, ir Sm, U1-RNP, SS-A, SS-B antigēni un PCNA. Šūnu dalīšanās procesā šūnas zaudē lielāko daļu izveidoto nukleoproteīnu kompleksu, tāpēc mitotiskās figūras šūnu līnijā ar granulētu luminiscences veidu netiek iekrāsotas. Granulētais kodolluminiscences veids tiek novērots pacientiem ar SLE, SS, SS, DM/PM, RA un vairākām citām autoimūnām slimībām. Klīniski veselu indivīdu ar ANF bez sistēmiskas slimības pazīmēm asins serumā dominē zemi granulētā tipa ANF titri.
Ļoti augstu ANF titru noteikšana (1:2560-1:10000) ar rupjš granulēts veids kodolluminiscence parasti norāda uz jauktas saistaudu slimības diagnozi un prasa papildu izmeklēšanu, lai identificētu RNP antigēnu, kas ir galvenais šīs slimības seroloģiskais marķieris.
Nukleolārie antigēni var darboties kā ANA mērķi, izraisot noteikšanu nukleolārais tips fluorescence. Nukleolārā mirdzuma veida noteikšana ir raksturīga sklerodermijai un tās šķirnēm. Nukleolārais tips fluorescence noteikts pacientiem ar antivielām pret kodola komponentiem, piemēram, RNS polimerāzi 1, NOR, U 3 RNP, PM/Scl.
Centromērs tips fluorescence tiek novērota, kad hromosomu centromēros parādās antivielas, un tā ir atrodama tikai dalīšanās šūnās. Tās klātbūtne ir raksturīga sklerodermijas CREST variantam.
Citoplazmas tips mirdzums norāda uz antivielām pret tRNS sintetāzēm, īpaši Jo-1, kas tiek novērotas polimiozīta gadījumā. Turklāt tas tiek atklāts pacientiem ar ANA, kas vērsta pret citiem šūnu citoplazmas komponentiem: antivielas pret aktīnu autoimūna hepatīta gadījumā, antivielas pret mitohondrijiem primārās biliārās cirozes gadījumā.
Var raksturot vairākus citus luminiscences veidus, un šāda veida šūnas kodola iekrāsošanās var būt raksturīga noteiktam ANA veidam. Tādējādi antivielas pret Scl-70 imunofluorescējošā testā ar HEp-20 šūnām rada smalku kodola un nukleolu krāsojumu, anti-p80 - gaismas punktus kodolā, kas mitotiskajās šūnās nav. Tomēr ir jānorāda uz šādu parādību retumu un daudzveidību, kas padara to identificēšanu rutīnas pētījumu laikā nevajadzīgu.
Bieži var rasties vairāku veidu luminiscences kombinācija, piemēram, smalki granulēta un nukleolāra, kas raksturīga antivielām pret Scl-70. Turklāt bieži vien zemos atšķaidījumos dominē viena veida fluorescence, piemēram, granulēta, un ar turpmākiem atšķaidījumiem atklājas viendabīgi vai centromēriski fluorescences veidi, kas norāda uz dažādu ANA veidu klātbūtni pacienta serumā. Lai gan mirdzuma veids ārstam sniedz noteiktus datus par labu konkrētai diagnozei, tomēr jāņem vērā tā salīdzinoši zemā specifika un sastopamo parādību dažādība, kas prasa turpmāku laboratorisku izmeklēšanu.
ANA noteikšana ir pamats citu laboratorisko izmeklējumu izmantošanai, kas precizē ANA spektru pacientu asinīs. Ņemot vērā šī testa ārkārtējo informācijas saturu, turpmākās pārbaudes un turpmākās pārbaudes rezultātu analīze jāinterpretē atkarībā no luminiscences veida un ANF titra novērtēšanas rezultātiem.
Lai gan nozīmīgu ANA titru neesamība gandrīz vienmēr izslēdz aktīvas sistēmiskas reimatiskas slimības diagnozi, lietojot HEp-2 šūnu līniju, 2-4% pacientu, kas atbilst SLE diagnozes kritērijiem, ANA netiek konstatēta vai titri tiek samazināti. zems. Šos pacientus dažreiz klasificē kā " ANF negatīvs SLE“Lai precizētu diagnozi šādiem pacientiem, nepieciešama turpmāka izmeklēšana, galvenokārt antivielu noteikšana pret SS-A antigēniem. Šie antigēni ir ļoti labi šķīstoši un var tikt zaudēti no šūnu kodoliem. Lai samazinātu šo pacientu kategoriju, tiek izmantota kompleksa pārbaude, tostarp antivielu noteikšana pret ekstrahētajiem kodolantigēniem, t.s. saistaudu slimību skrīnings», tests 000723. Šādas izmeklēšanas negatīvs rezultāts ļauj ar ļoti lielu varbūtību izslēgt SLE un citu sistēmisku reimatisko slimību diagnozi.
Pētījuma metode, izmantojot cilvēka epitēlija šūnas HEp-2, kas ļauj noteikt antinukleārās antivielas – vienu no sistēmisko saistaudu slimību marķieriem.
Sinonīmi krievu valoda
ANF, antinukleārās antivielas, antinukleārās antivielas (ANA).
Angļu sinonīmi
Antinukleārās antivielas (ANA), Hep-2 substrāts, ANA-Hep2, fluorescējošās antinukleāro antivielu noteikšana (FANA).
Pētījuma metode
Netiešā imunofluorescences reakcija.
Kādu biomateriālu var izmantot pētniecībai?
Venozās asinis.
Kā pareizi sagatavoties pētījumam?
Nesmēķējiet 30 minūtes pirms asins nodošanas.
Vispārīga informācija par pētījumu
Antinukleārā faktora (ANF) noteikšana ir “zelta standarts” antinukleāro antivielu (ANA) noteikšanai un autoimūno slimību diagnosticēšanai.
Sistēmisko saistaudu slimību (SCTD) patoģenēze ir cieši saistīta ar imūnsistēmas traucējumiem un paaugstinātu antivielu veidošanos pret savu šūnu struktūrām. Autoantivielas pret šūnas kodola sastāvdaļām - antinukleārās antivielas - mijiedarbojas ar nukleīnskābēm un kodolproteīniem, citoplazmas antigēniem, kas izpaužas ar iekaisuma izmaiņām audos un orgānos, sāpēm locītavās un muskuļos, spēcīgu nogurumu, svara zudumu, ādas izmaiņām. ANA ir sastopamas daudzās autoimūnās slimībās, bet visbiežāk tās ir sistēmiskās sarkanās vilkēdes (SLE) gadījumā. ANA sastopami vairāk nekā 90% pacientu ar sistēmiskām saistaudu slimībām šobrīd ir aprakstītas aptuveni 200 šķirnes, kuras vieno viens nosaukums - antinukleārais faktors;
Nosakot ANF ar netiešo fluorescenci, visbiežāk tiek izmantota cilvēka balsenes adenokarcinomas HEp-2 nepārtrauktā epitēlija šūnu līnija. HEp-2 šūnas ir ļoti ērts substrāts laboratorijas pētījumiem, jo tām ir lieli kodoli un tās aug vienā slānī uz stikla priekšmetstikliņiem. ANA nosaka, saistoties ar HEp-2 šūnu intracelulārajiem antigēniem.
Pētījuma laikā HEp-2 epitēlija šūnas tiek audzētas uz stikla priekšmetstikliņiem, fiksētas un inkubētas ar atšķaidītu pacienta serumu. Pēc seruma pārpalikuma noņemšanas šūnas inkubē ar fluoresceīnu iezīmētām antivielām, pēc tam vēlreiz mazgā un pārbauda ar fluorescences mikroskopu. Šajā gadījumā tiek noteikts antivielu titrs un mirdzuma veids. Titrs, kas lielāks par 1:160, tiek uzskatīts par diagnostiski nozīmīgu. Reimatisko slimību saasināšanās laikā tas pārsniedz 1:640, un remisijas laikā samazinās līdz 1:160-1:320. Jo vairāk antivielu, jo augstāks titrs. Pamatojoties uz mirdzuma veidu, ir iespējams identificēt antinukleāro antivielu mērķus, kam ir liela klīniskā nozīme un kas nosaka pacienta turpmākās izmeklēšanas taktiku. Galvenie no tiem ir perifērie, granulētie (mazi/lieli), nukleolāri, centromēri un citoplazmas kodolkrāsošanas veidi. Katram mirdzuma veidam ir ļoti raksturīgas iezīmes, kas ļauj atšķirt vienu iespēju no otras.
Homogēna (difūza) krāsošana ir saistīta ar antivielu klātbūtni pret divpavedienu DNS, histoniem un ir raksturīga SLE un zāļu izraisītai vilkēdei.
Perifēro luminiscenci izraisa hromatīna perifērais sadalījums kodolā, tā ir saistīta ar antivielām pret DNS un ir specifiska SLE. Ir svarīgi atšķirt šāda veida luminiscenci no kodola membrānas iekrāsošanās, kas rodas autoimūnu aknu slimību gadījumā.
Granulārais (raibs, retikulārais) krāsojums ir visizplatītākais un vismazāk specifiskais, kas tiek atklāts daudzu autoimūnu slimību gadījumā. Autoantigēni šajā gadījumā ir nukleoproteīnu kompleksi kodolā (Sm, U1-RNP, SS-A, SS-B antigēni un PCNA).
Ļoti augsti ANF titri ar rupji granulētu luminiscences veidu bieži norāda uz jauktu saistaudu slimību.
Kodolu (nukleolāro) iekrāsošanos izraisa antivielu veidošanās pret kodola komponentiem (RNS polimerāze-1, NOR, U 3 RNP, PM/Scl), kas konstatēta sklerodermijas, Šegrena slimības gadījumā. ANA dažkārt palielinās endokrīno slimību (1. tipa cukura diabēts, tireoidīts, tirotoksikoze, poliendokrīnais sindroms), ādas slimību (psoriāze, pemfigus) gadījumos, grūtniecības laikā, pēc orgānu un audu transplantācijas, hemodialīzes pacientiem.
Centromēra luminiscence parādās antivielu klātbūtnē pret hromosomu centromēriem un ir raksturīga sklerodermijas formai - CREST sindromam.
Citoplazmatiskais luminiscences veids ir saistīts ar antivielām pret tRNS sintetāzi, jo īpaši pret Jo-1, kas raksturīgs dermatomiozītam un polimiozītam. Šis krāsošanas veids tiek noteikts arī antivielu klātbūtnē pret citiem citoplazmas komponentiem autoimūna hepatīta un primārās biliārās cirozes gadījumā.
Vienlaicīga dažādu luminiscences veidu noteikšana norāda uz dažāda veida antivielu klātbūtni.
Veseliem indivīdiem smalkgraudainu luminiscenci var noteikt pie zemiem, vidējiem vai augstiem ANA titriem, bet parasti rupji graudaini vai viendabīgi luminiscences veidi nav jānosaka.
Atkarībā no mirdzuma veida novērtēšanas rezultātiem tiek izstrādāta turpmākā pacienta ārstēšanas taktika un tiek nozīmēti papildu pētījumi ANA spektra precizēšanai.
Kādam nolūkam tiek izmantots pētījums?
- Sistēmisku saistaudu slimību diagnostikai.
- Reimatisko slimību diferenciāldiagnozei.
- Novērtēt autoimūno slimību terapijas efektivitāti.
- Sistēmisko saistaudu slimību gaitas uzraudzībai.
Kad ir plānots pētījums?
- Autoimūnas slimības simptomiem (ilgstošs drudzis, locītavu sāpes, nogurums, svara zudums, ādas izmaiņas).
- Nosakot izmaiņas, kas raksturīgas sistēmiskām saistaudu slimībām (paaugstināts ESR, C-reaktīvā proteīna līmenis, cirkulējošie imūnkompleki).
Ko nozīmē rezultāti?
Atsauces vērtības
Rezultāts: negatīvs.
Nosaukums: 1:160.
Iemesli paaugstinātam ANF titram uz HEp-2 šūnām:
- sistēmiskā sarkanā vilkēde (95% gadījumu),
- dermatomiozīts/polimiozīts,
- sistēmiskā sklerodermija (60-90% gadījumu),
- Sjogrena sindroms (40-70% gadījumu)
- jaukta saistaudu slimība (Šarpa sindroms),
- Reino sindroms,
- diskoidā vilkēde,
- zāļu izraisīta vilkēde,
- reimatoīdais artrīts,
- nekrotizējošs vaskulīts,
- Infekciozā mononukleoze,
- leikēmija,
- ļaundabīgi audzēji (galvenokārt limfoma),
- myasthenia gravis,
- infekciozs endokardīts,
- hronisks autoimūns hepatīts,
- primārā biliārā aknu ciroze,
- tuberkuloze,
- pneimokonioze,
- intersticiāla plaušu fibroze.
Mirdzuma veidi
|
Mirdzuma veids |
Kam tas raksturīgs? |
|
Homogēns |
SLE, zāļu izraisītas vilkēdes, sistēmiskas sklerodermijas, hroniska aktīva hepatīta gadījumā |
|
Perifērijas |
|
|
granulēts |
Pret SLE, Šegrena sindromu, jauktu saistaudu slimību, reimatoīdo artrītu |
|
Nukleolārais |
Polimiozīta/dermatomiozīta, sklerodermijas, Šegrena sindroma, SLE ārstēšanai |
|
Centromērs |
CREST sindroma gadījumā (ādas kalcinoze, Reino sindroms, barības vada disfunkcija, sklerodaktilija, telangiektāzija) |
|
Citoplazmas |
Pret dermatomiozītu/polimiozītu, autoimūnu aknu slimību, primāro biliāro cirozi |
Kas var ietekmēt rezultātu?
- Kļūdaini pozitīvu rezultātu izraisa:
- vecums virs 60-65 gadiem (10-37% gadījumu);
- tādu zāļu lietošana, kas var izraisīt zāļu izraisītu sarkano vilkēdi (acetazolamīds, karbidopa, hlortiazīds, hlorpromazīns, klofibrāts, etosuksimīds, zelta sāļi, grizeofulvīns, hidralazīns, izoniazīds, litija sāļi, metildopa, perorālie kontracepcijas līdzekļi, penicilīns, prokicilīns, feninamīds, fenicilīns , propiluracils, hinidīns, rezerpīns, streptomicīns, sulfonamīds, tetraciklīns, tiazīdu grupas diurētiskie līdzekļi).
- Glikokortikosteroīdu (prednizolona, deksametazona, metipred) lietošana dažkārt izraisa kļūdaini negatīvu rezultātu.
Svarīgas piezīmes
- 5% SLE gadījumu ir iespējams negatīvs šī testa rezultāts (ANF negatīvs SLE). Šādās situācijās diagnozes precizēšanai nepieciešams noteikt antivielas pret SS antigēniem (Ro).
- Pozitīvs testa rezultāts nav absolūts autoimūnas slimības pierādījums. Veseliem cilvēkiem 3-13% gadījumu ANF titrs ir paaugstināts un sasniedz 1:320.
- Testa rezultāti jānovērtē kopā ar klīniskajiem datiem un citiem laboratorijas parametriem.
- Ja testa rezultāts ir pozitīvs, ieteicams noteikt ANA specifiku ar imūnblotēšanu.
- Anti-divpavedienu DNS antivielas (anti-dsDNS), skrīnings
- Antivielas pret kodolantigēniem (ANA), skrīnings
- Antivielas pret ekstrahējamu kodolantigēnu (ENA ekrāns)
- Antivielas pret kardiolipīnu, IgG un IgM
- Antinukleārās antivielas (anti-Sm, RNP, SS-A, SS-B, Scl-70, PM-Scl, PCNA, CENT-B, Jo-1, histoni, nukleosomas, Ribo P, AMA-M2), imūnblots