7378 0
Ista velika literatura posvećena je pitanjima antibakterijske terapije sepse kao i samom problemu u vezi sa klasifikacijom i definicijom sepse. Većina novorazvijenih antibiotika se nužno preporučuje za upotrebu u liječenju sepse. Preporuke se daju, po pravilu, najopštije (indikacija - septikemija!?), što unosi dodatnu zabunu u režime antibakterijske terapije. Situaciju dodatno otežava nepostojanje jedinstvene opšte prihvaćene klasifikacije sepse, a samim tim i uporedivih rezultata lečenja.
Situacija se dramatično promijenila u proteklih 10 godina uvođenjem u kliničku praksu završnih dokumenata Konferencije pomirenja, koji su postali široko rasprostranjeni u praksi. Upotreba termina kao što su sistemski inflamatorni odgovor (SIR), sepsa, teška sepsa i septički šok omogućila je da se ocrtaju određene grupe stanja (naravno, prilično uslovne, ali ipak definisane!), koje zahtijevaju različite pristupe u liječenju, uključujući i diferenciranu upotrebu režima antibakterijske terapije. Istraživači su uspjeli da se razviju manje-više opšti principi antibakterijskom terapijom generaliziranih inflamatornih reakcija, u odnosu na njihove oblike/faze (SVR, sepsa, teška sepsa, septički šok), uporediti efikasnost terapije različitim antibiotskim režimima i ocijeniti rezultate liječenja.
Razvoj principa medicine zasnovane na dokazima i njihova široka primjena u svakodnevnoj kliničkoj praksi dovela je do potrebe za evaluacijom razne metode, koristi se za liječenje generaliziranih upalnih procesa. Provedene studije sugeriraju da je upotreba antibiotika u liječenju sepse zasnovana na dokazima o nivou I (najpouzdaniji). To nam omogućava da smatramo da je upotreba antibiotika u liječenju sepse, teške sepse i septičkog šoka neophodna komponenta, čija se efikasnost ne dovodi u pitanje.
Na osnovu definicija sepse usvojenih na Konsenzus konferenciji, možemo reći da bi pojava dva ili više simptoma sindroma sistemskog upalnog odgovora (SIRS) trebala poslužiti kao uvjerljiva osnova za postavljanje pitanja kvalitativne prirode SIRS-a, te, shodno tome, moguće započinjanje antibiotske terapije ukoliko postoji infektivni proces. Prije svega, potrebno je dokazati (ili isključiti) infektivnu prirodu sistemske upalne reakcije. Ovo često nije lak zadatak. Približna, daleko od potpune, lista glavnih stanja koja mogu dovesti do razvoja kliničkih znakova sistemskog inflamatornog odgovora data je u nastavku.
- Akutni pankreatitis
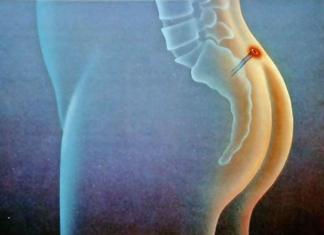
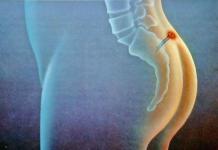
- Povreda kičme
- Krvarenje
- Plućne embolije
- Dijabetička ketoacidoza
- Infarkt miokarda
- Sistemski vaskulitis
- Sistemski eritematozni lupus
- Masivna aspiracija
Izvođenje diferencijalna dijagnoza Kako bi se provjerila kvalitativna priroda SIRS-a, to postaje potpuno neakademsko pitanje, budući da propisivanje antibiotika off-label može uzrokovati značajnu, ponekad nepopravljivu štetu. Da bi se definitivno utvrdio uzrok razvoja sindroma sistemskog upalnog odgovora, potrebno je poduzeti sve dostupne dijagnostičke mjere, uključujući dinamičku procjenu krvnih pretraga (povećanje leukocitoze, povećanje „pomaka formule ulijevo“), primjenu instrumentalnih dijagnostičkih metoda (rendgenski i ultrazvučni pregledi i dr.). U nizu slučajeva, radionuklidne studije su efikasne, kao i nova metoda, koji još nije dobio široku kliničku primjenu u domaćoj medicini, je određivanje koncentracije prokalcitonina u krvnom serumu.
Provjera infektivnosti sistemske upalne reakcije u skladu sa odlukama Konsenzus konferencije omogućava postavljanje dijagnoze sepse, što u skladu s tim zahtijeva propisivanje antibakterijske terapije.
Koje principe treba da se pridržava lekar pri odabiru režima antibakterijske terapije?
Dijagnoza „sepse“ (u tumačenju Konsenzusne konferencije 1991.), što ukazuje pojava sistemskih znakova zaraznog procesa, omogućava nam da smatramo dovoljnim razne droge“prvi” red kako u slučaju empirijske terapije tako i kod verifikovanog patogena. Identifikacija znakova zatajenja organa (2 ili više bodova na SOFA skali), što ukazuje na „tešku sepsu“, trebalo bi da natera doktora da se seti takozvanih „rezervnih“ antibiotika. savremenim principima"terapija deeskalacije"
Razvoj višeorganske insuficijencije ukazuje na izuzetno teško narušavanje funkcija organa i faktora odbrane organizma, što se mora uzeti u obzir pri odabiru odgovarajućeg antibakterijskog lijeka. Osim neposrednog direktnog toksičnog djelovanja na određene organe (aminoglikozidi - bubrezi, rifamicin - jetra, itd.), to je u direktnoj vezi sa činjenicom oslobađanja induktora medijatoze, koji su strukturni elementi bakterijskog zida, koji se oslobađaju tijekom raspad bakterijske ćelije. Tu spadaju lipopolisaharid (endotoksin) gram-negativnih mikroorganizama i teihoična kiselina - gram-pozitivni mikroorganizmi. Njihovo oslobađanje tokom propadanja ili lize mikroorganizama može značajno povećati disfunkciju organa (prvenstveno kardiovaskularni sistem), što se mora uzeti u obzir.
Naravno, ova primjedba se odnosi na lijekove koji imaju baktericidni učinak. Također imajte na umu da različiti antibakterijski lijekovi imaju različite efekte na oslobađanje lipopolisaharida. Ovo također treba uzeti u obzir pri odabiru lijeka (Tabela 1).
Tabela 1
Svojstva antibiotika da pojačaju ili oslabe oslobađanje endotoksina
Što se tiče izbora lijeka(a) za liječenje septičkog šoka, treba imati na umu sve što je već rečeno o „teškoj sepsi“. Potrebno je samo još više uzeti u obzir potrebu da se odmah započne sa „deeskalacijskom terapijom“, kao i odabirom lijekova s minimalnim oslobađanjem endotoksina. Trenutno se može smatrati da se jedinom grupom lijekova koji ispunjavaju ovaj zahtjev mogu smatrati samo karbapenemi (imipenem, meropenem).
Dakle, možemo reći da je jedan od glavnih i najvažnijih principa antibakterijske terapije sepse sljedeći: što je generalizirana upalna reakcija teža i izraženija (SIRS, sepsa, teška sepsa, septički šok), to je učinkovitija i sigurnija treba koristiti antibiotik.
Antibakterijska terapija za sepsu je pretežno empirijska, posebno na početku liječenja. Odmah se mora naglasiti da prije početka antibakterijske terapije treba izvršiti prikupljanje materijala za mikrobiološko ispitivanje (bojenje razmaza po Gramu, razne biološke tekućine i drenažni iscjedak i sl.). Nažalost, to nije uvijek moguće, posebno kada se pacijenti prebacuju iz jedne bolnice u drugu. Međutim, bez obzira na prethodnu terapiju i stanje pacijenta, novu fazu liječenja treba započeti procjenom mikrobiološkog statusa.
Izbor lijeka za empirijsku terapiju zasniva se na organskom pristupu (u kojem organu ili sistemu je lokaliziran infektivni proces), najvjerovatnijem patogenu na osnovu kliničkog pregleda, kao i uobičajenoj rezidentnoj flori prisutnoj u zahvaćenom organu. Na osnovu prvog principa odabire se lijek koji ima najveći tropizam za tkiva uključena u infektivni proces – osteotropni lijekovi za osteomijelitis, prodire kroz krvno-moždanu barijeru tokom infektivnih procesa u centralnom nervnom sistemu itd. Prilikom odabira antibakterijskog lijeka , morate zapamtiti da je priroda Uzročnik koji je izazvao zarazni proces, kompliciran generalizacijom, vodeći, odlučujući faktor. Nakon određivanja grupe lijekova koji djeluju na određeni patogen, vrši se naknadni odabir lijekova ovisno o težini generalizirane upalne reakcije.
Prilikom određivanja režima antibakterijske terapije i odabira odgovarajućeg antibiotika, uvijek smo suočeni s dilemom šta odabrati: monoterapiju lijekom širokog spektra (jeftiniji, manje toksični itd.) ili kombiniranu terapiju (uži spektar, manje rezistentnih sojeva). d.)? S tim u vezi, treba napomenuti sljedeće. Do danas ne postoji pouzdana baza dokaza o prednostima ove ili one metode terapije. Stoga bi izbor jednog ili drugog terapijskog režima (mono ili kombinovanog) vjerovatno trebao ostati stvar iskustva i ukusa ljekara.
Tako je napravljen izbor lijeka za terapiju. Možemo reći da je izbor lijeka najvažniji trenutak nakon što se formulišu indikacije za antibakterijsku terapiju. Ova faza se mora tretirati sa izuzetnom pažnjom. Samo uzimanje u obzir svih faktora koji utiču na tok i efikasnost antibakterijske terapije, minimiziraće je nuspojave i smanjiti rizik od neuspjeha.
Razvijanje znakova napredovanja infektivnog procesa (trajna temperatura, pomak leukocitna formula itd.) mora prije svega usmjeriti dijagnostički proces ka pronalaženju odgovora na pitanje: gdje, u kojoj fazi se zarazni proces počeo razvijati u smjeru drugačijem od predviđenog i zašto je to postalo moguće? Treba napomenuti da se umjesto postavljanja pitanja upravo u ovoj ravni, u velikoj većini slučajeva postavlja drugi zadatak - zamjena jednog antibiotika drugim zbog nedjelotvornosti prvog. A takve zamjene se ponekad dešavaju i nekoliko puta dnevno.
Još jednom vas želim podsjetiti da razvoj (progresija) infektivnog procesa na pozadini odabranog režima antibakterijske terapije, uzimajući u obzir sve faktore koji utječu na ovaj proces, u velikoj mjeri ukazuje na neadekvatno hirurško liječenje ili razvoj nedijagnosticirane bolesti. komplikacija, a ne neefikasnost antibiotika. Naprotiv, ako promjena antibakterijske terapije dovede do pozitivnog rezultata, to prije svega ukazuje da je u početku napravljena greška. Ovo su važni opšti principi koje svaki lekar koji primenjuje antibiotsku terapiju treba da ima na umu.
Statistike iz posljednjih godina pokazuju da se incidencija sepse i njenih komplikacija ne smanjuje, uprkos uvođenju savremenim metodama hirurški i konzervativno liječenje i korištenje najnovijih antibakterijskih sredstava.
Analiza učestalosti sepse u velikim centrima u Sjedinjenim Državama pokazala je da je incidencija teške sepse 3 slučaja na 1000 stanovnika ili 2,26 slučajeva na 100 hospitalizacija. Na odeljenje intenzivne nege primljeno je 51,1% pacijenata.
Američki Nacionalni centar za zdravstvenu statistiku objavio je veliku retrospektivnu analizu koja je otkrila da je 10 miliona slučajeva sepse prijavljeno u 500 bolnica u zajednici tokom 22-godišnjeg perioda praćenja. Sepsa je činila 1,3% svih razloga za boravak u bolnici. Incidencija sepse se trostruko povećala između 1979. i 2000. godine, sa 83 na 240 slučajeva na 100.000 stanovnika godišnje.
Treba napomenuti da je od 90-ih godina prošlog vijeka prisutna tendencija povećanja udjela gram-negativnih mikroorganizama kao najviše zajednički uzrok sepsa.
Ranije se vjerovalo da je sepsa problem prvenstveno u hirurškim bolnicama. Ali širenje bolničke infekcije, primjena invazivnih metoda istraživanja i praćenja stanja bolesnika, porast broja pacijenata sa stanjima imunodeficijencije, široka primjena citostatika i imunosupresiva, te porast broja mješovitih patologija doveli su do povećanja učestalost sepse kod pacijenata na nehirurškim odjeljenjima.
Postojeće moderne teorije o razvoju septičkog procesa ne dopuštaju nam da otkrijemo svu raznolikost prirode i mehanizama razvoja ovog procesa. U isto vrijeme, oni dopunjuju naše razumijevanje ovog složenog kliničkog i patogenetskog procesa.
Tradicionalni pristup problemu sepse sa stanovišta infektologije su podaci V.G. Bochoroshvili. Sepsa znači nozološki nezavisna infektivna bolest, koju karakteriziraju različiti etiološki uzročnici, manifestira se bakteremijom i malignim (acikličnim) tokom zbog imunosupresije. Acikličnost toka bolesti je jedan od odlučujućih faktora, jer Većina „klasičnih“ zaraznih bolesti (tifusna groznica, bruceloza, leptospiroza, tifus i druge) nastaju s bakteremijom, ali nisu sepsa i imaju ciklični tok s naknadnim oporavkom.
Prema A.V. Zinzerlinga, sepsu karakterišu opšti i specifični karakteristični klinički i kliničko-anatomski znaci, tj. prisutnost bakterijemije, septikemije, septikopiemije, ulaznih kapija i generalizacije infekcije.
Centralni aspekt u teoriji sepse oduvijek je bila interakcija mikro- i makroorganizama. Stoga sepsu karakterizira raznolik spektar mikrobioloških faktora, koji su u većini slučajeva predstavnici fakultativne flore otvorenih šupljina ljudskog tijela. Istovremeno, bakterijemija kod sepse se ne razlikuje od one kod „klasičnih“ zaraznih bolesti. Nije utvrđeno da patogeni sepse imaju posebna virulentna svojstva. Oni su pretežno predstavnici fakultativne flore ljudskog organizma, pa stoga nemaju izraženu imunogenost. Ovo objašnjava aciklični i fatalni klinički tok sepse.
Od 1992. godine sepsa se počela razmatrati u bliskoj vezi sa sindromom sistemskog inflamatornog odgovora (SIRS), nespecifičnom reakcijom imunog sistema na infektivni patogen ili oštećenje (Bone R.C., 1992.). Dakle, SIRS je patološko stanje uzrokovano jednim od oblika hirurške infekcije i/ili oštećenja tkiva neinfektivne prirode (trauma, pankreatitis, opekotina, ishemija ili oštećenje autoimunog tkiva itd.). Ovaj koncept su predložili American College of Chest Physicians i Society of Critical Care Medicine (ACCP/SCCM), što je dovelo do značajne revizije koncepta patogeneze, kliničke slike, liječenja i prevencije sepse i njenih komplikacija. SIRS karakterizira prisustvo više od jednog od sljedeća četiri glavna klinička znaka karakteristična za upalu: hipertermija, tahikardija, tahipneja, promene hemograma (leukocitoza/leukopenija) .
Gore navedeno Klinički znakovi može se javiti sa sepsom, ali u ovom slučaju je obavezno prisustvo infektivnog žarišta u tkivima ili organima.
Stoga je trenutna klasifikacija sepse zasnovana na dijagnostičkim kriterijumima predloženim na konsenzusnoj konferenciji ACCP/SCCM.
Lokalna upala, sepsa, teška sepsa i višestruko zatajenje organa su karike u jednom lancu u odgovoru tijela na upalu i, kao posljedicu, generalizaciju mikrobne infekcije. Teška sepsa i septički šok čine suštinski dio sindroma sistemskog upalnog odgovora organizma na infektivni agens, a rezultat progresije sistemske upale je razvoj disfunkcije sistema i organa.
Moderan koncept sepsa zasnovana na SIRS-u nije apsolutna i kritikovana je od strane mnogih domaćih i zapadnih naučnika. Kontroverze koje su u toku u vezi klinička definicija SIRS i njegova povezanost sa infektivnim procesom i specifičnost za sepsu i dalje postavlja pitanje bakteriološke dijagnoze, koja je u velikom broju slučajeva odlučujući faktor u potvrđivanju zarazne prirode patološkog procesa.
Bakterijemija je jedna od važnih, ali ne i obaveznih manifestacija sepse, jer je moguća periodičnost njenog ispoljavanja, posebno u slučajevima dugotrajne bolesti. Odsustvo potvrđene bakteremije ne bi trebalo da utiče na dijagnozu ako su prisutni gore navedeni klinički kriterijumi za sepsu, što je važno za lekara koji prisustvuje pri odlučivanju o obimu terapije. Čak i uz najsavjesnije pridržavanje tehnika uzimanja uzoraka krvi i korištenje modernih mikrobioloških tehnologija za dijagnostiku kod pacijenata s najtežim tokom sepse, učestalost pozitivnih rezultata u pravilu ne prelazi 40-45%.
Otkrivanje mikroorganizama u krvotoku bez kliničke i laboratorijske potvrde SIRS-a treba smatrati prolaznom bakteriemijom, koja se može javiti kod salmoneloze, jersinioze i niza drugih. crijevne infekcije. Visoka i produžena bakteremija, znaci generalizacije infektivnog procesa su značajni klinički značaj prilikom dijagnosticiranja sepse.
Detekcija uzročnika je važan argument u korist dijagnosticiranja sepse zbog:
- dokaz o mehanizmu razvoja sepse (na primjer infekcija povezana s kateterom, urosepsa, ginekološka sepsa);
— potvrda dijagnoze i utvrđivanje etiologije infektivnog procesa;
— obrazloženje za izbor režima liječenja antibioticima;
— procjena efikasnosti terapije.
Pozitivan rezultat hemokulture na sterilitet je dijagnostički najinformativnija metoda istraživanja. Hemokulture treba raditi najmanje 2 puta dnevno (unutar 3-5 dana), što je prije moguće nakon pojave groznice ili 1 sat prije primjene antibiotika. Da bi se povećala vjerojatnost izolacije patogena, 2-4 inokulacije se mogu izvršiti uzastopno s intervalom od 20 minuta. Antibakterijska terapija naglo smanjuje mogućnost izolacije patogena, ali ne isključuje pozitivan rezultat hemokulture na sterilitet.
Uloga polimeraze lančana reakcija u dijagnostici bakteremije i interpretaciji dobijenih rezultata ostaje nejasno za praktičnu upotrebu.
Negativni rezultati hemokulture ne isključuju sepsu. U takvim slučajevima potrebno je prikupiti materijal za mikrobiološki pregled iz sumnjivog izvora infekcije (likvor, urin, kultura sputuma, iscjedak iz rane i sl.). Prilikom traženja izvora infekcije potrebno je zapamtiti moguću translokaciju oportunističke mikroflore iz crijeva na pozadini smanjenja lokalnog otpora u crijevnom zidu - poremećena opskrba krvlju, kronična upala u kombinaciji s općom imunosupresijom.
Prilikom dijagnosticiranja sepse potrebno je uzeti u obzir sljedeće znakove koji ukazuju na generalizaciju infekcije:
- otkrivanje leukocita u tjelesnim tečnostima koje su normalno sterilne (pleuralna, likvor itd.);
— perforacija šupljeg organa;
- radiografski znaci upale pluća, prisustvo gnojnog sputuma;
— klinički sindromi kod kojih je velika vjerojatnost zaraznog procesa;
- groznica sa teškom intoksikacijom, moguće bakterijske prirode;
- hepatosplenomegalija;
— prisutnost regionalnog limfadenitisa na mjestu mogućih ulaznih vrata infekcije;
- zahvaćenost više organa (pneumonija, meningitis, pijelonefritis);
- kožni osip (polimorfni osip, česta kombinacija upalnih i hemoragijskih elemenata);
— znakovi DIC sindroma, itd.
Terapija sepse ima za cilj eliminaciju izvora infekcije, održavanje hemodinamike i disanja, te korekciju poremećaja homeostaze. Liječenje sepse je složen zadatak koji zahtijeva multidisciplinarni pristup, koji uključuje hiruršku sanaciju izvora infekcije, određivanje odgovarajuće etiologije antibakterijski tretman te korištenje tehnika intenzivne njege i prevencija komplikacija.
S obzirom da je početak sepse povezan sa proliferacijom i cirkulacijom mikroorganizama, a etiološka potvrda zahtijeva određeno vrijeme, pred ljekarom se postavlja pitanje izbora adekvatnog antibakterijskog lijeka (ABP) za empirijsku terapiju i kriterija za procjenu efikasnosti. terapija.
Prema retrospektivnim studijama, rana primjena efikasne antibakterijske terapije korelirala je sa smanjenjem mortaliteta u liječenju nekomplikovane sepse. Stoga je važna tačka u odabiru ABP za empirijsko liječenje sepse:
- očekivana etiologija procesa;
— spektar djelovanja lijeka;
— način i karakteristike doziranja;
— sigurnosni profil.
Priroda mikroflore koja je izazvala SIRS može se pretpostaviti na osnovu lokalizacije primarnog izvora infekcije (tabela 2).
2013/010/010_1.jpg)
Dakle, čak i prije dobijanja rezultata bakteriološke kulture, fokusiranje na namjeravani fokus bakterijska infekcija, mogu birati efektivna šema empirijska terapija antibioticima. Preporučuje se mikrobiološko praćenje zasijane mikroflore u svakoj klinici, što omogućava sastavljanje „mikrobiološkog pasoša bolnice“. Ovo se mora uzeti u obzir prilikom propisivanja ABP.
Treba uzeti u obzir lokalne epidemiološke podatke o strukturi patogena i njihovoj osjetljivosti na ALD, što može biti osnova za kreiranje lokalni protokoli empirijska terapija antibioticima.
U empirijskom liječenju sepse najčešće se koristi kombinacija dva antibakterijska lijeka. Argumenti u korist propisivanja kombinovane terapije su:
- nemogućnost razlikovanja gram-pozitivne ili gram-negativne etiologije infekcije po kliničku sliku;
— velika vjerovatnoća polimikrobne etiologije sepse;
- rizik od razvoja rezistencije na jedan od antibiotika.
Ako klinička učinkovitost ostane, nastavlja se provoditi antibakterijska terapija početnim lijekovima koji su propisani empirijski. U nedostatku kliničkog učinka u roku od 48-72 sata, antibiotik se mora zamijeniti uzimajući u obzir rezultate mikrobiološke studije ili, ako nisu dostupni, lijekovima koji pokrivaju praznine u aktivnosti početnih antibiotika, uzimajući uzeti u obzir moguću otpornost patogena.
U slučaju sepse, ABP treba davati samo intravenozno, birajući maksimalne doze i režimi doziranja na osnovu nivoa klirensa kreatinina. Ograničenje upotrebe lijekova za oralnu i intramuskularnu primjenu je mogući poremećaj apsorpcije u gastrointestinalnom traktu i poremećaj mikrocirkulacije i protoka limfe u mišićima. Trajanje antibakterijske terapije određuje se pojedinačno.
ALD terapija se suočava sa sljedećim izazovima:
— postići održivu regresiju upalnih promjena u primarnom infektivnom žarištu;
— dokazati nestanak bakterijemije i odsustvo novih infektivnih žarišta;
— zaustaviti reakciju sistemske upale.
Ali čak i uz vrlo brzo poboljšanje dobrobiti i postizanje potrebne pozitivne kliničke i laboratorijske dinamike (najmanje 3-5 dana normalne temperature), standardno trajanje terapije treba biti najmanje 10-14 dana, uzimajući u obzir oporavak laboratorijskih parametara. Duža antibiotska terapija je potrebna za stafilokoknu sepsu s bakteriemijom (posebno uzrokovanu sojevima MRSA) i lokalizacijom septičkog žarišta u kostima, endokardu i plućima.
Upotreba cefalosporina treće generacije u kombinaciji sa inhibitorima beta-laktamaze opravdana je u liječenju sepse.
Kombinacija cefoperazona i sulbaktama - Cefosulbin - je veoma efikasna. Cefoperazon je aktivan protiv aerobnih i anaerobnih gram-pozitivnih i gram-negativnih mikroorganizama (tabela 3). Sulbaktam je ireverzibilni inhibitor beta-laktamaza, koje luče mikroorganizmi otporni na beta-laktamske antibiotike. Sprječava uništavanje penicilina i cefalosporina beta-laktamazama. Osim toga, sulbaktam se vezuje za proteine koji vežu penicilin i pokazuje sinergizam u istovremena upotreba sa penicilinima i cefalosporinima.
2013/010/010_2.jpg)
Dakle, kombinacija sulbaktama i cefoperazona omogućava postizanje sinergističkog antimikrobnog efekta protiv mikroorganizama osjetljivih na cefoperazon, što smanjuje minimalnu inhibitornu koncentraciju za 4 puta za ove bakterije i povećava učinkovitost terapije.
Podaci iz brojnih studija pokazuju da je 80-90% sojeva mikroorganizama izolovanih od pacijenata sa sepsom osjetljivo na cefoperazon/sulbaktam (Cefosulbin), uključujući sojeve A. baumannii I P. aeruginosa. Primjena cefoperazon/sulbaktam (Cefosulbin) nije inferiorna u odnosu na karbapeneme u kliničkoj djelotvornosti i može biti alternativa često korištenoj kombinaciji cefalosporina treće generacije i aminoglikozida.
Pokazana je visoka klinička i mikrobiološka efikasnost u liječenju sepse (do 95%) uzrokovane multirezistentnim sojevima gram-negativnih i gram-pozitivnih mikroorganizama.
Dakle, raspon antibakterijske aktivnosti cefoperazona/sulbaktama (Cefosulbina) protiv anaerobnih patogena omogućava nam da preporučimo ovaj lijek u liječenju abdominalne, hirurške i ginekološke sepse.
Klinička efikasnost u liječenju infektivnih komplikacija primjenom cefoperazona/sulbaktama (Cefosulbin) pokazala se u grupi pacijenata sa opekotinama i patologijom raka.
Rano davanje efikasnog etiotropna terapija je važan faktor u liječenju sepse i često odlučuje o sudbini pacijenta. U velikom broju slučajeva ljekar nema vremensku rezervu za odabir antibakterijskog lijeka, što je zbog težine kliničkog toka sepse, pa je neophodno najefikasnije antibakterijsko sredstvo sa najširim mogućim spektrom antibakterijskog djelovanja. S obzirom na širok spektar antimikrobnog djelovanja, mogućnost intravenska upotreba, dobre farmakokinetike i farmakodinamike cefoperazon/sulbaktam (Cefosulbin), ovaj kombinovani antibakterijski lijek može se preporučiti kao prva linija empirijske terapije za liječenje sepse.
2013/011/011.jpg)
Dakle, uzimajući u obzir visoku kliničku efikasnost prikazanu u nizu kliničkim ispitivanjima, dobra farmakosigurnost, cefoperazon/sulbaktam (Cefosulbin) može biti lijek izbora u liječenju sepse dok se ne dobije bakteriološka potvrda.
Antimikrobna sredstva su bitna komponenta kompleksne terapije za sepsu. Posljednjih godina dobiveni su uvjerljivi dokazi da rana, adekvatna empirijska antibakterijska terapija za sepsu dovodi do smanjenja mortaliteta i stope komplikacija (kategorija dokaza C). Niz retrospektivnih studija također sugerira da adekvatna antibiotska terapija smanjuje smrtnost kod sepse uzrokovane gram-negativnim mikroorganizmima (kategorija dokaza C), gram-pozitivnim mikroorganizmima (kategorija dokaza D) i gljivama (kategorija dokaza C). S obzirom na podatke o poboljšanju ishoda bolesti uz ranu adekvatnu antibakterijsku terapiju, antibiotike za sepsu treba propisati hitno nakon razjašnjenja nozološke dijagnoze i prije dobijanja rezultata bakteriološkog ispitivanja (empirijske terapije). Nakon dobijanja rezultata bakteriološke studije, režim antibakterijske terapije može se promijeniti uzimajući u obzir izoliranu mikrofloru i njenu osjetljivost na antibiotike.
Etiološka dijagnoza sepse
Mikrobiološka dijagnoza sepse je odlučujuća u izboru adekvatnih režima antibakterijske terapije. Antibakterijska terapija usmjerena na poznati patogen pruža značajno bolji klinički učinak od empirijske terapije usmjerene na širok spektar vjerojatnih patogena. Zato mikrobiološkoj dijagnozi sepse treba posvetiti ništa manje pažnje nego izboru režima liječenja.
Mikrobiološka dijagnoza sepse uključuje ispitivanje mogućeg izvora infekcije i periferne krvi. Ako je isti mikroorganizam izoliran iz sumnjivog žarišta infekcije i iz periferne krvi, njegovu etiološku ulogu u nastanku sepse treba smatrati dokazanom.
Prilikom izolacije različitih patogena iz izvora infekcije i periferne krvi potrebno je procijeniti etiološki značaj svakog od njih. Na primjer, u slučaju sepse, nakon razvoja
nastaje u pozadini kasne bolničke pneumonije, kada je izolirana iz respiratornog trakta P. aeruginosa u visokom titru, a iz periferne krvi - koagulaza-negativni stafilokok, potonji, najvjerovatnije, treba smatrati kontaminirajućim mikroorganizmom.
Efikasnost mikrobiološke dijagnostike u potpunosti zavisi od pravilnog prikupljanja i transporta patološkog materijala. Glavni zahtjevi su: maksimalna blizina izvora infekcije, sprječavanje kontaminacije materijala stranom mikroflorom i proliferacija mikroorganizama tokom transporta i skladištenja prije početka mikrobioloških istraživanja. Navedeni zahtjevi mogu se u najvećoj mjeri zadovoljiti korištenjem posebno dizajniranih industrijskih uređaja (specijalne igle ili sistemi za prikupljanje krvi kompatibilni sa transportnim medijima, kontejnerima itd.).
Treba isključiti upotrebu hranjivih podloga za hemokulturu pripremljenih u laboratoriji, pamučnih štapića za sakupljanje materijala, kao i raznih vrsta improviziranih sredstava (posuda za hranu). Posebni protokoli za prikupljanje i transport patološkog materijala moraju biti dogovoreni sa mikrobiološkom službom ustanove i striktno se pridržavati.
Od posebnog značaja u dijagnozi sepse je proučavanje periferne krvi. Najbolji rezultati se postižu upotrebom medija za industrijsku proizvodnju (vias) u kombinaciji s automatskim analizatorima rasta bakterija. Međutim, mora se imati na umu da bakteremija – prisustvo mikroorganizma u sistemskoj cirkulaciji nije patognomoničan znak sepse. Detekciju mikroorganizama čak i u prisustvu faktora rizika, ali bez kliničke i laboratorijske potvrde sindroma sistemskog inflamatornog odgovora, ne treba posmatrati kao sepsu, već kao prolaznu bakteriemiju. Pojava je opisana nakon terapijskih i dijagnostičkih procedura, kao što su bronho- i fibrogastroskopija, kolonoskopija.
Uz stroge zahtjeve za pravilno prikupljanje materijala i korištenje savremenih mikrobioloških tehnika, pozitivna hemokultura kod sepse uočava se u više od 50% slučajeva. Prilikom izolacije tipičnih patogena kao npr Staphylococcus aureus, Klebsiella pneumoniae, Pseudomonas aeruginosa, gljive, jedan pozitivan rezultat obično je dovoljan za postavljanje dijagnoze. Međutim, kada se izoliraju mikroorganizmi koji su saprofiti kože i koji mogu kontaminirati uzorak ( Staphylococcus epidermidis, drugi koagulazno negativni stafilokoki, difteroidi), potrebne su dvije pozitivne hemokulture da bi se potvrdila prava bakteremija. Savremene automatske metode za proučavanje hemokulture omogućavaju snimanje rasta mikroorganizama tokom 6-8 sati inkubacije (do 24 sata), što omogućava tačnu identifikaciju patogena nakon još 24-48 sati.
Da bi se izvršio adekvatan mikrobiološki test krvi, potrebno je striktno poštovati sljedeća pravila.
1. Krv za testiranje se mora uzeti prije prepisivanja antibiotika. Ako pacijent već prima antibakterijsku terapiju, krv treba uzeti neposredno prije sljedeće primjene lijeka. Brojni komercijalni mediji za testiranje krvi sadrže sorbente antibakterijskih lijekova, što povećava njihovu osjetljivost.
2. Standard za ispitivanje krvi na sterilnost je uzimanje materijala iz dvije periferne vene u intervalu do 30 minuta, a iz svake vene krv se mora uzeti u dvije boce (sa podlogama za izolaciju aerobnih i anaerobnih). Međutim, nedavno je izvodljivost testiranja na anaerobe dovedena u pitanje zbog nezadovoljavajućeg omjera isplativosti. S obzirom na visoku cijenu potrošnog materijala za istraživanja, učestalost izolacije anaeroba je izuzetno niska. U praksi, uz ograničena finansijska sredstva, dovoljno je ograničiti uzimanje uzoraka krvi na jednu bočicu za proučavanje aeroba. Ako se sumnja na gljivičnu etiologiju, potrebno je koristiti posebne medije za izolaciju gljivica.
Pokazalo se da veći broj uzoraka nema prednost u pogledu stope detekcije patogena. Uzimanje krvi kod visoke temperature ne povećava osjetljivost metode ( kategorija dokaza C). Postoje preporuke za vađenje krvi dva sata prije vrhunca temperature, ali to je izvodljivo samo kod onih pacijenata kod kojih porast temperature ima stabilnu periodičnost.
3. Krv za istraživanje mora se uzeti iz periferne vene. Nije dokazana nikakva korist od uzimanja krvi iz arterije ( kategorija dokaza C).
Vađenje krvi iz katetera nije dozvoljeno! Izuzetak su slučajevi sumnje na sepsu uzrokovanu kateterom. U ovom slučaju, svrha studije je da se proceni stepen mikrobne kontaminacije unutrašnje površine katetera i da je uzorkovanje krvi iz katetera adekvatno za svrhu studije. Da biste to učinili, potrebno je provesti istovremenu kvantitativnu bakteriološku studiju krvi dobivene iz netaknute periferne vene i iz sumnjivog katetera. Ako je iz oba uzorka izoliran isti mikroorganizam, a kvantitativni omjer kontaminacije uzorka katetera i vene jednak ili veći od 5, onda je kateter najvjerovatnije izvor sepse. Osetljivost ove dijagnostičke metode je više od 80%, a specifičnost dostiže 100%.
4. Uzimanje krvi iz periferne vene treba obaviti uz pažljivu asepsu. Koža na mjestu venepunkcije tretira se dva puta jodom ili otopinom povidon-joda koncentričnim pokretima od centra prema periferiji u trajanju od najmanje 1 minute. Neposredno prije sakupljanja, koža se tretira 70% alkoholom. Prilikom izvođenja venepunkcije, operater koristi sterilne rukavice i sterilni suhi špric. Svaki uzorak (oko 10 ml krvi ili u količini koju preporučuje proizvođač boce) uzima se u posebnu špricu. Poklopac svake boce sa medijumom se tretira alkoholom pre nego što se probuši iglom za inokulaciju krvi iz šprica. U nekim sistemima za inokulaciju krvi koriste se specijalne linije koje omogućavaju uzimanje krvi iz vene bez pomoći šprica - gravitacijom, pod usisnim djelovanjem vakuuma u bočici s hranjivim podlogom. Ovi sistemi imaju prednost jer eliminira jednu od faza manipulacije koja potencijalno povećava vjerojatnost kontaminacije - korištenje šprica.
Pažljivo tretiranje kože, poklopca bočice i korištenje komercijalnih sistema za prikupljanje krvi s adapterom može smanjiti stupanj kontaminacije uzorka na 3% ili manje)