Lai saņemtu citātu: Bokarevs I.N., Dovgolis S.A. MIOKARDA INFRAKTA TROMBOLĪTISKĀ TERAPIJA // Krūts vēzis. 1998. Nr.3. S. 3
Rakstā apkopota globālā pieredze trombolītisko zāļu lietošanā akūta miokarda infarkta gadījumā un sniegti dati par salīdzinošo efektivitāti. dažādas narkotikas trombolītiskajai terapijai. Galvenais uzsvars tiek likts uz agrīnu ārstēšanas sākšanu. Ir sniegti ieteikumi trombolītiskās terapijas komplikāciju korekcijai.
Rakstā apkopota globālā pieredze trombolītisko zāļu lietošanā akūtā miokarda infarkta gadījumā un sniegti dati par dažādu medikamentu salīdzinošo efektivitāti trombolītiskajā terapijā. Galvenais uzsvars tiek likts uz agrīnu ārstēšanas sākšanu. Ir sniegti ieteikumi trombolītiskās terapijas komplikāciju korekcijai.
Darbā apkopota pasaules pieredze trombolītisko līdzekļu lietošanā akūtu miokarda infarkta ārstēšanā, sniegti pierādījumi dažādu trombolītisko līdzekļu salīdzinošai efektivitātei. Liels uzsvars tiek likts uz agrīnu ārstēšanu. Tiek sniegti ieteikumi trombolītisku komplikāciju korekcijai
terapija.
I.N. Bokarevs, S.A. Dovgolis. Maskava medicīnas akadēmija viņiem. VIŅI. Sečenovs
I.N. Bokarevs, S.A. Dovgolis I.M. Sečenova Maskavas Medicīnas akadēmija
UN
Miokarda infarkts (MI) ir visizplatītākais un bīstamākais patoloģiskais stāvoklis, kam nepieciešama neatliekama medicīniska iejaukšanās. 60. gadu sākumā tas izraisīja 30–50% skarto cilvēku ātru nāvi. Intensīvās terapijas nodaļu izveide, kas aprīkotas ar aparatūru ritma traucējumu novērošanai, apvienojumā ar elektrisko impulsu terapijas un jaunu antiaritmisko zāļu ieviešanu, gandrīz uz pusi samazināja mirstību no MI. Trombolītiskie medikamenti, kas šobrīd ir galvenie MI ārstēšanā, ļāvuši pasaules vadošajās klīnikās samazināt mirstību no šīs slimības līdz 7% un pat līdz 5%.
gadā pirmo reizi tika lietotas trombolītiskās zāles klīniskā prakse pateicoties V. Tileta un S. Šerijas pūlēm, tālajā 1949. gadā un 1958. gadā tā pati S. Šerija kopā ar A. Flečeru un N. Alkersigu jau ziņoja par veiksmīgu streptokināzes (SK) izmantošanu MI pacientu ārstēšana. Taču trombolītisko zāļu nepieciešamību šīs patoloģijas ārstēšanai visi atzina tikai pēc 1989. gada. Neapšaubāmi pašmāju zinātnieku nopelni šajā jomā praktisks pielietojums trombolītiskā terapija ir plaši pazīstama pasaulē. 1961. gadā iekšzemes fibrinolizīns, ko radīja G.V. Andreenko B.A. vadībā. Kudrjašova, pirmo reizi tika izmantots klīnikā A.L. Mjasņikova E.I. Čazovs. E.I. Čazovs izvirzīja pasaules prioritāti trombolītisko līdzekļu intrakoronārai ievadīšanai pacientiem ar miokarda infarktu 1976. gadā.
Kāda šobrīd ir situācija ar miokarda infarkta trombolītisko terapiju, un kas par to būtu jāzina katram praktizējošam ārstam?
Gandrīz 95% gadījumu MI pamatā ir tromboze.
Tas parasti attīstās pēc aterosklerozes plāksnes plīsuma. Plāksnes ar lielu lipīdu kodolu un makrofāgu infiltrāciju šķiedru virsmā ir īpaši jutīgas pret plīsumiem.
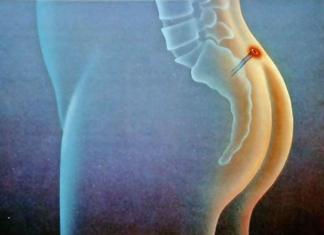
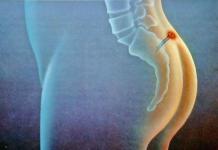
Miokarda šūnu nāve notiek virzienā no subendokarda uz epikardu.
Galvenie faktori, kas nosaka infarkta galīgo lielumu, ir laiks līdz miokarda reperfūzijai un blakus asinsrites attīstība.
Tas nosaka ārstēšanas taktiku, kuras mērķis ir panākt agrīnu un ilgstošu aizsprostotā asinsvada reperfūziju, kā rezultātā tiek saglabāts miokards, samazinās MI izplatība un samazinās miokarda elektriskā nestabilitāte. Bojāta asinsvada caurlaidības atjaunošana palīdz uzlabot kreisā kambara (LV) atlikušo funkciju, samazināt mirstību, MI komplikācijas un uzlabot dzīvildzi.
Reperfūzija var ierobežot MI izplatību vairākos veidos. Tas samazina apjomu, līdz kuram MI zona paplašinās, un apjomu, līdz kuram pagarinās perinfarkta zona. Pat ja MI izmērs nesamazinās, epikarda slāņa saglabāšana var izraisīt skartās zonas mazāku izspiedumu.
Infarkta miokarda dziedināšanas ceļš var būt tikpat svarīgs kā sākotnējais MI izmēra samazinājums. Arī išēmiska miokarda infarkta novēlota reperfūzija izraisa muskuļu saišķu nekrozes samazināšana un miokarda kontraktilās funkcijas saglabāšana.
Visbeidzot, reperfūzija var samazināt elektriskās nestabilitātes risku. Agrīna nāve MI rodas pēkšņi kambaru fibrilācijas rezultātā. Saskaņā ar elektrofizioloģiskajiem pētījumiem pacienti, kuriem ir bijusi reperfūzija, retāk cieš no ventrikulārām aritmijām, un viņiem ir mazāka iespēja novēloti repolarizācijas traucējumi EKG.
Ir zināms, ka reperfūzijas ietekme uz MI lieluma samazināšanu uzlabo dzīvildzi, taču šķiet, ka vairāki faktori ietekmē novirzi no lineārās attiecības starp agrīnu reperfūziju un mirstību. Lai reperfūzija būtu visizdevīgākā, tai nevajadzētu būt ļoti agrīnai, bet gan ilgstošai. Reoklūzija ir saistīta ar nāves riska dubultošanos. Atšķirības starp atsevišķiem trombolītiskiem līdzekļiem atkārtotas oklūzijas ātrumā ir grūti noteikt, un tiem ir nepieciešami lieli pētījumi.
Ir pētīti vairāki trobolītisko zāļu ievadīšanas ceļi, sākot no intrakoronārās trombolīzes līdz intravenoza ievadīšana gan slimnīcās, gan mājās. Liels klīniskie pētījumi ir skaidri parādījuši, ka intravenoza trombolīze ir saistīta ar vairāk zems līmenis mirstība pacientiem ar akūtām sāpēm in krūtis un ST pacēlums pirmajās 12 stundās no simptomu rašanās brīža.
Efektivitātes pierādījumi.
Iekšzemes fibrinolizīns izrādījās mazāk efektīvs un pašlaik netiek ražots.
Salīdzinošie trombolītiskās terapijas pētījumi ar placebo skaidri parādīja mirstības samazināšanos par 25-30%, neatkarīgi no izmantotajām trombolītiskajām zālēm.
Pašlaik ir veikti 10 lieli prospektīvi randomizēti pētījumi, lai novērtētu agrīnas trombolīzes ietekmi uz mirstību.
GISSI-1 pētījums (pirmais Itālijas trombolītisko līdzekļu kooperatīvais pētījums MI gadījumā), liels pētījums par agrīnu intravenozu trombolīzi, bija pagrieziena punkts, kas iezīmēja trombolītisko zāļu regulāras lietošanas laikmeta sākumu pacientiem ar agrīnu akūtu MI (AMI). ).
Šajā pētījumā 11 712 pacienti, kas tika uzņemti pirmajās 12 AMI stundās un kuriem nebija kontrindikāciju trombolītiskajai terapijai, pēc randomizācijas tika ārstēti ar intravenozu 1 500 000 vienību SA infūziju 1 stundas laikā vai parastā ārstēšana bez SC. Mirstība 21 dienā grupā, kas saņēma SA, bija 10,7%, salīdzinot ar 13% kontroles grupā (mirstība samazinājās par 18%, p = 0,0002). Ietekme netika novērota pacientiem, kuri tika ārstēti ar SC vēlāk nekā 6 stundas pēc sāpju sākuma. Tiem, kas tika ārstēti 6 stundu laikā, mirstības līmenis bija 10,2%, salīdzinot ar 12,8% kontroles grupā (mirstības samazinājums par 20%). Jo agrāk tika uzsākta ārstēšana, jo augstāka ir tā efektivitāte. Tādējādi pacientiem, kuri sāka ārstēšanu 3–6 stundu laikā, SC izraisīja mirstības samazināšanos par 17% (no 14,1 līdz 11,7%). Ja tas tika sākts no 0 līdz 3 stundām, mirstības samazināšanās bija 23% (no 12 līdz 9,2%). Tiem, kas tika ārstēti 1 stundas laikā pēc simptomu parādīšanās, mirstības samazināšanās sasniedza 47% (no 15,4 līdz 8,2%).
Ļoti svarīgs bija arī ISIS-2 (otrais starptautiskais MI izdzīvošanas pētījums). Pētnieki ziņoja par sākotnējiem un galīgajiem datiem par 17 187 pacientiem ar aizdomām par AMI, kuri tika reģistrēti 24 stundu laikā pēc sāpju parādīšanās. Pacienti tika randomizēti dubultmaskētā veidā. Tika pētīta SA (1 500 000 vienību 60 minūšu laikā) vai perorāla aspirīna (160 mg dienā 1 mēnesi) vai abu intravenozas ievadīšanas ietekme. Pacienti tika izslēgti no pētījuma, ja pagājušas vairāk nekā 24 stundas pēc simptomu parādīšanās. Nav Bija vecuma ierobežojumi. Mēs pētījām SC ietekmi uz kardiovaskulārās mirstības līmeni 5 nedēļas un vēlāk ietekmi uz kardiovaskulāro mirstību 5 nedēļas. Turklāt mēs analizējām SC ietekmi uz kardiovaskulāro mirstību tiem, kuri tika ārstēti agrāk nekā 4 stundas no plkst. sāpju parādīšanās tiem, kas ārstēti 4-12 stundu laikā un 12-24 stundu laikā.
Analizējot mirstību 5 nedēļu laikā no iekļaušanas brīža, tika konstatēts, ka no 8592 pacientiem, kuri tika ārstēti ar SC, 786 (9,1%) miruši no kardiovaskulāriem cēloņiem, salīdzinot ar 1016 no 8592 pacientiem. ārstēti ar placebo (mirstības samazināšanās par 23%, p<0,00001). Эта разница соизмерима с 18% снижением смертности в исследовании GISSI-1.
Laika posmā no 5 nedēļām līdz 1 gadam mirstības rādītāji SC un placebo grupā bija attiecīgi 5,7 un 6,2%.
ISIS-2 tikai 56% pacientu sākotnēji bija ST pacēlums, 8% bija ST depresija, 6% bija kūļa zaru blokāde, 27% bija Q-viļņa vai T-viļņa inversija, vai abi, 2% EKG bija normāla .
GISSI-1 un ISIS-2 pētījumi, kā arī pētījumi, kas veikti Nīderlandē, Vācijā, Jaunzēlandē un Vašingtonas štatā, sniedza pārliecinošus pierādījumus tam, ka SA, ko ievadīja agrīnā miokarda infarkta gaitas stadijā pacientiem bez kontrindikācijām, samazina mirstību 20-30%.
Līdzīgi dati tika iegūti par tPA un APSAC.
ASSET pētījumā (English-Scandinavian Early Trombolysis Study) 5011 pacienti ar aizdomām par AMI saņēma 100 mg alteplāzes (rTPA; 10 mg bolus, 50 mg 1. stundā, 20 mg 2. stundā) pirmajās 5 stundās pēc. slimības sākums pēc randomizācijas 1. un 3. stundā) vai placebo.ASSET neievēroja EKG kritērijus MI diagnosticēšanai, bet izslēdza pacientus, kas vecāki par 75 gadiem. Apmēram 18% pacientu pēc iekļaušanas pētījumā bija normāla EKG. Pēc 1 mēneša kopējais mirstības līmenis ārstēšanas grupā bija 7,2%, salīdzinot ar 9,8% placebo grupā (mirstības samazināšanās par 26%, p = 0,0011).
Eiropas kooperatīvā grupa ziņoja par randomizētu, dubultmaskētu pētījumu par rTPA (100 mg) efektivitāti 721 pacientam ar sāpēm krūtīs un agrīnu ST segmenta pacēlumu. 5 stundas no sāpju sākuma. Abas grupas saņēma aspirīnu un heparīnu. Pētnieki pētīja ārstēšanas ietekmi uz LV funkciju. Nāve 14 dienu laikā un nāve 3 mēnešu laikā tika pieņemti kā sekundārie mērķa kritēriji. 14 dienu mirstība bija 2,8% (10 no 355) rTPA grupā un 5,7% (21 no 366) placebo grupā. Mirstība samazinājās par 51% (p = 0,06). Izsviedes frakcija (EF) bija 2,2 reizes augstāka rTPA grupā, salīdzinot ar placebo grupu (attiecīgi 50,7 un 48,5). MI lielums, novērtēts pēc kopējās hidroksibutirāta dehidrogenāzes izdalīšanās, bija par 20% mazāks hTPA grupā (p = 0,0018).
Lielbritānijas AIMS pētniecības grupa veica daudzcentru, dubultmaskētu, placebo kontrolētu APSAC iedarbības pētījumu (30 vienības intravenozi vairāk nekā 5 min) pacientiem līdz 70 gadu vecumam, kas uzņemti ne vēlāk kā 6 stundas pēc sāpju sākuma ar ST segmenta pacēlumu EKG. Datu uzraudzības komiteja ieteica priekšlaicīgi pārtraukt pētījumu pēc starpposma datu atkārtotas analīzes, kad tika pieņemti darbā 50% no paredzamā pacientu skaita. Sākotnējā ziņojumā par 1004 pacientiem 30 dienu mirstība bija 12,2% (61 no 502) placebo grupā un 6,4% (32 no 502) APSAC grupā (p = 0,0016). Kopējais mirstības samazinājums pētījumā iekļautajiem pacientiem 4-6 stundu intervālā no slimības sākuma bija 47%, samazinājums bija ievērojami lielāks pētījumā iekļautajiem pirmajās 4 stundās (52 un 41%, attiecīgi). Kopējie ārstēšanas ieguvumi saglabājas un pat palielinās no 30 dienām līdz 1 gadam. Mirstība pēc 1 gada bija attiecīgi 19,4 un 10,8% placebo un APSAC grupā (mirstības samazinājums par 44%; P = 0,0006).
Tomēr ir pierādījumi, ka KS un APSAC terapija ir vienlīdz efektīva.
Divos pētījumos - European Coo perative Study un TIMI (Thrombolysis in Myocardial Infarction) - salīdzināja rTPA un SC ietekmi uz artēriju caurlaidību vai reperfūzijas līmeni. Eiropas kooperatīvajā pētījumā 129 pacienti saņēma vai nu rTPA, vai SC vidēji 3 stundas pēc uzsākšanas. VIŅI. Infūzijas artērijas caurlaidība tika pētīta 90 minūtes pēc infūzijas sākuma, tā bija attiecīgi 70 un 55% (p = 0,058). TIMI pētījumā tika izmantota arī rTPA un pirmsapstrādes arteriogrāfija. Autori novēroja 70 un 43% artēriju caurlaidības koeficients attiecīgi 90 minūtes pēc rTPA un SA infūzijas sākuma 290 pacientiem, kuri tika ārstēti vidēji 4,75 stundas pēc sāpju sākuma. Rezumējot, artēriju caurlaidības rādītāji abos pētījumos bija identiski gTAP (70%) un minimāli atšķirīgi MC (55% Eiropas sadarbības pētījumā un 43% TIMI).
TIMI pētījumā, kurā piedalījās 232 pacienti ar aizsprostotu artēriju, reperfūzija 90 minūšu laikā tika novērota attiecīgi 62 un 31% pacientu, kuri tika ārstēti ar rTPA un SA. Abos pētījumos, lietojot rTPA, koagulācijas sistēmas izmaiņas bija nenozīmīgas, lai gan ārstēšanas laikā ar SC un rTPA tika novērotas hemorāģiskas komplikācijas (galvenokārt hematomu veidošanās arteriālās punkcijas vietā).
Secinājums ir skaidrs: rTPA un SC ietekmē notiek trombolīze, kam seko reperfūzija, ierobežojot miokarda infarkta lielumu un uzlabojot LV remodelāciju, kas acīmredzami ir mirstības samazināšanas mehānisms.
Pastāv lineāra sakarība starp mirstību un laiku no simptomu rašanās līdz trombolītiskās terapijas uzsākšanai.
FTT (Fibrinolytic Therapy Trialists) pētījums parādīja tikai līdz 12 stundu atkarību no simptomu parādīšanās. 1 stundas laikā pēc simptomu parādīšanās trombolītisko līdzekļu iedarbība ir mazāk nozīmīga, ja zāles tika ievadītas 2 līdz 3 stundas pēc slimības sākuma. Pēc tam ārstēšanas ieguvums nepārprotami samazinās, palielinoties laikam no simptomu parādīšanās.
Vēlīnās trombolīzes ietekme AMI gadījumā, t.i., ārstēšana sākās pēc 6 stundām pēc simptomu parādīšanās, joprojām nav pilnībā skaidra.
ISIS-2 pētījumā pacientiem, kuri tika ārstēti pirmajās 4 stundās, mirstības līmenis SA un placebo grupā bija attiecīgi 8,2 un 12,1% (samazinājums par 32%). Starp pacientiem, kas ārstēti laika posmā no 4 līdz 12 stundām, mirstība no sirds un asinsvadu slimībām-asinsvadu cēloņi bija attiecīgi 10,3 un 11,8% (samazinājums par 13%), bet pacientiem, kas tika ārstēti 12 - 24 stundu laikā - 10,7 un 10,8% (samazinājums par 0,9%). Pacientiem, kuri tika ārstēti 1 stundas laikā, 5 nedēļu mirstība SC grupā samazinājās par 42% (līdzīgi kā 47% samazinājums 3 nedēļu mirstībai GISSI-1 pētījumā).
LATE (Delayed Thrombolysis Impact on Survival in MI) pētījums, kas izstrādāts, lai aplūkotu vēlīnās trombolīzes priekšrocības ar tPA, parādīja sekojošo.
5711 pacienti ar simptomiem un EKG parametriem, kas atbilst AMI, tika randomizēti, lai saņemtu alteplāzi (100 mg IV 3 stundu laikā) vai placebo 6 līdz 24 stundas pēc simptomu rašanās. Abas pacientu grupas saņēma aspirīnu. Tie tika novēroti 6 mēnešus, un 73% - 1 gada laikā.
Dzīvildzes analīze atklāja mirstības samazināšanos alteplāzes grupā (397/2836 nāves gadījumi), salīdzinot ar placebo (444/2875). 35 dienu mirstības rādītājs bija attiecīgi 8,86 un 10,31%, relatīvais samazinājums par 14,1%.
Papildu dzīvildzes analīze ārstēšanai līdz 12 stundām pēc simptomu parādīšanās uzrādīja būtisku mirstības samazināšanos ar alteplāzi: mirstība pēc 35 dienām bija 8,9% pret 11,97% placebo grupā, relatīvais samazinājums par 25,6% (p = 0,0299). Tiem, kas tika ārstēti no 12 līdz 24 stundām, mirstības rādītājs bija attiecīgi 8,7 un 9,2%, kas liecina, ka pēc 12 stundām ārstēšana var sniegt zināmu labumu. Šis pētījums parādīja, ka alteplāzes trombolīzes sākuma laiku var pagarināt līdz 12 stundām no plkst AMI simptomu parādīšanās.
Jautājums par trombolītiskās terapijas efektivitātes atkarību no miokarda infarkta lokalizācijas
šķita svarīgi, jo gandrīz vienmēr ir iespējams precīzi noteikt MI lokalizāciju: priekšējo, sānu, apakšējo vai apļveida, atkarībā no ST pacēluma vietas pirmajā EKG. Ir daudz grūtāk noteikt patiesa inferior Q-infarkta klātbūtni pacientiem, kuri uzņemti ar ST depresiju priekšējā sienā. GISSI-I pētījums un citi atklāja, ka priekšējā MI ir augstāks mirstības līmenis, un tāpēc pacienti ar priekšējo MI gūst lielāko labumu no trombolītiskās terapijas. GISSI-1 pētījumā trombolītiskās terapijas efektivitāte pacientiem ar zemāku miokarda infarktu nav tik skaidra, bet ieguvums no SA un aspirīna lietošanas tika parādīts ISIS-2. Pacientiem ar priekšējo MI, kuri saņēma trombolītisko terapiju, mirstība samazinājās par 30%, salīdzinot ar 15% pacientiem ar zemāku MI. Tajā pašā laikā daudzi klīnicisti uzskata, ka trombolītiskā terapija ir indicēta pacientiem ar hipotensiju, kardiogēnu šoku, īpaši pacientiem ar zemāks MI un labā kambara iesaistīšanās.
Trombolītiskās terapijas efektivitātes analīze atkarībā no vecuma
parādīja sekojošo. Pacientiem, kas jaunāki par 55 gadiem, dzīvības risks bez trombolītiskās terapijas nav ļoti augsts. Absolūtais ārstēšanas ieguvums palielinās līdz ar pacienta vecumu.
Gandrīz 50% no visiem nāves gadījumiem pacientiem, kas hospitalizēti AMI dēļ, notiek vecuma grupā virs 75 gadiem. Trombolītiskās terapijas pētījumos, izņemot ISIS-2 un GISSI-1, tika izslēgti pacienti, kas vecāki par 70 gadiem (AIMS) vai 75 gadi (ASSET, Eur. Coop. Pētījums).
ISIS-2 pētījums uzrādīja mirstības samazināšanos, lietojot SC par 16% 5 nedēļu laikā (18,2 un 21,6%) pacientu grupā, kas vecāki par 70 gadiem, par 26% (10,6 un 14,4%) grupā. 60-69 gadus vecu pacientu un par 28% (4,2 un 5,8%) pacientu grupā līdz 60 gadiem. GISSI-1 pētījums ziņoja par 13% mirstības samazināšanos pēc 3 nedēļām pacientu grupā, kas vecāki par 75 gadiem, par 8% grupā no 65 līdz 75 gadiem un par 26% grupā, kas nav vecāka par 65 gadiem. . Tas arī parāda, ka asiņošanas risks nav atkarīgs no vecuma.
Šobrīd notiek darbs pie veco zāļu efektivitātes objektivizācijas un efektīvāku jaunu trombolītisko zāļu radīšanas. Lai pierādītu jaunas zāles priekšrocības salīdzinājumā ar tās pašas klases priekšgājējiem, ir nepieciešams pētījums, kurā iesaistīti vismaz 20 000 pacientu.
Divi lieli pētījumi, GISSI-2 (20 891 pacients) un ISIS-3 (41 229 pacienti), tika izstrādāti, lai noteiktu alteplāzes priekšrocības salīdzinājumā ar SK (GISSI-2) vai alteplāzi un anistreplāzi salīdzinājumā ar SK (ISIS-3). Abos pētījumos tika konstatēts līdzīgs mirstības līmenis, ārstējot ar dažādiem trombolītiskiem līdzekļiem. SA lietošanu pavadīja ievērojami mazāks insultu biežums, salīdzinot ar anistreplāzes un alteplāzes lietošanu.
Blakusparādību biežums (%) trombolītiskās terapijas laikā
| Komplikācija |
GISSI-1 |
ISIS-2 |
AKTĪVS |
| Liela asiņošana | |||
| Neliela asiņošana | |||
| Alerģiska reakcija | |||
| Anafilakse | |||
| Hipotensija |
HP |
||
| Insults | |||
| Intrakraniālais spiediens |
HP |
Piezīme. HP - nav reģistrēts.
INJECT izmēģinājuma mērķis bija noteikt, vai jaunajai zāļu reteplāzei (rekombinantajam plazminogēna aktivatoram) ir tāda pati ietekme uz mirstību kā CK. 6010 pacienti tika randomizēti, lai saņemtu reteplāzi (3004 pacienti) vai SK (3006 pacienti).
Abas ārstēšanas grupas sasniedza līdzīgus rezultātus 6 mēnešu laikā attiecībā uz asiņošanas epizožu biežumu, miokarda infarkta pagarināšanos vai atkārtošanos un stacionāra insultu ar sekojošu invaliditāti.
Tiem, kas tika ārstēti ar reteplāzi, bija mazāk išēmijas gadījumu un nedaudz vairāk alerģisku reakciju. Diagnosticēto insultu skaits bija lielāks tiem, kuri tika ārstēti ar reteplāzi, taču insulti radās arī vairākiem pacientiem, kuri tika ārstēti ar SA.
Ar reteplāzi ārstētiem pacientiem mirstība 35 dienu laikā bija aptuveni par 0,5% zemāka nekā pacientiem, kuri tika ārstēti ar KS.
Divos angiogrāfiskos pētījumos, RAPID 1 un RAPID 2, iesaistot 324 pacientus, tika novērtēta asinsvadu caurlaidība pēc AMI, ārstējot ar reteplāzi vai alteplāzi.
RAPID 1 pētījumā tika pārbaudītas dažādas reteplāzes dozēšanas shēmas, salīdzinot ar 3 stundu alteplāzes infūziju. RAPID 2 pētījumā salīdzināja dubultā reteplāzes bolus ievadīšanas shēmu ar paātrinātu alteplāzes infūziju (90 min infūziju).
Šo pētījumu rezultāti parādīja, ka reteplāze atver vairāk artēriju ātrāk nekā alteplāze. Angiogrāfija pēc 60 un 90 minūtēm uzrādīja augstāku caurlaidības līmeni un 3 reizes augstāku miokarda perfūzijas līmeni ar reteplāzi, salīdzinot ar tiem, kuriem bija alteplāze. RAPID 1 90 minūtēs perfūzijas ātrums bija 63% reteplāzei, salīdzinot ar 49% alteplāzei (p< 0,05), в RAPID 2 уровень перфузии был равен соответственно 60 и 45% (р < 0,05). Ретеплаза была более удобной и простой в применении, не было неожиданных осложнений.
Šajos divos pētījumos parādītais reteplāzes angiogrāfiskais profils liecina, ka tas jaunam trombolītiskajam medikamentam ir priekšrocības salīdzinājumā ar alteplāzi; jo īpaši tā lietošana var izraisīt agrāku un pilnīgāku koronāro artēriju caurlaidību.
Divi nesen veikti pētījumi no Eiropas, GREAT (Anistreplase Early Treatment Trial) un EMIP (Eiropas MI projekts), parāda agrīnas trombolītiskās terapijas iespējamību, drošību un efektivitāti pirms hospitalizācijas. GREAT izmēģinājumā anistreplāzi (APSAC) ievadīja ģimenes ārsts mājās. EMIP tās pašas zāles ievadīja neatliekamās palīdzības personāls. Abos pētījumos ievadīšana pirms slimnīcas samazināja laiku starp simptomu rašanos un trombolītiskās terapijas sākšanu un bija saistīta ar zemāku mirstības līmeni. Jaunākais Eiropas sadarbības grupas pētījuma dati parādīja, ka trombolītiskās terapijas ieguvums saglabājas vismaz 5 gadus.
Papildu ieguvumus var iegūt, izmantojot jaunas trombolīzes metodes, kas sastāv no trombolītisko zāļu, īpaši SA un tPA, paātrinātas ievadīšanas.
1993. gadā GUSTO (Global Use of SK and TPA in Occluded Arteries) pētījumā tika iekļauts 41 021 pacients; šie pacienti tika randomizēti, lai saņemtu alteplāzi (paātrināta ievadīšana) un intravenozu heparīnu; alteplāzes, SA un heparīna kombinācija intravenozi; SA un heparīns intravenozi; SC un heparīnu subkutāni. Pirmo reizi tika pierādīts, ka jauna trombolītiskās terapijas metode, kas sastāv no paātrinātas tPA ievadīšanas, samazina mirstību vēl par 15%, salīdzinot ar SC, un nedaudz palielina intrakraniālas asiņošanas risku.
Pētnieki ieguva gaidītus un negaidītus rezultātus. Paātrinātā tPA ievadīšanas shēma tika papildināta ar ātru TIMI III pakāpes perfūzijas un asins plūsmas atjaunošanos, salīdzinot ar jebkuru SA ievadīšanas režīmu. Daudzi mērījumi ir parādījuši labāku LV sistolisko funkciju pēc paātrinātas tPA ievadīšanas. Turklāt ar paātrinātu tPA ievadīšanu mirstības rādītāji bija zemāki pēc 30 dienām un pēc 1 gada, kas atbilst 10 un 11 izglābtajām dzīvībām uz 1000 ārstētajiem pacientiem.
Mēs arī ziņojām par līdzīgiem novērojumiem, ārstējot 190 pacientus, kuri tika uzņemti ar akūtu MI ar Q vilni pirmajās 6 stundās pēc slimības sākuma. Visi pacienti saņēma trombolītisko terapiju ar SK. 160 pacientiem (1. grupa) SA tika ievadīts pēc standarta metodes (1 500 000 vienības intravenozi 1 stundas laikā), bet 30 pacientiem (2. grupa) - pēc ātrās shēmas (750 000 vienības 20 ml fizioloģiskā šķīduma 5 - 7 min. ). Trombolīze bija efektīva 110 (68,8%) 1. grupas pacientiem un 25 (83,3%) 2. grupas pacientiem. Agrīna tromboze (līdz 180 minūtēm) radās attiecīgi 7 (4,4%) un 2 (6,7%) gadījumos. Mirstība slimnīcā bija 15 (9,4%) gadījumi 1.grupā un 2 (6,7%) gadījumi 2.grupā. Starp grupām nebija būtisku atšķirību recidivējoša AMI, akūtas aneirismas, stenokardijas, asinsrites mazspējas, aritmiju un blokāžu biežumā.
Pašlaik lietotās trombolīzes metodes negarantē miokarda reperfūziju. Agrīna un pilnīga reperfūzija tiek sasniegta mazāk nekā 50% pacientu 90 minūtes pēc ārstēšanas sākuma, un atkārtota oklūzija notiek aptuveni 20 - 25% pacientu pirmajā novērošanas gadā. Turklāt tikai 3 līdz 4% pacientu saņem trombolītiskās zāles pirmajā stundā pēc simptomu parādīšanās, kad ieguvums var būt vislielākais. Tāpēc nav šaubu par nepieciešamību uzlabot AMI ārstēšanas metodes.
MI trombolītiskās terapijas shēma
Indikācijas
Sāpes krūtīs, raksturīgas akūtai miokarda išēmijai, kas ilgst līdz 12 stundām. Sāpes netiek mazinātas ar nitrātiem, un tām nav acīmredzama ekstrakardiālas izcelsmes cēloņa. Pēc 12 stundām trombolīze jāveic pacientiem ar visnelabvēlīgāko prognozi, kuriem sagaidāms vislielākais ieguvums (vecumā virs 75 gadiem, plašu bojājumu, ilgstošu stenokardijas sāpju, arteriālās hipotensijas gadījumos). Šādos gadījumos jūs varat sagaidīt 10 dzīvību glābšanu uz 1000 ārstētajiem.
. EKG izmaiņas:
- nesen vai, iespējams, nesen parādījušies Q viļņi, kas ilgst vairāk nekā 0,03 s ar amplitūdu lielāku par 0,2 mV; šīs izmaiņas jāatzīmē 2 no 3 “zemākiem” (II, III, aVF) vai 2 no 6 precordial (V1 - V6) vadiem vai I un aVL;
- nesen vai it kā nesen parādījies ST pacēlums 0,1 mV vai vairāk; ST pacēlumu mēra 0,02 s attālumā no S viļņa gala;
- saišķa zaru bloks.
Ja sistoliskais asinsspiediens pārsniedz 180 mm Hg. Art., vispirms ir jāpanāk tā samazināšana, vēlams ar atenolola vai labetalola intravenozas ievadīšanas palīdzību.
Kontrindikācijas
Absolūti:
- asiņošana pārbaudes laikā;
- insults;
- kuņģa-zarnu trakta asiņošana pēdējā mēneša laikā;
- nesen (iepriekšējo 3 nedēļu laikā) veikta liela operācija, smaga trauma vai galvas trauma;
- aortas aneirisma sadalīšana;
- zināma hemorāģiskā diatēze.
. Relatīvais (iespējamais risks ir rūpīgi jāizvērtē attiecībā pret ieguvumu):
- pārejoša smadzeņu išēmija iepriekšējos 6 mēnešos;
- ārstēšana ar perorāliem antikoagulantiem - antivitamīni K;
- grūtniecība;
- nesen veikta traumatiska kardiopulmonāla reanimācija (vairāk nekā 10 minūtes);
- refraktāra arteriālā hipertensija (BP > 180/100 mm Hg);
- nesen veikta nesaspiežama trauka punkcija;
- nesen veikta tīklenes lāzerterapija.
Metodoloģija
Vēlams, lai intervāls no pacienta uzņemšanas slimnīcā līdz trombolītiskās terapijas sākumam nepārsniegtu 30 minūtes.
Intravenoza SA ievadīšana tiek veikta šādi: 1 500 000 vienības tiek ievadītas 100 ml 5% glikozes vai 0,9% nātrija hlorīda 30–60 minūšu laikā. Heparīna ievadīšana nav nepieciešama 12 500 vienību subkutāni 2 reizes. Īpašas kontrindikācijas ir iepriekšēja (līdz 5 dienām) SA vai anistreplase lietošana.
TPA (alteplāze) ievada pēc šādas shēmas: 15 mg zāļu intravenozi bolus veidā, pēc tam 0,75 mg/kg 1 stundas laikā intravenozi 30 minūšu laikā, pēc tam 0,5 mg/kg 1 stundas laikā; kopējā deva 100 mg. Heparīnu ievada intravenozi 48 stundu laikā.
APSAC (anistreplāze) tiek ievadīts 30 vienību devā intravenozi 5 minūšu laikā. Īpašas kontrindikācijas ietver SA vai Anistreplase iepriekšēju lietošanu 5 dienas pirms un zināmu alerģiju pret SA/Anistreplase.
Urokināzi ievada 2 000 000 vienību devā intravenozi bolus veidā vai 1 500 000 vienību bolus veidā + 1 500 000 vienību 1 stundas laikā.
Ja rodas atkārtotas oklūzijas pazīmes vai atkārtots MI ar ST pacēlumu vai kūlīša zaru blokādi, atkārtoti jāveic trombolīze vai angioplastika. Laika posmā no 5 dienām līdz 2 gadiem SC vai APSAC nedrīkst lietot atkārtoti. Antivielas pret KS saglabājas vismaz 2 gadus. Alteplāzes un urokināzes lietošana neizraisa antivielu veidošanos.
Trombolītiskās terapijas efektivitātes novērtējums
Ir vairāki trombolītiskās terapijas panākumu marķieri. ST pacēluma samazināšana 12 standarta EKG pievadījumos 1 līdz 4 stundas pēc trombolīzes sākuma ir vienkāršākais un noderīgākais klīniskā pazīme lai novērtētu trombolītiskās terapijas efektivitāti. Šī indikatora paredzamo vērtību var uzlabot, kombinējot to ar seruma mioglobīna un troponīna T līmeni, ko var ātri noteikt.
Papildu pazīmes trombolītiskās terapijas efektivitātei var būt stenokardijas sāpju pārtraukšana un nozīmīgas (līdz 40 - 100%) enzīmu, galvenokārt kreatīnfosfokināzes, aktivitātes palielināšanās. Reperfūzijas aritmiju parādīšanās - paātrināts idioventrikulārs ritms, ventrikulāras ekstrasistoles, kambaru tahikardija, kambaru fibrilācija, atrioventrikulārā (AV) blokāde un utt - var arī ņemt vērā, bet var uzskatīt arī par komplikāciju.
Jāatzīmē, ka miokarda kontraktilitāte reperfūzijas laikā netiek nekavējoties atjaunota ("apdullināta miokarda" parādība).
Komplikācijas
Trombolītiskā terapija var būt saistīta ar blakusparādībām.
Komplikāciju iespējamība ir atkarīga no absolūto un relatīvo kontrindikāciju ņemšanas, zāļu izvēles un trombolītiskās terapijas metodes.
Reperfūzijas aritmijas, kas ir bieža trombolītiskās terapijas komplikācija un vienlaikus netieši pierādījumi tās efektivitātei, tiek novērotas 20–60% pacientu. Visizplatītākās ir paātrināts idioventrikulārs ritms, ventrikulāras ekstrasistoles, nestabilas ventrikulāras tahikardijas paroksizmi, pārejoša AV blokāde un kambaru fibrilācija. Aritmiju ārstēšana tiek veikta pēc tādiem pašiem principiem kā līdzīgu ritma un vadīšanas traucējumu ārstēšana, kas nav saistīta ar reperfūziju.
Koronārās artērijas atkārtota oklūzija tiek novērota 15 - 20% gadījumu un bieži vien ir asimptomātisks. Dažiem pacientiem atkārtota oklūzija izpaužas kā stenokardijas sāpju atsākšanās un hemodinamikas pasliktināšanās. Lai novērstu un ārstētu šo komplikāciju, nitroglicerīnu un heparīnu ievada intravenozi.
Arteriālā hipotensija parasti koriģē ar trombolītiskā līdzekļa ievadīšanas ātrumu. Ja ar to nepietiek, tad izrakstiet infūzijas terapija un kortikosteroīdu hormoni (prednizolons 30–60 mg, un, ja efekta nav, dopamīns 2–5 mcg/kg minūtē).
Alerģisku reakciju gadījumā nekavējoties jāpārtrauc trombolītisko zāļu lietošana un atkarībā no klīniskās izpausmes, izrakstot antihistamīna līdzekļus, kortikosteroīdu hormonus, bronhodilatatorus, bet anafilaktiskā šoka gadījumā - adrenalīnu.
Ja ir nepieciešama stimulēšana vai hemodinamikas kontrole, to ieteicams veikt pirms trombolītiskās terapijas uzsākšanas. Subklāvija vai iekšēja punkcija jūga vēna kontrindicēta.
Nopietna trombolītiskās terapijas komplikācija ir intrakraniāla asiņošana.
Plašu jaunu trombolītisko zāļu ievadīšanas veidu ieviešanu ir kavējušas bažas, ka uzlabota reperfūzija var palielināt intrakraniālas asiņošanas biežumu. Tos biežāk novēro, lietojot fibrīnam specifiskus līdzekļus, salīdzinot ar SC. Tas tika pierādīts pētījumos GUSTO 2 A, TIMI 9 un HIT 3.
Hemorāģiskais insults parasti attīstās gados vecākiem pacientiem ar nekontrolētu arteriālā hipertensija un apgrūtināta neiroloģiska vēsture, tāpēc trombolītiskā terapija ir kontrindicēta šai pacientu kategorijai. Ja attīstās hemorāģisks insults, tā ārstēšanu veic tāpat kā bez trombolītiskās terapijas.
Lietojot SA devu 1 500 000 vienību 1 stundā, intrakraniālas asiņošanas risks ir 1–10 uz 1000 ārstētiem pacientiem. Kuņģa-zarnu trakta asiņošana dažādas pakāpes smagumu var sagaidīt 5% pacientu, uroģenitālās asiņošanas - ar to tāda pati frekvence. Intrakraniālas asiņošanas biežums pēc rTPA ir atkarīgs no devas. 150 mg devā tas ir 15 - 20 uz 1000, bet 100 mg devā - 5 - 10 uz 1000. Intrakraniālas asiņošanas, lietojot APSAC, nav skaidri reģistrētas.
Pat ar efektīvu trombolīzi saglabājas paaugstināts išēmijas risks, jo saglabājas aterosklerozes aplikums. Šajā sakarā pacientiem joprojām pastāv recidīva un atkārtotas MI risks nākotnē.
Dažiem pacientiem, neskatoties uz terapiju ar aspirīnu un heparīnu, pēc veiksmīgas trombolīzes atkal parādās sāpes krūtīs un atkārtota koronāro artēriju tromboze ar MI attīstību. Koronārā trombolīze maz ietekmē tos aterosklerozes skarto koronāro artēriju hemodinamiskos faktorus, kas veicina fibrinogēna aktivāciju un asins recekļa veidošanos, tas tikai kādu laiku atjauno koronāro asinsriti. Pēc veiksmīgas trombolīzes pacientiem ieteicams veikt ārkārtas koronāro artēriju šuntēšanas operāciju vai balonangioplastiku ar stenta ievietošanu, lai novērstu atkārtotu koronāro artēriju trombozi.
AMI riska svārstības visas dienas garumā, iespējams, ir saistītas ar diennakts svārstībām koagulācijas aktivitātē un izcelšanās no gultas pēc miega. Vai ietekmē atšķirīgais līdzsvars starp koagulāciju un fibrinolīzi fizioloģiskais līmenis Par trombolītisko zāļu iedarbību joprojām nav skaidrs.
Tiek mēģināts izstrādāt drošākus un efektīvākus trombolītiskos līdzekļus. Sabiedrības informētība par MI simptomiem un ātrākas un efektīvākas ārkārtas reaģēšanas sistēmas izveide var arī uzlabot trombolītiskās terapijas iznākumu, saīsinot laiku starp simptomu rašanos un trombolītisko zāļu ievadīšanu.
Mūsdienu ārstam būtu jāzina, ka ātrāka trombolītisko zāļu ievadīšana pacientam ar MI ir labākais veids, kā glābt cilvēku un nodrošināt hemodinamikas drošību.
1. Alpert J., Francis G. Miokarda infarkta ārstēšana. Praktisks ceļvedis. Per. no angļu valodas - M.: Praktika, 1994. - P. 196-201.
2. Bokarevs I.N., Pavlovs A.V., Jankins V.V., Kazharskaja E.E., Dovgolis S.A., Inokentjevs I.K., Martynova I.G., Lando L.G., Fedorova S.Yu., Lepersky A.L., Blokhina I.V., M.lyAbyshe, M. Ātra trombolīze ar streptokināzes zālēm akūta miokarda infarkta gadījumā. /Tromboze, asinsizplūdumi, DIC sindroms. Ārstēšanas jautājumi. Starptautiskā konference. Maskava. 1997. gada 2.-4. aprīlis
3. Kardioloģija tabulās un diagrammās. Ed. M. Frīda un S. Grīns. Per. no angļu valodas - M.: Praktika, 1996. - P. 149-50.
4. Starptautiskās miokarda infarkta vadlīnijas. Ed.
Plašākai sabiedrībai jāzina, ka, ja pēkšņi ir sejas deformācija, vienas ķermeņa puses ekstremitāšu vājums vai nejutīgums, vai runas traucējumi, tas ir, ja pēkšņi parādās išēmiska insulta simptomi, nekavējoties jāzvana “ ātrā palīdzība"un uzstāt uz hospitalizāciju specializētā insulta centrā (vai slimnīcā ar neirovaskulāro nodaļu), kur ir iespējams veikt trombolīzi palātā/intensīvās terapijas nodaļā. Ja kopš slimības sākuma ir pagājušas mazāk nekā 6 stundas un pacienta stāvoklis nav kritisks, atbraukušajai brigādei parasti nevajadzētu veikt nekādu ārstēšanu, cenšoties pēc iespējas ātrāk nogādāt pacientu slimnīcā, brīdinot insultu komanda pa ceļam.
Saskaņā ar Pasaules Veselības organizācijas (vai PVO) datiem insults ir strauji attīstās fokusa vai globāls smadzeņu darbības traucējums, kas ilgst vairāk nekā 24 stundas vai izraisa nāvi, ja ir izslēgts cits slimības cēlonis. Išēmiskā insulta jēdziens atspoguļo slimības attīstības faktu, ko izraisa asins plūsmas samazināšanās noteiktā smadzeņu zonā un ko raksturo smadzeņu infarkta veidošanās. Smadzeņu infarkts ir nekrozes zona, kas veidojas noturīgu vielmaiņas traucējumu rezultātā, ko izraisa nepietiekama asins piegāde smadzeņu zonai.
Neskatoties uz daudzveidīgajām pieejām, ko izmanto pacientu ar išēmisku insultu (IS) ārstēšanā, tikai piecām normām ir augsta klase (I) un pierādījumu līmenis (A) attiecībā uz ietekmi uz slimības prognozi: [ 1 ] pacientu ar aizdomām par insultu neatliekamā hospitalizācija slimnīcās ar akūtu cerebrovaskulāru negadījumu (ACVA) pacientu ārstēšanas nodaļām; [ 2 ] medikamentu receptes acetilsalicilskābe pirmajās 48 stundās no brīža, kad parādās pirmie slimības simptomi; [ 3 ] Sistēmiskās trombolīzes veikšana ar rekombinanto audu plazminogēna aktivatoru (rtPA) rūpīgi atlasītiem pacientiem IS pirmajās 4,5 stundās (viena no efektīvākajām metodēm narkotiku ārstēšana AI); [ 4 ] veicot mehānisku trombu ekstrakciju, izmantojot retrīvera stentus pirmajās 6 insulta stundās pacientiem ar apstiprinātu vidējās smadzeņu artērijas (MCA) iekšējās miega artērijas (ICA) vai proksimālo daļu (M1 segmenta) oklūziju; [ 5 ] dekompresīvā hemikraniektomija smadzeņu tūskas ārstēšanai, ko izraisa MCA galvenā stumbra oklūzija pirmajās 48 insulta stundās.
« Zelta standarts» IS reperfūzijas terapija joprojām ir sistēmiska trombolīze. Līdz ar to, apsverot iespēju veikt endovaskulārās reperfūzijas ārstēšanu (skatīt zemāk) pacientiem, kuri atbilst sistēmiskās trombolīzes kritērijiem, to nepieciešams veikt, atbilstoši Ziemeļamerikas rekomendācijām akūta insulta ārstēšanai, kas aktualizētas 2015. gadā.
Sistēmiskās trombolīzes metodi kā jaunu medicīnas tehnoloģiju apstiprināja Federālais veselības aprūpes un sociālās attīstības uzraudzības dienests (01.08.2008. atļauja izmantot jaunu medicīnas tehnoloģiju FS Nr. 2008/169). Kopš 2008. gada trombolīze ir neatņemama sastāvdaļa medicīniskās palīdzības sniegšanā pacientiem ar insultu primārajos asinsvadu departamentos un reģionālajos asinsvadu centros, kas izveidota, īstenojot pasākumu kopumu, lai samazinātu mirstību no. asinsvadu slimības. Trombolītiskās terapijas (TLT) veikšanas kārtību reglamentē Krievijas Federācijas Veselības ministrijas 2009.07.06. rīkojums “Par medicīniskās palīdzības sniegšanas kārtības apstiprināšanu pacientiem ar akūtu insultu” Nr.389n (kā grozīts ar Krievijas Federācijas Veselības ministrijas 2010. gada 2. februāra rīkojumiem Nr. 44n un 2011. gada 4. 27. rīkojumu Nr. 357n), ar Krievijas Federācijas Veselības ministrijas 2012. gada 15. novembra rīkojumu Nr. 928n "Par medicīniskās palīdzības sniegšanas kārtības apstiprināšanu pacientiem ar akūtu cerebrovaskulāru negadījumu." 2014. gadā Viskrievijas neirologu biedrība apstiprināja iekšzemes Klīniskās vadlīnijas par TLT išēmiskajam insultam.
Agrīnas TLT izmantošana išēmiska insulta gadījumā ir balstīta uz koncepciju, ka ātra (vairāku stundu laikā) cirkulācijas atjaunošana skartajā baseinā aizsprostotas intrakraniālās artērijas rekanalizācijas laikā saglabā atgriezeniski bojātos smadzeņu audus išēmiskajā “pusumbra” zonā, jo smadzeņu šūnas tajā saglabā dzīvotspēju vēl 3 līdz 6 stundas (išēmisks “penumbra” vai pusumbra - smadzeņu audu apgabals ar kritiski samazinātu asins plūsmu ap nekrozes fokusu, pēdējo sauc arī par išēmiskā insulta “kodolu”).
 Išēmisks insults ir dinamisks process. Išēmisks insults ir patofizioloģisks process, kas sākas ar asinsvada aizsprostojumu un beidzas ar smadzeņu infarkta veidošanos. Tiklīdz asins plūsma smadzeņu artērijas baseinā samazinās līdz līmenim, kas ir mazāks par 40% no normas (zem 20 - 25 ml uz 100 g smadzeņu vielas minūtē), neironi pārstāj normāli funkcionēt un parādās fokālie simptomi. Šajā gadījumā rodas smadzeņu audu bojājumi: katru minūti bez ārstēšanas mirst gandrīz 2 miljoni neironu, tiek bojāti 14 miljardi sinapses un vairāk nekā 12 km mielinētu šķiedru. Vidējais infarkta tilpums ir 54 cm3, tas veidojas vidēji 10 stundās (Saver J. L., 2006). Kopš 80. gadiem Pagājušajā gadsimtā mēs zinām, ka tikai noteikta smadzeņu zona, kurā perfūzija ir zem 8-12 ml/100 g/min (išēmiska kodols), pirmajās minūtēs saņem neatgriezeniskus bojājumus. Apkārt, kā likums, ir liela zona (išēmiskā pustumsa jeb penumbra), kurā ir traucēta neironu darbība, bet tiek saglabāta to strukturālā integritāte un spēja atjaunoties. Vēl nesen bija ierasts attēlot išēmisko kodolu un pusumbru kā diagrammu, kurā viens apgabals vienkārši ieskauj otru (Att. A). Tomēr lielākajai daļai pacientu smadzeņu apgabali išēmiskajā zonā nav viendabīgi. Rīsi. B ilustrē išēmiskā insulta attīstības koncepciju, pamatojoties uz pozitronu emisijas tomogrāfijas datiem, kad ap centrālo kodolu atrodas hipoperfūzijas “salas”, ieskaitot zonas ar ļoti zemu asins plūsmu, kas raksturīga išēmiskajam kodolam (Lyden P. D., 2001). Asins plūsma pusmbras zonā ir mainīga un ir atkarīga no papildu asins piegādes līmeņa, ko nodrošina lielo artēriju zaru anastomozes. Penumbra liktenis ir atkarīgs no asins plūsmas līmeņa un hipoperfūzijas ilguma. Nekāda iejaukšanās nepalīdzēs atjaunot neatgriezeniski bojātus neironus. Tajā pašā laikā savlaicīga (tā sauktā "terapeitiskā loga" ietvaros) asins apgādes atjaunošana ļauj saglabāt un pēc tam atjaunot ievērojamu daļu dzīvotspējīgo šūnu, kas nozīmē smadzeņu infarkta izmēra samazināšanos un neiroloģiskā deficīta smagums. Vienīgā reperfūzijas metode, kas ir klīniskā nozīme, ir asinsrites atjaunošana aizsprostotā traukā. Rekanalizācijai ir cieša tieša saikne ar laba išēmiskā insulta iznākuma iespējamību.
Išēmisks insults ir dinamisks process. Išēmisks insults ir patofizioloģisks process, kas sākas ar asinsvada aizsprostojumu un beidzas ar smadzeņu infarkta veidošanos. Tiklīdz asins plūsma smadzeņu artērijas baseinā samazinās līdz līmenim, kas ir mazāks par 40% no normas (zem 20 - 25 ml uz 100 g smadzeņu vielas minūtē), neironi pārstāj normāli funkcionēt un parādās fokālie simptomi. Šajā gadījumā rodas smadzeņu audu bojājumi: katru minūti bez ārstēšanas mirst gandrīz 2 miljoni neironu, tiek bojāti 14 miljardi sinapses un vairāk nekā 12 km mielinētu šķiedru. Vidējais infarkta tilpums ir 54 cm3, tas veidojas vidēji 10 stundās (Saver J. L., 2006). Kopš 80. gadiem Pagājušajā gadsimtā mēs zinām, ka tikai noteikta smadzeņu zona, kurā perfūzija ir zem 8-12 ml/100 g/min (išēmiska kodols), pirmajās minūtēs saņem neatgriezeniskus bojājumus. Apkārt, kā likums, ir liela zona (išēmiskā pustumsa jeb penumbra), kurā ir traucēta neironu darbība, bet tiek saglabāta to strukturālā integritāte un spēja atjaunoties. Vēl nesen bija ierasts attēlot išēmisko kodolu un pusumbru kā diagrammu, kurā viens apgabals vienkārši ieskauj otru (Att. A). Tomēr lielākajai daļai pacientu smadzeņu apgabali išēmiskajā zonā nav viendabīgi. Rīsi. B ilustrē išēmiskā insulta attīstības koncepciju, pamatojoties uz pozitronu emisijas tomogrāfijas datiem, kad ap centrālo kodolu atrodas hipoperfūzijas “salas”, ieskaitot zonas ar ļoti zemu asins plūsmu, kas raksturīga išēmiskajam kodolam (Lyden P. D., 2001). Asins plūsma pusmbras zonā ir mainīga un ir atkarīga no papildu asins piegādes līmeņa, ko nodrošina lielo artēriju zaru anastomozes. Penumbra liktenis ir atkarīgs no asins plūsmas līmeņa un hipoperfūzijas ilguma. Nekāda iejaukšanās nepalīdzēs atjaunot neatgriezeniski bojātus neironus. Tajā pašā laikā savlaicīga (tā sauktā "terapeitiskā loga" ietvaros) asins apgādes atjaunošana ļauj saglabāt un pēc tam atjaunot ievērojamu daļu dzīvotspējīgo šūnu, kas nozīmē smadzeņu infarkta izmēra samazināšanos un neiroloģiskā deficīta smagums. Vienīgā reperfūzijas metode, kas ir klīniskā nozīme, ir asinsrites atjaunošana aizsprostotā traukā. Rekanalizācijai ir cieša tieša saikne ar laba išēmiskā insulta iznākuma iespējamību.

lasi arī [1 ] raksts: “Penumbras vizualizācijas metodes išēmiskā insulta gadījumā” M.Yu. Maksimova, medicīnas zinātņu doktore, profesore, galvenā pētniece cerebrovaskulāro negadījumu nodaļas ar intensīvās terapijas nodaļām; D.Z. Korobkova, neiroloģe, maģistrantūra; M.V. Krotenkova, medicīnas zinātņu doktore, Federālās valsts budžeta iestādes Radiācijas diagnostikas nodaļas vadītāja. Zinātnes centrs neiroloģija" RAMS (žurnāls "Bulletin of Radiology and Radiology" Nr. 6, 2013) [lasīt] un [ 2 ] disertācija doktora grāda iegūšanai. “Klīniskie un tomogrāfiskie marķieri, kas nosaka smadzeņu infarktu akūtā perioda gaitu karotīdu sistēmas arteriālajā baseinā” D.Z. Korobkova, Krievijas Medicīnas zinātņu akadēmijas federālā valsts budžeta iestāde “Neiroloģijas zinātniskais centrs”; Maskava, 2014 (22. - 28. lpp.) [lasīt]
atsauces informācija: 

sīkāk rakstā “Pacientu ar akūtu cerebrovaskulāru negadījumu hospitalizācijas procesa standartizācijas īstenošanas rezultāti reģionālajā asinsvadu centrā” P.G. Šņakins, E.E. Korčagins, N.M. Nikolajeva, I.S. Usatova, S.V. Draņišņikovs (žurnāls “Nervu slimības” Nr. 1, 2017) [lasīt]
TLT drīkst veikt tikai tad, ja diagnozi veic ārsts, kurš specializējas insulta pacientu ārstēšanā, tas ir, un kuram ir pieredze neiroattēlveidošanas rezultātu interpretēšanā, jo pacientiem 6 stundu “terapeitiskā loga” ietvaros ir indikācijas trombolīzes veikšanai. precizēts, izmantojot magnētiskās rezonanses attēlveidošanu - rezonanses attēlveidošanu (MRI) difūzijas un perfūzijas režīmā, vai, alternatīvi, izmantojot datortomogrāfiju (CT). Īpaši jāuzsver, ka modernas metodes neiroattēlveidošana (CT un MR angiogrāfija, CT un MRI perfūzija) ar minimālu risku pacientam ļauj objektivizēt gan artērijas oklūziju, kas izraisīja išēmiska insulta attīstību, gan trombolīzes procesā sasniegto rekanalizāciju.
CT un MRI smadzeņu infarkta diagnostikā[lasīt]
lasi arī rakstu“Secībai specifiskas MRI pazīmes, lai palīdzētu datēt išēmisku insultu” Laura M. Allen, MD; Antons N. Hasso, MD; Džeisons Handverkers, MD; Hameds Farids, MD; Radiografika 2012; 32:1285–1297; doi: 10.1148/rg.325115760 [lasīt]
izlasi arī ziņu: Perfūzija datortomogrāfija (uz vietni)
CT joprojām ir izvēles metode, novērtējot trombolīzes kandidātus. Metodes priekšrocības ietver minimālo pētījuma ilgumu, pieejamību, spēju vizualizēt smadzeņu infarktu pirmajās minūtēs un stundās, izmantojot kontrasta tehnikas, ātri atšķirt išēmisku insultu no hemorāģiskā insulta, ticami diagnosticēt intrakraniālu asiņošanu, izslēgt citas slimības, kas atdarina. išēmisks insults (piemēram, audzēji, encefalīts, arteriovenozās malformācijas). Tiešas smadzeņu infarkta pazīmes parādās nekontrastiskās datortomogrāfijas izmeklējumos pirmās dienas beigās pēc insulta simptomu parādīšanās. Agrīnās išēmiskā insulta CT pazīmes ir: hiperblīvas artērijas simptoms (palielināts blīvums), izolētas līnijas zudums, lentiformis kodola robežu izplūšana un normālu kontūru zudums, kompresija (subarahnoidālo telpu izlīdzināšana), zudums. diferenciācija pelēkajā un baltajā vielā išēmiskajā zonā.
Papildus 4,5 stundu “terapeitiskā loga” klātbūtnei (sistēmiskai TLT) un neiroattēlveidošanas datiem trombolīzes gadījumā ir nepieciešams novērtēt neiroloģisko simptomu smagumu išēmiska insulta akūtā periodā, izmantojot NIHSS skalu (National Institutes of Veselības insults Skala), kas ļauj objektīvi pietuvoties insulta pacienta stāvoklim (novērtējuma vērtība palielinās, ja novērtējums tiek veikts laika gaitā: stundu pēc trombolīzes, pēc tam ik pēc 8 stundām pirmajās dienās). Kopējais skalas punktu skaits ļauj aptuveni noteikt slimības prognozi, kas ir būtiski svarīga TLT plānošanai un tā efektivitātes uzraudzībai. Tādējādi trombolīzes indikācija ir neiroloģiska deficīta klātbūtne (saskaņā ar dažādiem avotiem vairāk nekā 3 - 5 punkti NIHSS skalā), kas liecina par invaliditātes attīstību. Smags neiroloģisks deficīts (saskaņā ar dažādiem avotiem vairāk nekā 24 - 25 punkti NIHSS skalā) ir kontrindikācija trombolīzei un būtiski neietekmē slimības iznākumu [sk. NIHSS skala ].
Par Kā pareizi aizpildīt ASV Nacionālā insulta smaguma institūta skalu (NIHSS) Var lasīt izvēles kursā “Ievads angioneiroloģijā”, 16. nodarbībā “Neiroloģiskās un rehabilitācijas skalas angioneiroloģijā: US National Institutes of Health Stroke Scale, Rankin Scale, Rivermead Scale and Barthel Index, Glasgow Coma Scale”; Šmonins A.A.; Pirmā Sanktpēterburgas valsts medicīnas universitāte viņiem. akad. I.P. Pavlova, Neiroloģijas un neiroķirurģijas nodaļa ar klīniku; Sanktpēterburga, 2014 - 2015 [lasīt];
vairāk detalizētas instrukcijas par NIHSS skalas aizpildīšanu var iegūt no grāmatas “Klīniskie ieteikumi pacientu ar išēmisku insultu un pārejošu išēmiski lēkmes"(Praktiķa bibliotēka, sērija "Neiroloģija") prof. L.V. Stahovskojs, Maskava, 2017
[Sistēmiskās] trombolīzes kandidāti ir pacienti vecumā no 18 līdz 80 gadiem, kuriem ir skaidri fiksēts insulta simptomu rašanās laiks (gadījumos, kad insults attīstās nakts miega laikā vai bez aculiecinieka klātbūtnes, jāņem vērā brīdis, kad pacients pēdējo reizi novērots asimptomātiski), ar sākotnējo NIHSS punktu skaitu ≥5 punkti. Priekšnosacījumi: CT vai MRI nav intrakraniālas asiņošanas pazīmju [sk. kontrindikācijas trombolīzei], “terapeitiskā loga” klātbūtne (laiks no pirmo slimības simptomu parādīšanās līdz ārstēšanas sākumam nepārsniedz 4,5 stundas), saņemot pacienta vai tuvinieku informētu piekrišanu manipulācijas veikšanai. .
Piezīme! Būtisks pēdējo 10 gadu sasniegums ir terapeitisko iespēju loga paplašināšana no 3 līdz 4,5 stundām. Tajā pašā laikā TLT ir simptomātiska, jo tā darbības mērķis ir tikai trombs vai embolija, kas izraisīja vienas vai cita intracerebrāla vai ekstracerebrāla artērija, nevis trombu veidošanās avots (trombs kreisā priekškambara piedēklī, “nestabils” aterosklerozes aplikums utt.). Tas ir saistīts ar augsto agrīnas reoklūzijas un trombozes procentuālo daļu (20–34) pat pēc veiksmīgi veiktas trombolīzes (avots: raksts “Insults: problēmas novērtējums (15 gadus vēlāk)”, M. Yu. Maksimova et al., Federal Krievijas Medicīnas zinātņu akadēmijas valsts budžeta iestāde “Neiroloģijas zinātniskais centrs”, Maskava, S. S. Korsakova vārdā nosauktais Neiroloģijas un psihiatrijas žurnāls.
Ir šādi trombolīzes veidi: sistēmiska (sin.: intravenoza), selektīva (sin.: intraarteriāls, reģionālais katetrs), trombolīze, izmantojot mehāniskas ierīces rekanalizācijai (aspirācijas katetru, Penumbra, Catch, Merci Retrieval System ierīces, ultraskaņas iznīcināšanu trombu uc), kombinēti (intravenozi + intraarteriāli; intraarteriāli + mehāniski). Sistēmiskā (intravenozā) trombolīzē kā trombolītisku līdzekli lieto rekombinanto audu fibrinogēna aktivatoru (rt-PA) [alteplāze, Actilyse] devā 0,9 mg/kg no pacienta ķermeņa masas, 10% zāļu ievada intravenozi kā bolus, atlikušo devu ievada intravenozi pa pilienam 60 minūšu laikā pēc iespējas agrāk. Vispārējā datu analīze par rtPA lietošanu 6 stundu laikā liecina, ka trombolīze ir efektīva vismaz 4,5 stundas un, iespējams, līdz 6 stundām pēc išēmiska insulta sākuma.
 Fibrinolīzes shēma un dažu fibrinolītisko zāļu iedarbība
Fibrinolīzes shēma un dažu fibrinolītisko zāļu iedarbība
Klīniskais protokols trombolīzes diagnostika un ārstēšana išēmiska insulta gadījumā (2014) [lasīt]; Ieteikumi trombolītiskajai terapijai pacientiem ar išēmisku insultu (2014) [lasīt]; rokasgrāmata ārstiem “Antitrombotiskā terapija išēmiskajam insultam”, ko izstrādājis Krievijas Medicīnas zinātņu akadēmijas akadēmiķis Ševčenko Ju.L. (Krievijas Federācijas Veselības ministrijas Ņ.I. Pirogova vārdā nosauktā Nacionālā medicīnas un ķirurģijas centra bibliotēka) [lasīt]
Selektīva trombolīze ir minimāli invazīva metode trombolītisko zāļu ievadīšanai rentgena kontrolē tieši trombā, izmantojot endovaskulāru katetru, ko izmanto, lai pilnībā vai daļēji atjaunotu asinsvada trombozes zonas caurlaidību. Selektīva trombolīze ir indicēta pacientiem ar intracerebrālo artēriju proksimālo segmentu oklūziju. Lai izmantotu intraarteriālo trombolīzi, pacientam jāpaliek augsta līmeņa insulta centrā ar 24 stundu piekļuvi smadzeņu angiogrāfijai. Intraarteriālā trombolīze ir izvēles metode pacientiem ar smagu išēmisku insultu, kas ilgst līdz 6 stundām, un insulta gadījumā vertebrobazilārajā reģionā līdz 12 stundām. Intraarteriālā trombolīze ietver lokālu ilgstošu trombolītisko līdzekļu (rt-PA vai urokināzes) infūziju, kas ilgst ne vairāk kā 2 stundas angiogrāfiskā vadībā.
Selektīvas trombolīzes metodei ir vairākas būtiskas priekšrocības salīdzinājumā ar sistēmisko trombolīzi: pirmkārt, tā palīdz noskaidrot oklūzijas lokalizāciju, būtību un noskaidrot. individuālās īpašības smadzeņu asinsrite; otrkārt, tas ievērojami samazina fibrinolītiskā līdzekļa devu un tādējādi samazina hemorāģisko komplikāciju risku; treškārt, tas nodrošina iespēju papildu mehāniskai ietekmei uz trombu, izmantojot mikrokatetru vai vadītāju; ceturtkārt, to var veikt ārpus 3 stundu laika loga, un, visbeidzot, katetra klātbūtne skartajā artērijā ļauj izmantot frakcionētu angiogrāfiju, lai uzraudzītu trombu sabrukšanas procesu un asinsrites atjaunošanos.
Klīniskais protokols ķirurģiskai un diagnostikas iejaukšanās: reģionālā katetra (selektīva) trombolīze (2015) [lasīt]
Šobrīd bojātās artērijas zonas mehāniskā rekanalizācija, izmantojot īpašus instrumentus – trombembolektomija – ir efektīvāka par intraarteriālo trombolīzi. Šī ķirurģiskā iejaukšanās tiek veikta kata laboratorijā. Tromboembolektomijas priekšrocības ietver sistēmisku hemorāģisko komplikāciju riska samazināšanu un iespēju mērķēt uz trombu vai emboliju pēc neveiksmīgas intravenozas trombolīzes. Līdz šim ir publicēti pētījumi par tādām ierīcēm kā Merci, Penumbra un Catch.
Ķirurģiskas un diagnostiskas iejaukšanās klīniskais protokols: išēmiska insulta endovaskulāra ārstēšana akūtā periodā (2015) [lasīt]
Pašlaik išēmiska insulta TLT var izmantot gan miega, gan vertebrobazilāro apgabalu artēriju bojājumiem. Neskatoties uz to, visas pašlaik esošās trombozes vadlīnijas galvenokārt ir vērstas uz asinsvadu katastrofu miegainajā reģionā, galvenokārt vidējā smadzeņu artērijā; tas galvenokārt ir saistīts ar acīmredzamu neiroloģisku deficītu šādiem pacientiem smagas parēzes un jušanas traucējumu veidā. Tipisku funkcionālo deficītu pacientam ar infarktu smadzeņu aizmugurējā artērijā (PCA) akūtā periodā ārsts ne vienmēr uzskata par invaliditāti. Neiroloģiskā deficīta novērtējums pēc Nacionālā veselības institūta insulta skalas (NIHSS), kas ir viens no kritērijiem pacientu atlasei TLT, parasti nespēj pilnībā atspoguļot pacienta ar vertebrobazilāru infarktu stāvokļa smagumu. Attiecībā uz izolētu redzes lauka defektu akūtā infarkta gadījumā PCA teritorijā ieteikumu vispār nav. Tāpēc TLT pacientiem ar infarktiem PCA teritorijā netiek plaši izmantots. Tomēr, ņemot vērā, ka hemiparēze atsevišķos gadījumos ir nozīmīga infarktu klīniskā sastāvdaļa PCA teritorijā, šādus pacientus, ja nav kontrindikāciju, pamatoti ārstē ar sistēmisku un/vai intraarteriālu (selektīvu) trombolīzi. Salīdzinot intravenozas trombolīzes efektivitātes un drošības profilus, kas ievadīti pirmajās trīs stundās pēc simptomu rašanās pacientiem ar karotīdu infarktu un PCA infarktu, būtiskas atšķirības drošībā un ārstēšanas iznākumā netika konstatētas. Tajā pašā laikā, pēc vairāku autoru domām, veicot intravenozu TLT vertebrobazilārās sistēmas išēmiskiem bojājumiem un jo īpaši PCA, ir iespējams paplašināt terapeitisko logu līdz 6,5-7 stundām un pat vairāk, salīdzinot ar 4,5 stundām. par infarktiem miega sistēmā . Intraarteriāla trombolīze smadzeņu vidējās artērijas oklūzijai ieteicama 6 stundu laikā no simptomu rašanās brīža, bet bazilārās artērijas oklūzijai – ne vēlāk kā 12 stundu laikā. Tomēr šodien nav skaidru ieteikumu par intraarteriālās trombolīzes termiņiem pacientiem ar PCA bojājumiem ( avots: raksts “Išēmisks insults aizmugurējās smadzeņu artērijās: diagnostikas, ārstēšanas problēmas” I.A. Khasanovs (pacientu ar akūtu cerebrovaskulāru negadījumu neiroloģiskās nodaļas ārsts), E.I. Bogdanovs; Tatarstānas Republikas Veselības ministrijas Republikas klīniskā slimnīca, Kazaņa; Kazaņas Valsts medicīnas universitāte (2013) [lasīt] vai [lasīt]).
Trombolīzes laikā un pēc tās pabeigšanas jāveic intensīva uzraudzība (asinsspiediena, pulsa, elpošanas ātruma, ķermeņa temperatūras un neiroloģiskā stāvokļa kontrole: zīlītes izmērs, fotoreakcija, muskuļu spēks un ekstremitāšu aktīvo kustību diapazons) saskaņā ar noteikumiem. starptautisko un vietējo protokolu [trombolīzes laikā - ik pēc 15 minūtēm; pēc trombolītiskās ievadīšanas: pirmās 6 stundas - ik pēc 30 minūtēm; līdz 24 stundām - ik pēc 60 minūtēm]. Dienu pēc trombolīzes ir nepieciešama atkārtota neiroattēlveidošana (MRI/CT).
Tā kā trombolīze (t.i., trombolītisko līdzekļu lietošana) ir saistīta ar lielas asiņošanas risku, trombolīzes potenciālie ieguvumi un iespējamie riski pirms ārstēšanas, kad vien iespējams, jāapspriež ar pacientu un ģimeni.
Izšķir šādus asiņošanas veidus, kas saistīti ar TLT: neliela asiņošana (parasti smaganu asinsvadu punkcijas vai bojājuma dēļ), liela asiņošana (centrālajā daļā). nervu sistēma, kuņģa-zarnu traktā vai uroģenitālajā traktā, retroperitoneālajā telpā vai asiņošana no parenhīmas orgāniem). Pirms trombolīzes procedūras un 24 stundu laikā pēc tās, lai novērstu asiņošanu, nevajadzētu veikt intramuskulāras injekcijas. Ja nepieciešams uzstādīt urīna katetru vai nazogastrālo zondi, šīs manipulācijas vēlams veikt pirms trombolīzes, jo pretējā gadījumā pastāv asiņošanas risks no ievainotām gļotādām. Centrālo nesaspiežamo vēnu (subklāviju, jūga) kateterizācija ir aizliegta 24 stundu laikā pēc trombolīzes. Nav ieteicams barot pacientus pēc trombolīzes 24 stundas. Antitrombotisku terapiju kā daļu no sekundārās profilakses var uzsākt tikai 24 stundas pēc intravenozas TLT ievadīšanas.
Ja trombolīzes laikā (vai pēc tās) pacientam rodas stipras galvassāpes, akūtas asinsspiediens, slikta dūša un vemšana, psihomotorais uzbudinājums, veģetatīvie simptomi (sejas un sklera hiperēmija, hiperhidroze), būtisks fokālo neiroloģisko simptomu pieaugums, kas var liecināt par trombotiskas infūzijas attīstības pārtraukšanu (ja tā joprojām turpinās) un tiek veikta ārkārtas CT skenēšana. . Smadzeņu infarkta zonas hemorāģiskās transformācijas pazīmju pārbaudes gadījumā ievadīšana svaigi saldēta plazma. Ja rodas lokālas asiņošanas (no injekcijas vietām vai smaganām [simptoms "vampīrs smaids"]), trombolīzes procedūras pārtraukšana nav nepieciešama, nospiežot.

Smadzeņu bojājuma hemorāģiskā transformācija ir simptomātiska, ja tās attīstība palielina kopējo punktu skaitu NIHSS insulta skalā par 4 vai vairāk punktiem. Vairumā gadījumu intracerebrālo asiņošanu pēc trombolīzes reģistrē asimptomātiskas hemorāģiskas transformācijas veidošanās, kas noteikta ar CT/MRI metodēm, kas bieži vien ir pavada klīniskais uzlabojums un tas liecina par reperfūziju.
Pacientam, kurš pārcietis išēmisku insultu, galvenie trombolīzes efektivitātes kritēriji ir: dzīvības funkciju pilnīga stabilizācija (elpošana, centrālā hemodinamika, oksigenācija, ūdens-elektrolītu līdzsvars, ogļhidrātu vielmaiņa), neiroloģisko komplikāciju trūkums (smadzeņu tūska, konvulsīvs sindroms, akūta okluzīva hidrocefālija, asiņošana infarkta zonā, izmežģījums), neiroloģiskā deficīta samazināšana (ideālā gadījumā ikdienas neatkarības un, ja iespējams, darba spēju atjaunošana), stenozējoša [aizsprostota] asinsvada asinsrites atjaunošana (to apstiprina angiogrāfisko un ultraskaņas pētījumu rezultāti), somatisko komplikāciju neesamība (pneimonija, PE, dziļo vēnu trombembolija apakšējās ekstremitātes, izgulējumi, peptiskas čūlas, urīnceļu infekcijas u.c.), asinsspiediena līmeņa normalizēšana u.c.
© Vietnes materiālu izmantošana tikai pēc vienošanās ar administrāciju.
Diemžēl laiks cilvēkus nepadara jaunākus. Ķermenis noveco, un līdz ar to noveco arī asinsvadi. Audos mainās vielmaiņa, tiek traucēta asins recēšana. Hroniskas slimības paātrina šos procesus. Tā rezultātā traukos veidojas asins recekļi, kas var bloķēt asins plūsmu. Šo slimību sauc.
Atkarībā no atrašanās vietas cilvēkam var attīstīties miokarda infarkts, insults (cerebrāls infarkts) un citas tikpat bīstamas komplikācijas. Vai ir iespējams palīdzēt cietušajam? Ir glābiņš – trombolīze jeb trombolītiskā terapija (TLT)!
Neapšaubāmi, savlaicīga palīdzība ne tikai izglābs cilvēka dzīvību, bet arī dos cerību uz pilnīgu rehabilitāciju. Ne visi par to zina, un tāpēc tērē dārgo laiku. Bet ir diezgan loģiski pieņemt, ka asinsriti var atjaunot, vienā vai otrā veidā noņemot nelaimīgo trombu. Tāda ir TLT būtība.
TLT veidi:
- Selektīva trombolīze. Ar šo metodi bojātās artērijas rezervuārā injicē zāles, kas izšķīdina asinis. Šī darbība ir iespējama sešu stundu laikā pēc asinsrites pārtraukšanas.
- Neselektīva trombolīze – intravenoza. Šī metode aizņem vēl mazāk laika – 3 stundas.
Trombolīze smadzeņu infarkta (išēmiska insulta) gadījumā

Akūtus insultus, kas provocē smagus neiroloģiskus traucējumus, sauc par insultu. Insulta diagnoze izklausās pēc nāvessoda. Krievijā. Puse pacientu mirst, lielākā daļa no viņiem pirmajā mēnesī. Un jūs nevarat apskaust izdzīvojušos - daudzi paliek bezpalīdzīgi un invalīdi līdz savu dienu beigām.
Tomēr valstīs, kuras TLT lieto jau daudzus gadus, statistika ir atšķirīga: mirst ne vairāk kā 20% pacientu. Daudzi pacienti piedzīvo pilnīgu neiroloģiskās funkcijas atjaunošanos. Un tas ir pateicoties pašai trombolīzei efektīva metode išēmiska insulta ārstēšana.
TLT procedūra nav īpaši sarežģīta – traukā tiek ievadīti īpaši fermenti, kas spēj izšķīdināt asins recekli. Tomēr ir kontrindikācijas:
- Dažādas lokalizācijas asiņošana. TLT laikā visi asins recekļi tiek izšķīdināti traukos, un tie, kas veidojas asiņošanas rezultātā, nav izslēgti.
- Iespējama aortas sadalīšana.
- Intrakraniālie audzēji.
- (asiņošana, ko izraisa smadzeņu asinsvadu sieniņu plīsums).
- Aknu slimības.
- Grūtniecība.
- Smadzeņu operācijas.
Pacienta vecums nekavē trombolītisko terapiju!
Starp uzskaitītajām kontrindikācijām dažas ir absolūtas, citas ir relatīvas. Vissvarīgākā absolūtā kontrindikācija ir asiņošana.
Trombolīzes veikšanu var apgrūtināt nepieciešamo apstākļu trūkums: datortomogrāfs, laboratorija, neirointensīvās terapijas nodaļa. Un pats galvenais, var vienkārši nepietikt laika. Trīs (ne vairāk kā sešas) stundas no slimības sākuma - šis periods ir jāievēro, veicot trombolītisko terapiju. Šis ir tas gadījums, kad laiks nav nauda, bet dzīve! Tāpēc ir tik svarīgi pievērst uzmanību pirmajām insulta pazīmēm:
- Vienpusējs rokas vai kājas nejutīgums;
- Nesakarīga runa;
- Izkropļota seja.
Jūs varat lūgt personai izstiept rokas uz priekšu un kaut ko pateikt. Ja šāds uzdevums izrādās ārpus viņa spēka, nekavējoties izsauciet ātro palīdzību. Atcerieties: atpakaļskaitīšana ir sākusies, un pacientam no tā ir maz!
Sirds un TLT
Jebkurš ķermeņa asinsvads var aizsērēt, ieskaitot koronāro artēriju. Šajā gadījumā attīstās miokarda infarkts. Protams, veselā organismā asins recekļa rašanās ir maz ticama. Raksturīgi, ka šo procesu veicina vispārēji traucējumi. Starp tiem: antikoagulantu komponentu daudzuma samazināšanās asinīs: heparīns un fibrinolizīns, koagulācijas komponentu satura palielināšanās. Turklāt traukā parādās lokāli traucējumi: iekšējā siena kļūst raupja, čūlas, palēninās asins plūsma.

Tāpat kā insulta gadījumā ar miokarda infarktu, svarīgi ir savlaicīgi izņemt trombu un atjaunot sirds muskuļa asins piegādi. Tomēr ārsti vilcinās veikt šo procedūru bez rūpīgas pacienta pārbaudes, baidoties no negatīvām sekām.
Šis izmeklējums ietver duplekso skenēšanu, datortomogrāfiju,. Tas viss ļauj visprecīzāk noteikt asins recekļa atrašanās vietu un injicēt zāles tieši skartajā traukā. Izmantojot šo pieeju, komplikāciju risks tiek samazināts vairākas reizes.
Bet tomēr dažreiz, kad pacientam nav atlicis laika, pat neatliekamās palīdzības ārsti veic trombolīzi. Patiešām, šādā gadījumā kavēšanās patiešām ir kā nāve! noteikti, šo procedūru drīkst veikt tikai kvalificēti speciālisti – kardioloģijas brigāde. Trombolīzes ilgums var svārstīties no 10 minūtēm līdz divām stundām.
Miokarda infarkta, kā arī insulta trombolītiskajai terapijai ir kontrindikācijas. Un arī galvenais šķērslis ir jebkuras vietas asiņošana.
Asins recekļa šķīdināšanas procedūra nekādā gadījumā nav lēts prieks. Trombolītisko līdzekļu, īpaši importēto, izmaksas sasniedz 1000 USD par injekciju. Bet kas var būt vērtīgāks par dzīvību?! Tā kā šī procedūra ir neatliekama, izmaksas par to ir iekļautas ātrās palīdzības brigādes obligātās veselības apdrošināšanas tarifos.
Trombolīzes veikšanas metodes
Trombolīzi veic ar divām galvenajām metodēm:

- Sistēmisks;
- Vietējais.
Pirmā metode ir izdevīga, jo zāles var injicēt vēnā, nezinot, kur ir paslēpts asins receklis. Ar asinsriti zāles tiek pārnestas pa visu asinsriti, kur ceļā sastopas ar šķērsli asins recekļa veidā un izšķīdina to. Bet sistēmiskajai trombolīzei ir būtisks trūkums: ir nepieciešama palielināta zāļu deva, un tas ir papildu slogs visai asinsrites sistēmai.
Veicot lokālu trombolīzi, zāles injicē tieši tromba lokalizācijas vietā. Zāles tiek piegādātas caur katetru, tāpēc šo metodi sauc par katetra trombolīzi. Tomēr šo metodi ir grūtāk īstenot nekā pirmo, un tā ir saistīta ar zināmām briesmām. Procedūras laikā ārsts uzrauga katetra kustību, izmantojot rentgena starus. Šīs metodes priekšrocība ir tās zemā invazivitāte. To lieto pat liela daudzuma klātbūtnē hroniskas slimības pie pacienta.
Kas izšķīdina asins recekļus?
Galvenie trombolītiskie līdzekļi, ko izmanto, ja ir trombolīzes indikācijas, ir:

TLT komplikācijas
- Asiņošana. Iespējamas gan nelielas, gan ļoti bīstamas.
- Sirds muskuļa saraušanās funkcija ir traucēta, kas izpaužas ar pazīmēm.
- Hemorāģisks insults. Šī komplikācija var rasties gados vecākiem pacientiem streptokināzes lietošanas rezultātā.
- Alerģiskas reakcijas.
- Reperfūzija. To novēro gandrīz pusei pacientu.
- Koronārās artērijas atkārtota oklūzija. Rodas 19% pacientu.
- . Tās saistību ar asiņošanu nevar izslēgt.
- Drudzis, izsitumi, drebuļi.
TLT pirmsslimnīcas stadijā
Kādas pazīmes liecina par traucējumiem smadzeņu asinsvados:
- Sāpes galvā;
- Reibonis;
- Samazināta uzmanība, redze, atmiņa.
Kurš gan nezina šos simptomus? Noteiktos dzīves periodos tie var parādīties pilnīgi veseliem cilvēkiem. Tomēr šīs pašas pazīmes tiek novērotas smadzeņu asinsrites traucējumu agrīnā stadijā. Lai izslēgtu šo iespēju un nepalaistu garām insultu, ikvienam piecdesmit gadus vecam cilvēkam katru gadu jāveic smadzeņu asinsvadu ultraskaņa, kā arī dupleksā skenēšana. miega artērijas.
Turklāt ir ieteicams veikt visinformatīvāko pētījumu. Tas ir īpaši indicēts riska grupas pacientiem: tiem, kas cieš cukura diabēts, hipertensija, aptaukošanās, sirds disfunkcija. Nopietns faktors ir fiziskā neaktivitāte un iedzimtība (īpaši mātes). Ir arī lietderīgi veikt koronāro asinsvadu izpēti.

(infografika: “Ukrainas veselība”)
Ja izmeklējuma laikā tiek konstatēta noteiktu asinsvadu tromboze, pareizākais risinājums būtu trombolīze. Spītīga statistika pierāda šīs metodes efektivitāti. Tā ir kļuvusi par aksiomu, ka jebkuru slimību ir vieglāk novērst, nekā to ārstēt. Pirmshospitāla trombolīze samazina mirstību no insulta un sirdslēkmes līdz pat 17%.
Trombolītiskā terapija ir ieteicama pirmsslimnīcas stadijā, ja ir pieejams apmācīts medicīnas personāls, neatliekamās palīdzības personāls un vietējā pieejamība. Šajā gadījumā TLT var sākties 30 minūšu laikā pēc tikšanās ar pacientu.
Panaceja?
Iespaidīgs trombolītiskās terapijas kontrindikāciju un komplikāciju saraksts norāda uz tās rūpīgu lietošanu. Šo metodi vajadzētu izmantot tikai izņēmuma gadījumos, kad uz spēles ir likta cilvēka dzīvība.
Svarīgs! Efektīva ir tikai agrīna metodes pielietošana: 3 (maksimums 6 stundu) laikā no pirmajiem slimības “zvaniem”.
Pēc tam sirds muskulis vai smadzeņu šūnas mirst. Trombolīzes izmantošana šajā gadījumā ir ne tikai bezjēdzīga, bet vēl ārkārtīgi bīstama!
Video: stāsts par neatliekamās palīdzības ārstu trombolīzes lietošanu
Trombolītiskā terapija- ļoti efektīva palīdzība išēmiska insulta gadījumā, kas ļauj atjaunot asinsriti skartajā traukā un novērst neatgriezeniskas izmaiņas smadzeņu audos.
Pašlaik trombolīzes gadījumā išēmiska insulta gadījumā priekšroka tiek dota alteplāzei (Actilyse) - zāles ir izgājušas klīniskos pētījumus un ir labi pierādījušas sevi randomizētos pētījumos. Kā tas darbojas: Rekombinanto audu plazminogēna aktivators (Actilyse) tieši aktivizē plazminogēna pārvēršanu plazmīnā. Pēc intravenozas ievadīšanas alteplāze paliek relatīvi neaktīva cirkulācijā. Tas tiek aktivizēts, saistoties ar fibrīnu, kas izraisa plazminogēna pārvēršanos par plazmīnu un noved pie fibrīna recekļa (asins recekļa galvenās sastāvdaļas) šķīšanas.
Pacientiem ar insultu trombolīzi veic pirmajās 3-4,5 stundās no neiroloģisko simptomu rašanās brīža. Tikai slimnīcā, pēc indikāciju/kontrindikāciju kritēriju noteikšanas un vairāku nepieciešamo pētījumu veikšanas.
Mūsdienās VTT ir standarta metode pacientu ārstēšanai akūtākajā IS periodā, ja nav kontrindikāciju. Metode ir piemērojama lielākajā daļā neiroloģisko slimnīcu, un tai nav nepieciešama ilgstoša vai sarežģīta sagatavošana. Lai pieņemtu lēmumu par VTT uzsākšanu, salīdzinoši neliels daudzums klīnisko, instrumentālo un laboratorijas pētījumi. Tajā pašā laikā ievērojama skaita kontrindikāciju dēļ šāda veida ārstēšanai potenciāli var izvēlēties tikai aptuveni 5-10% pacientu ar akūtu išēmisku cerebrovaskulāru negadījumu (ACVA), un šaurs "terapeitiskais logs" (4,5 stundas) izvirza augstas prasības pacienta transportēšanas un izmeklēšanas ātrumam. Izvēlētās zāles - rekombinantā audu plazminogēna aktivatora - efektivitāte ir atkarīga no plazminogēna līmeņa serumā, tromba tilpuma un ilguma.
Tomēr ir kontrindikācijas:
- Dažādas lokalizācijas asiņošana. TLT laikā visi asins recekļi tiek izšķīdināti traukos, un tie, kas veidojas asiņošanas rezultātā, nav izslēgti.
- Iespējama aortas sadalīšana.
- Arteriālā hipertensija.
- Intrakraniālie audzēji.
- Hemorāģisks insults (asiņošana, ko izraisa smadzeņu asinsvadu sieniņu plīsums).
- Aknu slimības.
- Grūtniecība.
- Smadzeņu operācijas.
Išēmiska insulta trombolītiskā terapija jāveic intensīvās terapijas nodaļā.
Saskaņā ar starptautiskajiem ieteikumiem laiks no pacienta uzņemšanas slimnīcā līdz trombolītiskās terapijas sākumam nedrīkst pārsniegt 60 minūtes (laiks no durvīm līdz adatai). Šajā laikā ir nepieciešams noteikt indikācijas un izslēgt trombolītiskās terapijas kontrindikācijas.
Nepieciešams:
1. Neirologa apskate un anamnēzes apkopošana, dzīvības funkciju un neiroloģiskā stāvokļa novērtējums. Nepieciešama pārbaude, izmantojot NIHSS insulta skalu. Trombolītiskā terapija ir indicēta NIHSS rādītājiem no 5 līdz 25.
2. Nekavējoties veiciet smadzeņu datortomogrāfiju.
3. Asinsspiediena līmeņa izmaiņas abās rokās.
4. Kubitālā perifēro vēnu katetra uzstādīšana.
5. Glikozes līmeņa mērīšana serumā.
6. Asins ņemšana un šādu laboratorisko izmeklējumu veikšana:
a) trombocītu skaits;
b) APTT;
c) INR.
7. Nodrošiniet vismaz 24 stundu uzraudzību:
1) asinsspiediena līmenis;
2) sirdsdarbība;
3) elpošanas kustību biežums;
4) ķermeņa temperatūra;
5) skābekļa piesātinājums.
Trombolīze var būt:
- Sistēmisks;
- Vietējais.
Trombolītiskās terapijas metodes
Pirmā metode ir izdevīga, jo zāles var injicēt vēnā, nezinot, kur ir paslēpts asins receklis. Ar asinsriti zāles tiek pārnestas pa visu asinsriti, kur ceļā sastopas ar šķērsli asins recekļa veidā un izšķīdina to. Bet sistēmiskajai trombolīzei ir būtisks trūkums: ir nepieciešama palielināta zāļu deva, un tas ir papildu slogs visai asinsrites sistēmai.
INDIKĀCIJAS TROMBOLĪZEI AKŪTA IŠĒMISKĀ INSTRUKTA gadījumā:
Smags neiroloģisks deficīts, kas saistīts ar akūtu išēmisku insultu un, acīmredzot, ko izraisa lielas artērijas (bazilāras, mugurkaula, iekšējās miega artērijas) oklūzija: kustību, runas, sejas parēzes, apziņas līmeņa traucējumu veidā. Izmantojot īpašas skalas (NIHS skalu), neirologs novērtē neiroloģiskā deficīta līmeni.
. asiņošanas neesamība saskaņā ar datortomogrāfiju
. attīstības laiks no klīnikas sākuma līdz 3 stundām (līdz 6 stundām ar selektīvu trombolīzi, līdz 12 stundām ar sirdslēkmi bazilārās artērijas baseinā)
TROMBOLĪZE IR KONTRINDIKĀTA:
ABSOLŪTAS KONTRINDIKĀCIJAS:
1) neliels un strauji regresējošs neiroloģisks deficīts
2) asiņošana, skaidri redzama, plaša akūta sirdslēkme smadzenes vai citi CT dati, kas ir kontrindikācijas (audzējs, abscess utt.)
3) pārliecinoši pierādījumi, ka pacientam ir asinsvadu anomālijas vai centrālās nervu sistēmas audzējs.
4) bakteriāls endokardīts
REATĪVĀS KONTRINDIKĀCIJAS:
1) smaga trauma vai insults pēdējo 3 mēnešu laikā
2) intrakraniāla asiņošana anamnēzē vai aizdomas par subarahnoidālo asiņošanu
3) liela operācija pēdējo 2 nedēļu laikā
4) neliela operācija pēdējo 14 dienu laikā, ieskaitot aknu vai nieru biopsiju, toracentēzi un jostas punkciju
5) arteriāla punkcija pēdējo 2 nedēļu laikā
6) grūtniecība (desmit dienas pēc dzemdībām) un zīdīšana
7) akūta kuņģa-zarnu trakta asiņošana, uroloģiska vai plaušu asiņošana pēdējo trīs nedēļu laikā
8) hemorāģiskā diatēze anamnēzē (ieskaitot nieru un aknu mazspēju)
9) peritoneālā vai hemodialīze
10) izmaiņas koagulogrammā (PTT vairāk nekā 40 sekundes, protrombīna laiks vairāk nekā 15 (INR vairāk nekā 1,7), trombocītu skaits mazāks par 100 000)
11) krampju lēkmes kā insulta sākums (nepieciešama rūpīga diferenciāldiagnoze)
12) glikozes līmeņa izmaiņas asinīs (hipo vai hiperglikēmija)
ADMINISTRĀCIJA:
Visbiežāk tiek veikta neselektīva trombolīze. To veikt pēc minimālas pacienta izmeklēšanas (neirologa apskate, datortomogrāfija, lai izslēgtu asiņošanu), vispārīga analīze tiek veikta asinis ar trombocītu līmeni, asins bioķīmija (glikozes līmenis), koagulogramma, ja iespējams intravenoza ievadīšana 100 mg zāļu Akilyse: 10 mg ievada bolus veidā, atlikušos 90 mg ievada intravenozi ar pilienu fizikālās terapijas laikā. šķīdums 0,9% 400,0 1 stundu.
TROMBOLĪZES KOMPlikācijas:
Galvenās komplikācijas ir asiņošanas risks (deguna, kuņģa-zarnu trakta, nieru) un išēmiskā fokusa pārvēršanās risks smadzeņu asiņošanā.
Trombolītiskā terapija ļauj novērot patiesi dramatisku pacienta stāvokļa uzlabošanos, kad smagi neiroloģiski traucējumi burtiski pazūd “uz adatas”, un viņš ne tikai izdzīvo, bet arī atveseļojas, kas iepriekš bija gandrīz neiespējami.
Lokālā trombolīze: lokālās trombolīzes laikā zāles injicē tieši tromba vietā. Zāles tiek piegādātas caur katetru, tāpēc šo metodi sauc par katetra trombolīzi. Tomēr šo metodi ir grūtāk īstenot nekā pirmo, un tā ir saistīta ar zināmām briesmām. Procedūras laikā ārsts uzrauga katetra kustību, izmantojot rentgena starus. Šīs metodes priekšrocība ir tās zemā invazivitāte. To lieto pat tad, ja pacientam ir liels skaits hronisku slimību.